益生菌对儿童与青少年功能性便秘治疗效果的Meta分析
王俊丽,陈涛,李锋,盛晓阳,薛敏波
上海交通大学医学院附属新华医院儿童与青少年保健科(中国上海200092)
·论著Article·
益生菌对儿童与青少年功能性便秘治疗效果的Meta分析
王俊丽,陈涛,李锋,盛晓阳,薛敏波*
上海交通大学医学院附属新华医院儿童与青少年保健科(中国上海200092)
目的评价益生菌对儿童与青少年功能性便秘治疗的有效性,为临床应用提供循证依据。方法通过计算机检索等途径,收集国内外文献,纳入与本研究主题相关的随机对照研究。使用Revman5.1软件对结局指标进行统计分析及描述。结果共纳入6个随机对照研究。Meta分析结果显示,益生菌对儿童与青少年功能性便秘无明显治疗效果。亚组分析显示,益生菌的应用对便秘患儿的各种临床症状,包括腹痛情况、大便频次、大便硬度、大便潴留及用泻药频次均无明显改善。结论Meta分析结果提示益生菌的应用对儿童与青少年功能性便秘无明显治疗效果。
功能性便秘;儿童与青少年;益生菌;Meta分析
便秘是儿童和青少年消化系统常见症状,其中约90%为功能性便秘[1]。据统计,我国城市儿童(<12岁)便秘者占12.8%,且有研究[2]发现,其中约50%的儿童便秘症状会长期存在甚至延续至成年,从而严重影响其生活质量以及学习工作发展。
目前临床上对儿童和青少年功能性便秘的药物治疗还没有统一认可,益生菌因其对胃肠道的调节作用,在便秘的临床治疗中经常应用,但很多临床医师忽略了其副作用即菌群转移[3],且就其疗效在临床上确无一致的意见。本研究采用Meta分析方法对国内外相关研究结果进行定量综合,旨在探讨益生菌治疗儿童和青少年便秘的有效性。
1 资料与方法
1.1 文献纳入标准
1.1.1 研究对象2~20岁的儿童或青少年,排除其他器质性疾病,便秘的诊断标准遵循研究当时的罗马研究组规定。其性别、种族、国籍不限。
1.1.2 干预措施有单独的试验组患儿的干预以益生菌制剂或含有益生菌的某种媒介如酸奶为主要干预手段;对照组患儿给予安慰剂或给予不含益生菌的奶类。
1.1.3 研究类型入选研究为有关益生菌与安慰剂或空白对照比较的随机对照研究(randomized controlled trial)。
1.1.4 评价指标益生菌应用有效的指标为每周大便次数≥3次,同时大便失禁≤1次。
1.2 资料收集和信息提取
1.2.1 文献检索策略
应用主题词“益生菌/probiotic”、“儿童/childhood”(或“child”或“children”)、“青少年adolescent”、“便秘/constipation”、“肠易激综合征/ irritable bowel syndrome”、“随机对照试验/randomized controlled trials”。通过计算机检索PubMed、EMBASE、Scopus、The Cochrane Central Register of Controlled Trials(Clinical Trials)、Clinical Evidence、MICROMEDEX临床暨循证医药学数据库、万方数据知识平台、维普中文科技期刊全文数据库(VIP)、中国生物医学文献数据库和中国知网(CNKI)的文献,并辅以文献追溯、手工检索等方法。检索语言为英文和中文。检索年限为建库至2013年11月。
1.2.2 文献纳入和排除标准
文献纳入标准:①国内外以论文形式公开发表的益生菌治疗儿童便秘的随机对照研究;②研究开展的年限和地区明确;③研究对象的年龄为2~20岁;④样本大小、病例和对照来源明确;⑤便秘诊断的标准遵循当时的罗马研究组规定;⑥研究结果内至少有以下一项可利用的数据:排便频次(infrequent bowel habits);大便硬度(hard stools);大便不尽(excessive straining);阻塞感(a sense of anorectal blockage);用手辅助排便(the use of manual manoeuvres during evacuation);腹痛(abdominal pain);原始数据提供比值比(odds ratio,OR)及95%置信区间(confidence interval,CI)或可通过数据计算。
文献排除标准:①研究对象:无法单独提取功能性便秘儿童数据的文献;②试验组和对照组间基线资料不可比;③无可利用数据(如无纳入标准所列项目),计量资料以非s表示或计数资料以非具体阳性人数和总人数表示,但又无法通过数据计算而得。
由2名研究者按上述文献纳入和排除标准独立筛选文献,对阅读摘要后不能排除或纳入的文献,在获取全文阅读后决定;2名研究者文献纳入和排除意见不一致时,由第3名研究者评价后讨论决定。
1.2.3 文献质量评估
按照Cochrane协作网系统评价手册推荐的“偏移风险评估工具”,包括以下方面:①随机分配方法,分配方案隐藏;②对研究对象和方案实施者采用盲法;③对结果测量者采用盲法;④数据结果的完整性(退出/失访);⑤选择性报告研究结果;⑥其他偏倚。针对每项研究,对上述项目做出“是”(低度偏倚)、“否”(高度偏倚)或“不清楚”(缺乏相关信息或偏倚情况不确定)的判断。各项判断结果均为“是”时,发生各种偏倚的可能性最小,质量等级为A;判断结果仅部分为“是”时,质量等级为B;判断结果均为“否”时,发生各种偏倚的可能性最大,质量等级为C。
1.3 统计分析
按Meta分析要求整理、核对数据,以Excel 2007建立数据库。采用Revman5.1软件对文献数据进行合并,计量资料用标准化均数差(SMD)及其95%CI表示,计数资料用比值比(odds ratio,OR)及其95%CI表示,同质性检验、敏感性分析及亚组分析。当结果不存在异质性(P≥0.10和I2<50%)时,采用固定效应模型描述;当结果存在异质性(P<0.10和I2≥50%)时,采用随机效应模型进行合并分析。对无法合并效应量进行Meta分析的数据采用描述性分析。采用漏斗图进行发表偏倚分析。采用敏感性分析对Meta分析结果稳定性进行判读。P<0.05为差异有统计学意义。
2 结果
2.1 文献基本情况
共检索到74篇文献,根据纳入标准和排除标准,其中7篇符合标准,进一步阅读全文,文献中有1篇不能单独提取功能性便秘数据,予以排除。最终有6篇文献纳入Meta分析,研究分布于6个国家或地区,各研究中性别分布差异无统计学意义。
2.2 纳入文献的基本信息和方法质量评价
6项研究累计共纳入便秘患儿421例,其中试验组220例,对照组201例。所有研究均对两组便秘患儿的年龄、性别、每周排便次数、便秘持续时间、大便干结程度及腹痛情况等基线资料进行了统计学评价,具有可比性(P>0.05)。文献具体信息见表1。
2.3 Meta分析结果
对6项研究报道中益生菌对功能性便秘患儿治疗效果进行Meta分析,如图1所示同质性检验P= 0.05,I2=54%,用随机效应模型OR=1.11(95%CI:0.83~1.50),敏感性分析剔除权重较大的文献报道,其结论不变。根据漏斗图示研究无偏倚。提示益生菌制剂对儿童功能性便秘无明显治疗效果。
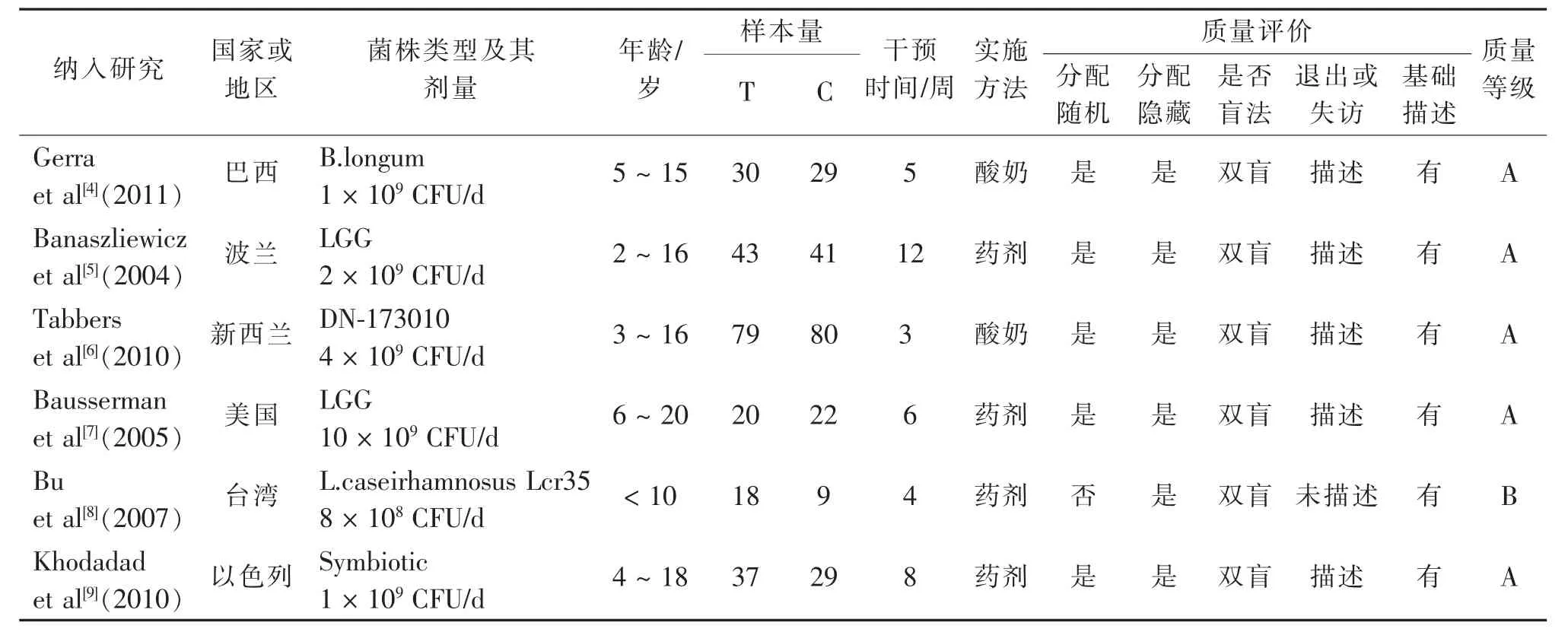
表1 纳入文献的基本信息和质量评价
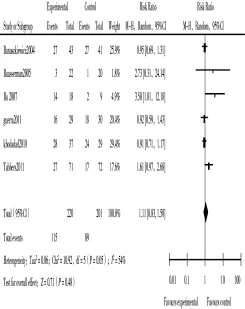
图1 益生菌组及对照组儿童功能性便秘治疗效果的Meta分析森林图
2.4 益生菌对功能性便秘相关症状的改善情况
在应用益生菌治疗儿童功能性便秘的研究中,关于功能性便秘的临床症状,根据其报告数据是分类变量还是连续性变量分别进行Meta分析,且根据其临床症状的不同进行亚组分析(图2、图3)。
数据为分类变量的临床症状亚组分析中,经同质性检验,各研究间不存在统计学异质性(P= 0.33,I2=14%),采用固定效应模型进行分析。益生菌的应用在改善儿童功能性便秘临床症状,包括腹痛情况(OR=1.09,95%CI:0.65~1.82)、大便伴疼痛(OR=1.46,95%CI:0.79~2.72)、用泻药情况(OR=0.83,95%CI:0.47~1.45)、硬便情况(OR=0.42,95%CI:0.14~1.27)及肠胀气情况(OR=0.72,95%CI:0.34~1.50)与对照组比较均无统计学意义。
数据为连续性变量的临床症状亚组分析中,经同质性检验,各研究间不存在统计学异质性(P= 0.28,I2=10%),采用固定效应模型进行分析。益生菌的应用在改善儿童功能性便秘临床症状,包括大便频率(SMD=0.02,95%CI:-0.21~0.25)、大便失禁频次(SMD=0.06,95%CI:-0.24~0.36)及用力排便频次(SMD=-0.18,95%CI:-0.61~0.25)与对照组比较亦均无统计学意义。

图2 益生菌组与对照组便秘患儿临床症状改善状况的Meta分析森林图(数据为分类变量)

图3 益生菌组与对照组便秘患儿临床症状改善状况的Meta分析森林图(数据为连续性变量)
3 讨论
3.1 益生菌对儿童功能性便秘的治疗无明显效果
Meta分析作为对多个研究结果综合评价和定量分析的方法,只有严格评价文献和妥善处理数据才能防止新的偏倚的产生,得到可靠的结论。益生菌的种类繁多,且某一菌属又有菌种和菌株的差异,为此我们进行了亚组分析。其中鼠李糖菌属组[5,7]的同质性检验P=0.34,OR=1.05(95%CI:0.46~2.33);通过酸奶[6,10]作为干预措施的研究组同质性检验P=0.34,OR=1.30(95%CI:0.84~2.02)。由此也可提示益生菌对儿童功能性便秘的治疗无明显效果。
3.2 儿童功能性便秘的相关症状
儿童与青少年功能性便秘的临床症状,根据功能性胃肠病的罗马Ⅲ诊断标准,其核心症状包括大便频次、腹痛、大便时伴疼痛、大便失禁、用力排便、大便硬度引起堵塞等。在前述的Meta分析森林图中,图2和图3提示益生菌的应用对便秘患儿的临床症状并未有效改善。此外,在纳入的研究中,因未显示数据而没有纳入Meta分析的图表,我们在此就益生菌对便秘相关的腹痛及大便频次的改善进行讨论。
3.2.1 腹痛症状
有3项研究对便秘相关腹痛进行了数据报道,此外还有2项研究通过图示提示益生菌能改善便秘相关的腹痛症状。Guerra等[4]在巴西的研究为临床随机、交叉、双盲、对照试验,研究对象为5~15岁学生,诊断标准为功能性胃肠病罗马Ⅲ中儿童功能性便秘诊断标准,干预菌株为Bifidobacterium longum。其中干预组30人,对照组29人,总研究时间为6周,其益生菌的研究存在媒介即酸奶,作者认为对照组(酸奶组,酸奶内主要存在两种菌株)和干预组(加双歧杆菌株的酸奶,即干预组内主要存在3种菌株)均可改善儿童功能性便秘的腹痛症状,但干预组的改善程度高于对照组。作者的结果多以图例进行展示,没有明确的数据,且对腹痛的评价以每周一次作为阳性标准,相对宽泛,不足以支撑该结论。Bu等[8]在台湾研究是以Lactobacillus casei rhamnosus(Lcr35)为干预菌株,研究对象为<10岁的功能性便秘患儿,分为Lcr35组(n=18)、氧化镁组(n=18)和安慰剂组(n=9),作者认为Lcr35可以缓解便秘患儿的腹痛症状,但该研究的样本量较少,可能不足以支撑该结论。这与Horvath等[11]于2011年关于Lactobacillus rhamnosus GG(LGG)的Meta分析的观点一致,作者在文章中的观点是LGG可改善肠易激综合征导致的腹痛,但对其他的腹痛相关性胃肠病无明显改善作用。腹痛是一种症状,它的评级具有主观性,因此益生菌是否能够改善儿童便秘相关的腹痛有待进一步的研究。
3.2.2 大便频次
纳入分析的各研究中大便频次的改善益生菌组与对照组无明显差异(除Bu等[8]在台湾的研究),但纳入Meta分析后,并未改变总体Meta分析的统计结果(图3)。在Tabbers等[6]在新西兰和波兰的研究中,益生菌组饮用主要含有Bifidobactrium lactis DN-173010的酸奶3周,对照组饮用不含任何益生菌的外观相同的奶制品;在研究结果中两组的大便频次均有改善,且无统计学差异,益生菌组和对照组大便频次的改善数据分别为2.9±3.2和2.6±2.6。Banaszkiewicz等[5]的研究因其应用益生菌的同时也应用了乳果糖,剔除或纳入Meta分析均未改变Meta分析的统计结果。Guerra等[4]在巴西的研究结果中,大便频次在应用益生菌3周后,益生菌组和对照组均有改善,而且更有意思的是交叉后两组的大便频次在交叉前的基础上几乎没有改变。在这两个研究中,作者在研究过程中都进行了排便训练的指导,而且在其他的关于儿童便秘的研究中,研究前后无论是试验组还是对照组,大便频次在研究结束时均较研究初明显改善,具有统计学意义,提示排便训练可能是改善儿童与青少年功能性便秘的有效途径。
综上所述,益生菌对儿童与青少年功能性便秘的治疗效果并不明显。而且益生菌的副作用在各研究中都未观察到,因此临床医师很可能会忽视益生菌是有副作用的,它的副作用是细菌的转移即益生菌在肠道受损或免疫力低下时有可能转移到血内引起菌血症,尤其是对于先天存在免疫缺陷的患儿[3]。随着饮食结构的改变,我国儿童与青少年功能性便秘的发生率有所上升,近年来也有研究认为儿童便秘的临床症状中大便频次不是诊断便秘的主要依据[12],即治疗效果的评价也有待进一步完善,因此综合性评价益生菌对其治疗效果有待进一步的研究,但临床上对于功能性便秘患儿应用益生菌应慎重考虑。
[1]Tabbers M M,Boluyt N,Berger M Y,et al.Constipation in children[J].Clinical Evidence(Online),2010.
[2]Bongers M E,Benninga M A,Maurice-Stam H,et al. Health-related quality of life in young adults with symptoms of constipation continuing from childhood into adulthood[J].Health and Quality of Life Outcomes,2009,7:20.
[3]Foligne B,Daniel C,Pot B.Probiotics from research to market:the possibilities,risks and challenges[J].Current Opinion in Microbiology,2013,16(3):284-292.
[4]Guerra P V,Lima L N,Souza T C,et al.Pediatric functional constipation treatmentwithBifidobacteriumcontaining yogurt:a crossover,double-blind,controlled trial[J].World Journal of Gastroenterology,2011,17(34):3916-3921.
[5]Banaszkiewicz A,Szajewska H.Ineffectiveness of Lactobacillus GG as an adjunct to lactulose for the treatment of constipation in children:a double-blind,placebo-controlled randomized trial[J].Journal of Pediatrics,2005,146(3):364-369.
[6]Tabbers M M,Chmielewska A,Roseboom M G,et al. Fermented milk containing Bifidobacterium lactis DN-173010 in childhood constipation:a randomized,doubleblind,controlled trial[J].Pediatrics,2011,127(6):e1392-1399.
[7]Bausserman M,Michail S.The use of Lactobacillus GG in irritable bowel syndrome in children:a double-blind randomized control trial[J].Journal of Pediatrics,2005,147(2):197-201.
[8]Bu L N,Chang M H,Ni Y H,et al.Lactobacillus casei rhamnosus Lcr35 in children with chronic constipation[J].Pediatrics International,2007,49(4):485-490.
[9]Khodadad A,Sabbaghian M.Role of synbiotics in the treatment of childhood constipation:a double-blind randomized placebo controlled trial[J].Iran Journal of Pediatrics,2010,20(4):387-392.
[10]Guandalini S,Magazzu G,Chiaro A,et al.VSL#3 improvessymptomsinchildrenwithirritablebowel syndrome:a multicenter,randomized,placebo-controlled,double-blind,crossover study[J].Journal of Pediatric Gastroenterology and Nutrition,2010,51(1):24-30.
[11]Horvath A,Dziechciarz P,Szajewska H.Meta-analysis:Lactobacillus rhamnosus GG for abdominal pain-related functionalgastrointestinaldisordersinchildhood[J]. Alimentary Pharmacology&Therapeutics,2011,33(12):1302-1310.
[12]李俊,黎海芪.6岁以下儿童排便状况503例调查[J].中国儿童保健杂志,2011,19(9):853-855.
Efficacy of probiotic supplementation for treatment of functional constipation in children and adolescents:Meta-analysis
WANG Junli,CHEN Tao,LI Feng,SHENG Xiaoyang,XUE Minbo*
Department of Child and Adolescent Healthcare,Xinhua Hospital affiliated to Shanghai Jiaotong University School of Medicine,Shanghai200092,China
ObjectiveTo assess the efficacy of probiotic supplementation for treatment of functional constipation in children and adolescents,and provide evidence for clinical practice.MethodsRelevant randomized controlled trials were collected by electronic searching for domestic and overseas literature.Revman 5.1 software was adopted for statistical analysis and description of outcome parameters.ResultsSix randomized controlled trials were included.Meta-analysis revealed that probiotic supplementation had no significant therapeutic effect in overall participants with functional constipation.Subgroup analysis demonstrated that probiotic supplementation did not significantly ameliorate symptoms(abdominal pain,stool frequency,stool hardness and fecal soiling)of participants with functional constipation.ConclusionMetaanalysis indicates that probiotic supplementation may not have therapeutic effect on functional constipation in children and adolescents.
functional constipation;child and adolescent;probiotic;Meta-analysis
10.3969/j.issn.2095-4301.2014.03.006
*通信作者(Corresponding author)薛敏波,硕士,主治医师;电子信箱:xue_minbo66@hotmail.com
2014-09-02

