三聚氰胺荧光猝灭法测定维生素K3
董存智,吴雯辉
(淮北师范大学 化学与材料科学学院,安徽 淮北 235000)
维生素K3(VK3)具有萘醌结构,其主要生理作用是促进血浆凝血因子的合成并参与人体的钙代谢,可用于治疗维生素K缺乏所引起的出血性疾病,属于促凝血药[1].测定VK3的方法有光度法[2-3]、电化学法[4-5]、荧光法[6-7]、色谱法[8]等.由于VK3的不饱和酮结构共轭体系较小,不能产生荧光,因此,测定VK3的荧光光度法主要是基于将VK3还原成具有荧光的醌萘酚化合物,通过测定醌萘酚化合物的荧光强度,求得VK3的含量,还原程度有可能对测量准确度产生影响.三聚氰胺俗称蛋白精,是三嗪类含氮杂环化合物,其分子中含有共轭双键(π键)结构.在碱性介质中,当受到紫外光照射后,其环外氨基上的n电子激发转移到环上,由于n电子的电子云几乎与环上π轨道平行,共享了共轭π电子结构,扩大了其共轭双键体系,故可发出较强的荧光[9].基于其与Ag(I)发生络合反应,生成不发荧光的络合物,已用于定影废液中Ag(I)的测定[10].实验发现,在B-R缓冲溶液中,VK3与三聚氰胺作用,使三聚氰胺的荧光发生猝灭.由此,建立了荧光猝灭法测定VK3的新方法.
1 实验部分
1.1 仪器与试剂
FP-6500荧光分光光度计(日本分光株式会社).三聚氰胺溶液:2.0 g/L.VK3乙醇溶液:0.10 g/L(20%乙醇).伯瑞坦-罗比森缓冲溶液(B-R):pH 7.0.本实验用水均为超纯水,试剂均为分析纯.
1.2 测定方法
在2只10 mL比色管中分别加入2.0 g/L的三聚氰胺溶液2.0 mL;pH 7.0的B-R缓冲溶液0.5 mL;其中一支加入适量0.10 g/L VK3溶液或待测液,另一支为试剂空白;用水定容至10 mL;混匀后静置20 min.在λex/λem=256 nm/366 nm 处测量荧光强度,其中含VK3者的荧光强度为F,试剂空白的荧光强度为F0,计算ΔF=F0-F.
2 结果与讨论
2.1 荧光光谱
三聚氰胺荧光光谱如图1所示.由图1可知,在pH 7.0的B-R缓冲溶液中,当激发波长为256 nm时,三聚氰胺的发射峰位于366 nm处.三聚氰胺的荧光强度随着VK3浓度的增加而减弱,其减弱程度与VK3的浓度呈线性关系.实验选择的激发波长为256 nm,发射波长为366 nm.

图1 荧光光谱Fig 1 Fluorescence spectrum 1~3:Melamine +VK3 (0、4、8 mg/L)

图2 pH的影响Fig 2 Effect of pH
2.2 酸度的影响
按照实验方法,考察了Tris-HCl,硼酸-硼砂,B-R,巴比妥钠-HCl 等缓冲溶液的影响.试验结果表明,在B-R缓冲溶液中体系的荧光猝灭效果最好.改变B-R缓冲溶液的pH值,实验结果如图2所示,实验发现pH在4.1~11.5之间时体系的测量结果变化不明显,ΔF在7.0时有最大值.改变pH 7.0的B-R缓冲溶液用量,试验发现加入量为0.5 mL时体系的ΔF有最大值,因此,实验选择pH 7.0的B-R缓冲溶液的加入量为0.5 mL.
2.3 反应时间的影响
按实验方法,改变反应时间测量荧光强度与反应时间的关系,实验发现,反应20 min后体系的荧光强度趋于稳定,体系的ΔF值在20-150 min内保持稳定,因此,反应时间选择为20 min.

图3 反应时间的影响Fig 3 Effect of reacting time
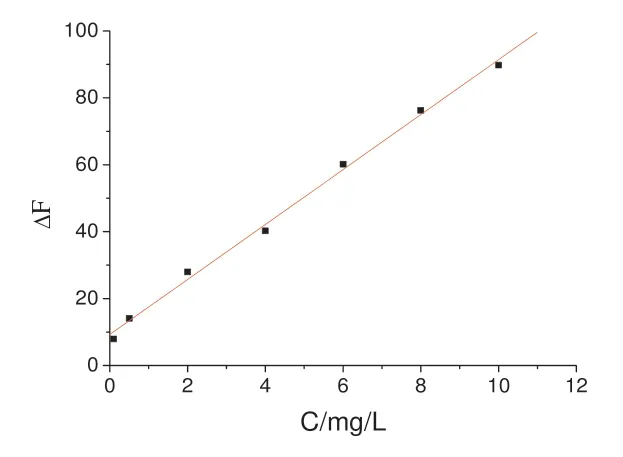
图4 工作曲线Fig.4 Working curve
2.4 三聚氰胺用量的影响
按实验方法,改变2.0 g/L的三聚氰胺溶液的加入量,实验结果表明,随着三聚氰胺用量的增大,体系的ΔF值增加,但用量过大时,三聚氰胺本身发生自体淬灭作用,综合考虑灵敏度和线性范围,实验选择三聚氰胺溶液的加入量为2.0 mL.
2.5 干扰试验
在实验条件下,试验了不同物质对VK3测定的影响,当VK3浓度为6 mg/L,实验相对误差在±5%以内时,各种物质的允许共存倍数分别为:β-环糊精600倍;NH4+500倍;K+400倍;葡萄糖、Zn2+、SO42-、Mg2+、肝素钠、VC50倍;木瓜蛋白酶、胃蛋白酶、尿素30倍;甘氨酸 20倍;辅酶15倍.
2.6 工作曲线
按实验方法,改变VK3的加入量测量荧光强度.实验结果用最小二乘法进行拟合,得到回归方程为:
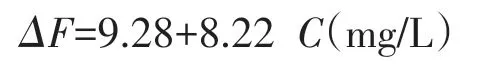
相关系数为0.998,方法的线性范围为0.10~10.00 mg/L,根据12次空白实验的3σ值求得方法的检出限为0.085 mg/L.
2.7 样品分析
取不同厂家生产的维生素K3粉(饲料添加剂)0.10 g(标示量为每克含有5%的VK3),于研钵中研细混匀后置于小烧杯中,加0.10 mol/L NaOH 数滴及少量水使之溶解,转移到100 mL容量瓶中,用水定容.实验时移取0.40 mL试液,按照实验方法对样品中VK3进行测定,并做加标回收试验,实验结果见表1.由实验结果求得所测的维生素K3粉中VK3的含量为5.04%-5.33%.

表1 样品分析结果(n=5)Tab.1 Analytical results of samples
2.8 猝灭机理与热力学参数
引起体系荧光猝灭的原因可能包括动态猝灭和静态猝灭两种.动态猝灭是猝灭剂和荧光物质的激发态分子之间的相互作用过程,其过程遵循Stern-Volmer方程[11]:

式(1)中F、F0分别为猝灭剂(即VK3)存在和猝灭剂不存在时的荧光强度,Ksv为动态猝灭常数,Kq为双分子猝灭过程速率常数,[Q]为猝灭剂浓度,τ0为无猝灭剂时荧光分子的平均寿命.而静态猝灭是猝灭剂和荧光物质分子在基态时生成不发光的配合物,从而导致荧光强度降低的过程,此过程可用下式描述:

式(2)中,K是配合物的形成常数.
2.8.1 温度的影响
按实验方法,分别恒定温度为20 ℃、30 ℃、40 ℃,测定体系荧光强度随猝灭剂浓度的变化情况,以F0/F对[Q]作图(图5),求出20 ℃、30 ℃、40 ℃下的K值分别为 1.49×104L·mol-1、1.25×104L·mol-1、1.10×104L·mol-1.按照一般荧光分子τ0为10-8s 计算的Kq数值为1012L·mol-1·s-1,远大于扩散碰撞速率常数2.0×1010L·mol-1·s-1,且随着温度的升高K值降低.说明在实验条件下,VK3对三聚氰胺的猝灭属于静态猝灭,此时VK3与三聚氰胺之间可能形成不发荧光的基态配合物.
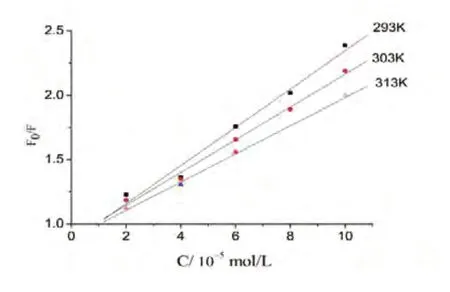
图5 Stern-Volmer 曲线Fig 5 Stern-Volmer curve
2.8.2 热力学参数
根据如下热力学公式:


由20 ℃、30 ℃的K值,计算热力学参数焓变ΔH、熵变ΔS和自由能变ΔG,结果列于表2.从表2可看出VK3与三聚氰胺结合过程的ΔH<0,表明反应为放热反应,升高温度将不利于其向生成VK3-三聚氰胺配合物的方向进行,VK3与三聚氰胺的结合常数随温度升高而减小,配合物稳定性下降;反应的ΔG<0,说明VK3与三聚氰胺结合过程是一个自发过程.

表2 VK3与三聚氰胺结合的热力学参数Tab.2 Thermodynamic parameters of melamine–VK3 binding procedure
[1]王汝龙,原正平.化工产品手册:药物[M].北京:化学工业出版社,1999.
[2]阳泽平,刘忠芳,胡小莉.甲基绿褪色分光光度法测定维生素K3[J].分析化学,2006,34(S1):269-271.
[3]陈彩萍,杜黎明,段亚丽,等.离子对缔合物萃取分光光度法测定维生素K3[J].分析化学,2005,33(2):237-240.
[4]史学丽,左志宇,王方,等.溶出伏安法测定血清中维生素K3[J].天津医科大学学报,2012,18(1):125-128.
[5]顾玲,贺亚梅,张苗,等.维生素K3在二茂铁修饰碳糊电极上的电化学行为及其测定[J].分析试验室,2013,32(1):117.
[6]ZHOU Yunyou,XU Hongwei,WU Lian,et al.Spectrofluorimetric study on the inclusion interaction between vitamin K3with p-(p-sulfonated benzeneazo)calix[6]arene and determination of VK3[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2008,71(2):597–602.
[7]韩一秀,李松青.荧光法测定维生素K3[J].分析科学学报,2008,24(6):738-740.
[8]朱伟.动物用维生素预混合饲料中VK3含量测定[J].化学工程与装备,2011(3):153-154.
[9]黄晖,李丽,马乔,等.表面活性剂增敏荧光光度法测定牛奶中的三聚氰胺.分析化学,2010,38(2):249-252.
[10]龙立平,赵丽丽,肖谷清.三聚氰胺荧光熄灭法测定Ag(Ⅰ)的研究[J].工业水处理,2011,31(5):72-75.
[11]许金钩,王尊本.荧光分析法[M].3版.北京:科学出版社,2006.

