化学镀法制备HMX/Cu复合粒子及其热分解特性的研究
熊烺录,郭效德,李凤生
(南京理工大学国家特种超细粉体工程技术研究中心,江苏南京 210094)
化学镀法制备HMX/Cu复合粒子及其热分解特性的研究
熊烺录,郭效德,李凤生
(南京理工大学国家特种超细粉体工程技术研究中心,江苏南京 210094)
采用化学镀法制备了HMX/Cu复合粒子,利用SEM和XRD研究其大小、形貌和物相组成,并通过DSC对其热分解特性进行了分析。研究结果表明:HMX/Cu复合粒子表面负载Cu的粒径约为80 nm,包覆比较均匀;负载的纳米Cu对HMX的固相分解有明显催化作用,前期分解热量百分比值从2.37%增加到97.29%,热分解峰向低温方向移动35.53℃,并且热分解放缓;当升温速率为15℃/min时HMX/Cu的热分解变得非常剧烈;与HMX相比,HMX/Cu的表观活化能降低了33.16 kJ/mol;适量O2存在有利于纳米HMX/Cu的热分解。对纳米Cu的催化机理进行分析,提出了催化剂的“空间分布效应”。
兵器科学与技术;化学镀;负载催化剂;纳米Cu;热分解;催化作用
0 引言
奥克托今(HMX)有4种晶型,分别为α、β、γ、δ,其中最稳定的是β型。β型的热分解有以下两个过程:1)在195℃左右发生β-γ晶型转变;2)在280℃左右开始液化,同时发生剧烈的热分解。HMX分解放热的速率很快,在DSC曲线呈陡峭的尖峰。
HMX具有高爆热、高爆速和爆轰稳定等优点,广泛地应用在固体推进剂、发射药和混合炸药中。通常在HMX中加入纳米金属或金属化合物来改变其热分解特性。江治等[1]用纳米Cu与HMX混合,分析其热分解特性,发现HMX的起始分解温度提前了33.42℃,分解峰向低温方向移动了15.92℃;范夕萍等[2]对纳米Cu与HMX进行机械研磨混合,并分析其热分解特性,发现HMX的起始分解温度提前了25.5℃,Cu粉的稀释和分散作用使放热焓下降;洪伟良等[3]研究了纳米CuO对黑索今(RDX)热分解的影响时发现,RDX的热分解峰温降低了12℃.目前研究铜粉对HMX热分解催化作用的主要过程是先制备出铜粉,然后再将铜粉与HMX混合,最后测试混合物的热分解特性[4-5]。由于机械混合很难使铜粉与HMX充分混匀,难以最大限度地发挥Cu的催化作用,使得其在实际应用中受到很大限制。
化学镀法可以很好地在惰性基体上负载一层由纳米颗粒组成的包覆层。Song等[6]采用化学镀法制备出包覆完整的PS/Ni微球,其包覆层的厚度约为150 nm.
本文采用化学镀法制备出HMX/Cu复合粒子,并通过DSC技术研究了负载的纳米Cu对HMX热分解的催化作用和热分解动力学,以及热分解条件对HMX热分解特性影响的规律。
1 实验方案
1.1 HMX/Cu复合粒子的制备
实验采用化学镀法制备HMX/Cu复合粒子,其工艺流程如图1所示。
实验参照文献[7]的胶体钯配方,把7.5 mL (10 g/L)的PdCl2溶液与10 mL浓盐酸和37.5 mL的去离子水混合,在机械搅拌下缓慢加入4.5 g SnCl2,制备出A溶液;另称取45 g NaCl溶于195 mL去离子水中,制备出B溶液;将B溶液缓慢地加入到A溶液中,在不断搅拌下混合,并在50℃温度下保温2 h,即可得到初步的胶体钯溶液,然后将其放在70℃水浴干燥箱中保温2 d,形成稳定、高活性的胶体钯溶液。化学镀铜在pH=9,反应温度为50℃的情况下进行,其镀液配方如表1所示。
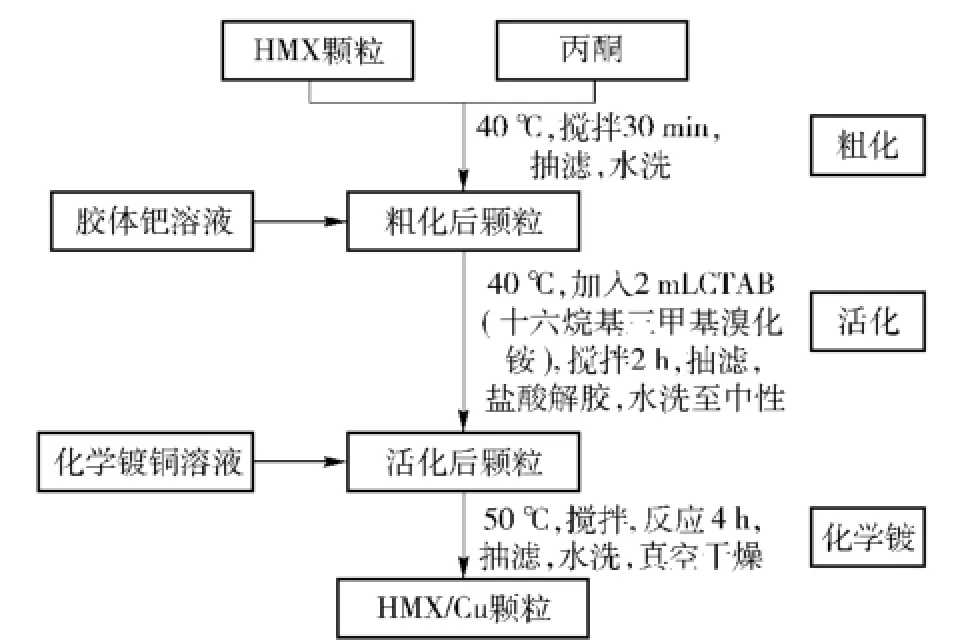
图1 HMX/Cu复合粒子的制备工艺流程图Fig.1 Flow chart of experimental process

表1 化学镀铜溶液Tab.1 Solution of electroless plating copper
1.2 实验仪器
实验采用复纳科学仪器(上海)有限公司生产的G2 pro型台式扫描电子显微镜;日本日立公司生产的S4800Ⅱ型扫描电子显微镜;德国Bruker公司生产的D8型X射线粉末衍射仪;美国TA公司生产的SDT-Q600型差热分析仪。
2 结果与讨论
2.1 HMX/Cu的SEM和XRD表征
对HMX化学镀前后进行SEM表征,结果如图2所示。
由图2(a)和图2(b)可知,HMX颗粒大小在100 μm左右,晶体呈规则的多面体型,且表面光滑。由图2(c)和图2(d)可以看出,HMX/Cu复合粒子大小也在100 μm左右,复合粒子大小没有明显的变化。HMX表面上负载Cu后形成的白色颗粒,棱角没有那么明显,包覆较均匀。由图2(e)可知,负载在HMX表面的Cu颗粒大小约为80 nm.对HMX和HMX/Cu复合粒子进行XRD表征,结果如图3所示。
由图3可知,HMX/Cu复合粒子的衍射图谱上比HMX多3个衍射峰,在45.51°、50.60°、74.31°处分别对应面心立方体结构Cu的(111)、(200)、(220)晶面,说明Cu已成功负载到HMX的表面上。

图2 HMX和HMX/Cu的SEM图Fig.2 SEM images of HMX and HMX/Cu
2.2 纳米Cu对HMX的热分解特性影响
分别对HMX和HMX/Cu进行DSC测试,DSC测试的条件为升温速率10℃/min,在N2的气氛下气体流速为20 mL/min,结果如图4、图5和表2所示。
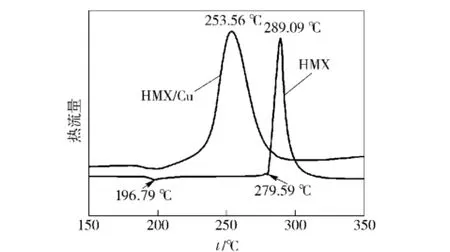
图4 HMX和HMX/Cu的DSC曲线Fig.4 DSC curves of HMX and HMX/Cu
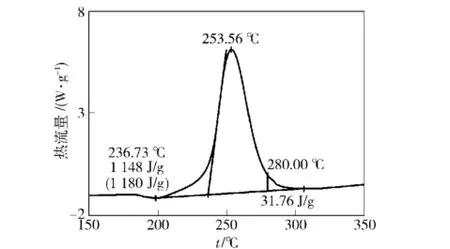
图5 HMX/Cu的能量分布图Fig.5 Energy distribution pattern of HMX/Cu
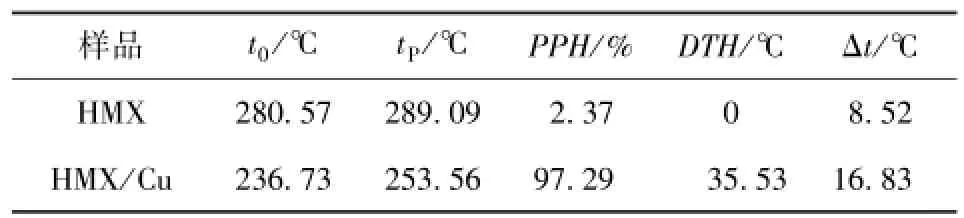
表2 HMX与HMX/Cu的DSC结果Tab.2 DSC results of HMX and HMX/Cu
由图4可知,HMX的热分解放热分为两部分:一是熔化前(279.59℃之前)有部分分解放热;二是熔化(279.59℃之后)伴随激烈分解放热。而负载了纳米Cu的HMX热分解曲线发生了很大变化:首先,热分解峰温从289.09℃降低至253.56℃,整个放热峰向低温方向移动;其次,主要的开始分解温度从279.59℃降低至196.79℃左右;最后,分解过程中没有伴随激烈的分解放热。
由表2数据可知,由于在HMX表面上负载了纳米Cu,使得HMX起始分解温度t0提前了43.85℃,热分解峰温向低温方向移动大小DTH为35.53℃,表明负载的纳米Cu对HMX热分解反应有很好催化作用。HMX/Cu复合粒子的分解峰温与起始分解温度的差值Δt达16.83℃,而HMX的Δt为8.52℃,表明纳米Cu可以使HMX的热分解均匀、稳定进行。
HMX是熔化前有部分分解、熔化伴随着激烈分解的化合物,熔化温度在280℃附近(见图4),从形态可以看出,熔化前是固态,所以把熔化前的热分解称之为固相反应,熔化后的热分解称之为液相反应。本文采用“前期分解热量百分比”这一参数来表示HMX热分解时固相与液相(气相)的相互作用,记为PPH.该参数是以280℃为分界线,280℃之前为分解热量与整体分解热量之比值,如图5所示,整个热分解放出的热量为1 180 J/g,其中固相热分解反应放出的热量为1 140 J/g,液相反应放出的热量为31.76 J/g,所以其PPH=1 140/1 180×100%.由表2可知,HMX的PPH值为2.37%,而HMX/Cu高达97.29%,表明HMX大部分热分解的热量是由HMX液化之后放出的,主要发生的是液相反应。HMX/Cu热分解的热量主要固相反应放出的。这说明纳米Cu对HMX热分解的催化作用主要在固相反应中。
2.3 升温速率对HMX/Cu热分解特性影响及其表观活化能
分别以5℃/min、10℃/min、15℃/min、20℃/min和30℃/min升温速率,在N2气氛和10 mL/min气体流速下对HMX和HMX/Cu进行DSC测试,结果如表3、图6和图7所示。
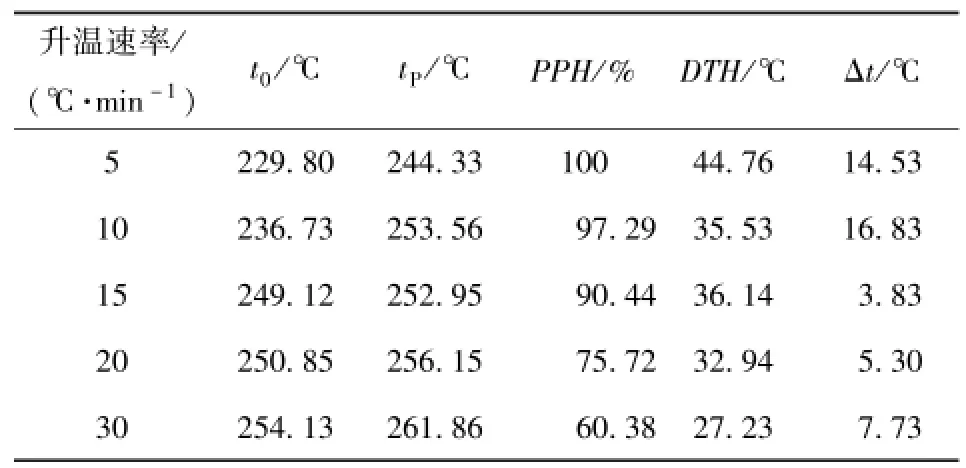
表3 升温速率对HMX/Cu的DSC结果Tab.3 DSC results of HMX/Cu at different heating rates
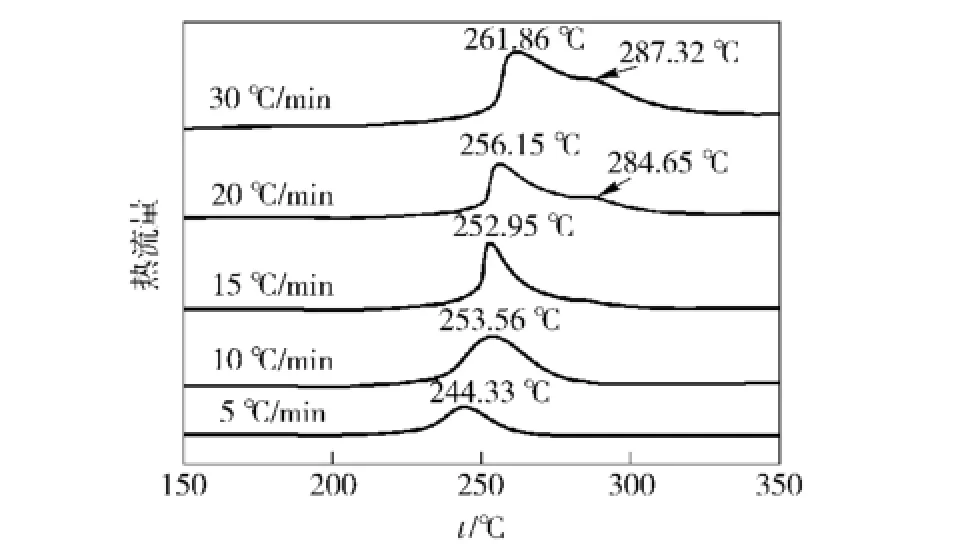
图6 不同升温速率下HMX/Cu的DSC曲线Fig.6 DSC curves of HMX/Cu at different heating rates

图7 不同升温速率下HMX的DSC曲线Fig.7 DSC curves of HMX at different heating rates
由表3可知,随着升温速率的增加,HMX/Cu的起始分解温度逐渐后移,PPH逐渐降低,如图6所示,在20℃/min和30℃/min分别出现了284.65℃和287.32℃液相反应分解峰,表明:升温速率的增加不利于HMX的固相分解反应;DTH随着升温速率的增加呈现下降趋势,升温速率越慢,纳米Cu对HMX的热分解催化化用越明显;对于Δt,随着升温速率增加,呈现先增大,后减小,然后再增大的趋势;升温速率为15℃/min时,HMX的热分解非常剧烈。升温速率是HMX热分解的重要参数,当升温速率小于10℃/min时,HMX热分解表现为均匀、稳定的;当升温速率超过15℃/min时,HMX热分解变得非常剧烈,又由于升温过快,使得部分HMX在280℃左右没有分解,就出现液相分解峰,并且升温速率越大,液相分解峰越明显(见图6所示)。
根据图6和图7所示的数据,采用(1)式计算HMX与HMX/Cu的表观活化能,结果如表4所示。
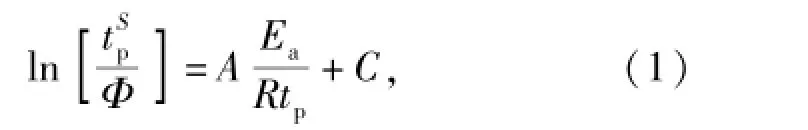
式中:Ea为表观活化能(kJ/mol);Φ为升温速率(K/min);C为常数;R为气体常数,取8.314 J/(K·mol);S为常数;A是与S相关的常数。当采用Kissinger方法时,S=2,A= 1;当采用Ozawa方法时,S=0,A=1.051 8;当采用Starink方法时,S= 1.8,A=1.007 0-1.2×10-8Ea.
如表4所示,分别有Kissinger方法、Starink方法以及Ozawa方法计算出的表观活化能基本相同,取三者的平均值表示HMX和HMX/Cu的表观活化能,分别为262.51 kJ/mol和229.35 kJ/mol,二者相差33.16 kJ/mol.经化学镀铜后的表观活化能降低了12.63%,表明负载的纳米Cu可以很好地降低HMX热分解的活化能,有效地促进HMX的热分解。

表4 HMX和HMX/Cu的表观活化能Tab.4 Apparent activation energies of HMX and HMX/Cu
2.4 气体流速对HMX/Cu的热分解影响
分别以5 mL/min、10 mL/min、20 mL/min和30 mL/min的气体流速,在升温速率为10℃/min和N2气氛中对HMX/Cu进行DSC测试,结果如表5和图8所示。

表5 气体流速对HMX/Cu的DSC结果Tab.4 DSC results of HMX/Cu at different flowing rates

图8 不同气体流速下HMX/Cu的DSC曲线Fig.8 DSC curves of HMX/Cu at different fliowing rates
由表5可知,随着气体流速的增加,PPH值也随着增加,这是由于气体流速的增加,能更快地带走固相反应的产物,促进固相反应进行。当通气速度小于一定数值(5 mL/min)时,因为气体流速较小,热量流失得少,使得HMX自身分解作用加强,导致其DTH较大,同时热分解反应剧烈,出现液相反应放热峰(如图8所示)。随着气体流速的增加,反应逐渐趋于稳定。
2.5 通气种类对HMX/Cu的热分解影响
分别让HMX/Cu在N2、O2和空气3种气氛中进行热分解,将单位质量放出的热量记为ΔH,结果如表6所示。
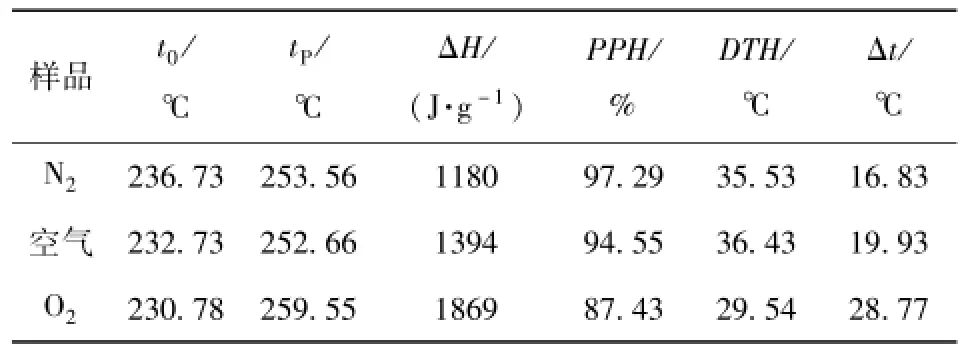
表6 通气种类对HMX/Cu的DSC结果Tab.6 DSC results of HMX/Cu in different flowing gases
由表6可知,随着O2含量的增加,起始反应温度t0和PPH逐渐下降,ΔH和Δt逐渐增加。显然, O2加入会使HMX的起始分解温度降低,增加了反应的放热量,同时也使热分解变得缓慢。出现这种现象的原因是,O2的加入加快了HMX的热分解,使得HMX热分解更加充分,放出的热量更多。HMX/ Cu在空气的气氛中热分解时,HMX热分解峰温tp会降低;当气氛变为纯O2时,HMX热分解放出了大量的热量,热量没有及时“排出”,就会“推高”tp.所以,通入空气有利于纳米Cu对HMX的催化作用。
3 HMX/Cu的催化机理分析
3.1 纳米Cu的催化机理分析
由文献[8-11]可知,过渡金属及过渡金属化合物对硝胺类炸药的热分解有很强的催化作用。按照过渡状态催化理论的观点,认为催化剂之所以可加速化学反应,是由于催化剂表面的活性中心容易与反应物发生化学吸附,生成不稳定的络合物。过渡金属由于外层电子轨道可实现Sd电子轨道杂化,导电的电子数小于1,使其具有一定导电作用,并且其化学活性较弱,因而能参与有电子转移的氧化还原反应,可与氧化剂反应形成不稳定氧化性络合物。此络合物与还原物反应后,放出过渡金属,可再参与催化。这就降低了氧化还原反应的活化能,提高了反应速率。
纳米Cu对HMX热分解分为二次催化作用[1]:第一次是由于纳米Cu中存在着大量的孪晶缺陷以及孔洞缺陷,可以将NO2和H从HMX分子中移走,导致了HMX分子中的C—N键和N—N键的键能变弱,促进了HMX的单分子分解;第二次是纳米Cu催化了HMX分解产物中的氮氧化物的分解反应,从而进一步促进了HMX的凝聚相(固相)分解。
HMX的固相分解时,原始分子中C—N键和N—N的是从两个互不相关的2个平行反应进行的[12]。
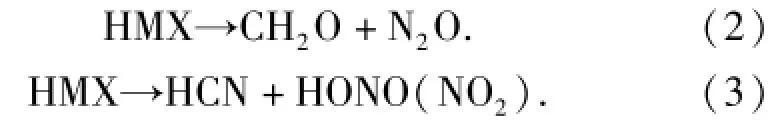
反应(2)是C—N键断裂,而反应(3)是N—N键断裂,二者是相互竞争的关系,文献[13-14]认为HMX初期分解反应的竞争机理受温度影响。温度较低时,HMX的分解以C—N键断裂为主,提高温度会使N—N键断裂增加。温度为230℃时, HMX的固相分解产物中40%为N2O,控制与N2O的反应也就控制固相分解的速率。HMX/Cu的反应起始温度在230~250℃之间,在这个温度时,HMX的固相分解产物大部分是N2O.Cu容易与N2O反应,促进HMX的固相分解,此时假定Cu催化反应如下:


3.2 负载型催化剂的催化机理分析
目前对复相催化反应的催化剂使用方式主要是将催化剂与反应物直接混合,或者先将催化剂负载到某个基体中,再与反应物混合。这样会使得催化剂与反应物的接触面积不是很充分。而将催化剂直接负载到反应物表面上的报道很少。
在复相催化反应的各个化学基元步骤序列中,速控步骤可以是吸附、表面反应或脱附。速控步骤不同,速控方程的形式也会有很大不同。根据复相催化反应的动力学方程[16],对于反应(4)的反应速率为r=kθN2O,式中:θN2O为反应时N2O在纳米Cu的表面覆盖度;k为催化活性常数。从动力学方程可知,在相同的催化剂中,催化反应速率与N2O在纳米Cu的接触量呈正比。HMX的化学镀以及热分解过程如图9所示。
由图9可知,化学法制备的HMX/Cu表面均匀负载催化剂。当HMX在固相分解时,释放出来的N2O能很好与纳米Cu接触,加快了催化速率。文献[1-2,4]制备出纳米Cu与HMX通过机械混合,其热分解催化作用不如化学镀制备的HMX/Cu,主要是因为纳米Cu分布形式不同。像这种因为催化剂分布形式不同而导致催化效果不同的现象称之为催化剂的“空间分布效应”。
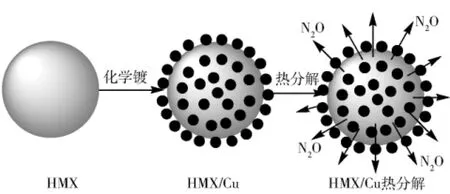
图9 HMX/Cu的制备与热分解Fig.9 Synthesis and thermal decomposition of HMX/Cu
4 结论
1)采用化学镀法成功制备了HMX/Cu复合粒子,Cu粒子的粒径在80 nm左右,包覆比较均匀。
2)与HMX相比,化学镀法制备的HMX/Cu的PPH值从2.37%提高到97.29%,热分解峰向低温方向移动35.53℃,并且热分解放缓;随着升温速率的提高,HMX/Cu的PPH值逐渐降低,当升温速率达到15℃/min时,热分解变得异常剧烈;HMX/Cu复合粒子较原料HMX的表观活化能降低了33.16 kJ/mol.随着气体流速的增加,HMX/Cu热分解趋于稳定;适当的O2存在有利于HMX/Cu的热分解。
3)对纳米Cu的催化机理进行了分析,并且化学渡法产生催化剂具有很好的“空间分布效应”;在催化剂的使用上提出了一种新的方式和思路。
References)
[1] 江治,李疏芬,赵凤起,等.纳米金属粉对HMX热分解特性的影响[J].推进技术,2002,23(3):258-261.
JIANG Zhi,LI Shu-fen,ZHAO Feng-qi,et al.Effect of nano metal powder on the thermal decomposition characteristics of HMX [J].Journal of Propulsion Technology,2002,23(3):258-261. (in Chinese)
[2] 范夕萍,王霞,刘子如,等.纳米Cu粉对HMX和RDX热分解的催化作用[J].含能材料,2005,13(5):284-287.
FAN Xi-ping,WANG Xia,LIU Zi-ru,et al.Catalysis of nano Cu powder on the themal decomposition of HMX and RDX[J].Chinese Journal of Energetic Materials,2005,13(5):284-287.(in Chinese)
[3] 洪伟良,刘剑洪,陈沛,等.纳米CuO的制备及其对RDX热分解特性的影响[J].推进技术,2001,23(3):254-257.
HONG Wei-liang,LIU Jian-hong,CHEN Pei,et al.Effect of nanometal CuO powder and its effect on themal decompositionchatacteristics of RDX[J].Journal of Propulsion Technology, 2001,23(3):254-257.(in Chinese)
[4] Dubey R,Srivastava P,Kapoor I P S,et al.Synthesis,characterization and catalytic behavior of Cu nanoparticles on thermal decomposition of AP,HMX,NTO and composite solidpropellants, Part-83[J].Thermochimica Acta,2012,549:102-109.
[5] Wei J P,Zhang D,Yang Q,et al.0D Cu(Ⅱ)and 1D mixed-valence Cu(Ⅰ)/Cu(Ⅱ)Coordination compounds based on mixed ligands:Syntheses,structures and catalytic thermal decomposition for HMX[J].Inorganic Chemistry Communications,2013,30: 13-16.
[6] Song D,Zhou J D,Wei J P,et al.A novel activation for electroless plating on preparing PS/Ni microspheres[J].Materials Letters.2009,63(2):282-284.
[7] 赵丹,宋红章,孙洪巍,等.化学镀法制备铜包覆SiC颗粒的研究[J].表面技术,2012,41(3):105-108,129.
ZHAO Dan,SONG Hong-zhang,SUN Hong-wei,et al.Study on the preparation of Cu-coated SiC particles by electroless plating [J].Journal of Surface Technology,2012,41(3):105-108, 129.(in Chinese)
[8] 高红旭,赵凤起,罗阳,等.纳米复合物PbO·SnO2的制备及对双基和RDX-CMDB推进剂燃烧性能的影响[J].火炸药学报, 2012,35(6):15-18,27.
GAO Hong-xu,ZHAO Feng-qi,LUO Yang,et al.Synthesis of nanocomposite PbO·SnO2and its effect on the combustion propreties of DB and RDX-CMDB propellants[J].Chinese Journal of Explosives&Propellants,2012,35(6):15-18,27.(in Chinese)
[9] 洪伟良,刘剑洪,田德余,等.纳米铜铬复全氧化物对RDX热分解的催化作用[J].推进技术,2003,24(1):83-86.
HONG Wei-liang,LIU Jian-hong,TIAN De-yu,et al.Catalysis of nanocomposite CuO·Cr2O3on thermal decomposition of RDX [J].Journal of Propulsion Technology,2003,24(1):83-86. (in Chinese)
[10] 洪伟良,刘剑洪,田德余,等.纳米PbSnO3的制备及其燃烧催化性能的研究[J].无机化学学报,2004,20(3):278-282.
HONG Wei-liang,LIU Jian-hong,TIAN De-yu,et al.Synthesis and combustion cataytic actiyity of nanocomposete PbSnO3[J]. Chinese Journal of Inorganic Chemistry,2004,20(3):278-282.(in Chinese)
[11] 焦宝娟,晏志军,陈三平.5,5′-偶氮四唑过渡金属含能配合物对RDX和HMX热分解行为的影响[J].火炸药学报, 2012,35(3):52-55.
JIAO Bao-juan,YAN Zhi-jun,CHEN San-ping.Effects of transition Metal 5,5'-azoterazolate energetic complexes on thermal decomposition behaviours of RDX and HMX[J].Chinese Journal of Explosives&Propellants,2012,35(3):52-55.(in Chinese)
[12] 任晓宁,邵颖惠,王晓红,等.奥克托金(HMX)的T-Jump/FTIR快速热裂解研究[J].化学学报,2010,68(12):1193-1198.
REN Xiao-ning,SHAO Ying-hui,WANG Xiao-hong,et al.An investigation on the flash pyrolysis process of octahydro-1,3,5,7-tetranitro-1,3,5,7-tetrazocine(HMX)by T-Jump/RTIR Spectroscopy[J].Acta Chimica Sinica,2010,68(12):1193-1198. (in Chinese)
[13] 刘子如.含能材料热分析[M].北京:国防工业出版社, 2008:109-114.
LIU Zhi-ru.Thermal analyses for energetic materials[M].Beijing:National Defense Industry Press,2008:109-114.(in Chinese)
[14] Brill T B,Brush P J,Gray P,et al.Condensed phase chemistry of explosives and propellants at high temperature:HMX,RDX and BAMO and discussion[J].Philosophical Transactions of the Royal Society of London.Series A:Physical and Engineering Sciences,1992,339(1654):377-385.
[15] 傅献彩,沈文霞,姚天扬.物理化学:上册[M].北京:高等教育出版社,2005.
FU Xian-cai,SHEN Wen-xia,YAO Tian-yang.Physical chemistry:volume one[M].Beijing:Higher Education Press,2005. (in Chinese)
[16] 王伯羲,冯增国,杨荣杰.火药燃烧理论[M].北京:北京理工大学出版社,1997:105-108.
WANG Bo-xi,FENG Zeng-guo,YANG Rong-jie.Theory for gunpowder combustion[M].Beijing:Beijing Institude of Technology Press,1997:105-108.(in Chinese)
Preparation of HMX/Cu Composite Particles by Electroless Plating Method and their Thermal Decomposition Characteristics
XIONG Lang-lu,GUO Xiao-de,LI Feng-sheng
(National Special Super Powder Engineering Research Center,Nanjing University of Science and Technology, Nanjing 210094,Jiangsu,China)
HMX/Cu composite particles are prepared by the electroless plating method.The size,morphology and phase of particles are analyzed by SEM and XRD.And the DSC is applied to study their thermal decomposition characteristic.The results show that the composite particles coated with Cu of 80 nm in diameter have obvious catalysis effect on solid phase decomposition of HMX.The percentage of the prophase decomposition heat increases from 2.37%to 97.29%.On the other hand,the thermal decomposition peak moves to the low temperature of 35.53℃and the rate slows down.Especially,the thermal decomposition of HMX/Cu become to be very intense at the heating rate of 15℃/min.Compared with HMX,the apparent activation energy of HMX/Cu is decreased by 33.16 kJ/mol.It is advantageous to the thermal decomposition of nano HMX/Cu through adding a moderate amount of O2.Moreover,“Effect of spatial distribution”of catalyst is presented based on the analysis of nanometer Cu catalyst mechanism. Key words:ordnance science and technology;electroless plating;loaded catalyst;nanometer Cu;thermal decomposition;catalysis action
TJ55
:A
1000-1093(2014)01-0035-07
10.3969/j.issn.1000-1093.2014.01.005
2013-05-03
熊烺录(1986—),男,硕士研究生。E-mail:xiong_hlsm@163.com;
郭效德(1968—),男,副研究员,硕士生导师。E-mail:guoxiaodenj@sina.com

