妊娠晚期羊水过少胎膜与胎盘绒毛上皮DNA-RNA反应观察*
石凡华
(泰安市妇幼保健院,山东 泰安 271000)
羊水过少(oligohydramnios,OR)是胎儿在宫内生长环境不佳的指征之一,围生医学的迅猛发展及超声技术的不断提高,生存环境及生活节奏的变化,临床上羊水过少的诊断率及发生率明显增加[1]。对围产儿的不良影响日益受到产科工作者的重视。病因不明确,一般认为与胎儿畸形、胎盘功能异常及病理性妊娠如妊娠高血压、胎儿生长受限、过期妊娠等因素有关[2]。目前对晚发单纯OR的发生机理,尚缺乏有力的证据,而且对不同病理性妊娠的研究,多集中于胎盘,忽略了对孕晚期羊膜形态和功能的研究。本研究对羊膜和胎盘组织进行病理组织学及组织化学研究,目的是寻找在OR形成过程中的形态学证据。
1 材料和方法
1.1标本选择与分组 选择近年在泰山医学院附属医院产科和泰安市妇幼保健院产科足月分娩产妇,其中羊水过少15例(OR组),正常妊娠15例(对照组)。应用羊水指数(AFI)法,羊水量产前超声检测提示AFI≤8.0 cm,破膜时羊水量少于300 ml确定为羊水过少。两组产妇均为选择性剖宫产,并排除内科合并症及其他产科并发症,无药物服用史,无缩宫素引产史及母体脱水等因素。
1.2标本采集与处理 每例标本取羊膜1.5 cm×1.5 cm各两块;胎盘取中央和边缘部(距胎盘边缘约1 cm)1.0 cm×1.0 cm×全厚各两块。所取材料迅速用生理盐水冲洗,放入10%甲醛固定6~12 h后,前者修至约1.0 cm×1.0 cm,后者0.6 cm×0.6 cm×全厚,胎盘组织继续固定24 h。梯度酒精脱水,常规石蜡包埋,连续切片厚5 μm,隔5片取相邻2片(每例共取6片)分别进行常规(HE)染色和组织化学甲基绿-派洛宁(DNA- RNA)染色,光镜下观察。
1.3统计学处理 利用统计学软件SPSS 17.0对数据进行分析并比较组间差异,均数的比较采用两独立样本t检验的方法,组织化学反应强度的差异用完全随机设计样本比较的秩和检验。
2 结 果
DNA阳性反应物定位于细胞核呈绿色,RNA主要定位在细胞质,呈淡红色。
2.1羊膜
光镜下对照组和OR组5层结构清晰可辨,依次为上皮细胞层(羊膜细胞)、基膜、致密层、纤维母细胞层和海绵层,平均厚度约0.5 mm。由于前两层(羊膜细胞和基膜)与相邻层连接疏松,常易与深层分离(图1)。
对照组:羊膜细胞多呈立方形和低柱状,细胞界限清楚,排列整齐紧密,平均高度为5.5 μm,胞质呈均质状,HE染色弱嗜酸性;核椭圆形或圆形。DNA-RNA染色胞质呈淡红色,RNA阳性反应,多数细胞核DNA弱阳性反应,着色浅淡(图1)。
OR组:羊膜细胞形态差别较大,从扁平形至宽大的高柱状不等,以高低不同的柱状为主,平均高度约为8.5 μm。胞质呈泡沫状,甚至大量空泡形成,核相对较小,其中2例上皮鳞状化生(图2),2例羊膜表层纤维化,羊膜细胞胞质极少,胞核固缩。DNA-RNA染色羊膜细胞胞质RNA(派洛宁)着色浅淡,呈弱阳性;而核内DNA(甲基绿)着色浓深,强阳性者居多。参照David及岳淑红等[3]的分级标准,光镜下对羊膜和胎盘绒毛DNA-RNA染色反应产物强度划分为5级,分别用0、+、++、+++、++++来表示。0级阴性或分辨不清;Ⅰ级有反应但很弱,染色很浅;Ⅱ级反应中等,介于1和3级之间;Ⅲ级反应较强,染色深;Ⅳ级反应最强,染色深重[4]。
对两组DNA染色强阳性细胞计数,每张切片高倍镜下(400倍)选取5个不重复视野,计数羊膜细胞总数和强阳性细胞数,最后计算平均百分数,结果如表1。
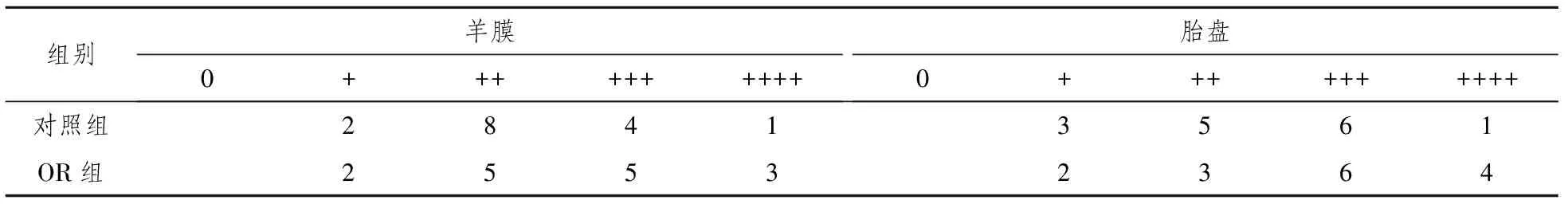
表1 羊膜和胎盘滋养细胞DNA-RNA组织化学反应强度比较
注:秩和检验,羊膜:对照组与RO组比较P<0.05,胎盘两组比较P<0.01。
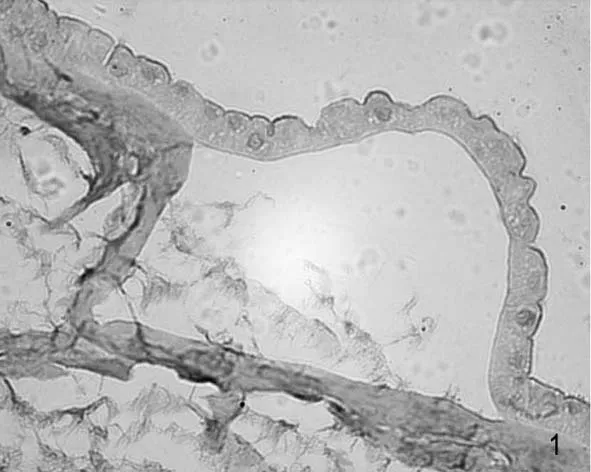
图1 对照组羊膜,细胞核DNA着色浅淡。×400

图2 OR组羊膜,上皮复层化生,细胞核DNA深染。×400
2.2胎盘
在两种染色的标本上,胎盘中央及边缘部结构无明显差别,故不再分别描述。绒毛多被横断,绒毛壁上皮细胞滋养层较少不连续,以合体滋养细胞为主。
对照组:绒毛上皮合体细胞界限不清,合胞体结节(syncytail knot) 较多、深染。DNA-RNA染色滋养层细胞核以弱阳性者为主,胞质呈阳性反应(图3)。
OR组:绒毛间隙与绒毛结构与对照组相似,合体结节比对照组明显增多、深染。绒毛中轴血管扩张,间质水肿。滋养细胞,DNA-RNA染色滋养层细胞核强阳性者比对照组明显增多,并可见较多核碎解现象,高度深染及核碎解者,符合凋亡细胞的形态学特征,多集中在合体结节处,胞质呈RNA阳性反应(图4),高倍镜下对两组凋亡细胞进行计数,计数方法同羊膜,结果见表2。
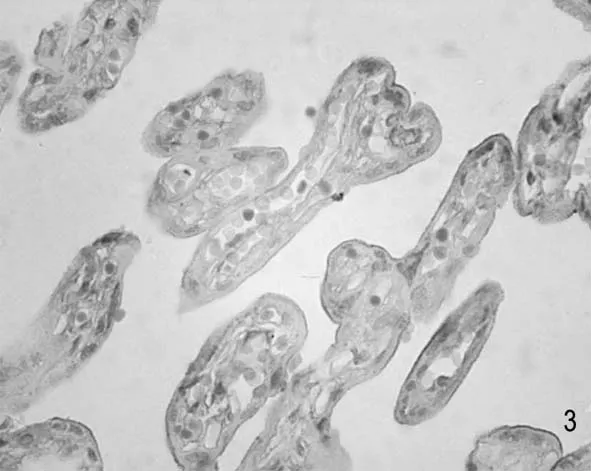
图3 对照组胎盘绒毛横断面,滋养层细胞形状,多数细胞核DNA着色浅淡。×400
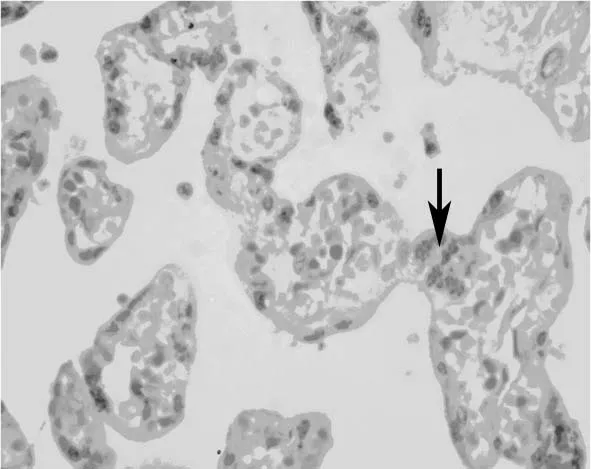
图4 OR组胎盘绒毛,细胞核DNA深染,合体结节(箭头)。×400
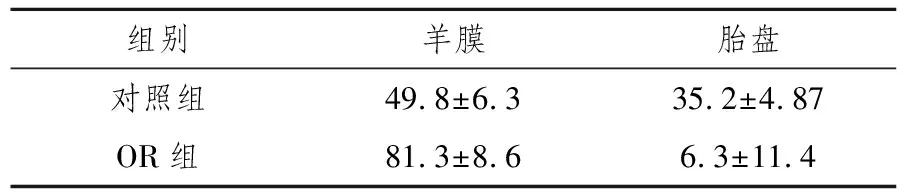
组别羊膜胎盘对照组OR组49.8±6.381.3±8.635.2±4.876.3±11.4
注:两组比较,P<0.01。
3 讨 论
虽然目前有多种检测细胞凋亡的方法[4],但是尚缺乏简便易行的形态学检测方法。DNA-RNA染色是对比显示DNA和RNA分布的经典组织化学方法。甲基绿多与DNA特异结合的活性染料,显示蓝绿色,DNA聚合程度越高着色越深;派洛宁则多选择性的与RNA结合显示红色。根据凋亡细胞典型的形态特征,如染色质浓缩、边缘化,核膜裂解、染色质分割成块状及凋亡小体形成等,镜下比较容易观察。恰恰聚合程度高的DNA是光镜下凝聚的异染色质,碎解的颗粒状染色质是异染色质遭受损伤、破坏的结果。染色质的凝集与断裂是细胞凋亡过程中的一个重要变化。根据此原理对显示羊膜细胞和胎盘滋养细胞的活性,并以此推断羊膜和胎盘的功能状态,有很好的应用价值。胎盘自妊娠37周以后开始有老化改变并逐渐加重,胎盘老化改变主要表现为胎盘生长减慢甚至停止,胎盘表面、绒毛板和绒毛间隙出现纤维蛋白沉着和钙化灶,绒毛上皮和血管基底膜增厚,常伴有胎盘功能减退[5-6]。本实验结果显示,对照组羊膜和胎盘滋养细胞核甲基绿染色弱阳性者为多,说明细胞功能尚可抑或活跃;而实验组则强阳性者为多(凋亡细胞)(P<0.01),DNA-RNA组织化学反应强度比较(P<0.01)。细胞凋亡增加可能是胎盘提前老化的发病机制之一,34周前即已开始[7-8]。妊娠终、末期应利用其它手段严密观察胎膜、胎盘及胎儿的发育情况,以便尽早发现问题。
至于对照组羊膜细胞及胎盘滋养层细胞出现的一定数量的凋亡,是基因控制的正常妊娠的生理现象,胎盘通过绒毛滋养细胞及蜕膜细胞的凋亡与增殖来共同调节胎盘的发育和成熟,是妊娠过程的必然,可能与分娩的发动有关。
本实验OR组羊膜细胞所显示的反应DNA-RNA反应与胎盘绒毛滋养层细胞一致性,进一步说明过多的羊膜细胞凋亡对羊膜功能的影响,羊膜细胞过度凋亡参与OR的形成过程。结合羊膜和胎盘的诸多形态学变化,说明羊膜、尤其是胎盘老化,组织结构受损,有效功能组织结构减少,导致脐血流减少,胎盘的气体交换及物质运输、合成能力降低,是造成羊水过少的病理学基础。
[1] 谢惠,尹春艳.羊水过少的病因学分析[J].医学综述,2013(19):884-886.
[2] Ohana O, Holcberg G, Sergienko R, et al. Risk factors for intrauterine fetal death (1988-2009)[J].J Matern Fetal Neonatal Med, 2011, 24(9):1079-1083.
[3] 岳淑芬,赵紫薇,何金鑫. 孕产妇孕期锌缺乏对胎盘碱性磷酸酶的影响[J].中国优生与遗传杂志,2005,13(6):29-30.
[4] 杨连君, 司晓辉, 王文亮,等.六种染色后光镜观察法检测肝癌细胞凋亡[J]. 实用医技杂志, 2006,13 (1): 8-10.
[5] Levis RM,Cleal JK, Hanson MA. Review: Placenta, evolution and lifelong health[J]. Placenta,2012,33: 828-832.
[6] 丁丽, 王冬梅. 病理妊娠胎盘结构研究的新进展[J].医学综述,2003,9(6): 377-379.
[8] Chhabra S,Daragan R,Bawaskar R.Oligohydramnios:a potential marker for serious obstetric complications[J].J Obstet Gynaecol,2007,27(7): 680-683.
[9] Zhang LY, Yu YH, Hu ML. Association between ultrasonographic signs of placental premature aging and pregnancy outcome[J]. 2005,25(3):318-320.

