27例肝肾综合征临床分析
廖舒 陈婧 康永慧
1 成都市核工业四一六医院ICU 四川成都 610051
2 成都中医药大学感染科 四川成都 611130
3 什邡市中医院普通内科 四川什邡 618400
27例肝肾综合征临床分析
廖舒1陈婧2康永慧3
1 成都市核工业四一六医院ICU 四川成都 610051
2 成都中医药大学感染科 四川成都 611130
3 什邡市中医院普通内科 四川什邡 618400
目的:探讨肝肾综合征的基础疾病、诱因、临床特征、预防及治疗方法。方法:总结2008年4月~2013年4月来我院收治的肝肾综合征的临床资料,通过回顾性分析和统计学方法,分析其基础疾病、诱因、肝肾功,尿量变化及生存率等。结果:纳入患者中,8例Ⅰ型HRS均院内死亡;18例Ⅱ型HRS中,4例好转出院;1例未予分型患者院内死亡。结论:肝肾综合征预后差,一旦发生,死亡率高,积极预防肝肾综合征的各种诱因,提高对肝肾综合征早期诊断对肝肾综合征的诊治有重要价值。
肝肾综合征;肝硬化;临床分析
肝肾综合征(hepatorenal syndrome,HRS)是在严重肝病基础上发生的急性功能性肾衰竭,以少尿或无尿、低钠血症、血肌酐及尿素氮升高为主要临床表现,目前尚无特效治疗措施,预后差,病死率高。现本文对2008年4月-2013年4月本院收治的27肝肾综合征的临床资料进行回顾性分析,具体分析如下:
1 资料和方法
1.1 一般资料
选择我院2008年4月~2013年4月收治的HRS患者共27例,其中HRSⅠ型8例,Ⅱ型18例,其中1例入院时已发生HRS,因缺乏既往生化检查,故未予分型。男17例,女10例,年龄23~74(平均50.7)岁,其中<30岁2例(7.4%),其中30~39岁4例(14.8%),40~49岁7例( 27.6%),50~59岁5例(18.5%),60~69岁7例(27.6%),70以上2例(7.4%)。
1.2 诊断依据
纳入患者均符合2010年欧洲肝病学会指南推荐HRS诊断标准[1]:肝硬化腹水患者,血肌酐≥133μmol/L并排除其他肾实质疾病及休克等原因便可诊断HRS。特别是在住院期间动态监测血清肌酐有助于早期诊断HRS。1型HRS为一种急进性肾功能不全,2周内血肌酐增加超过原水平2倍或血肌酐水平>226μmol/L(2.5 mg/dl)。Ⅱ型HRS是以稳定或进展缓慢的肾功能受损为表现。
1.3 治疗方法
HRS目前尚无特效疗法,在积极治疗原发肝病,改善肝功能前提下,密切监测HRS患者小便量、血肌酐、电解质等指标变化,早诊断,早治疗。积极防治HRS各种诱因,如快速控制消化道出血、感染;避免使用肾毒性药物、强烈利尿、大量放腹水等;监测出入量,纠正水、电解质及酸碱平衡紊乱;根据情况输入人血白蛋白、血浆或浓缩腹水回输,纠正低血容量,改善肾脏血流,在扩容基础上应用适当利尿药。还可以选择特利加压素、奥曲肽、多巴胺等血管活性药物治疗。
1.4 观察指标
分析患者的基础疾病及诱因;Child-Pugh改良肝功能计分分级[2];比较Ⅰ型、Ⅱ型肝肾综合征发病前后的血钠、肌酐、胆红素、尿量变化及其住院天数、生存率。
1.5 统计学处理
采用SPSS 16.0软件进行统计学处理。计量资料采用t检验,计数资料采用卡方检验。P<0.05为差异有统计学意义。
2 结果
2.1 原发疾病及诱因
在纳入27例HRS患者中,原发疾病肝硬化24例(77.8%),其中乙肝肝硬化18例(75%),丙肝肝硬化1例(4.2%),酒精性肝硬化2例(8.3%),胆汁性肝硬化1例(4.2%),隐源性肝硬化2例(8.3%);肝硬化合并原发性肝癌2例(7.4%);急性重型肝炎1例(3.7%)。I型、Ⅱ型HRS的发生多伴有诱因,部分病人多种诱因可同时存在,见表1。
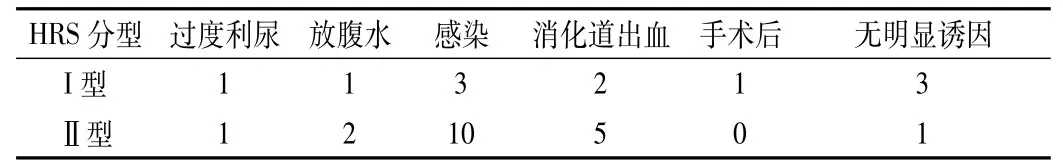
表1 I型与Ⅱ型HRS诱因分析
2.2 肝功能分级
27例HRS患者中,Child-Pugh B级2例(7.4%),Child-Pugh
C级25例(92.6%),无A级。
2.3 生化指标
Ⅰ型及Ⅱ型HRS患者血肌酐、血钠、尿量、总胆红素水平前后变化比较见表2。
表2 HRS血肌酐、血钠、尿量、胆红素变化(±s)
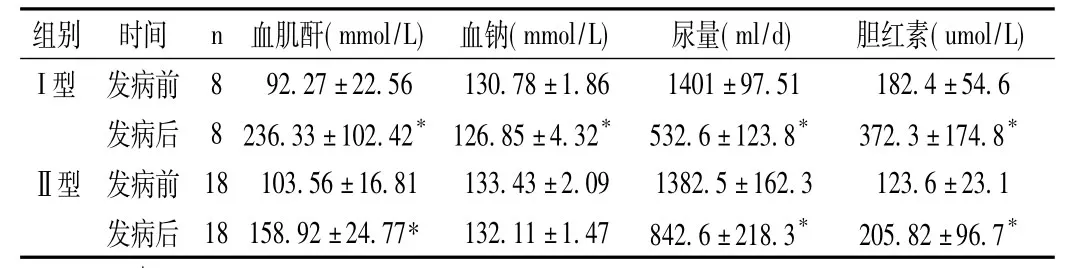
表2 HRS血肌酐、血钠、尿量、胆红素变化(±s)
注:*Ⅱ型、I型发病前后比较及发病后Ⅱ型与I型比较P<0.05
组别时间n血肌酐(mmol/L)血钠(mmol/L)尿量(ml/d)胆红素(umol/L) 54.6发病后8 236.33±102.42*126.85±4.32*532.6±123.8*372.3±174.8*Ⅱ型发病前18 103.56±16.81 133.43±2.09 1382.5±162.3 123.6±23.1发病后18 158.92±24.77*132.11±1.47 842.6±218.3*205.82±96.7 I型发病前8 92.27±22.56 130.78±1.86 1401±97.51 182.4± *
2.4 预后
I型8例,生存率为0,平均生存时间为7.8d;Ⅱ型18例,其中4例经药物治疗后好转,其余死亡,死亡患者平均生存时间为15.6d;1例未予分型患者死亡,生存时间4天;总死亡率为85.2%。
3 讨论
HRS是在严重肝病基础上发生的急性功能性肾衰竭,其主要病理生理特点是内脏小动脉明显扩张,全身动脉低血压,从而导致肾脏血管强烈收缩,从而导致肾小球滤过率下降[3]。尽管肝肾综合征是一种功能性、可逆性的肾功能损伤,但一旦发生,进行性发展,治疗困难,预后差,存活率很低,是重症肝病最常见的死亡原因之一。
从原发疾病及其诱因来看,纳入27例HRS患者原发疾病绝大部分为肝硬化,其中以乙肝肝硬化为主,这与我国肝硬化病因分布一致,和国内同类报道结果相一致[4]。在27例HRS患者中,诱因以感染、消化道出血、放腹水为主,其中感染占据着重要地位。感染包括自发性腹膜炎、肠道感染、肺部感染等,肝硬化腹水患者中肠道细菌移位造成的肠源性腹腔细菌性感染是诱发肝肾综合征的重要因素。同时患者的免疫力异常激活以及机体高动力循环状态也是肝肾综合征发病的关键因素[5]。且部分患者多种诱因同时存在,故使得肝肾综合征的治疗相当困难。
纳入27例HRS患者中,Child-Pugh B级2例(7.4%),Child-Pugh C级25例(92.6%),无A级。这说明肝功能与HRS发生有紧密联系。
纳入HRS患者的治疗主要包括保肝,抗炎,止血,利尿,纠正电解质紊乱,补充热量,补充氨基酸,血浆置换,血液透析,白蛋白扩容治疗等,部分患者给予多巴胺或特利加压素联合白蛋白治疗,但总体疗效不佳。在治疗的过程中我们注意到,需要重视以下几个方面:应积极处理重症肝病出现的消化道出血、自发性腹膜炎、电解质紊乱等并发症,控制病情进一步恶化,并动态监测肾功能变化情况;避免使用肾毒性药物或主要从肾脏排泄的药物,以免加重肾功能损害上,诱发或加重肝肾综合征;补充血容量,特别是胶体液,可预防性使用多巴胺及ACEI,改善肾脏微循环,使肾小球滤过率增加;④控制感染,防止内毒素的生成和吸收,防止内毒素强烈收缩血管导致肾血流量减少;⑤促进肝细胞再生与修复,改善肝细胞功能;⑥各种支持治疗;⑦肝移植是治疗HRS具有确切疗效的方法之一,如条件允许,可进行肝移植。
另外,在肝肾综合征的诊断过程中,需要注意两点:目前临床上常通过血肌酐和尿素氮来评价肾功能。在大部分患者中,血肌酐及尿素氮升高对诊断肾脏功能不全有较高的特异性与敏感性,但对于重症肝病患者,其敏感性就受到一定的影响。一方面,肝功能受损导致内源性肌酐生成减少,故少数肾功能已较差的患者血肌酐水平趋于正常或仅轻度升高;另一方面,肝病患者肝脏合成尿素能力下降,且从饮食中摄取的蛋白质下降,故尿素氮含量较低,故在诊断肝肾综合征时需将以上考虑在内,密切监测肾功能的动态变化,并结合早期肾功能指标、胱抑素-C、同型半胱氨酸等指标;诊断肝肾综合征时,需排除器质性肾病及肾前性肾衰竭。
本研究资料表明,HRS重在预防,避免强烈利尿、单纯大量放腹水及使用肾毒性药物、积极控制感染等。HRS的预后差,早期诊断HRS对其预后有重要意义。目前,肝移植仍为治疗终末期肝病伴HRS最有效的手段。
参考资料
[1]EASL clinical practice guidelines on themanagement of ascites,spontaneous:bacterial peritonitis,and hepatorenal syndrome in cirrhosis.European Association for the Study of the Liver.JHepatol.2010,3(3): 397~417..
[2]Form an LM,Lucey MR.Pred icting the prognos is of chronic liver disease:an evolution from Child to MELD[J].H epatology,2001,33( 2):473-475.
[3]贾继东.肝肾综合征的发病机制[J].中华肝脏病杂志,2003,11 (10):626.
[4]陈胜鹏,何卫平,胡瑾华,等.肝肾综合征329例预后分析[J].传染病信息,2010,23(2).
[5]袁春,叶进.肝硬化和肠道细菌移位[J].临床消化病杂志,2008,20(2):121.
R575
B
1009-6019(2014)10-0234-02

