高压CO2对水酶法乳状液破乳影响的研究
韩宗元 江连洲 李 杨 齐宝坤 王中江 王胜男
(东北农业大学食品学院1,哈尔滨 150030)
(沈阳工学院生命工程学院2,抚顺 150030)
在水酶法提取大豆油脂过程中,乳状液破乳是十分关键的步骤,破乳越彻底大豆油的提取率越高。化学破乳主要是加破乳剂[1]。物理破乳包括静电场、微波、冷冻解冻、超声波破乳[2-5]。生物破乳主要是酶法破乳[6]。Nastaran等[1]提出吐温试剂作为高分子量化学破乳剂可以提高乳状液破乳率。Kuo等[7]指出微波产生的热量可以更快地去除水分,破坏电解质平衡,破乳率可达到90%。Wu等[6]利用不同酶对大豆乳状液进行破乳,比较各种酶的破乳效果。水酶法是一种绿色、环保的提油工艺,可以避免油脂提取过程中使用有机溶剂和有毒有害化学试剂。
高压CO2作为一种新兴的物理方法主要作用于蛋白沉降[8]。Nawal等[8]利用高压 CO2沉降大豆蛋白,使pH值降至3~5以加快蛋白沉降从而释放油脂[6]。Nael等[9]证明 CO2可以对油包水型乳状液进行破乳,增加CO2的压力和停留时间可以提高沉降速率,加速破乳过程。因此,高压CO2可以通过沉降乳状液中蛋白有效地进行破乳,而且作用时间短,效果明显。本研究目的:1)通过设计响应面优化试验对高压CO2压力、温度、处理时间、浓度进行优化,得到最优结果,将其应用到油脂破乳过程中,提高油脂提取率;2)通过透射电镜观察高压CO2破乳过程,掌握破乳前后乳状液变化情况,有助于高压CO2破乳参数的优化。
1 材料与方法
1.1 材料与仪器
大豆:吉林风正食品有限公司;Protex6L碱性蛋白酶:诺维信公司;LDZ5-2型台式低速离心机:上海安亭科学仪器厂;pHS-3C型酸度计:上海雷磁仪器厂;CO2(纯度99.5%):北京医疗设备二厂;耐高压不锈钢锅(1 200 mL)、数显温度调节计、数显压力调节计:上海一恒科学仪器有限公司;数显流量调节计:常州国华电器有限公司。
1.2 方法
1.2.1 高压CO2破乳
大豆压片粉碎后过60目筛,将过筛后物料与水混合得到混合液,向混合液中加入Protex6L碱性蛋白酶进行酶解,酶解后5 000 r/min离心分离得到游离油、乳状液、水解液与残渣;提取乳状液与水解液并放入高压CO2耐高压不锈钢锅中,通入一定量CO2进行破乳,利用温度、压力和流量调节计控制参数。破乳后,在4 500 r/min下离心分离15 min后得到大豆油脂。
1.2.2 单因素试验
高压CO2温度150℃、浓度0.5 g/cm3、作用时间21 s、压力14 MPa。保证3个因素不变,只改变1个因素,通过研究CO2压力为8~20 MPa,蒸汽温度为120~190℃,蒸汽处理时间12~30 s,CO2浓度0.1~0.8 g/cm3确定各因素对破乳率的影响。
1.2.3 响应面优化试验
选取高压CO2温度、浓度、作用时间、压力4个因素为自变量,以破乳率为响应值,根据中心组合设计原理,设计响应面分析试验,见表1。
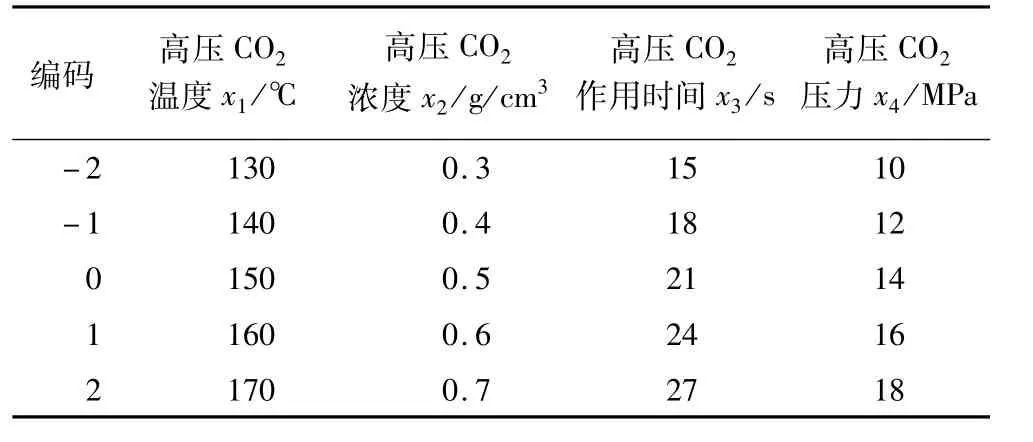
表1 因素水平编码表
1.2.4 破乳率的测定
检测方法及计算参考文献[6]。
破乳率=破乳后油的质量(g)/乳状液中油的质量(g)×100%
1.2.5 透射电镜
前固定→漂洗→后固定→漂洗→50%乙醇脱水→70%乙醇脱水→90%乙醇脱水→100%乙醇脱水→100%乙醇和100%丙酮(1∶1)脱水→100%丙酮脱水→纯丙酮和包埋液浸透→包埋→聚合→修块→超薄切片机切片→染色→观察、拍片。
1.3 数据处理
所有试验数据均为“平均值±标准差”,n=3。采用SAS9.18统计分析软件对试验数据进行分析。
2 结果与讨论
2.1 高压CO2破乳单因素条件对破乳率的影响
2.1.1 高压CO2温度对破乳率的影响
由图1可以看出,高压CO2温度高于130℃时破乳率明显增加,但当温度超过160℃时,破乳率开始大幅降低,可见温度对破乳率影响很大,因为CO2在130~160℃时,易溶于水,使pH降低,达到等电点,从而加快蛋白沉降,超过160℃时,CO2溶解度降低,导致蛋白沉降减慢使破乳率降低。因此蒸汽温度选择130~170℃。
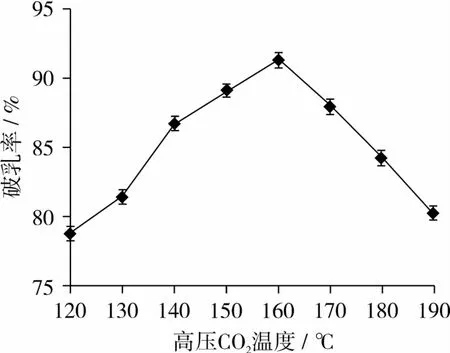
图1 高压CO2温度对破乳率的影响
2.1.2 高压CO2浓度对破乳率的影响
由图2可以看出,浓度在0.5 g/cm3附近破乳率有最大值出现,浓度过高不利于 CO2溶解,导致蛋白沉降减慢,从而影响破乳率,所以选择浓度0.3~0.7 g/cm3。
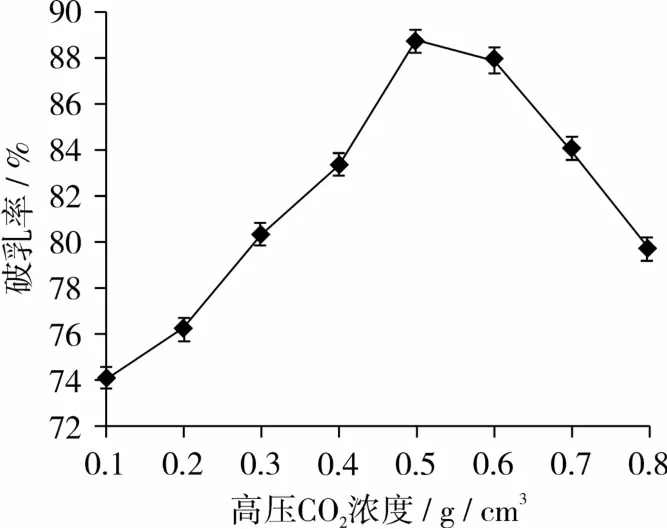
图2 高压CO2浓度对破乳率的影响
2.1.3 高压CO2处理时间对破乳率的影响
由图3可以看出,当处理时间大于24 s时破乳率明显降低,因为通入过多CO2,导致CO2析出,降低蛋白沉降速率,所以在响应面试验设计中处理时间选择15~27 s。

图3 高压CO2作用时间对破乳率的影响
2.1.4 高压CO2压力对破乳率的影响
由图4可以看出,当压力为14 MPa时破乳率达到最大,因为溶解度和压力有关,压力过大使CO2溶解度降低,所以在响应面试验设计中压力选择10~18 MPa。
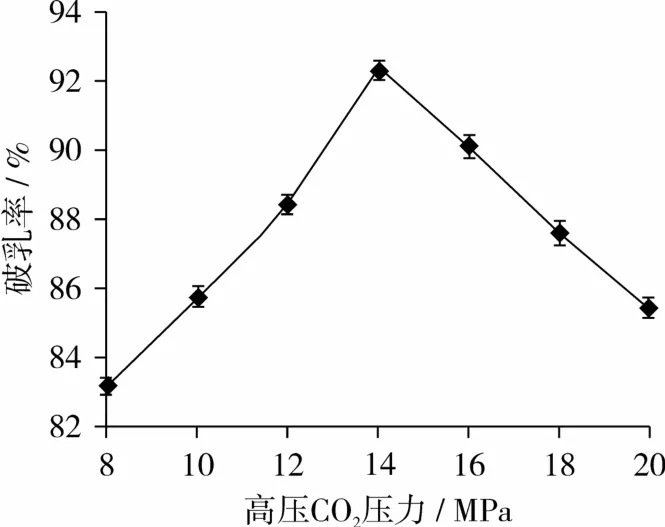
图4 高压CO2压力对破乳率的影响
2.2 高压CO2破乳条件的优化
应用响应面优化法进行过程优化,以x1、x2、x3、x4为自变量,以破乳率为响应值y,响应面试验方案及结果见表2。试验号1~24为析因试验,25~36为中心试验,用以估计试验误差。

表2 响应面试验方案及试验结果
2.3 响应面试验结果分析
通过统计分析软件SAS9.18进行数据分析,建立二次响应面回归模型。
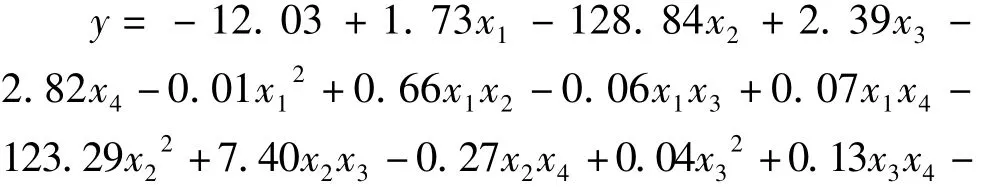
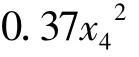
回归分析与方差分析结果见表3,交互项显著的响应面分析见图5~图9。
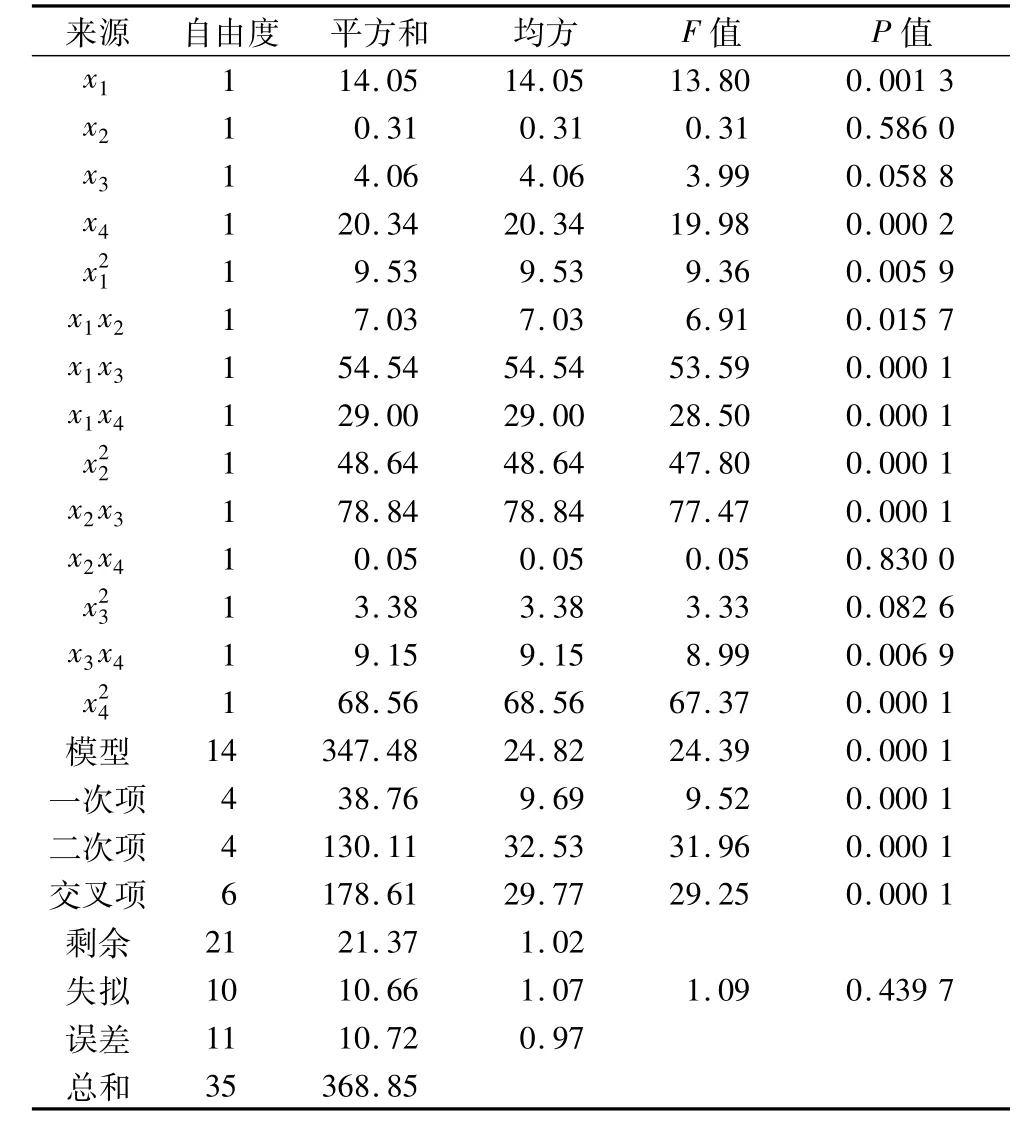
表3 回归与方差分析结果
由表3可知,方程因变量与自变量之间的线性关系明显,该模型回归显著(P<0.000 1),失拟项不显著,并且该模型,说明该模型与试验拟合良好,自变量与响应值之间线性关系显著,可以用于该反应的理论推测。由F检验可以得到因子贡献率为:x4>x1>x3>x2,即高压CO2压力>高压CO2温度>高压CO2作用时间>高压CO2浓度。
当固定2个因素的零水平,图5~图9表示另外两个显著交互项的响应面和等高线。显著交互项可从表3获得,分别为:高压CO2的温度和浓度,高压CO2的温度和作用时间,高压CO2的温度和压力,高压CO2的浓度和时间,高压CO2的压力和时间。图5表明:当把x3和x4调节到零水平时,高压CO2的温度和浓度对破乳率影响的变化趋势都是先增加后减小。图6表示当把x2和x4调节到零水平,高压CO2的温度和作用时间对破乳率影响的变化趋势也都是先增加后减小。图7表明当把x2和x3调节到零水平,高压CO2的温度和压力对破乳率影响的变化趋势都是先保持稳定后减小。图8表示当把x1和x4调节到零水平,高压CO2的浓度和时间对破乳率影响的变化趋势是先增加后减小。图9表示当把x1和x2调节到零水平时,高压CO2的压力和时间对破乳率影响的变化趋势逐渐减小。
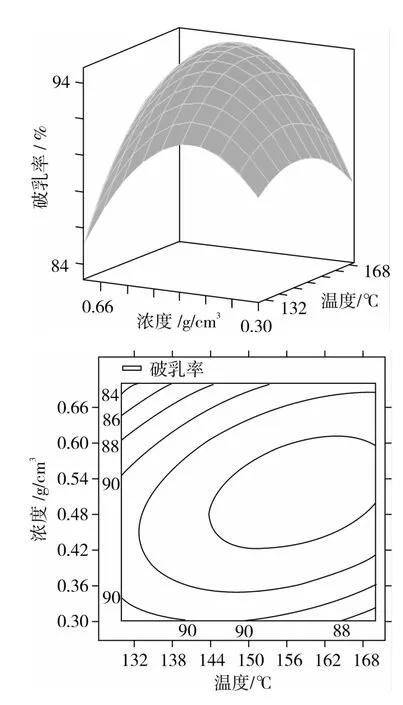
图5 高压CO2的温度和浓度的交互作用对破乳率的影响

图6 高压CO2的温度和作用时间的交互作用对破乳率的影响
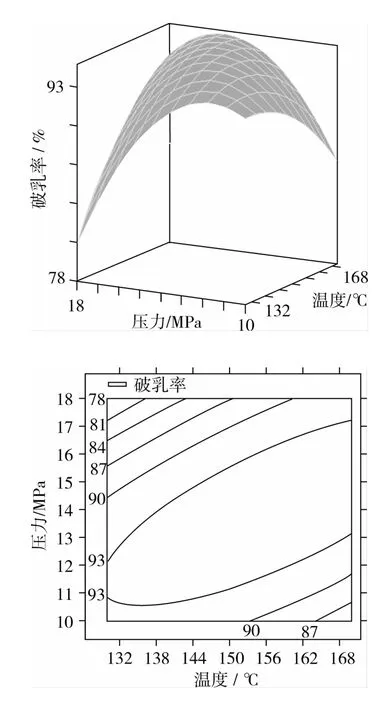
图7 高压CO2的温度和压力的交互作用对破乳率的影响
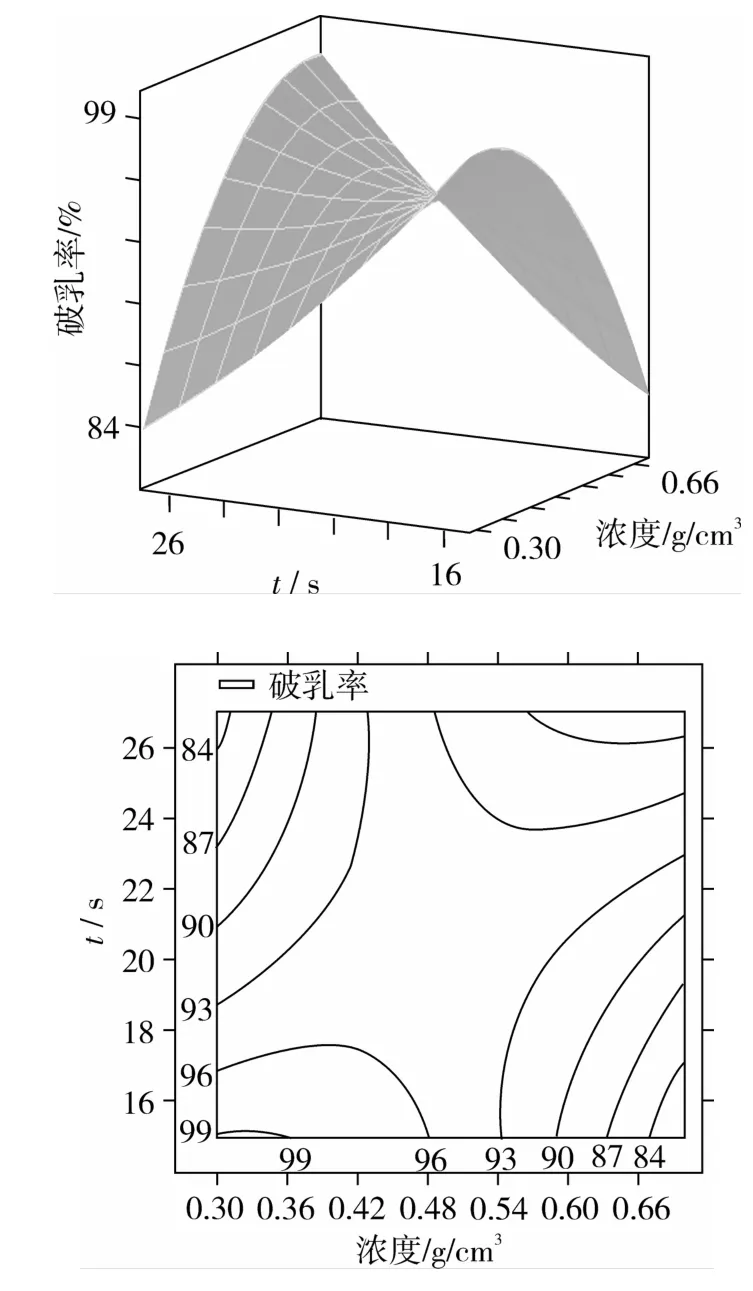
图8 高压CO2的浓度和时间的交互作用对破乳率的影响
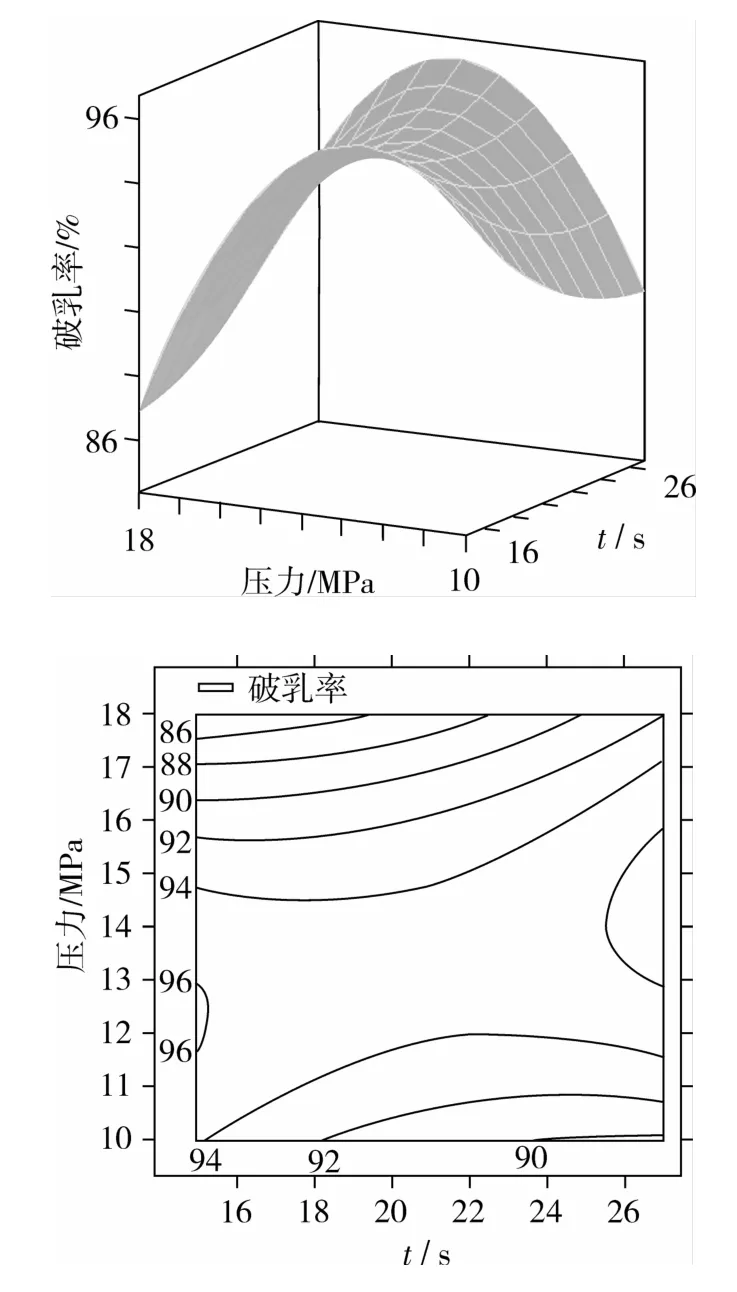
图9 高压CO2的压力和时间的交互作用对破乳率的影响
应用响应面寻优分析方法对回归模型进行分析,寻找最优响应结果:高压CO2压力13.96 MPa,高压CO2温度155.64℃,高压CO2处理时间21.46 s,CO2浓度0.53 g/cm3,响应面最优值(94.88±0.30)%。
2.4 验证试验与对比试验
在响应面分析法求得的最佳条件下,进行3次平行试验,破乳率的平均值为95.06%。破乳率预测值为(94.88±0.30)%,说明响应值的试验值与回归方程预测值吻合良好。
2.5 透射电镜分析
Wu等[6]研究指出水酶法提取大豆油脂过程中,破乳是关键步骤,而大豆乳状液中含有大豆蛋白,是保持乳状液稳定的重要成分,采用不同蛋白酶对其乳状液破乳,使油脂从蛋白包裹中释放出来。通过透射电镜观察,乳状液内部油脂被大量蛋白包围,无法聚合在一起释放出来,所以破乳是油脂释放的前提。图10a为破乳前乳状液中油脂和蛋白分布情况,可发现酶解后细胞壁被破坏,蛋白质大量聚集在一起,油滴被镶嵌在蛋白中,使油滴很难释放出来;图10b为乳状液经过高压CO2破乳后的分布情况,包裹油脂的蛋白膜大部分破碎、变小,而油体聚在一起形成油滴,小油滴变大,从包裹的蛋白中释放出来,并且聚集在一起[3]。通过透射电镜观察可以发现高压CO2可以破坏乳状液的稳定体系并有效地使油脂从乳状液中释放出来,进而解决了乳状液破乳的难题,最终提高了水酶法提取大豆油脂的提取率。

图10 乳状液破乳前后透射电镜对乳状液结构分析
2.6 物理破乳方法比较
通过比较表4中4种物理破乳方法对破乳率的作用,得到以下结果:高压CO2>微波>超声波>冷冻解冻,说明高压CO2破乳法比其他物理破乳法的破乳率更高,作用时间短,可以更好地用于水酶法破乳,提高大豆油脂提取率[3-5]。

表4 4种不同破乳方法对破乳率影响
3 结论
本试验利用响应面分析方法对高压CO2破乳工艺参数进行了优化,得到最优参数条件:高压CO2压力为13.96 MPa,高压CO2温度为155.64℃,高压CO2处理时间 21.46 s,CO2浓度 0.53 g/cm3,响应面最优值(94.88±0.30)%。采用透射电镜,观察破乳前后乳状液中油和蛋白的分布情况,发现高压CO2可以使蛋白质沉降,进而使乳状液稳定结构瓦解,油脂正常释放,解决了水酶法提取大豆油脂的难题,有利于水酶法提取大豆油脂的工业化生产。
[1]Nastaran H R,Alireza B,Esmaiel Setal.Tweens demulsification effects on heavy crude oil/water emulsion[J].Arabian Journal of Chemistry,2011,10:1016-1022
[2]Tsuneki I.Electrical demulsification of oil-in-water emulsion[J].Colloids and Surfaces,2007,302:581-586
[3]Rafael M P,Ricardo CC,Benjamín C etal.Demulsification of heavy crude oil-in-water emulsions:A comparative study between microwave and thermal heating[J].Fuel,2013,113:407-414
[4]Lin Chang,He Gaohong,Li Xiangcun,et al.Freeze/thaw induced demulsification of water-in-oil emulsions with loosely packed droplets[J].Separation and Purification Technology,2007,56:175-183
[5]Susumu N,Shunsuke K,Hideaki T.Quantitative approach to ultrasonic emulsion separation[J].Ultrasonics Sonochemistry,2009,16:145-149
[6]Wu J,Johnson L A,Jung S.Demulsification of oil-rich emulsion from enzyme-assisted aqueous extraction of extruded soybean flakes[J].Bioresource Technology,2009,100:527-533
[7]Kuo Chin-Hsing,Lee Chon-Lin.Treatment of oil/water emulsions using seawater-assisted microwave irradiation[J].Separation and Purification Technology,2010,74:288-293
[8]Nawal K,Hossain M M,Farid M M.Precipitation of food protein using high pressure carbon dioxide[J].Journal of Food Engineering,2007,79:1214-1220
[9]Nael N Z,Ruben G C,Peter K K.A novel process for demulsification ofwater-in-crude oil emulsions by dense carbon dioxide[J].Industrial and Engineering Chemistry Research,2003,42:6661-6672.

