氯离子对典型不锈钢材料腐蚀的EIS分析*
王 磊 胡 军 郑茂盛 余历军
(西北大学化工学院)
电化学阻抗谱(EIS)方法是一种以小振幅的正弦波电位为扰动信号的电化学测量方法,相比其他常规电化学方法,EIS会得到更多关于腐蚀动力学和电极界面结构的信息。
对腐蚀体系的电化学阻抗谱研究由来已久,并已取得了丰硕成果。安闻讯等研究了低合金钢腐蚀的电化学阻抗谱,认为在浸泡初期腐蚀受阳极活化过程的控制,随着腐蚀的加剧,电极表面形成由金属表面的锈层和附着腐蚀产物构成的致密腐蚀产物层,影响电极过程。Shim 等研究了铜在水中的腐蚀行为,通过电化学阻抗谱的分析表明电荷转移阻力很大,且随着浸泡时间的延长电荷转移阻力快速增大。Betova I等对Alloy 690和316L的动力学过程进行了分析,并且得到了氧化膜转换过程的一些关键参数[1,2]。Li X H等利用EIS 分析了温度和压力对Alloy 690腐蚀动力学行为的影响规律[3]。Huang J B等分析了在高温水环境下,溶液的酸碱性对氧化膜电子结构的影响[4]。潘旭东和王向明简要论述了不锈钢腐蚀的机理和形态[5]。安洋研究了工业循环冷却水中氯离子等重要离子对不锈钢点蚀行为的影响[6]。解群等研究了阳离子对316L不锈钢钝化膜耐蚀性能的影响[7]。李劲等详细介绍了交流阻抗技术在复杂组织晶间腐蚀敏感性评价中的应用[8]。秦丽雁尝试采用电化学阻抗技术检测晶间腐蚀,初步分析了晶间腐蚀的电化学等效电路[9]。Hu J等利用EIS实验,分析了在钝态、亚稳态和稳态情况下阻抗谱的特征,归纳了氧化膜随时间损伤的演化过程,并利用量子力学的相关知识解释腐蚀过程中的动力学曲线[10]。这些研究对腐蚀机理的微观理解尤其是腐蚀过程中氧化膜特性的转变都有举足轻重的意义。氯离子是影响可钝化金属腐蚀的关键因素,任爱等利用微观观测研究表明溶液中的Cl-能够影响腐蚀产物膜的结构,当溶液中不含有Cl-时,腐蚀产物膜为双层结构,外层腐蚀产物为颗粒状,当溶液中含有Cl-时,腐蚀产物膜具有单层结构[11]。但关于氯离子对腐蚀过程中电化学阻抗谱的变化规律研究并不多,Li X H等探讨了在不同温度和不同压力下的电化学阻抗谱的变化规律[3]。
笔者利用电化学阻抗谱法研究Alloy 600、Alloy 690和X80 3种金属在不同浓度的KCl溶液中的腐蚀行为,验证关于氯离子对腐蚀影响的机理,探讨含氯离子腐蚀过程中的阻抗谱特性。
1 电化学阻抗谱实验设计
实验材料选用耐腐蚀性较好的Alloy 690、Alloy 600和X80,3种材料的化学成分见表1。
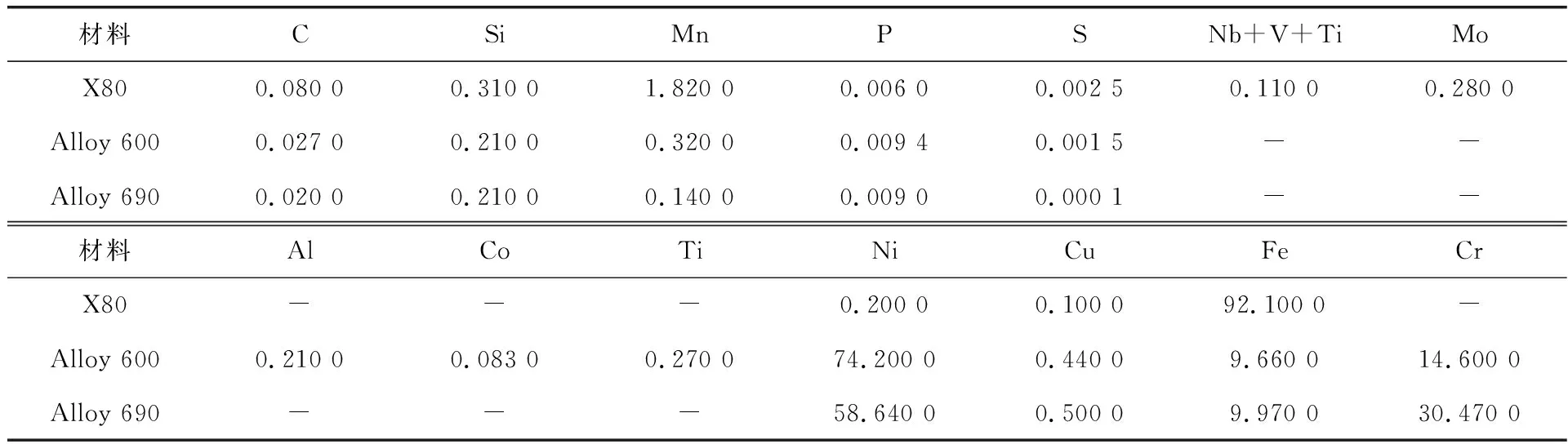
表1 Alloy 690、Alloy 600和X80的化学成分
用线切割机将材料加工为10mm×10mm×10mm的立方体,将导线和样品在一个面上点焊连接起来,留一个面作为测试表面,其余面用环氧树脂封装。等环氧树脂固化完全后,把测试表面依次用粒度为840.0、24.0、12.0、6.5μm的砂纸打磨,然后用抛光机抛光,用蒸馏水冲洗干净,接着用烘干机烘干待用。
KCl溶液是用工业纯试剂与蒸馏水配置而成,实验温度为25℃,测试采用Parstat2263电化学测试系统。测试按照经典三电极体系设计,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极。交流阻抗谱的频率响应范围为10mHz~100kHz,交流激励信号幅值为5MV,KCl溶液浓度梯度为0.05、0.50、1.00、2.50、4.20mol/L。测试过程中将样品放在相应的溶液中极化600s使测试系统稳定。利用PowerSuite软件观察腐蚀曲线并导出数据进行拟合。
2 实验结果与讨论
2.1 Nyquist图分析
3种金属的Nyquist图如图1所示,图1中横坐标表示阻抗的实部,纵坐标表示阻抗的虚部。通过对比可以看出3种金属都表现出半圆弧的特征,说明3种金属都具有电容特性,即在腐蚀表面都有氧化膜生成;Alloy 690、Alloy 600和X80的阻抗值依次减小,腐蚀速率依次增加,说明3种金属的抗腐蚀性能依次减小。
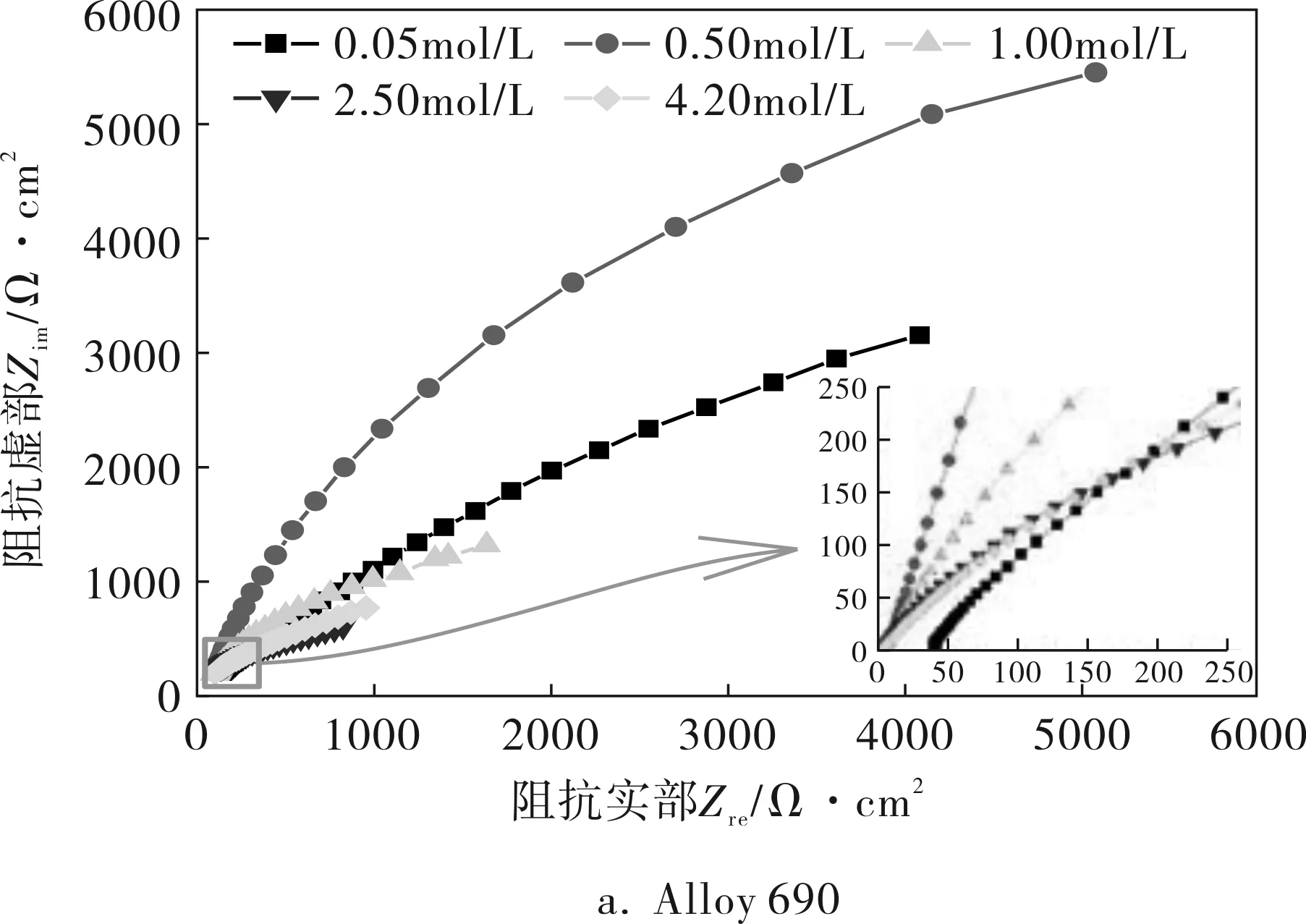


图1 3种金属在KCl溶液中的Nyquist图
对比同一种金属在不同溶液中的腐蚀,在0.05mol/L的KCl溶液中,实轴阻抗起始位置均不在零点,而是在偏离实轴的一定位置,这是由于溶液浓度比较小的情况下,溶液的阻值相对较大,因此起始位置不在零点。当溶液浓度增加到一定值时,起始位置均在零点附近,说明此时腐蚀溶液的电阻较小,已经对系统的影响不大。另外,当氯离子含量超过一定值时,继续增加氯离子,腐蚀的倾向性反而会减小。对于不同的金属,对应的临界值不一样。当氯离子含量比较少时,随氯离子浓度的增加,腐蚀的倾向性逐步增加;但当氯离子含量超过一定值时,继续增加氯离子,有时腐蚀的倾向性反而会减小。
2.2 Bode图分析
在腐蚀Bode图(图2)中,高频区域代表氧化膜电阻特性的快速响应,低频区域代表双电层及法拉第过程等的慢速响应[3]。从图2可以看出,在高频阶段,不同浓度溶液中阻抗值差别较大,0.05mol/L KCl溶液中的阻抗值比其他浓度溶液的阻抗值较大,这主要是由两方面的原因造成的:一是因为溶液浓度很小,导致溶液的电阻很大;二是因为氯离子对氧化膜的破坏较小,氧化膜相对比较完整。另外,在高频阶段阻抗值变化不大,这也说明系统的电容特性明显,氧化膜相对比较完整,可以阻止或延缓氯离子渗透到金属基体,增加腐蚀的阻力。在中频阶段,log|Z|-logf近似为一条45°的斜直线,表明质量传递控制着腐蚀的过程[12]。质量传递主要就是氯离子在氧化膜中的渗透。这也说明氧化膜比较完整,可以抑制腐蚀剂在氧化膜中的快速渗透。从图2也可以看出,不同金属的这条斜线的起始位置不一样,例如在1.00mol/L的KCl溶液中,Alloy 690、Alloy 600和X80的起始位置分别为10 000、4 000、10kHz。其主要原因为:Alloy 690的氧化膜比较完整,氯离子比较难渗透,质量传递更容易成为腐蚀的控制步骤。在低频阶段,log |Z|-logf的斜率有所下降,这主要是由于在频率变化较慢时,扩散就会起到一定的作用,也就意味着氧化膜还是有缺陷存在,会有部分离子在氧化膜两端电势差作用下,缓慢迁移。
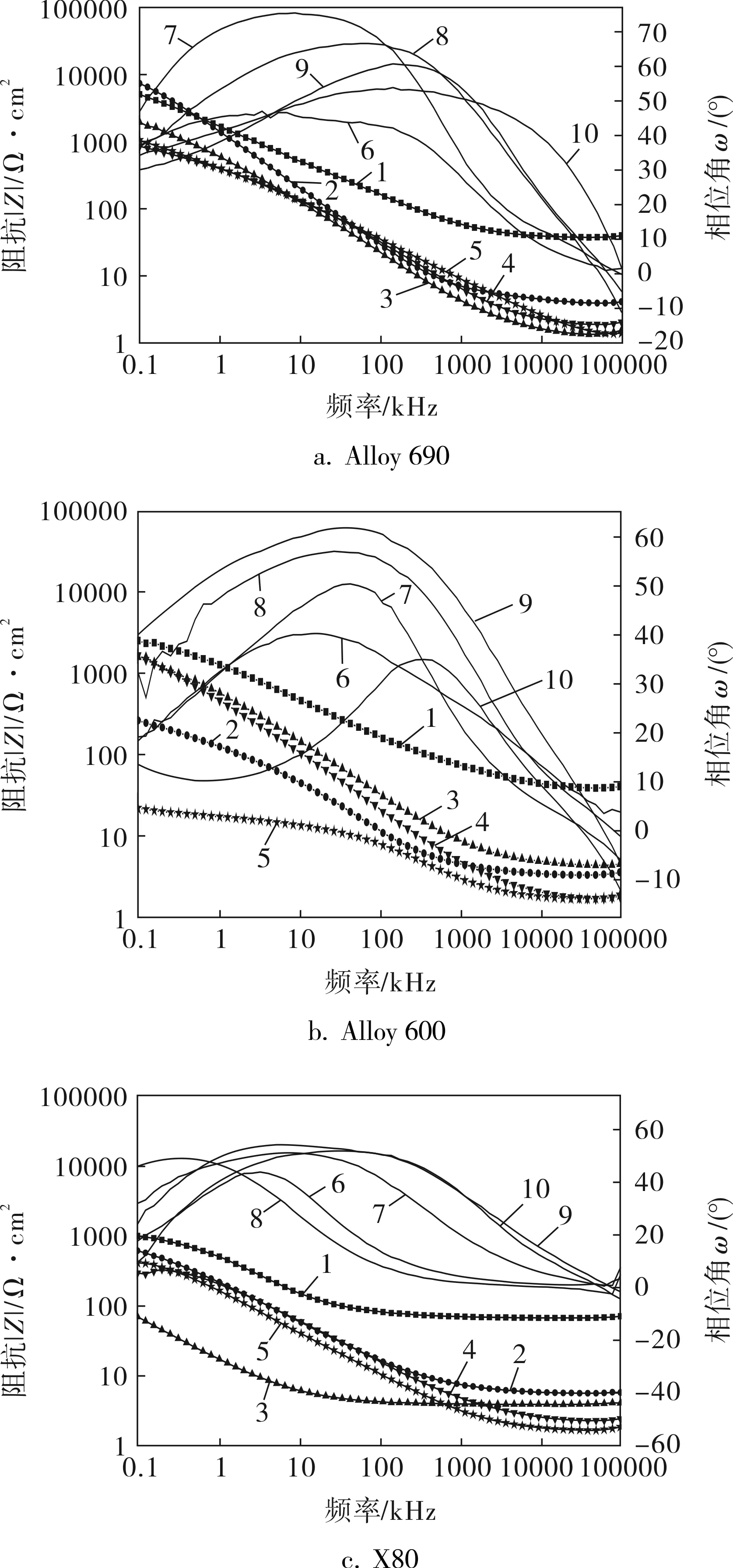
图2 3种金属在KCl溶液中的Bode图
相位角越接近90°,系统越具有理想电容特性。从相位角可以看出,Alloy 690、Alloy 600和X80的相位角在中频阶段依次降低,说明3种金属所形成的氧化膜完整性依次降低,即腐蚀性依次增加。
2.3 等效电路图
将原始数据导入拟合软件,选择R(RQ)(RQ)作为等效电路(图3)。
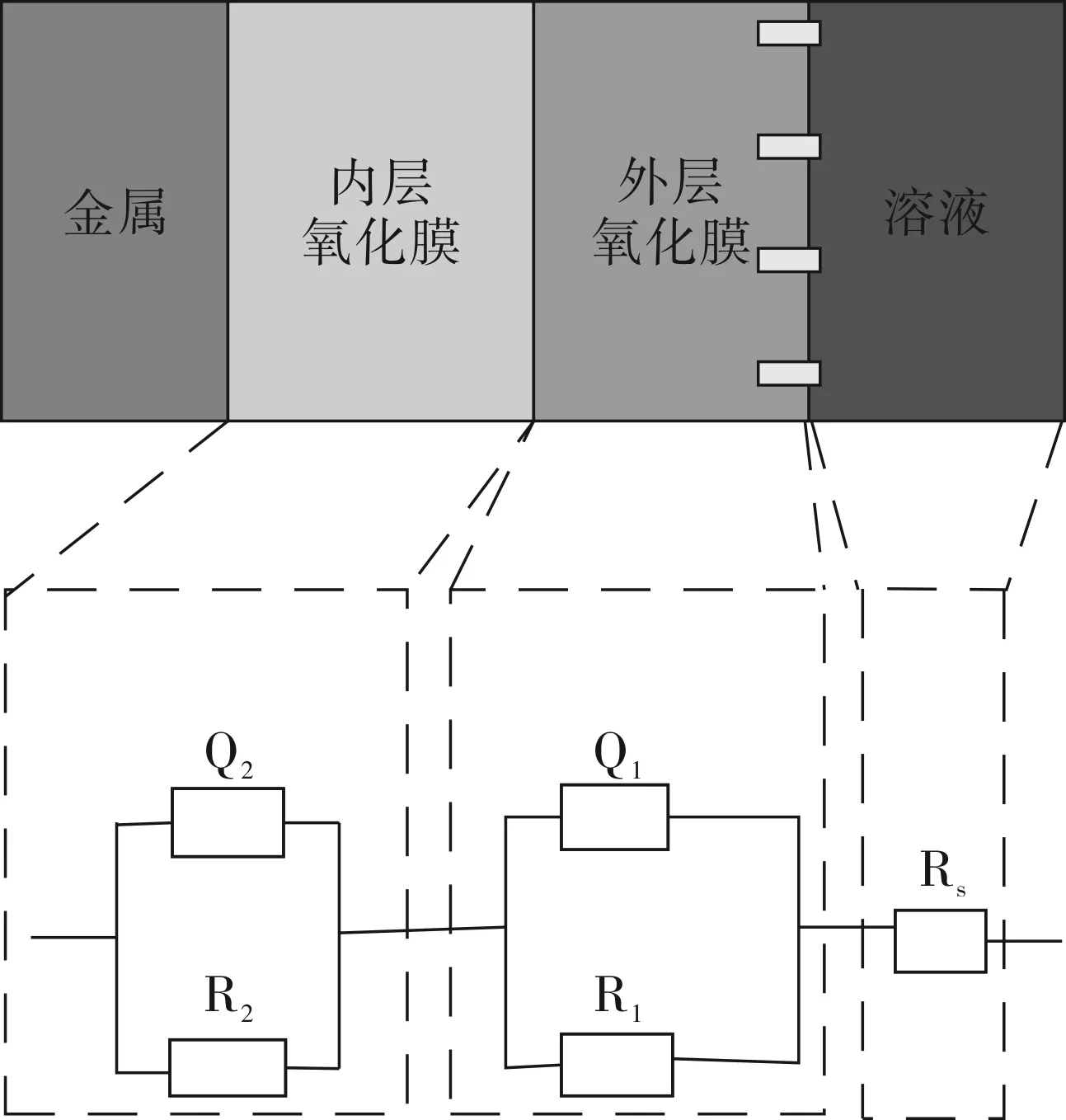
图3 等效电路图
图3中Rs为溶液电阻,Q1和R1代表外层氧化膜的非理想电容(由金属腐蚀的弥散效应引起)和电阻,Q2和R2代表内层氧化膜非理想电容和电阻。其中非理想电容Q可表示为:
Q=Y×(jω)n
式中 j——虚数单位;
n——非理想电容器指数;
Y——非理想电容器幅值;
ω——相位角。
拟合的结果见表2,表2中c为溶液浓度,Rs为溶液电阻,Y1为外层氧化膜非理想电容器幅值,n1为外层氧化膜非理想电容器指数,Y2为内层氧化膜非理想电容幅值,n2为内层氧化膜非理想电容指数,R1、R2分别为外、内层氧化膜的电阻特性。
从表2可以看出,R(QR)(QR)电路拟合阻抗谱数据的平方根误差在2.48×10-4~43.60×10-4之间,误差较小,所以这种电路能够在各种情况下比较好的拟合阻抗谱数据。Rs在0.05mol/L KCl溶液中阻值比较大,当浓度继续增加后,变化不大,说明在氯离子浓度较低时,溶液会消耗掉一部分电压,总电压一定情况下,施加在氧化膜两端的电压必然减小,可以降低腐蚀速率,但是当浓度增加到一定值时,靠溶液消耗电压来防止腐蚀的效果极其微小。对于外层氧化膜而言,n1在0.52~0.83之间,均值为0.70,说明外层氧化膜具有非理想电容器特征,这主要是由腐蚀过程中腐蚀表面的凹凸不平引起的。另外,这层氧化膜的电阻相对较小,也说明外层氧化膜可能会含有可供溶液离子扩散的通道。内层氧化膜n2在0.53~1.00之间,均值为0.75,这说明内层氧化膜结构相比外层氧化膜而言,更接近于理想电容器。另外,不同金属的内层氧化膜的电阻相差很大,Alloy 690的阻值相对较高,Alloy 600次之,X80的阻值最小,这也是3种金属抗氯离子腐蚀性能差别较大的原因所在,这说明内层氧化膜的结构对材料的抗腐蚀性能影响明显。另外,还应该注意到有些情况下,内层氧化膜的电阻值变的非常小(如0.05 mol/L KCl溶液中的Alloy 600、4.20mol/L KCl溶液中的Alloy 690 和1.00mol/L KCl溶液中的X80),这主要是由氧化膜的半导体性质决定的,在这样浓度的溶液中,金属的电子可以相对无阻碍地通过费米能级穿过内层氧化膜到达外层氧化膜中。
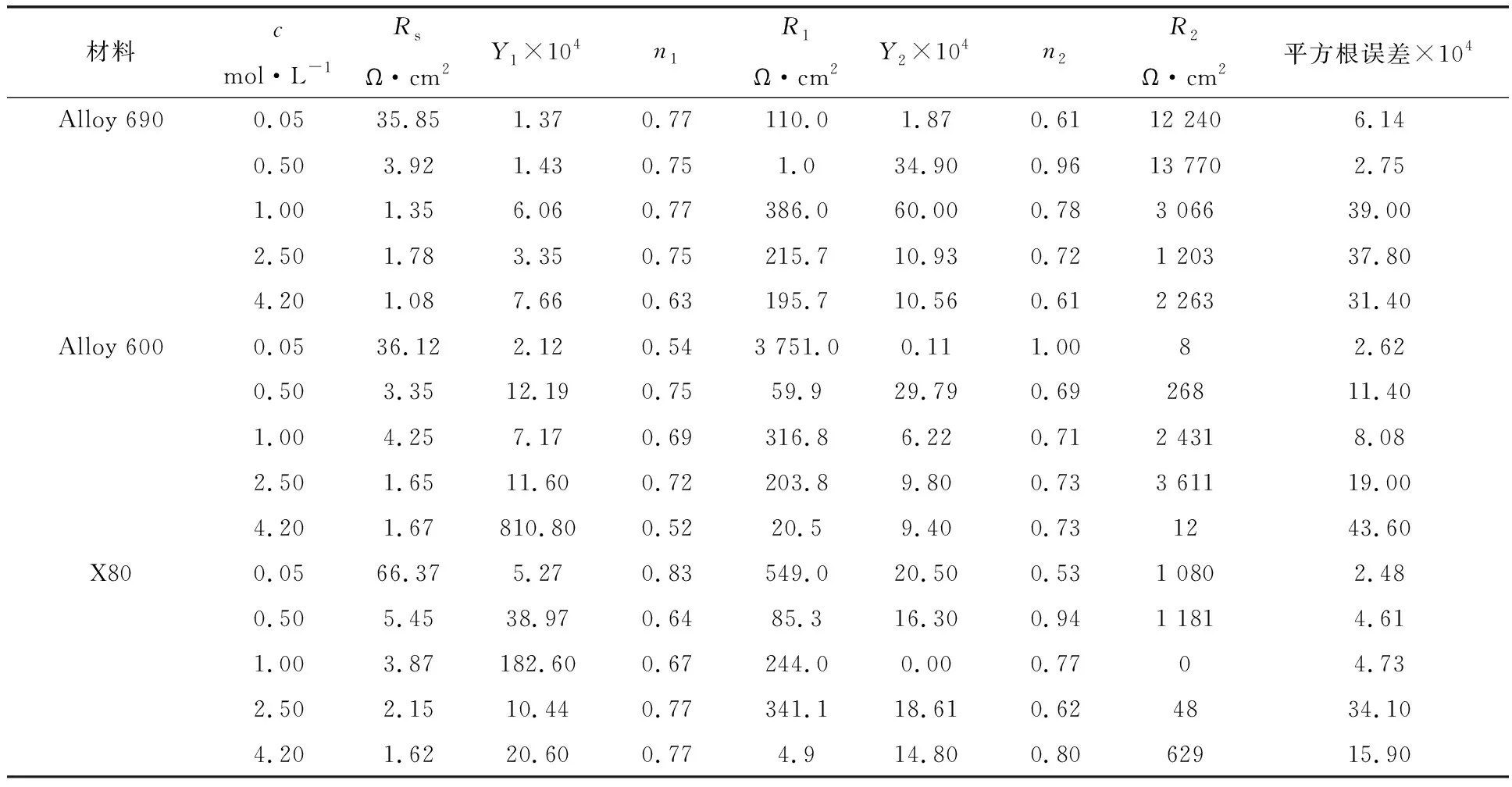
表2 3种金属在不同Cl-浓度的溶液中腐蚀的EIS等效电路拟合结果
3 结束语
通过对Alloy 690、Alloy 600和X80 3种典型的不锈钢材料在不同浓度的KCl溶液中阻抗谱实验研究与分析,得到Alloy 690、Alloy 600和X80抗氯离子腐蚀的性能依次降低,当氯离子含量比较少时,随氯离子浓度的增加,腐蚀的倾向性逐步增加;但当氯离子含量超过一定值时,继续增加氯离子,有时腐蚀的倾向性反而会减小。R(QR)(QR)电路能够在各种情况下比较好地拟合阻抗谱数据,当溶液浓度大于0.05mol/L时,溶液的电阻较小,可以忽略。外层氧化膜的电阻相对较小,可能会含有可供溶液离子扩散的通道,具有非理想电容器特征。内层氧化膜的结构对材料的抗腐蚀性能影响明显。内层氧化膜组织突然变小是由于电子通过费米能级从金属向氧化膜渗透,阻力较小。
[1] Bojinov M,Saario T,Betova I,et al.Effect of Water Chemistry on the Oxide Film on Alloy 690 During Simulated Hot Functional Testing of Apressurised Water Reactor[J].Corrosion Science,2012,58(5):20~32.
[2] Betova I,Bojinov M,Kinnunen P,et.al.Mixed-conduction Model for Stainless Steel in a High-temperature Electrolyte: Estimation of Kinetic Parameter of Inner Layer Constituents[J].Journal of Electrochemcal Society, 2008,155(2):81~92.
[3] Li X H,Wang J Q,Han E H,et al.Corrosion Behavior for Alloy 690 and Alloy 800 Tubes in Simulated Primary Water[J]. Corrosion Science, 2013, 67(2): 169~178.
[4] Huang J B,Wu X Q,Han E H.Influence of pH on Electrochemical Properties of Passive Films Formed on Alloy 690 in High Temperature Aqueous Environments[J].Corrosion Science,2009,51(12):2976~2982.
[5] 潘旭东,王向明.循环水中氯离子控制及对不锈钢腐蚀机理探讨[J].工业水处理, 2013, 33(3): 14~16.
[6] 安洋.不锈钢及碳钢在工业循环冷却水中腐蚀行为的研究[D].天津:天津大学,2010.
[7] 解群,翟祥华,葛红花.氯离子和硫离子对不锈钢侵蚀性比较[J].华东电力,2003, 31(12): 860~862.
[8] 李劲,邓博,蒋益明.不锈钢腐蚀评价技术研究及其应用[J].腐蚀与防护, 2009,30(9): 595~603.
[9] 秦丽雁.不锈钢应用中几个腐蚀问题的研究[D].天津:天津大学, 2006.
[10] Hu J,Duan Q,Cheng G X,et al.Investigation of the Impedance Characteristics in the Pitting Evolutionary Process of Alloy 690 [J]. Annals of Nuclear Energy, 2013,58: 25~32.
[11] 任爱,李成涛,刘飞华,等. Cl-对690合金在高温高压水中腐蚀行为的影响[J]. 中国有色金属学报, 2012, 22(4): 1082~1087.
[12] Dong C F, Fu A Q, Li X G, et al. Localized EIS Characterization of Corrosion of Steel at Coating Defect under Cathodic Protection[J].Electrochim Acta, 2008, 54(2): 628~633.

