槲皮素对结直肠癌细胞SW480增殖与Bcl-2、C-myc表达的影响Δ
罗辉燕,冯冬冬,于伟娜,丁陈波,李静,冯继红#(.重庆市第三人民医院肿瘤科,重庆 40004;.寿县中医院心内科,安徽 寿县 00;.遵义医学院附属医院肿瘤医院,贵州 遵义 5600)
结直肠癌(Colorectal carcinoma,CRC)是常见消化系统恶性肿瘤之一。全球范围内,CRC分别位居男、女性恶性肿瘤的第三、四位,导致每年61万人死亡[1-2]。在中国,近年CRC发病率逐年上升,且发病年龄提前,每年约有40万新增病例,目前在我国消化系统恶性肿瘤中列第二位[3]。
槲皮素是黄酮类化合物重要的一员,据研究发现,槲皮素及其衍生物可抑制多种肿瘤细胞的增殖和侵袭能力,具有较为广阔的应用前景。槲皮素具有明确的抗肿瘤作用,对乳腺癌、前列腺癌、结肠癌和肺癌等都具有预防作用和一定的治疗作用[4]。槲皮素抗肿瘤作用涉及多种机制,但对结直肠癌的作用机制尚不清楚。本研究旨在通过观察槲皮素对结直肠癌SW480细胞增殖的抑制作用及对其B细胞淋巴瘤/白血病-2(Bcl-2)、癌基因C-myc表达的影响,探讨其抗肿瘤作用机制,为槲皮素在结直肠癌化疗中的应用提供理论依据。
1 材料
1.1 仪器
CKX31型显微镜(日本Olympus公司);CJ-2 F型超净工作台(苏州冯氏实验动物设备有限公司);MCO175型CO2培养箱(日本Sanyo公司);Spectra Mr型全波长酶标仪(美国Dynex公司);聚合酶链反应(PCR)扩增仪、垂直电泳槽、凝胶成像分析仪(美国Bio-Rad公司)
1.2 试剂
L-15培养基(Leibovitz’s L-15 Medium,美国Gibco公司);胎牛血清(FBS,美国Hyclone公司);兔抗人Bcl-2单抗、兔抗人C-myc单抗(美国Epitomics公司);兔抗人β-actin单抗(北京中衫金桥公司);槲皮素(纯度≥98.5%)、MTT、二甲亚枫(DMSO)购自美国Sigma公司;Trizol、实时荧光定量反相(qRT)PCR(qRT-PCR)试剂盒、Premix Taq酶、Marker均购自大连宝生物工程有限公司;凯基全蛋白提取试剂盒(南京凯基生物科技有限公司);BCA蛋白定量试剂盒、SDS-PAGE凝胶配制试剂盒、聚偏二氟乙烯膜(PVDF)膜、琼脂糖(Agarose)、TAE(50×)均购自上海碧云天生物技术有限公司;ECL发光试剂盒(美国Millipore公司)。
1.3 细胞
人结直肠癌细胞株SW480购自中国科学院上海细胞库。
2 方法
2.1 细胞培养
SW480细胞培养于含10%FBS的L-15培养基中,在5%的CO2饱和湿度、37Ⅸ恒温培养箱中常规培养。SW480细胞呈单层贴壁生长,每2~3 d用0.25%胰酶消化,以1∶2传代。SW480细胞生长状态稳定,呈对数生长期时用于试验。
2.2 药物处理与分组
槲皮素用DMSO制备成贮备液,-20Ⅸ贮藏,备用。试验时用L-15培养基稀释,DMSO的最终质量分数<0.1%。试验分3大组,即空白对照(200μl L-15培养液)组、溶剂对照(200μl L-15培养液+150μl DMSO)组、试验(200μl L-15培养基+不同梯度浓度的槲皮素,槲皮素的终浓度分别为5、10、20、40、80、160 μmol/L)组。
2.3 MTT法检测
取对数生长期的SW480细胞悬液,以每孔3×103个细胞接种于96孔培养板,每孔加含10%FBS的L-15培养液200μl,于37Ⅸ、5%CO2培养箱培养8 h,在倒置显微镜下观察细胞贴壁后按“2.2”项下方法给药。继续培养24、48、72h,每一浓度设5个复孔,于各时间段前4h每孔避光加入MTT(5g/L,PBS稀释)20µl,培养终止后弃上清加入DMSO 150µl/孔,振荡溶解10min,待结晶完全溶解后于酶标仪570nm波长处检测各个浓度的光密度(OD),计算细胞增殖抑制率。细胞增殖抑制率(IR)=[1-(试验组OD-溶剂对照组OD)/(空白对照组OD-溶剂对照组OD)]×100%。
2.4 qRT-PCR检测SW480细胞中Bcl-2、C-myc mRNA的表达
Bcl-2引物序列 ,上 游 :5′-TGTGGCCTTCTTTGAGTTCG-3′,下游:5′-ATCCCAGCCTCCGTTATCC-3′,扩增片段长度为137bp;C-myc引物序列,上游:5′-CGAGGAGGAGAACTTCTACCAGC-3′,下 游:5′-CGAGAAGCCGCTCCACATACAGTCC-3′,扩增片段长度为471bp;β-actin引物序列,上游:5′-ACAGAGCCTCGCCTTTGCCGATC-3′,下游:5′-TGGGTCATCTTCTCGCGGTTGG-3′,扩增片段长度为 417 bp。分别培养细胞24、48、72h后,收集细胞,Trizol法提取RNA,鉴定完RNA纯度和完整性后,反转录制备cDNA;PCR反应条件为:95Ⅸ预变性lmin;95Ⅸ变性15 s,58Ⅸ退火20 s,72Ⅸ延伸20 s,循环40次;72Ⅸ延伸5min终止反应。qRTPCR反应结束后,定量分析PCR获得的熔解曲线和扩增曲线结果的可靠性并设定循环阈值(Ct),以Bcl-2/β-actin、C-myc/β-actin比值分别代表各自相对表达水平,计算Bcl-2、C-myc mRNA的相对表达强度。各组设3个复孔,试验重复3次。
2.5 Western blot法检测SW480细胞中Bcl-2、C-myc蛋白的表达
分组收集用药物干预SW480细胞48 h后的细胞,加入适量细胞裂解液,冰浴30min,高速离心后取上清采用BCA法测定蛋白浓度,调整到标准浓度后分别取50µl样品进行SDS-PAGE电泳,半干转膜法转至PVDF膜。5%的脱脂奶粉封闭1 h,分别加一抗稀释液(兔抗人单抗)4Ⅸ孵育过夜,再用辣根酶标记山羊抗兔IgG二抗37Ⅸ孵育1 h。PBST缓冲液洗膜10min×3次。ECL荧光显色后在暗室中进行X片曝光,结果用凝胶成像系统分析拍照并对凝胶条带的信号强度进行半定量分析,以Bcl-2/β-actin、C-myc/β-actin的比值作为各自蛋白的相对表达强度。试验重复3次。
2.6 统计学方法
3 结果
3.1 槲皮素对SW480细胞增殖的抑制作用
不同浓度的槲皮素对SW480细胞增殖有明显抑制作用。由于OD可间接反映活细胞的数目,槲皮素浓度范围为20~160 μmol/L时,随着槲皮素浓度的增加,SW480细胞在各个时间点的OD均降低,说明抑制率呈上升趋势,显示抑制作用呈剂量依赖关系。槲皮素在作用不同时间时对SW480细胞增殖抑制有不同作用,当槲皮素浓度<20 μmol/L时,与溶剂对照组比较,作用24、48、72h后的抑制率均无明显变化(P>0.05),但都起到一定抑制作用;当槲皮素浓度在20~160 μmol/L时,随着时间的延长,对SW480细胞增殖的抑制明显增强(P<0.05),显示抑制作用呈时间依赖关系。槲皮素对SW480细胞增殖的抑制作用见图1。

图1 槲皮素对SW480细胞增殖的抑制作用Fig 1 Inhibition of quercetin on the proliferation SW480 cells
3.2 槲皮素(40μmol/L)作用SW480细胞不同时间对Bcl-2、C-myc mRNA表达的影响
槲皮素(40 μmol/L)作用SW480细胞0、24、48、72h后,与溶剂对照组比较,试验组SW480细胞Bcl-2、C-myc mRNA表达强度随槲皮素作用时间的延长而减弱,差异有统计学意义(P<0.05)。Bcl-2、C-myc mRNA的表达见图2。
3.3 槲皮素(40μmol/L)作用SW480细胞不同时间对Bcl-2、C-myc蛋白表达的影响

图2 Bcl-2、C-myc mRNA的表达Fig 2 mRNAexpression of Bcl-2and C-myc
槲皮素(40μmol/L)作用SW480细胞48、72h后,与溶剂对照组比较,试验组Bcl-2、C-myc蛋白表达强度随槲皮素作用时间的延长而减弱,差异有统计学意义(P<0.05)。Bcl-2、C-myc蛋白的表达见图3。
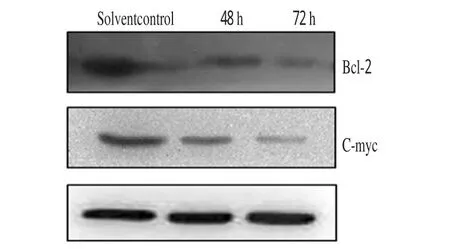
图3 Bcl-2、C-myc蛋白的表达Fig 3 Protein expression of Bcl-2and C-myc
4 讨论
CRC是我国常见的恶性肿瘤,其发病率和病死率在我国呈逐年上升趋势。肝转移是导致结直肠癌患者死亡的主要原因,尽管国内外有关CRC转移已有很多研究,但仍无解决临床实际问题的成果[4]。目前CRC的治疗以综合治疗为主,多采用中药联合化疗、放疗和手术。中药及其有效成分的对CRC作用的研究越来越深入,部分已应用到临床,并取得了一定的效果[5-6]。
已有多项研究表明,槲皮素对多种恶性肿瘤如胃癌、乳腺癌、肝癌、宫颈癌、结肠癌、卵巢癌、胆囊癌等均有抑制其生长的作用,并可促进恶性肿瘤细胞的凋亡[7]。槲皮素可通过多途径来发挥抗肿瘤效果、抑制多种肿瘤细胞的分裂增殖,通过多种途径促进其凋亡,抑制肿瘤细胞迁移及侵袭,降低其耐药性,在临床抗肿瘤治疗中,发挥着重要作用[8]。近年研究结果表明,槲皮素可抑制SW480、结肠癌细胞HCT116、结肠腺癌细胞Caco-2等CRC细胞的增殖,诱导其凋亡[9-11]。本研究结果表明,不同浓度的槲皮素对SW480细胞的生长和增殖有明显抑制作用,并呈剂量-效应关系。由此可见,槲皮素在体外对结直肠癌细胞的增殖具有明显抑制作用,且能够诱导肿瘤细胞凋亡。
为阐明槲皮素诱导的细胞凋亡机制,笔者进一步研究了SW480细胞中Bcl-2和C-myc mRNA和蛋白表达的变化,且二者的表达随作用时间延长而减弱。已知Bcl-2是抗凋亡基因,可稳定细胞内质膜系统、抑制线粒体内离子及细胞色素C的释放,从而抑制凋亡的发生;能抑制许多抗肿瘤药物诱导细胞凋亡,降低其细胞毒性;还可与其他癌基因如C-myc和抗癌基因p53相互作用,间接地调控细胞程序性死亡[12]。C-myc癌基因具有促进细胞增殖和诱导细胞凋亡的双重作用。槲皮素是否通过抗凋亡基因Bcl-2作用于C-myc导致其表达变化尚不得而知,其关联调节作用尚需证实。综上所述,一定浓度的槲皮素在体外能诱导SW480细胞中Bcl-2和C-myc的表达下调,说明槲皮素可能通过Bcl-2和c-myc基因对细胞增殖起抑制作用并诱导其凋亡,具体作用机制有待于进一步研究。
[1]Siegel R,Naishadham D,JemalA.Cancer statistics[J].CA Cancer J Clin,2012,62(1):10.
[2]American Cancer Society.American Cancer Society:Colorectal cancer facts&figures 2011-2013[R].Atlanta,2011.
[3]王锡山.结直肠癌综合治疗的规范化实施[J].中国实用外科杂志,2010,30(4):260.
[4]刘明学,魏光辉.槲皮素的药理学作用及临床应用前景[J].中国药房,2010,21(27):2581.
[5]朱淑珍,张红河,来茂德.上皮间质转化与结直肠癌转移[J].中华病理学杂志,2013,42(7):490.
[6]周喜汉,黄赞松,向发良.中药抗结直肠癌作用的研究进展[J].世界华人消化杂志,2013,21(18):1720.
[7]孙涓,余世春.槲皮素的研究进展[J].现代中药研究与实践,2011,25(3):85.
[8]王惠丽,胡子有,苑召虎,等.槲皮素抗肿瘤机制的研究进展[J].热带医学杂志,2013,12(1):126.
[9]林增海,马涛,孟勇.槲皮素对人结肠癌SW480细胞增殖的抑制作用[J].实用医学杂志,2012,28(5):699.
[10]Kim HS,Wannatung T,Lee S,et al.Quercetin enhances hypoxia-mediated apoptosis via direct inhibition of AMPK activity in HCT116colon cancer[J].Apoptosis,2012,17:938.
[11]Dihal AA,Woutersen RA,van Ommen B,et al.Modulatory effects of quercetin on proliferation and differentiation of the human colorectal cell line Caco-2[J].Cancer Lett,2006,238(2):248.
[12]王海燕,郭良淼,陈勇,等.槲皮素抑制人胃癌MGC803细胞增殖并诱导其凋亡的研究[J].细胞与分子免疫学杂志,2006,22(5):585.

