度洛西汀中间体手性拆分工艺的研究
刘艳梅,刘 杰, 李海华,刘娅静,陈晓超,官儒奇,赵亚娟
(1.温州大学化学与材料工程学院,浙江 温州 325027;2.中国昆仑工程公司辽宁分公司,辽宁 沈阳 111003)
度洛西汀中间体手性拆分工艺的研究
刘艳梅1,刘 杰2, 李海华1,刘娅静1,陈晓超1,官儒奇1,赵亚娟1
(1.温州大学化学与材料工程学院,浙江 温州 325027;2.中国昆仑工程公司辽宁分公司,辽宁 沈阳 111003)
以噻吩和3-氯丙酰氯为原料,经傅克反应生成3-氯-1-(2-噻吩)-丙酮,用硼氢化钠加氢还原得到混旋的度洛西汀中间体3-氯-1-(2-噻吩)-丙醇中间体。利用D-扁桃酸为拆分剂对其中间体进行手性拆分得到较纯的(S)-3-氯-1-(2-噻吩)-丙醇。实验结果表明,3-氯-1-(2-噻吩)-丙醇与D-扁桃酸摩尔的量的比值为主要因素,析出晶体温度和溶剂为次要因素。以苯为溶剂时,3-氯-1-(2-噻吩)-丙醇与D-扁桃酸的量的摩尔比值为1∶0.4,析出温度为0℃,拆分效果较好,其o.p.值为74%。
抗抑郁药;度洛西汀中间体;手性拆分
度洛西汀(Duloxetine),商品名为“Cymbalta(欣百达)”,化学名:(S)-(+)-N-甲基-3-(1-萘氧基)-3-(2-噻吩基)-1-丙胺,其结构式如图1所示。度洛西汀包含1个立体中心,具有(R)-度洛西汀和(S)-度洛西汀2种对应异构体,而只有(S)-度洛西汀具有抗抑郁的药理活性[1-3]。

图1 度洛西汀的结构式
度洛西汀是一种二环类的苯乙胺族化合物,它的结构或者化学特性与三环类、四环类不一样[4-6]。度洛西汀具有化学稳定性好、安全有效、副作用少、对其他神经系统亲和力低等特点[7-8],在治疗抑郁症方面比目前其他西汀类药物作用更好[9-10]。以SSRI类抗抑郁药氟西汀为对照,得出的结果是度洛西汀与氟西汀疗效相当,但是度洛西汀起效快,尤其改善抑郁症患者的躯体症状效果明显,不良反应轻,依从性好[11-12]。
度洛西汀能够治疗抑郁障碍的机理主要是通过抑制5-羟色胺(5-HT)和去甲肾上腺素(NE)再摄取发挥抗抑郁作用[13-14]。国外的其中一项在对1279名重性抑郁症患者的开放性研究表明,给予度洛西汀80mg·d-1或者120mg·d-1,经过52周的治疗以后,其中有效率高达79%,完全缓解率为65%。大量的实验研究表明,度洛西汀对于抑郁症有较好的治疗效果[15]。
1 实验部分
1.1 实验仪器
DHF-4002低温恒温搅拌反应浴,100mL、50mL烧杯,250mL三颈烧瓶,125mL恒压滴液漏斗,HH-1恒温水浴锅,YLA-6000电热鼓风干燥箱,BS124S电子天平,RE-2000旋转蒸发器,WZZ-2A数显自动旋光仪,GC7900气相色谱仪。
1.2 实验药品及试剂
乙酸乙酯(AR),无水乙醇(AR),甲苯(AR),硼氢化钠(≥96.0%),无水三氯化铝(AR),噻吩(AR),3-氯丙酰氯(AR),二氯甲烷(AR),D-扁桃酸(AR),苯(AR),二甲苯(AR),对二甲苯(AR)。
1.3 实验步骤
第1步实验步骤如图2所示,之后将还原得到的3-氯-1-(2-噻吩)-丙醇通过气相色谱仪分析其产率。第2步如图3所示,之后测量(S)-3-氯-1-(2-噻吩)-丙醇的旋光度。第3步如图4所示。
在最适温度下,称取一定量的3-氯-1-(2-噻吩)-丙醇,再往里加入由步骤(1)中得知最高配比的D-扁桃酸,最后分别用20mL的甲苯、苯、二甲苯、对二甲苯、甲苯与苯、甲苯与二甲苯在固定温度下溶解。在室温下析出晶体,过滤,烘干晶体,再将晶体溶于适量乙醇,用氢氧化钠溶液中和D-扁桃酸,通过萃取,分液,最后除去溶剂乙醇即得(S)-3-氯-1-(2-噻吩)-丙醇,最后测量(S)-3-氯-1-(2-噻吩)-丙醇的旋光度。

图2 第1步实验步骤

图3 第2步实验步骤

图4 第3步实验步骤
在本次实验中,选择3-氯-1-(2-噻吩)-丙醇与D-扁桃酸的量的摩尔比值、析出晶体温度、溶剂3个因素来分别进行实验。
1.4 表征方法
(1)将傅克反应制得并提纯的3-氯-1-(2-噻吩)-丙酮和还原得到的3-氯-1-(2-噻吩)-丙醇依次在傅里叶红外光谱仪上测定物质的官能团,并依次在气质联用仪上测量物质的相对分子质量。
(2)光学纯度(optical purity)是衡量旋光性样品中一个对映体超过另一个对映体的量的量度,我们用o.p.值表示
2 结果与讨论
2.1 D-扁桃酸的量对3-氯-1-(2-噻吩)-丙醇拆分的影响
在拆分过程中保持3-氯-1-(2-噻吩)-丙醇的量、析出晶体的温度及溶剂不变,改变加入D-扁桃酸的量,测其旋光度,再计算收率和o.p(光学纯度)值,结果如表1、图5所示。

表1 D-扁桃酸的量对3-氯-1-(2-噻吩)-丙醇拆分的影响

图5 D-扁桃酸的量对3-氯-1-(2-噻吩)-丙醇拆分的影响
从实验结果可以看出,D-扁桃酸从不足增加到过量的过程中,测得的醇的旋光度先由大变小,后又变大。从图5我们发现,收率虽然随着D-扁桃酸的量的增加而增加,但o.p.值大约在1∶0.4的时候达到最大。说明此时醇的量析出最多,而且纯度高。
2.2 不同温度对3-氯-1-(2-噻吩)-丙醇拆分的影响
摩尔比D-扁桃酸∶3-氯-1-(2-噻吩)-丙醇=0.4∶1,保持溶剂不变,改变析出晶体的温度,测其旋光度,再计算收率和o.p值,结果如表2、图6所示。
从实验结果中可以看出,在摩尔比D-扁桃酸∶3-氯-1-(2-噻吩)-丙醇=0.4∶1,保持溶剂不变的情况下,收率随着析出温度的降低而增加,但o.p.值大约在0℃的时候达到最大,说明此时醇的量析出较多,而且纯度高。

表2 不同温度对3-氯-1-(2-噻吩)-丙醇拆分的影响

图6 不同温度对3-氯-1-(2-噻吩)-丙醇拆分的影响
2.3 不同溶剂对3-氯-1-(2-噻吩)-丙醇拆分的影响
保持析出晶体温度在0℃,摩尔比D-扁桃酸∶3-氯-1-(2-噻吩)-丙醇=0.4∶1,改变溶剂,测其旋光度,再计算收率和o.p值,结果如表3、图7所示。

表3 不同溶剂对3-氯-1-(2-噻吩)-丙醇拆分的影响

图7 不同溶剂对3-氯-1-(2-噻吩)-丙醇拆分的影响
从实验结果中可以看出,在摩尔比D-扁桃酸∶3-氯-1-(2-噻吩)-丙醇=0.4∶1,保持温度为0℃不变的情况下,溶剂的改变会对收率及o.p.值产生影响,例如利用苯作溶剂的话,它的收率及o.p.值都比较高。
2.4 正交实验
在本次实验中,选择3个因素分别为3-氯-1-(2-噻吩)-丙醇与D-扁桃酸的量的摩尔比值、析出晶体温度、溶剂,分别用A、B、C来表示这3个因素。三水平分别为:A1=1∶0.3、A2=1∶0.4、A3=1∶0.5; B1=10℃、B2=0℃、B3=-10℃;C1=苯、C2=甲苯、C3=二甲苯。

表4 正交实验表
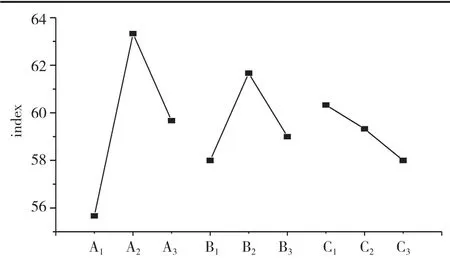
图7 指标-因素图
对正交实验结果进行极差分析,得出影响因素的强弱顺序为:A>B>C。选取图形中最高的水平点得到最优生产条件为A2B2C2,即3-氯-1-(2-噻吩)-丙醇与D-扁桃酸的摩尔的量比值为1∶0.4,析出温度为0℃,溶剂为苯时较好,与单因素拆分结果相符。
3 结论
利用噻吩和3-氯丙酰氯,通过傅克酰基化反应制得3-氯-1-(2-噻吩)-丙酮,然后用硼氢化钠还原成3-氯-1-(2-噻吩)-丙醇。对度洛西汀中间体3-氯-1-(2-噻吩)-丙醇进行拆分,得出的最佳条件为:3-氯-1-(2-噻吩)-丙醇与D-扁桃酸的摩尔的量比值为1∶0.4,析出温度为0℃,溶剂为苯。
致谢:感谢浙江省重中之重化学一级学科(316 406125020301)和浙江省公益技术应用研究计划项目(2013C31129)的资助。
[1] 徐静,于相芬.度洛西汀的临床应用进展[J].西南军医,2011,13(4):695-698.
[2] 林子斌.度洛西汀与氟西汀治疗抑郁症对照研究[J].中国名族民间医药,2011(3):96-97.
[3] 凌云熹,阳中明.度洛西汀治疗抑郁症对照研究的Meta分析[J].四川精神卫生,2011,24(1):18-20.
[4] 赵贵财,徐刚,吴坚平.3-氯-1- (2-噻吩)-丙酮合成工艺的研究[J].化学反应工程与工艺,2006,22(2):176-179.
[5] 赵金凤,窦海建,周宇涵,等.(S,S)-TsDPEN-Ru 催化不对称氢转移还原β-胺基酮及在度洛西汀合成中的应用[J].高等学校化学学报,2011,32(10):2331-2334.
[6] John R.Cashman, Senait Ghirmai.Inhibition of serotonin and norepinephrine reuptake and inhibition of phosphodiesterase by multi-target inhibitors as potential agents for depression[J].Bioorganic&Medicinal Chemistry, 2009(17):6890-6897.
[7] 温新民,毛庆华,汤建,等.度洛西汀的合成进展[J].合成化学,2004,12(6):551-554.
[8] Rex S.Lott,DAnial E.Baker.Duloxeline:A New Antidepressant. Advances in Pharmacy, 2003(3):288-241.
[9] 雷旭伟,梁铁美.抗抑郁药物——盐酸度洛西汀[J].海峡药学,2008,20(4):93-94.
[10] Scofer S H,Kaftzik N,Wasserschweid P,et al.Enzyme catalysis in ionic liquids:lipase catalysed kinetic resolution of l-Phenylethanol with improved enantioseletivity[J]. Chemical Communication,2001(5):4215-4216.
[11] 张玮,张珅玲.手性有机化合物与手性拆分[J].石家庄职业技术学院,2005,17(2):62-64.
[12] Holden C.Global survey examines impact of depression[J]. Scinece,2000,288 (5463):39-40.
[13] Fava M. Somatic symptoms,depression and antidepressant treatment[J].Journal of Clinical Psychiatry, 2002,63(4):305-307.
[14] 阴彩霞.盐酸度洛西汀的合成研究[D].天津:天津大学,2007.
[15] 邓金根,吴同飞,崔欣,等.光学纯氟西汀的制备方法:中国, 00120507[P]. 2003-10-15.
Technics Study on Chiral Separation of Duloxetine Intermediate
LIU Yan-mei, LIU Jie, GUAN Ru-qi, LI Hai-hua, CHEN Xiao-chao,CHAO Guo-ku, TAI Yu-lei, ZHAO Ya-juan
(College of Chemistry and Materials Engineering, Wenzhou University, Wenzhou 325027, China)
Starting from thiophene and 3-chloropropinylchloride, 3-chloro-1-(2-thienyl)propanone was prepared by Friedel-Crafts reaction. Then using sodium borohydride, 3-chloro-1-(2-thienyl)propanol was prepared through hydrogenation reduction. Through chiral separation, the relatively pure product (S)-3-chloro-1-(2-thienyl)propanol was got. The results of experiment indicated that the molar ratio of 3-chloro-1-(2-thienyl)propanol to D-(-)-mandelic acid was the main factor, and the crystallized temperature and the solvent were secondary factors. When the solvent was benzene and the molar ratio of D-(-)-mandelic acid to 3-chloro-1-(2-thienyl) propanol was 0.4 : 1, the crystallized temperature was 0℃, the better results of separation was got, the value of o.p. (optical purity) was 74%.
antidepressants; duloxetine intermediate; chiral separation
O 626.12
A
1671-9905(2014)04-0028-04
2014-01-10

