几丁聚糖纳米颗粒的动态光散射研究
娄本浊
(陕西理工学院物理与电信工程学院,陕西 汉中 723003)
研究与开发
几丁聚糖纳米颗粒的动态光散射研究
娄本浊
(陕西理工学院物理与电信工程学院,陕西 汉中 723003)
利用离子凝胶法制备几丁聚糖纳米颗粒,并用动态光散射测量所得颗粒的粒径分布与界面电位。研究结果发现,随着CS/TPP比值的减小,几丁聚糖纳米颗粒的粒径由单峰分布转变为双峰分布,说明三聚磷酸钠含量的增加会使几丁聚糖纳米颗粒之间产生聚集效应。界面电位值随着CS/TPP比值的减小而逐渐下降,原因是三聚磷酸钠浓度的增加使几丁聚糖纳米颗粒表面上更多的NH3+离子与三聚磷酸根离子反应中和的缘故。
动态光散射;纳米颗粒;几丁聚糖;Zeta电位;粒径分布
几丁聚糖是一种天然的生物可降解性高分子物质,具有良好的生物相容性、抗菌性及来源范围广等优点,广泛应用于生医材料学的研究中[1-3]。Bodmeier等[4]首先提出以离子凝胶法制备几丁聚糖微粒;Calvo等[5]对离子凝胶法提出改进,用三聚磷酸钠和聚氧化乙烯-聚氧化丙烯的嵌段共聚物交联制备出几丁聚糖微粒;Janes等[6]指出几丁聚糖微粒粒径会随着几丁聚糖分子量增加而增大,而在分子量大于20kDa时分子量变因的影响不再显著。Zhang等[7]提出去乙酰度越高的几丁聚糖可制备出较小粒径的几丁聚糖微粒,且其粒径也比较均一。本研究将以三聚磷酸钠作为几丁聚糖的凝胶试剂,利用离子凝胶法制备几丁聚糖纳米颗粒,并利用动态光散射技术分析不同成分比例下纳米颗粒的粒度分布与界面电位。
1 基本原理
在动态光散射中,散射光强自相关函数强度G(2)(τ)与电场自相关函数g(1)(τ)之间满足Siegert关系[8]:

其中β为相干因子,τ为延迟时间。对单分散球形颗粒而言,其电场自相关函数为:

则光强自相关函数可改写为:
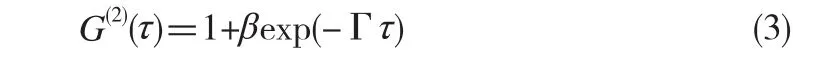
其中Г为半宽衰减系数,它与平移扩散系数D之间满足:
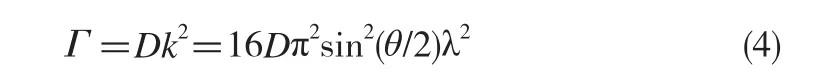
其中k为散射矢量,且有k=4πsin(θ/2)/λ。利用Stocks-Einstein公式[9]可计算出悬浮颗粒的平均流体力学半径R,即:

其中kB为玻尔兹曼常数,T为热力学温度,η为溶剂的黏滞系数。通过式(5)由平移扩散系数D就可以反演出流体力学半径R。
进行界面电位测量时,特定电压下带电粒子因静电吸引力而朝相反电性的电极移动,由于黏滞力会抑制带电粒子移动,当这2种力达到平衡时,带电粒子会以固定速度移动。该速度与电场强度、溶液的介电常数、黏度及界面电位有关,利用动态光散射可测得该移动速度的大小。当电场强度、溶液的介电常数及黏度已知时,即可根据Henry方程求得界面电位,即:

其中μE为电泳移动率,ε为溶液的介电常数,ξ为颗粒的Zeta电位,η为溶液粘度,f (ka)为分散颗粒的参数。若分散颗粒为球形,且当cR很小时,则有:
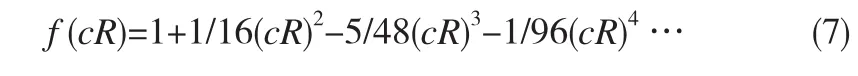
而当cR非常大时,则有:
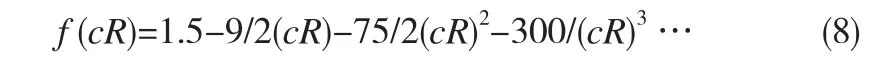
其中R为球形颗粒的半径,c为德拜-霍克参数,且c=3.288I1/2,I为溶液中的离子强度。
2 实验
利用离子凝胶法制备几丁聚糖纳米颗粒。将几丁聚糖(简称CS,食品级)溶于1wt%的醋酸溶液中,再加入8wt%的氢氧化钠溶液,沉淀产生后用滤纸过滤烘干,将滤得的上层物反复水洗即可获得纯化后的几丁聚糖。接着将纯化后的几丁聚糖溶于0.175wt%的醋酸溶液中制得0.1wt%的几丁聚糖溶液,再配制1.25mg·mL-1的三聚磷酸钠(简称TPP)溶液,按相应体积比将这2种溶液混合并于室温下搅拌10min,再用0.1μm的滤纸过滤即可获得不同CS/TPP重量比的几丁聚糖纳米颗粒。
首先用塑胶吸管将样品分散液注入测量专用的一次性样品池中至八分满,注入时要避免产生气泡以免影响到界面电位的测量;然后将样品池放入动态光散射实验系统的样品平台上,分别分析纳米颗粒的粒径分布与界面电位。所用仪器为Nano-ZS型激光光散射法粒径与界面电位测定仪,测量时温度为25℃,散射角设为173°。
3 结果与讨论
图1表示的是不同CS/TPP比值下的几丁聚糖纳米颗粒的动态光散射粒径测量结果。由图1可以发现,CS/TPP=5.3时几丁聚糖纳米颗粒粒径为单峰分布;CS/TPP=4.0时几丁聚糖纳米颗粒粒径开始呈现双峰分布,但不是很明显;CS/TPP=3.2时几丁聚糖纳米颗粒粒径呈明显的双峰分布状态。这说明几丁聚糖纳米颗粒随着CS/TPP比值的减小而变得不均匀,亦即三聚磷酸钠含量的增大会使纳米颗粒之间产生聚集效应。造成以上结果的原因是:当CS/ TPP<4时三聚磷酸钠含量较低,单位三聚磷酸钠可与较多的几丁聚糖分子产生交联,因此在该情况下粒径会随之下降;而CS/TPP<5时三聚磷酸钠浓度较高,会产生较多的几丁聚糖纳米颗粒,纳米颗粒之间也越容易产生离子型聚集。
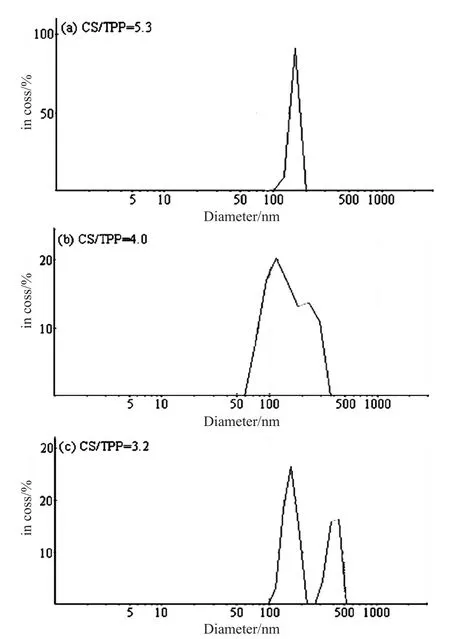
图1 几丁聚糖纳米颗粒的粒度分布Fig.1 the chitosan nano-particle size distribution
界面电位是颗粒分散状态的重要指标,可很好地指示颗粒间作用强度,从而它的测量可用来预测胶体系统的稳定性,界面电位绝对值越大越不易发生凝聚现象。表1给出的是由动态光散射测得的几丁聚糖纳米颗粒的界面电位。当几丁聚糖溶于醋酸溶液时,官能基上的NH2被质子化形成带正电的NH3+离子,此时加入三聚磷酸钠会在溶液中解离成带负电的三聚磷酸根离子,2种离子形成中和反应产生几丁聚糖纳米颗粒,而在纳米颗粒表面上所存在的正电荷,即为未与三聚磷酸根离子形成相互作用的NH3+离子。由表1结果可发现,随着CS/TPP比值的减小,界面电位值也会随之下降,造成该结果的原因是三聚磷酸钠浓度的增加使几丁聚糖纳米颗粒表面上更多的NH3+离子与三聚磷酸根离子反应中和,从而降低了界面电位值。
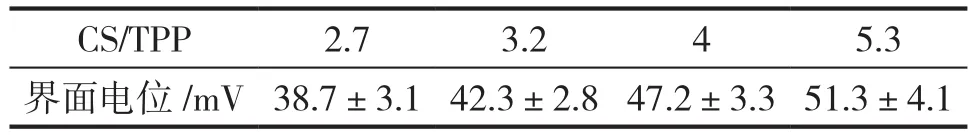
表1 几丁聚糖纳米颗粒的界面电位Tab.1 the Zeta potential of chitosan nano-particle
4 结论
几丁聚糖具有成本低、来源广、生物分解性与相容性好及抗菌性强等优点,一直以来被视为生医材料的研究热点。本研究以三聚磷酸钠为交联剂,采用离子凝胶法制备了不同CS/TPP重量比的几丁聚糖纳米颗粒,并利用动态光散射法分析了CS/TPP重量比对纳米颗粒的粒径分布与界面电位影响。研究结果表明,当三聚磷酸钠含量较低时,单位三聚磷酸钠可与较多的几丁聚糖分子产生交联作用,纳米颗粒粒径会随之下降;而当三聚磷酸钠浓度较高时会产生较多的几丁聚糖纳米颗粒,纳米颗粒之间就容易产生离子型聚集效应。三聚磷酸钠浓度增大会使几丁聚糖纳米颗粒表面上产生较多的NH3+离子,从而与三聚磷酸根离子反应中和,进而降低了纳米颗粒的界面电位。
[1] 李欣, 陈立仁.海藻酸钙-几丁聚糖微胶囊制备方法的研究[J].武汉理工大学学报,2010,32(24):42-44.
[2] 徐飞海,王士斌,黄晓楠,等.海藻酸钙-几丁聚糖微胶囊的形态与粒径[J].膜科学与技术,2006,26(6):12-16.
[3] 万里,田伟.几丁聚糖在临床中的应用[J].沈阳医学院学报,2013,15(2):122-124.
[4] R Bodmeier, H Chen, O Paeratakul. A novel approach to the oral delivery of micro-and nanoparticles[J]. Pharmaceutical Research, 1989, 6(5): 413-417.
[5] P Calvo, C Remuñán-López, J. L Vila-Jato, et al. Novel hydrophilic chitosan-polyethylene oxide nanoparticles as protein carriers[J]. Journal of Applied Polymer Science, 1997, 63(1): 125-132.
[6] K. A Janes, M. J Alonso. Depolymerized chitosan nanoparticles for protein delivery: Preparation and characterization[J]. Journal of Applied Polymer Science, 2003, 88(12): 2769-2776.
[7] H Zhang, M Oh, C Allen, et al. Monodisperse chitosan nanoparticles for mucosal drug delivery[J]. Biomacromolecules, 2004, 5(6): 2461-2468.
[8] 刘晓艳,申晋,朱新军,等.动态光散射技术的角度依赖性[J].光学学报,2012,32(6):259-264
[9] 夏辉,黄生祥,李宏建.应用低相干动态光散射检测乳制品品质[J].中国激光,2008,35(1):102-105.
Research on Chitosan Nanoparticles based on Dynamic Light Scattering
LOU Ben-zhuo
(School of Physics and Telecommunication Engineering, Shaanxi University of Technology, Hanzhong 723003, China)
The chitosan nanoparticles were prepared by ionic gelation method and the size distribution and Zeta potential were measured by dynamic light scattering technique. The results showed that the size distribution of chitosan nanoparticles was from unimodal to bimodal with the TPP content decreasing and it indicated that the aggregation effect between nanoparticles was caused by the TPP content decreasing. The Zeta potential reduced gradually with the TPP content decreased. This was because more NH3+ions on the surface of chitosan nanoparticles neutralized triphosphoric groups for TPP content increasing.
dynamic light scattering; nanoparticle; chitosan; Zeta potential; particle size distribution
O 631.3
A
1671-9905(2014)04-0001-03
国家自然科学基金(41105107);陕西省自然科学基础研究计划基金(2012JM5014);陕西省教育厅专项科研计划项目(2013JK0617)
娄本浊(1982-),男,汉,山东济南人,讲师,硕士,主要从事光学技术在生化材料领域中的应用研究,电话:13891646451,E-mail: benzhuolou@126.com
2014-01-10

