304不锈钢点蚀行为的电化学阻抗谱研究
杜 楠,叶 超,田文明,赵 晴
(南昌航空大学 轻合金加工科学与技术国防重点学科实验室,南昌330063)
不锈钢具有良好的加工成型性能以及良好的耐腐蚀及抗氧化性能,因此在航空航天领域得到了较为广泛的应用。近些年来,在航空工业产品上,不少用结构钢制造的零件,有逐步被各类不锈钢代替的趋势,这样可以减少表面防护及防锈措施,降低零件的失效概率。随着飞机向着长寿命、高安全性发展,采用高强度不锈钢制作某些重要零部件已成为主要发展趋势[1]。
但是在含有侵蚀性离子(如Cl-)的介质中,不锈钢非常容易发生点蚀[2],点蚀的存在,不但降低了不锈钢件的整体强度,而且蚀孔容易成为应力集中的区域[3],造成工件的破坏,这明显增加了航空母舰上的飞机及沿海部署的飞机的维护成本。点蚀具有口小孔深的特点,孔口又常常被腐蚀产物覆盖,使其隐蔽不易被发现,在实际应用中存在很大的安全隐患[4,5]。
动电位电化学阻抗谱(DEIS)可以通过宽频率范围的测量得到不同电位下双电层及钝化膜状态的相关信息,从而研究材料从钝化态到稳定点蚀的连续变化过程,可以比传统的动电位极化和电化学阻抗谱技术获得更多的动力学信息[6-9]。时间扫描模式下的电化学阻抗谱(TSEIS)可以连续监测某一电位下电极状态随时间的变化情况,得到点蚀发展过程中的动态信息,为研究点蚀的动力学规律提供了条件。
本工作以304不锈钢作为研究对象,使用动电位电化学阻抗谱(DEIS)和时间扫描模式下的电化学阻抗谱(TSEIS)共同研究了该材料在3.5%(质量分数,下同)NaCl溶液中的点蚀行为,得到了电极状态在点蚀发展过程中的变化规律,解释了点蚀在不同发展阶段腐蚀行为变化的原因。
1 实验材料与方法
研究电极为304不锈钢,化学成分由QSN750直读光谱测出,如表1所示。实验材料的热处理状态是1060℃ 保温0.5h,水冷,再加热到650℃ 保温2h,空冷,以利于点蚀的发生[10]。实验所用304不锈钢在3.5%NaCl溶液中的自腐蚀电位为(-0.30±0.05)V。将304不锈钢线切割成φ10mm的圆片作为电极。电极用酚醛树脂镶嵌,焊接导线,非工作面用环氧树脂封装。实验前工作面依次用400,600,800,1200#Al2O3水砂纸打磨平整,依次用酒精、丙酮擦拭,经去离子水洗并吹干后,放入干燥皿中备用。

表1 304不锈钢的化学成分Table 1 Chemical composition of 304 stainless steel
试样进行相应的电化学测试时先在-1.3V下进行阴极极化5min,以去除电极表面的氧化膜,再浸泡3h,使电极表面生成稳定的钝化膜[11]。电化学测试所用仪器为Autolab PGSTAT30电化学工作站,测试采用经典的三电极体系,以饱和甘汞电极(SCE)作为参比电极。先对试样进行动电位扫描测试,扫描速率为1m V/s;根据动电位扫描得到的结果,确定动电位电化学阻抗谱测试的电位区间为-0.2~0.4V,电位步进长度为0.02V,施加的正弦波电位阶跃信号幅值为5m V,频率扫描范围为10k Hz~1Hz,每组测试采集60个数据点。
时间扫描模式下的电化学阻抗谱测试在0.05V极化条件下进行,正弦波激励信号幅值为5m V,频率扫描范围为10k Hz~50m Hz,每组测试采集70个数据点,每组扫描时间为260s。介质溶液是质量分数为3.5%的NaCl溶液,采用二次蒸馏水与分析纯NaCl配制而成,未经除氧处理,实验在室温(约20℃)下进行。
2 实验结果与讨论
2.1 动电位极化
点蚀电位的判定根据国家标准(GB/T17899—1999)[12]进行,当电流突然增大时,将电流密度为100μA/cm2对应的最正的电位值定义为点蚀电位。图1为304不锈钢在3.5%NaCl溶液中进行动电位扫描时的极化曲线图,扫描速率为1m V·s-1。从图1可以清楚地得到电极材料在介质中的点蚀电位Eb100vsSCE=0.15V,自腐蚀电位EcorrvsSCE=-0.332V,其中-0.2~0.15V处于稳定钝化区,0.15~0.4V 处于过钝化区,所以选取-0.2~0.4V作为动电位电化学阻抗谱测试的电位区间。
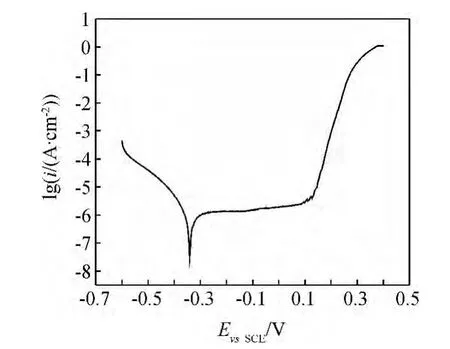
图1 304不锈钢动电位极化曲线Fig.1 Dynamic potential polarization curve of 304 stainless steel
2.2 动电位电化学阻抗谱
图2为304不锈钢在3.5%NaCl溶液中动电位电化学阻抗谱测试结果,从图2中可以发现在-0.2~0V内,阻抗谱Nyquist图中曲线半径随电位的增高逐渐增大,但在0.02V之后阻抗谱半径开始减小,并且在0.1V之后剧烈减小,形状逐渐由弧线变为完整的半圆。
进行动电位电化学阻抗谱测试的同时,采集电化学体系的直流电信号,得到了电流-电位关系图,如图3所示。由图3可知,在0.02V之后,电流开始剧烈波动,表明电极状态开始发生变化;在0.1V之后电流随电位的升高而快速增加,表明稳态点蚀开始出现。结合图2中阻抗谱半径的变化规律可以认为在-0.2~0.02V之间,电极处于稳定的钝化状态;电位为0.02~0.1V时,是亚稳态蚀孔的生长和发展期;0.1V之后,点蚀生长速度随电位的升高而加快,电极处于过钝化状态。从图1中的动电位极化曲线无法获得亚稳态蚀孔生长发展的相关信息,但通过动电位电化学阻抗谱技术就可以研究亚稳态点蚀的形核、发展对电极状态的影响。
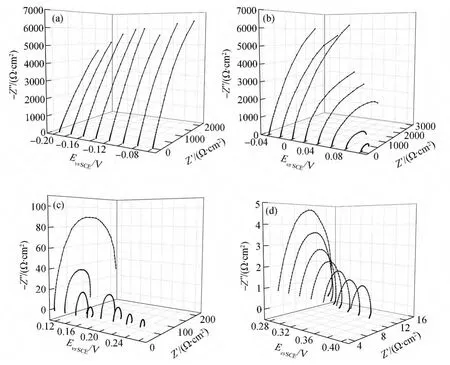
图2 304不锈钢DEIS测试Nyquist图(a)-0.2~-0.06V;(b)-0.04~0.10V;(c)0.12~0.26V;(d)0.28~0.40VFig.2 Nyquist plots of 304 stainless steel during DEIS measurement(a)-0.2--0.06V;(b)-0.04-0.10V;(c)0.12-0.26V;(d)0.28-0.40V
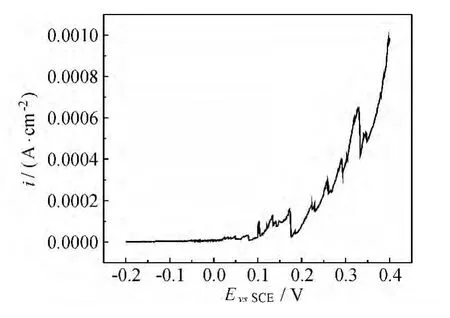
图3 304不锈钢DEIS测试的直流电信号Fig.3 DC signals for 304 stainless steel during DEIS measurement
图4为-0.2 V下获得的阻抗谱的Bode图,从图4中可以明显观察到两个峰,所以电极系统有2个时间常数,这表明电极系统中至少有两个对状态变量响应的弛豫过程[13,14],由此确定动电位电化学阻抗谱的等效电路如图5所示,其中,Rsol是溶液电阻,CPE1是与双电层电容相关的常相位角元件,CPE2是与界面电容相关的常相位角元件,Rt是电荷转移电阻,Rf是钝化膜电阻[6]。由于电极表面的微观不平整,以及不均匀腐蚀造成的微观形貌的改变,会使界面表面存在“弥散效应”,因此使用常相位角元件代替了纯电容,以获得更好的拟合结果[15]。根据图5的等效电路得到的拟合结果误差率均在10%以下。
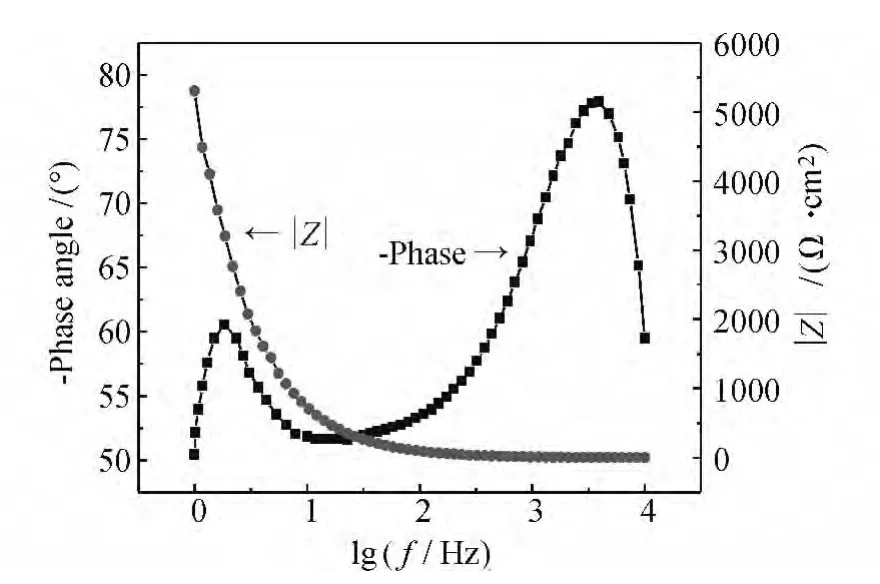
图4 304不锈钢EIS的Bode图Fig.4 Bode plots for EIS of 304 stainless steel
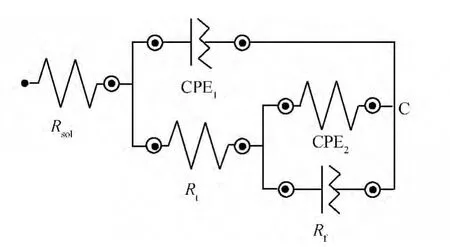
图5 304不锈钢DEIS测试阻抗谱等效电路Fig.5 Equivalent circuit for DEIS of 304 stainless steel
图6是有弥散效应的双电层电容CPE1与电位之间的关系图,由图6可知在0.02 V之前,CPE1的电容值随电压的升高大致呈线性减小,由电容的表达式C=ξ0·ξr/h可知,当介电常数一定时,电容的减小,意味着双电层的厚度增加了。图7为电荷转移电阻Rt与电位之间的关系图,在0.02V之前,Rt随电压的正移呈线性缓慢增大,这也印证了双电层厚度增加了,离子通过双电层到达钝化膜表面的路径增长了。当电位处于0.02~0.1V之间时,可以发现CPE1和Rt的值均产生了很大的波动,说明亚稳态蚀孔的生成和钝化对双电层的电化学特性产生了较大的影响。当电压升高到0.1V之后时,稳态蚀孔开始大量生成,稳定发展的蚀孔处于活化溶解中,此时的双电层由两部分并联组成,一部分是溶液与钝化膜之间的双电层,另一部分为溶液与蚀孔底部活化溶解区域之间的双电层,随着稳态蚀孔的活化生长和其数量的增加,活化溶解区域所占比重越来越大,这就解释了在0.1V之后CPE1随电压增加而线性增加和电荷转移电阻Rt随电压增加而快速减小的现象。同时,Burstein等[16]的相关研究表明在开放的稳态蚀孔的活化溶解区电位值比钝化区更正,因此此处会吸附更多的Cl-,造成Cl-的局部浓缩,使得电化学反应在此处的反应阻力明显降低,所以Rt在0.1 V之后会剧烈减小并趋于稳定。

图6 304不锈钢DEIS测试的CPE1与极化电位的关系Fig.6 Curve of CPE1 and potential for DEIS measurement of 304 stainless steel
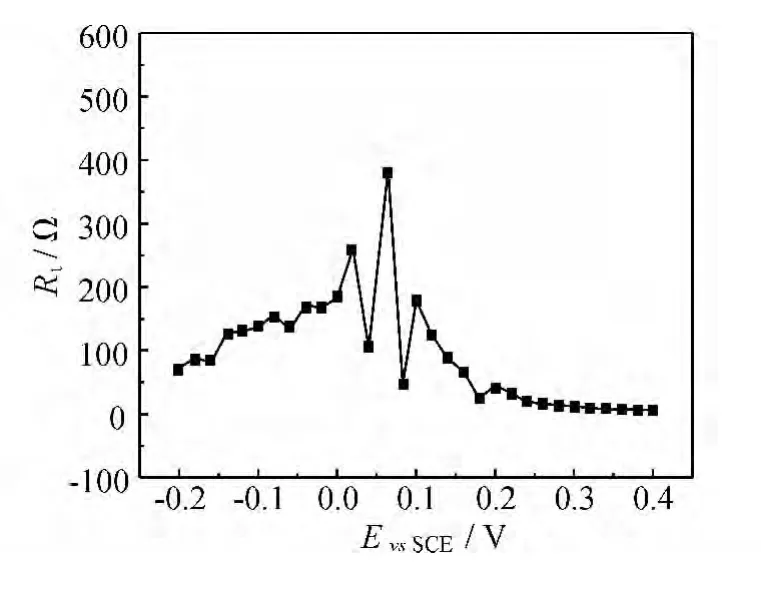
图7 304不锈钢DEIS测试的R t与极化电位的关系Fig.7 Curve of R t and potential for DEIS measurement of 304 stainless steel
图8和图9分别是有弥散效应的钝化膜电容CPE2和钝化膜电阻Rf与电位之间的关系图,从图8,9可知电位在0.02V以下时,CPE2随电位正移而减小,并且近似于线性;钝化膜电阻随电压的升高而线性增大,这表明在亚稳态点蚀发生之前,钝化膜的厚度随电压升高而增加,并且其致密性并未发生明显的改变。在0.02~0.1V的区间内,电极处于亚稳态点蚀阶段,此时CPE2和Rf的值均产生了较为明显的波动,这表明在亚稳态点蚀阶段,钝化膜上存在着破裂和修复的交替过程,这也说明了亚稳态蚀孔的产生与再钝化是随机的,在某一电位下会处于动态平衡当中,随着电位的升高,新点蚀的产生和长大逐渐成为主要过程。在0.1V之后,电极进入稳态点蚀阶段,CPE2开始随电位升高而增大,而钝化膜电阻则随着电位升高而剧烈减小,并且在0.18V之后维持在很小的数值。这是由于钝化膜一旦穿孔且得不到修复,就使得Cl-可以顺利迁移到金属基体,并由于电极电位较正而大量吸附于稳态蚀孔的活性溶解部位,促进了金属的活化溶解,同时阻止了点蚀部位的再钝化。随着时间的推移和电位的升高,钝化膜的厚度在减薄的同时,其完整性也遭到愈发严重的破坏,点蚀活性区域所占比重不断上升,因此产生了CPE2的增大和Rf的剧烈减小。
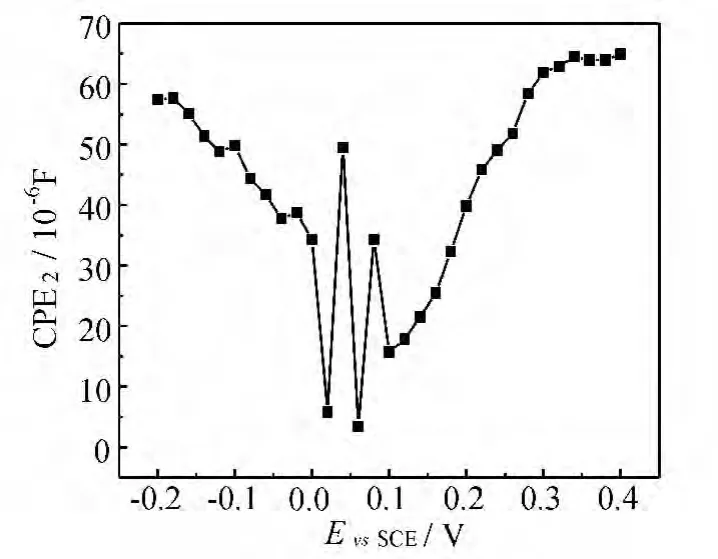
图8 304不锈钢DEIS测试的CPE2与极化电位的关系Fig.8 Curve of CPE2 and potential for DEIS measurement of 304 stainless steel
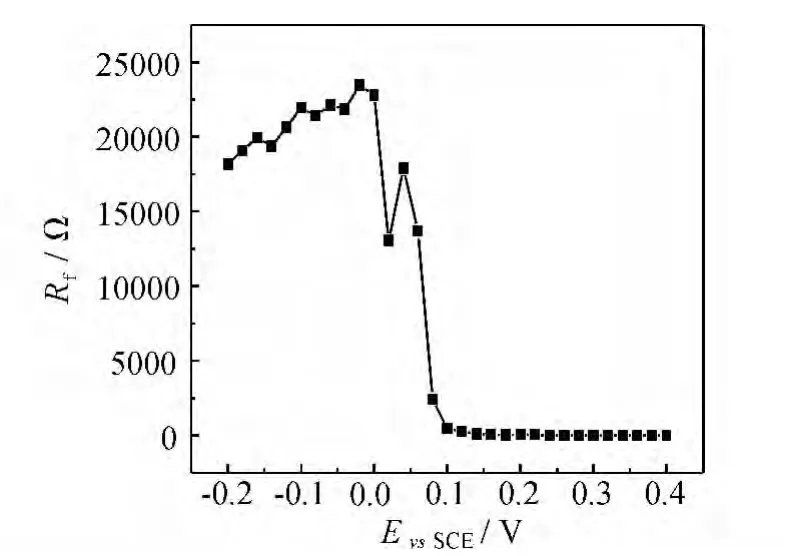
图9 304不锈钢DEIS测试中R f与极化电位的关系Fig.9 Curve of R f and potential for DEIS measurement of 304 stainless steel
2.3 时间扫描电化学阻抗谱
通过动电位电化学阻抗谱的测试,发现在0.02~0.1V的区间内,电极处于亚稳态点蚀阶段,因此在进行时间扫描模式下的电化学阻抗谱测试时,选取0.05V作为测试中的极化电压。图10所示为相应的Nyquist图,图11为在自腐蚀电位下获得的电化学阻抗谱图。通过对比图10和图11可以发现在前520s中,随着极化的进行,Nyquist图中阻抗谱的半径明显减小,但仍表现为明显的容抗弧,此时使用KH-7700型三维数字显微镜观察电极表面,发现并没有明显的蚀点生成,这表明此时钝化膜在均匀减薄。使用图5中的等效电路进行分析,得到了很好的拟合结果,列于表2中。
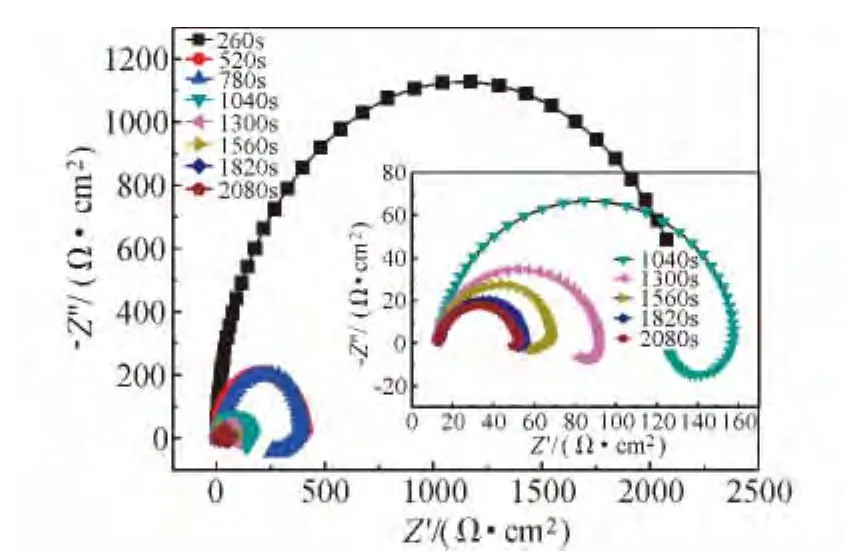
图10 304不锈钢TSEIS测试的Nyquist图Fig.10 Nyquist plots for TSEIS measurement of 304 stainless steel
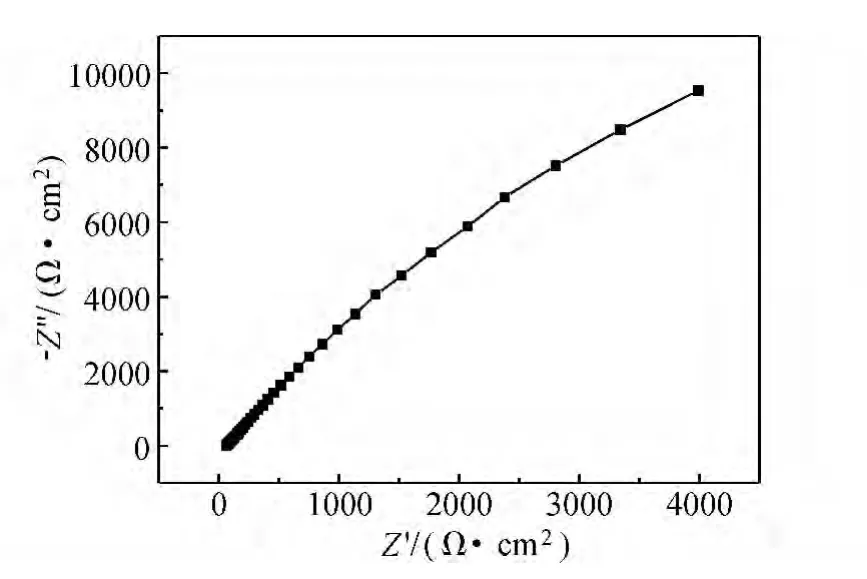
图11 304不锈钢自腐蚀电位下EIS测试Nyquist图Fig.11 Nyquist plot for EIS measurement of 304 stainless steel under corrosion potential
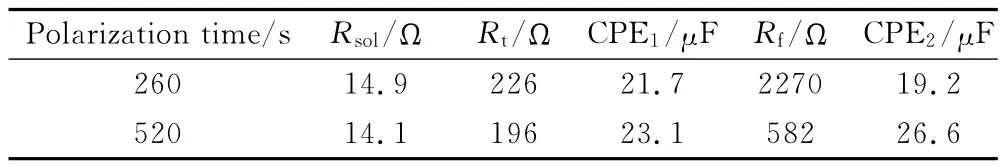
表2 304不锈钢TSEIS测试0~520s的阻抗谱拟合数据Table 2 Fitting data for TSEIS measurement of 304 stainless steel during 0-520s
当极化时间超过780s时,阻抗谱的高频部分仍表现为容抗特征,但低频部分出现了明显的感抗弧,而且随着极化时间的延长,容抗弧的半径明显减小,低频部分的感抗弧则一直存在。曹楚南等[17,18]相关研究指出,当电极表面有点蚀核形成,进入点蚀诱导期时,电化学阻抗谱的Nyquist图中的低频部分会出现感抗成分。感抗响应主要来自于孔蚀诱导期膜厚的变化或吸附膜覆盖率的变化[19]。极化进行到780s之后时,图5的等效电路不再适用,此时使用图12所示的等效电路可得到良好的拟合结果,各元件的参数见表3,其中Rs为溶液电阻,CPE为与界面电容相关的常相位角元素,Rt1为电荷转移电阻,Ro为点蚀发生处与膜的生长溶解相关的电阻,L为蚀形核处与膜厚变化相关的等效电感。
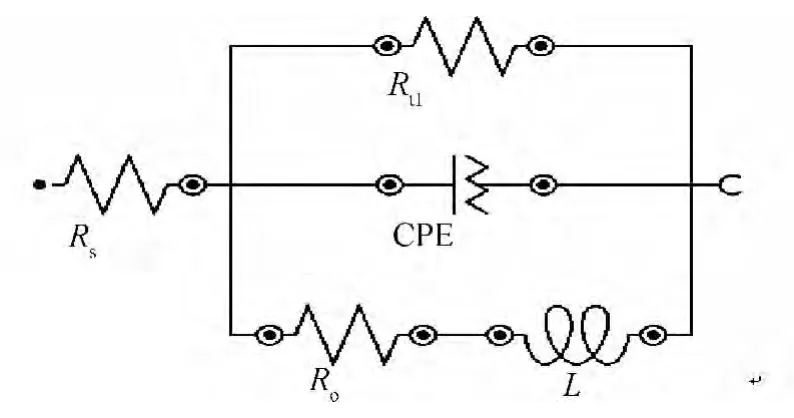
图12 304不锈钢780~2080s TSEIS等效电路Fig.12 TSEIS equivalent circuit of 304 stainless steel during 780-2080s
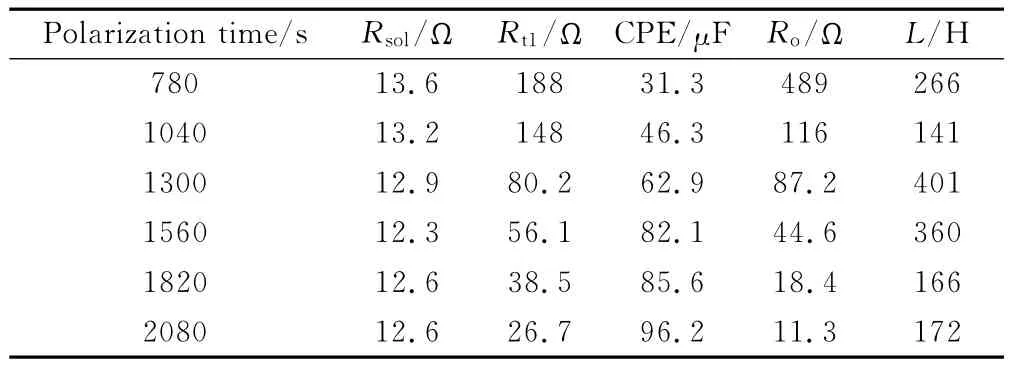
表3 304不锈钢780~2080s TSEIS拟合数据Table 3 TSEIS fitting data of 304 stainless steel during 780-2080s
动电位电化学阻抗谱测试中,也有点蚀的形核,亚稳态蚀孔的生成和钝化,并未出现如时间扫描阻抗谱测试中的电感弧,这是因为在时间扫描模式下,测试的截止频率为50m Hz,远远低于动电位模式下的1Hz的截止频率,而图10中的感抗成分主要来自于1Hz以下的低频响应,所以动电位模式下并未观察到明显的感抗成分。
比较表3中的数据可以发现,电荷转移电阻Rt1随着点蚀的发展而迅速减小,主要是由于钝化膜破裂后,蚀孔处形成了若干Cl-向金属基体迁移的通道,稳定发展的点蚀区域所占比重不断增加。Ro的迅速减小是由于Cl-的聚集,导致蚀孔处的再钝化遭到抑制,亚稳态点蚀向稳定点蚀的转化变得更加容易。虽然点蚀成核变得容易了,但由于稳态蚀孔随极化时间的延长而增加,降低了点蚀成核时产生的响应信号所占的比重,因此电感弧的半径减小。从图10发现,在前520s中并没有电感的产生,这说明只有钝化膜减薄到一定程度时点蚀形核才能发生;在520s以后的极化中,点蚀的形核从未间断,亚稳态蚀孔的出现与再钝化也从未停止,只是由于钝化膜完整度的下降及膜厚的降低,使得亚稳态蚀孔向稳态蚀孔的转化成为了主要过程,所以一直可以观察到电感成分的存在。
3 结论
(1)通过动电位电化学阻抗谱测试发现,亚稳态蚀点对钝化膜的本身结构及双电层中的电化学反应特性具有很大的影响,使其处于剧烈的变化当中,稳定点蚀对上述结构的影响不如亚稳蚀点明显。
(2)亚稳态点蚀阶段,模拟电路中电化学元件参数的剧烈波动,表明了亚稳态蚀点的产生与再钝化是随机的。
(3)时间扫描模式下的电化学阻抗谱测试表明,当钝化膜减薄到一定程度时点蚀的形核才会发生,而且进入稳态点蚀阶段后,亚稳态点蚀的发生与再钝化也从未停止,只是亚稳态点蚀向稳态点蚀的转化成为主要过程。
[1] 桥本政哲(日).不锈钢及其应用[M].北京:冶金工业出版社,2011.226—238.
[2] 杜楠,田文明,赵晴,等.SO24-浓度对304不锈钢在NaCl溶液中点蚀行为影响的研究[J].材料工程,2012,(7):64—70.
DU Nan,TIAN Wen-ming,ZHAO Qing,et al.Effect ofconcentration on the 304 stainless steel pitting corrosion in NaCl solution[J].Journal of Materials Engineering,2012,(7):64—70.
[3] 丁宝峰,吴荫顺,曹备,等.304不锈钢点蚀孔边应力集中的有限元分析[A].第四届全国腐蚀大会论文集[C].北京:中国腐蚀与防护学会,2003.
[4] LI H B,JIANG Z H,YANG Y,et al.Pitting corrosion and crevice corrosion behaviors of high nitrogen austenitic stainless steels[J].Metallurgy and Materials,2009,16(5):517—524.
[5] LI G M,GUO X P,ZHENG J S.Pitting corrosion behavior of stainless steel 304 in carbon diocide journal of environments[J].Iron and Steel Research,2004,11(4):47—51.
[6] JIA Z J,DU C W,LI C T,et al.Study on pitting process of 316L stainless steel by means of staircase potential electrochemical impedance spectroscopy[J].Metallurgy and Materials,2011,18(1):48—52.
[7] DAROWICKI K,KRAKOWIAK S,SLEPSKI P.Evaluation of pitting corrosion by means of dynamic electrochemical impedance spectroscopy[J].Electrochimica Acta,2004,49(17):2909—2918.
[8] NAGARAJAN S,KARTHEGA M,RAJENDRAN N.Pitting corrosion studies of super austenitic stainless steels in natural sea water using dynamic electrochemical impedance spectroscopy[J].Journal of Applied Electrochemistry,2007,37(2):195—201.
[9] 闫瑞霞,杜翠薇,刘智勇,等.敏化态00Cr12Ti的动电位电化学阻抗谱研究[J].中国腐蚀与防护学报,2011,31(6):419—424.
YAN Rui-xia,DU Cui-wei,LIU Zhi-yong,et al.Dynamic electrochemical impedance spectroscopy characteritics of sensitized steel 00Cr12Ti[J].Journal of Chinese Society Corrosion and Protection,2011,31(6):419—424.
[10] 梁成浩,高扬.304不锈钢敏化热处理对耐蚀性的影响[J].化工机械,1995,22(2):87—90.
LIANG Cheng-hao,GAO Yang.Influence of sensibilization heat treatment on corrosion resistance of 304 stainless steel[J].Chemical Engineering & Machinery,1995,22(2):87—90.
[11] 曲炎淼,黄峰,刘静,等.不同组织X80钢点蚀电化学行为研究[A].第五届全国腐蚀大会论文集[C].北京:中国腐蚀与防护学会,2009.
[12] GB/T 17899-1999,不锈钢点蚀电位测量方法[S].
[13] ZHANG G Z,CAI C,CAO F H,et al.Evolution of the electrochemical characteristics during pitting corrosion of pure aluminum in sodium chloride solution[J].Acta Metallurgica Sinica,2005,18(4):525—532.
[14] JAFARZADEH K,SHAHRABIL T,HOSSEINI M G.EIS study on pitting corrosion of AA5083-H321 aluminum-magnesium alloy in stagnant 3.5%NaCl solution[J].Journal of Materials Science,2008,24(2):215—219.
[15] LI W S,LUO J L.Electrochemical investigations on formation and pitting susceptibility of passive films on iron and iron-based alloys[J].International Journal of Electrochemical Science,2007,2(8):627—663.
[16] BURSTEIN G T,LIU C,SOUTO R M,et al.Origins of pitting corrosion[J].Corrosion Engineering Science and Technology,2004,39(1):25—30.
[17] 曹楚南.电化学阻抗谱导论[M].北京:科学出版社,2002.190—194.
[18] 曹楚南.腐蚀电化学原理[M].2版.北京:化学工业出版社,2004.196—201.
[19] 赵卫民,王勇,薛锦,等.镍基合金涂层包覆钢腐蚀失效过程的电化学阻抗谱研究[J].金属学报,2005,41(2):178—184.
ZHAO Wei-min,WANG Yong,XUE Jin,et al.EIS study of the corrosion failure process of steel coated by nickel base alloy[J].Acta Metallurgica Sinica,2005,41(2):178—184.

