益母草化学成分研究Ⅲ*
邓 屾,刘丽丽,陈 玥,李晓霞,王 涛,张 祎
(天津市中药化学与分析重点实验室,天津 300193)
益母草化学成分研究Ⅲ*
邓 屾,刘丽丽,陈 玥,李晓霞,王 涛,张 祎
(天津市中药化学与分析重点实验室,天津 300193)
[目的]继续对益母草(Leonurus japonicus Houtt.)的化学成分进行研究,为进一步开发利用该植物资源提供依据。[方法]采用正相硅胶、反相ODS、Sephadex LH-20等柱色谱及高效液相色谱法等方法进行分离纯化,并通过理化性质及光谱分析鉴定化合物的结构。[结果]从益母草体积分数为50%的乙醇提取物中分离鉴定了7个化合物,分别为(E)-4-hydroxy-dodec-2-enedioic acid(1)、益母草碱(2)、水苏碱(3)、次黄苷(4)、鸟苷(5)、左旋色氨酸(6)、苯丙氨酸(7)。[结论]1、4、5、7为从益母草种中首次分离得到的化合物。
益母草;化学成分;结构鉴定
益母草(Leonurus japonicus Houtt.)又名坤草,为唇形科益母草属1 a或2 a生草本植物,以其地上部分的干燥全草用药。在中国大部分地区均有分布,常生用或熬膏用。中医理论认为益母草苦、辛,微寒,归肝、心包、膀胱经。具有活血调经,利尿消肿,清热解毒的功效。主要用于月经不调,水肿尿少,疮疡肿毒[1]。课题组在对该植物体积分数50%乙醇提取液化学成分的研究过程中,分离得到了7个单体化合物,利用与文献类似的方法对结构进行了鉴定[2-8]。其中,1、4、5、7为从益母草种中首次分离得到的化合物。
1 仪器与材料
安捷伦6520 Q-TOF LC/MS,Bruker 500 MR超导核磁共振波谱仪(TMS为内标,德国Bruker公司)。柱层析硅胶、薄层层析硅胶H(青岛海洋化工厂),薄层色谱硅胶预板、高效色谱用硅胶GF254(天津思利达科技有限公司),ODS(日本Fuji Silisia Chemical公司),Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司),D101大孔吸附树脂(天津海光化工有限公司),Cosmosil 5 C18-MS-II分析柱及制备柱(日本Nacalai Tesque公司)。旋转蒸发仪(德国IKA公司,IKA RV 10、上海亚荣生化仪器厂,RE52CS);高速离心机(美国Beckman Coulter有限公司,ALLEGRA-64R)。
实验所用试剂(色谱纯或分析纯)均天津康科德科技有限公司产品。
所用药材益母草于2009年10月购自安国市场,由天津中医药大学中药标本馆李天祥副教授鉴定为益母草(Leonurus japonicus Houtt.)全草。植物标本存放于天津中医药大学中医药研究中心。
2 提取分离
取益母草干燥全草6.0 kg,粉碎,用9倍量体积分数50%的乙醇溶液加热回流提取3次,每次分别为3、1、1 h,减压回收溶剂,得到浸膏600 g。取浸膏480 g,用氯仿-水萃取,水层经过D101大孔吸附树脂进行梯度洗脱,水、体积分数为70%、95%的乙醇溶液为洗脱液,得到体积分数为70%的乙醇洗脱物75 g,该洗脱物用硅胶柱色谱进行分离,经氯仿-甲醇(100∶0→100∶5,V∶V)→氯仿-甲醇-水(10∶3∶1→7∶3∶1→6∶4∶1,V∶V∶V,下层)甲醇洗脱,得到5个组分(Fr.1~5)。Fraction 2(15.0 g)经ODS柱层析[MeOHH2O(10∶90→20∶80→30∶70→40∶60→50∶50→60∶40→70∶30→100∶0,V∶V)],共得到12个组分[Fr.2-1~12]。Fraction2-3与2-4合并(Fr.2-3+4)后,总样取1.80 g经制备型高效液相色谱法(PHPLC)分离制备[CH3CNH2O(15∶85,V∶V)],得到6个组分(Fr.2-3+4-1~6);Fraction 2-3+4-2经PHPLC再次分离制备 [CH3CNH2O(5∶95,V∶V)],得到苯丙氨酸(7,55.4 mg);Fraction2-3+4-4经制备型高效液相色谱法(PHPLC)再次分离制备 [CH3CN-H2O(6∶94,V∶V)],得到次黄苷(4,22.1 mg);Fraction 2-3+4-5经PHPLC再次分离制备[CH3CN-H2O(7∶93,V∶V)],得到左旋色氨酸(6,21.9 mg)。Fraction 2-9经 PHPLC分离制备[CH3CN-H2O(22∶78,V∶V)],得到9个组分(Fr.2-9-1~9)。Fraction 2-9-6+7经PHPLC分离制备[MeOHH2O(54∶46,V∶V)],得到(E)-4-hydroxy-dodec-2-enedioic acid(1,12.7 mg)。Fraction 3(20.0 g)经PHPLC分离制备 [MeOH-H2O(10∶90→20∶80→40∶60→60∶40→80∶20→100∶0,V∶V)],共得到12个组分(Fr.3~12)。Fraction 3-1经 PHPLC分离制备[CH3CN-H2O(5∶95,V∶V)],得到鸟苷(5,16.8 mg)。Fraction 3-3经ODS柱层析[MeOH-H2O(10∶90→30∶70→40∶60→100∶0,V∶V)]共得到4个组分(Fr.3-3-1~4)。Fraction 3-3-1通过硅胶柱层析[CHCl3-MeOH-H2O(10∶3∶1→7∶3∶1→6∶4∶1,V∶V∶V,下层)→MeOH],得4个组分(Fr.3-3-1-1~4)。Fraction 3-3-1-1经PHPLC分离制备[CH3CN-H2O(10∶90,V∶V)]得到益母草碱(2,25.6 mg)。
取益母草大孔树脂水洗部分干燥粉末(100 g),溶解、过滤后得86.6 g。经强酸性阳离子交换树脂(300 mL,pH=1,2 mol/L NaCl)分离后得到粗生物碱样品7.9 g。样品经Sephadex LH-20处理[MeOHH2O(9∶1,V∶V)]得到纯化后的生物碱2.8 g。最后将纯化后的生物碱经ODS柱层析,用纯水洗脱后,得到水苏碱(3 713.5 mg)。见图1。
3 结构鉴定
化合物1:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 243.130 2[M-H]-,确定其分子式为C12H20O5(calcd for C12H19O5,243.123 8)。1HNMR(CD3OD,500 MHz)δ:5.86(1H,d,J=15.5 Hz,H-2),6.77(1H,dd,J=1.0、15.5 Hz,H-3),4.12(1H,m,H-4),1.44(2H,m,H-5),1.25(8H,m,H-6~9),1.48(2H,m,H-10),2.19(2H,t,J=7.0 Hz,H-11)。13CNMR(CD3OD,125 MHz)δ:167.4(C-1),119.8(C-2),151.6(C-3),69.1(C-4),36.1(C-5),24.7(C-6),28.7(C-7),28.4(C-8),28.6(C-9),24.4(C-10),33.6(C-11),174.5(C-12)。上述1H-NMR和13C-NMR谱数据与参考文献[9]中报道的(E)-4-hydroxy-dodec-2-enedioic acid的数据基本一致,故鉴定化合物1为(E)-4-hydroxy-dodec-2-enedioic acid。
化合物2:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 310.140 1[M-H]-,确定其分子式为C14H21N3O5(calcd for C14H20N3O5,310.140 8)。1H-NMR(CD3OD,500 MHz)δ:2.27(2H,t,J=7.0 Hz,H-3),1.75(2H,m,H-4),1.85(1H,m,H-5),4.33(2H,t,J=6.5 Hz,H-6),7.32(2H,s,H-2′,6′),3.90(6H,s,3′,5′-OCH3)。13C-NMR(CD3OD,125 MHz)δ:158.7(C-1),42.2(C-3),26.6(C-4),27.1(C-5),65.8(C-6),119.8(C-1′),108.2(C-2′,6′),149.3(C-3′,5′),144.6(C-4′),168.5(C-7′),56.9(3′,5′-OCH3)。上述1H-NMR和13C-NMR谱数据与参考文献[10]中报道的益母草碱的数据基本一致,故鉴定化合物2为益母草碱(leonurine)。
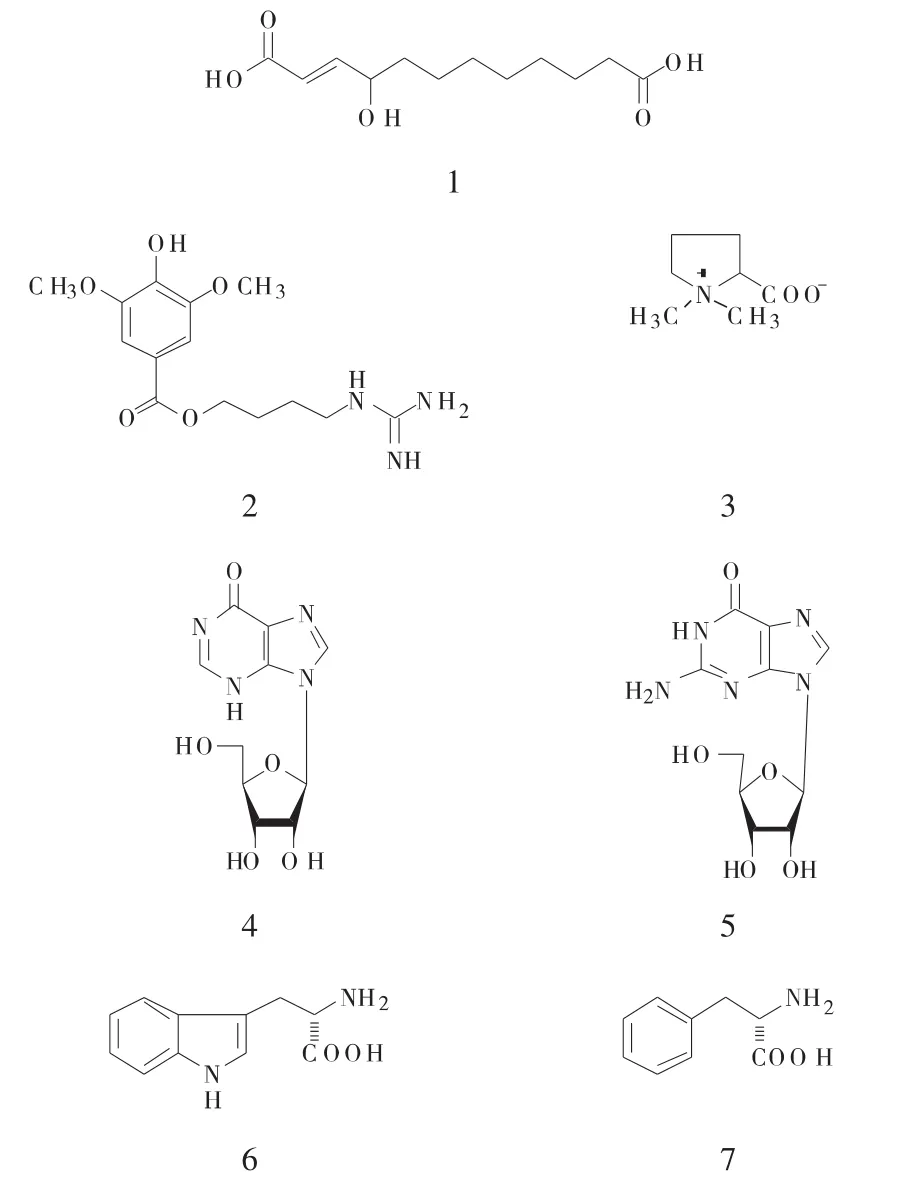
图1 益母草中分离得到的化合物
化合物3:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 178.062 7[M+Cl]-,确定其分子式为C7H13NO2(calcd for C7H13NO2Cl,178.064)。1H-NMR(CD3OD,500 MHz)δ:4.55(1H,dd,J=9.0、10.5 Hz,H-2),[2.44(1H,m),2.61(1H,m),H2-3)],2.23(2H,m,H2-4),[3.67(1H,br.dd,ca.J=10、12 Hz),3.81(1H,ddd,J=3.5、8.5、11.5 Hz),H2-5],3.20(3H,s,1-NCH3),3.40(3H,s,1-NCH3)。13C-NMR(CD3OD,125 MHz)δ:74.6(C-2),25.9(C-3),19.9(C-4),69.0(C-5),168.4(C-6),52.9(1-NCH3),46.9(1-NCH3)。上述1H-NMR和13C-NMR谱数据与参考文献[11]中报道的水苏碱的数据基本一致,故鉴定化合物3为水苏碱(stachydrine)。
化合物4:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 267.074 3[M-H]-,确定其分子式为C10H12N4O5(calcd for C10H11N4O5,310.140 8)。1H-NMR(DMSO-d6,500 MHz)δ:8.14(1H,s,H-2),8.35(1H,s,H-8),5.89(1H,d,J=6.0 Hz,H-1′),4.15(1H,t,J=6.0 Hz,H-2'),4.62(1H,t,J=6.0 Hz,H-3′),3.98(1H,m,H-4′),[3.56(1H,dd,J=3.0、12.0 Hz),3.67(1H,dd,J=3.0、12.0 Hz),H2-5′]。13C-NMR(DMSO-d6,125 MHz)δ:152.3(C-2),149.0(C-4),156.0(C-6),139.8(C-8),87.8(C-1′),70.6(C-2′),73.4(C-3′),85.8(C-4′),61.6(C-5′)。上述1H-NMR和13C-NMR谱数据与参考文献[12]中报道的次黄苷的数据基本一致,故鉴定化合物4为次黄苷(hypoxanthine-9-β-D-ribofuranoside)。
化合物5:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 282.083 8[M-H]-,确定其分子式为C10H13N5O5(calcdforC10H12N5O5,282.0844)。1H-NMR(DMSO-d6,500 MHz)δ:7.93(1H,br.s,H-8),5.70(1H,d,J=5.5 Hz,H-1′),4.07(1H,t,J=5.5 Hz,H-2′),4.40(1H,t,J=5.5 Hz,H-3′),3.87(1H,m,H-4′),[3.52(1H,dd,J=3.0、12.0 Hz),3.61(1H,dd,J= 3.0、12.0 Hz),H2-5′]。13C-NMR(DMSO-d6,125 MHz)δ:153.6(C-2),151.2(C-4),116.6(C-5),156.7(C-6),135.5(C-8),86.2(C-1′),70.2(C-2′),73.5(C-3′),85.1(C-4′),61.3(C-5′)。上述1H-NMR和13CNMR谱数据与参考文献[13]中报道的鸟苷的数据基本一致,故鉴定化合物5为鸟苷(guanosine)。
化合物6:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 203.082 3[M-H]-,确定其分子式为C11H12N2O2(calcdforC11H11N2O2,203.0826)。1H-NMR(DMSO-d6,500 MHz)δ:7.26(1H,br.s,H-2),7.59(1H,d,J=8.0 Hz,H-5),6.96(1H,dd,J=8.0、8.0 Hz,H-6),7.05(1H,dd,J=8.0、8.0 Hz,H-7),[3.05(1H,dd,J=8.5、15.0 Hz),3.33(1H,dd,J=3.0、15.0 Hz),H2-10],3.57(1H,dd,J=3.0、8.5 Hz,H-11)。13C-NMR(DMSO-d6,125 MHz)δ:124.2(C-2),109.2(C-3),118.1(C-4),120.7(C-5),118.3(C-6),111.3(C-7),26.9(C-8),54.6(C-9),127.2(C-4′),136.2(C-7′)。上述1H-NMR和13C-NMR谱数据与参考文献[14]中报道的左旋色氨酸的数据基本一致,故鉴定化合物6为左旋色氨酸(L-tryptophan)。
化合物7:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 164.070 5[M-H]-,确定其分子式为C9H11NO2(calcd for C9H10NO2,164.017 1)。1H-NMR(CD3OD,500MHz)δ:3.97(1H,dd,J=5.0、8.0Hz,H-2),[3.11(1H,dd,J=8.0、14.0 Hz),3.29(1H,dd,J= 5.0、14.5 Hz),H2-3)],7.32(2H,br.d,ca.J=8 Hz,H-5,9),7.41(2H,br.d,ca.J=8 Hz,H-6,8),7.37(1H,m,H-7)。13C-NMR(CD3OD,125 MHz)δ:174.8(C-1),57.1(C-2),37.5(C-3),136.2(C-4),130.4(C-5,9),130.1(C-6,8),128.7(C-7)。上述1H-NMR和13CNMR谱数据与参考文献[15]中报道的苯丙氨酸的数据基本一致,故鉴定化合物7为苯丙氨酸(phenylalanine)。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2010:272-273.
[2]吴 帅,刘二伟,张 祎,等.川续断中化学成分的研究[J].天津中医药大学学报,2010,29(3):147-150.
[3]吴克磊,康利平,熊呈琦,等.蒺藜全草中甾体皂苷类化学成分研究[J].天津中医药大学学报,2012,31(4):225-228.
[4]张 琳,蔡晓菡,高慧媛,等.益母草化学成分的分离与鉴定[J].沈阳药科大学学报,2009,26(1):15-18.
[5]张 祎,邓 屾,李晓霞,等.益母草化学成分的分享鉴定Ⅱ[J].中国药物化学杂志,2013,23(6):480-485.
[6]刘丽丽,李晓霞,陈 玥,等.槐米化学成分研究[J].天津中医药大学学报,2014,33(4):230-233.
[7]刘丽丽,李晓霞,陈 玥,等.槐米中酚酸类化学成分研究[J].天津中医药大学学报,2014,33(1):39-41.
[8]王 强,张 祎,韩立峰,等.中药川续断化学成分的研究Ⅲ[J].天津中医药大学学报,2014,33(2):108-111.
[9] Song CZ,Wang YH,Hua Y,et al.Chemical constituents of Clematis montana[J].中国天然药物,2008,6(2):116-119.
[10]丛 悦,王金辉,郭洪仁,等.益母草化学成分的分离与鉴定Ⅱ[J].中国药物化学杂志,2003,13(6):349-352.
[11]何黎琴,王效山.水苏碱的合成[J].化学世界,2005,5:296-298.
[12]黄伟晖,宋纯清.当归化学成分研究[J].药学学报,2003,38 (9):680-683.
[13]苏东敏,唐文照,庾石山,等.棒锤瓜化学成分研究[J].中国中药杂志,2012,37(11):1593-1596.
[14]徐方方,范春林,王 磊,等.枳椇子的化学成分[J].暨南大学学报:自然科学版,2011,32(3):304-306.
[15]彭 燕,刘永宏.黄海海燕的化学成分研究[J].中国药学杂志,2011,46(24):1883-1885.
Study on chemical constituents of Leonurus japonicus Houtt.Ⅲ
DENG Shen,LIU Li-li,CHEN Yue,LI Xiao-xia,WANG Tao,ZHANG Yi
(Key Laboratory of Traditional Chinese Medicinal Chemistry and Ana lytical Chemistry of Tianjin, Tianjin 300193,China)
[Objective]To investigate the chemical components of the herb Leonurus japonicus Houtt.Ⅲ.[Methods]The chemical components were obtained by chromatographies,such as silica gel,ODS,Sephadex LH-20 and HPLC.They were identified by the chemical and physical methods,especially spectral analysis.[Results]Seven compounds were obtained and identified as(E)-4-hydroxy-dodec-2-enedioic acid(1),leonurine(2),stachydrine(3), hypoxanthine-9-β-D-ribofuranoside (4),guanosine (5),L-tryptophan (6),and phenylalanine (7),respectively.[Conclusion]Compounds 1,4,5,and 7 are the obtained species firstly.
Leonurus japonicus Houtt.;chemical component;structural elucidation
R284
:A
:1673-9043(2014)06-0362-04
2014-07-11)
10.11656/j.issn.1673-9043.2014.06.12
国家自然基金项目(81202995);国家科技重大专项项目-重大新药创制(2011ZX09307-002-01);新世纪优秀人才支持计划资助(NCET-12-1069,NCET-10-0958)。
邓 屾(1988-),男,硕士,主要从事中药化学研究。
张 祎,E-mail:zhwwxzh@263.net。

