抗宫炎凝胶剂的定性鉴别
刘 玠 曲海影 张 迪
1.黑龙江中医药大学研究生学院,黑龙江哈尔滨 150040;2.哈尔滨医科大学附属第四医院静脉用药调配中心,黑龙江哈尔滨 150001
抗宫炎凝胶剂由广东紫珠、益母草、乌药三味中药组成[1],是在抗宫炎片的基础上研制的现代中成药[2],抗宫炎片现收录于《中国药典》2010 年版一部[3],用于慢性宫颈炎引起的湿热下注、赤白带下、宫颈糜烂、出血症等[4]。 慢性宫颈炎是女性生殖系统最为常见的炎症性疾病,多由急性宫颈炎治疗不彻底转化而来[5],该病在已婚或有性生活的妇女中发病率高达50%以上,且是宫颈癌发病的高危因素之一[6],其治疗方法有物理疗法、手术疗法和药物疗法[7],其中药物疗法因属非创伤性治疗,操作简单,对患者要求低而应用广泛[8]。在药物治疗中,与抗宫炎片相比,抗宫炎凝胶剂直接作用于病灶[9],不需要通过肝脏首过作用和胃肠道生理关卡效应[10],因而不会降低其病灶部位的有效浓度,也不会延长其起效时间及降低药物的疗效[11]。 而且抗宫炎凝胶剂与阴道黏膜具有良好的偶合和水合作用,可较长时间与病灶部位黏附紧密,能充盈整个阴道[12],有较好的生物相容性,有利于药物的释放,能更好地发挥疗效[13-14],在中药新药研制中,几乎所有的新药都必须提供定性鉴别的分析。薄层色谱技术和高效液相色谱技术在中药成药的定性鉴别中均是最常用的方法,均具有良好的专属性、可比性及较高的灵敏度,依据高效液相色谱中色谱峰的位置以及薄层色谱板上斑点的有无、颜色、位置来判定中成药所含原料药物的真伪,同时其斑点的大小、颜色的深浅亦可在一定程度上直接反映出所用原料药材的优劣。采用高效液相色谱分析技术和薄层色谱分析与其他色谱分析相比,二者显著不同的是得到的图谱是直观性很强的图像。为此,本研究决定改变原制剂的给药途径,将抗宫炎片改为抗宫炎凝胶剂,从新药研究角度出发,参照《中国药典》2010 年版一部抗宫炎片下的规定,采用高效液相色谱法(HPLC)和薄层色谱法(TLC)对抗宫炎凝胶剂处方中主要药味进行定性鉴别,旨在为制订其质量标准奠定基础,为慢性宫颈炎及宫颈糜烂的临床治疗提供更多的基础。
1 仪器与试药
1.1 仪器
高效液相色谱仪(Waters 1525-2489);METTLER AE 200 电子天平(梅特勒托利多仪器公司);AB204-N 电子分析天平(梅特勒托利多仪器公司);指针式电热恒温水浴锅(上海跃进医疗器械厂);KQ-500DB 超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药
盐酸水苏碱对照品(批号:110712-201111,中国药品生物制品检定所);乌药醚内酯对照品(批号:111568-200603,中国药品生物制品检定所);金石蚕苷对照品(批号:111812-201001,中国药品生物制品检定所);乌药对照药材(批号:121096-201004,中国药品生物制品检验所);抗宫炎凝胶剂(自制,批号:20110901、20110902、20110903)。
2 方法与结果
2.1 TLC 鉴别
2.1.1 益母草TLC 鉴别
取抗宫炎凝胶剂1 支(5.00 g),加入甲醇溶液50 mL使药物溶解,将溶解的药物溶液超声处理30 min,将超声处理后的溶液全部滤过,滤液蒸干,所得的残渣加入乙醇溶液1 mL 使其溶解,即可以得到抗宫炎凝胶剂供试品溶液。 另取适量的盐酸水苏碱对照品,加适量乙醇溶液制成1 mL 含2 mg 的溶液,即可作为益母草对照品溶液。 按照上述的处方比例,使用相同的方法制成益母草阴性对照品溶液,照薄层色谱法(附录ⅥB)试验,吸取抗宫炎凝胶剂供试品溶液和益母草阴性对照品溶液各2 μL 以及益母草对照品溶液4 μL,后分别点于同一硅胶G 薄层板上,以丙酮-无水乙醇-盐酸(10∶6∶1)为本品所用的展开剂,将薄层色谱板放入展开缸内完全展开后取出,晾干,先喷以10%硫酸乙醇溶液,再喷以新配制的稀碘化铋钾试液-碘化钾碘试液(1∶1)混合液,后冷风吹干,结果供试品色谱中,在与对照品色谱相应位置上,显相同颜色的斑点,且阴性对照无干扰,见图1。

图1 益母草薄层色谱法
2.1.2 乌药TLC 鉴别
取抗宫炎凝胶剂1 支(5.00 g),加入甲醇溶液25 mL使药物溶解,所得的甲醇溶液水浴加热回流30 min后将溶液滤过,滤液蒸干,将得到的药物残渣加蒸馏水20 mL,所得药物溶液加热使溶解,用三氯甲烷溶液连续振摇提取2 次,每次均用20 mL 的三氯甲烷溶液,合并三氯甲烷提取液,将提取液蒸干,所得残渣加乙酸乙酯1 mL 使其溶解,即可得到抗宫炎凝胶剂供试品溶液。另精密量取乌药对照药材2 g,加入蒸馏水50 mL,煎煮30 min,所得的全部溶液滤过,滤液离心,取得到的上清液浓缩至20 mL,用三氯甲烷溶液振摇提取2 次,每次均用20 mL 的三氯甲烷溶液,合并三氯甲烷提取液,将提取液蒸干,所得的残渣加乙酸乙酯1 mL 使溶解,制成乌药对照药材溶液。另精密量取乌药醚内酯对照品,加乙酸乙酯溶液适量制成每1 毫升含2 mg 的溶液,作为乌药对照品溶液,按照原处方比例,同法制成乌药阴性对照品溶液。 照薄层色谱法(附录ⅥB)试验,分别吸取抗宫炎凝胶剂供试品溶液16 μL、乌药对照药材溶液4 μL、乌药对照品溶液1 μL,以及乌药阴性对照品溶液1 μL 后分别点于同一硅胶G 薄层板上,以甲苯-乙酸乙酯(15∶1)为展开剂,将薄层色谱板放入展开缸内完全展开后取出,晾干,喷以1%香草醛硫酸试液,用冷风吹干。 日光检视,在供试品色谱中,分别在与对照药材、对照品色谱相应位置上,显相同颜色的斑点,阴性对照无干扰,见图2。
2.2 HPLC 定性鉴别
2.2.1 色谱条件
色谱柱:以十八烷基硅烷键合硅胶为填充剂;流动相:乙腈-0.5%磷酸(18∶82);检测波长:332 nm;流速:1.0 mL/min;理论板数按金石蚕苷峰计算应不低于3000。

图2 乌药薄层色谱法
2.2.2 溶液的制备
2.2.2.1 供试品制备方法的考察 ①超声:称取抗宫炎凝胶剂供试品5.00 g,将药物置于圆底烧瓶中,精密吸取50%甲醇溶液50 mL,将溶液超声处理60 min后所得溶液转移至50 mL 容量瓶中,用适量50%甲醇溶液洗涤锥形瓶,洗液并入容量瓶,用50%甲醇溶液定容,摇匀,过滤,取续滤液用微孔滤膜(0.45 μm)滤过,作为抗宫炎凝胶剂的供试品溶液。②水浴回流:称取抗宫炎凝胶剂供试品5.00 g, 置圆底烧瓶中,精密加入50%甲醇溶液50 mL 后,精密称定溶液重量,水浴加热回流1 h 后,所得溶液放冷,再精密称定溶液重量,用50%甲醇溶液补足减失溶液的重量,摇匀,溶液过滤,取续滤液用微孔滤膜(0.45 μm)将其滤过,即可以得到抗宫炎凝胶剂供试品溶液。 ③测定法:分别精密吸取金石蚕苷对照品溶液10 μL 与上述两种抗宫炎凝胶剂供试品溶液各5 μL,注入液相色谱仪,测定、记录色谱图。结果显示,加热回流提取的效果明显优于超声提取,故本实验选用加热回流提取方法。见表1。

表1 供试品制备提取时间及方法筛选
2.2.2.2 提取时间的选择 取抗宫炎凝胶剂5.00 g 3 份,精密称定药物的重量,3 份药物分别置圆底烧瓶中,精密加入50%甲醇溶液50 mL, 精密称定溶液重量,将3 份药物溶液分别用水浴加热回流提取0.5、1、1.5 h后放冷,再精密称定溶液重量,用50%甲醇溶液补足减失的重量,摇匀,过滤,取续滤液用微孔滤膜(0.45 μm)滤过,作为抗宫炎凝胶剂供试品溶液。并按拟定的色谱条件测定。通过比较超声与加热回流提取方法与选择提取时间的试验,优化了供试品制备的条件,确定了样品处理方法:精密称取供试品5.00 g,将药物置于圆底烧瓶中,精密加入50%甲醇溶液50 mL,称定溶液重量,用水浴加热回流1 h 后放冷,再称定溶液重量,用50%甲醇补足减失的重量,摇匀,过滤,取续滤液用微孔滤膜(0.45 μm)滤过,作为供试品溶液。 见表1。
2.2.2.3 溶液的制备 ①对照品溶液的制备:精密称取适量的金石蚕苷对照品,加入50%色谱甲醇溶液制成每1 毫升含金石蚕苷约0.156 mg 的对照品溶液。 ②供试品溶液的制备:取抗宫炎凝胶剂样品5.00 g,精密称定其重量,将药物置于锥形瓶中,精密加入50%甲醇溶液50 mL,称定溶液重量,水浴加热回流1 h,放冷,再称定溶液重量,用50%甲醇溶液补足减失的重量,摇匀,滤过,取续滤液用微孔滤膜(0.45 μm)滤过,作为供试品溶液。
2.2.3 测定法
分别精密吸取对照品溶液10 μL 与供试品溶液5 μL 注入液相色谱仪,测定和记录色谱图,结果广东紫珠在供试品色谱中呈现出与对照品色谱中保留时间相同的金石蚕苷色谱峰(t = 5.51 min),见图3、4。
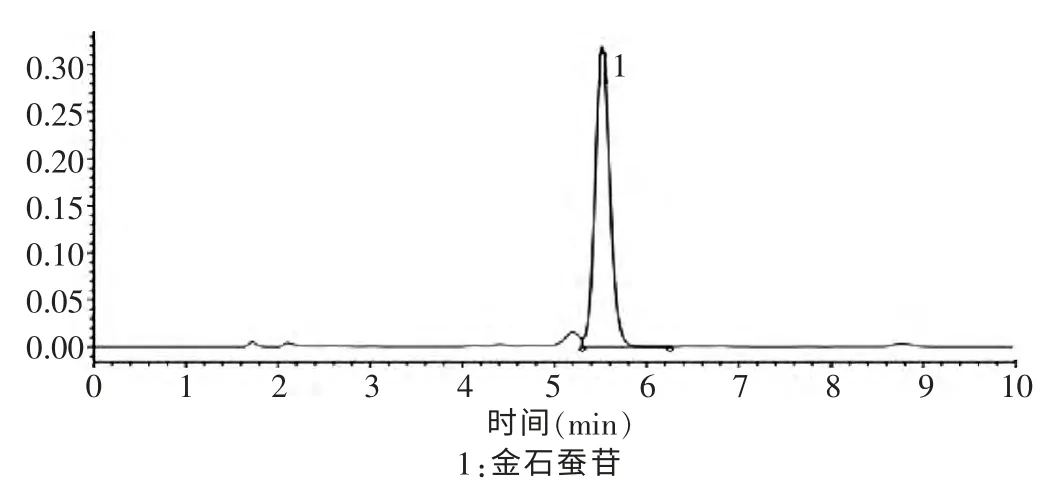
图3 金石蚕苷对照品高效液相色谱图
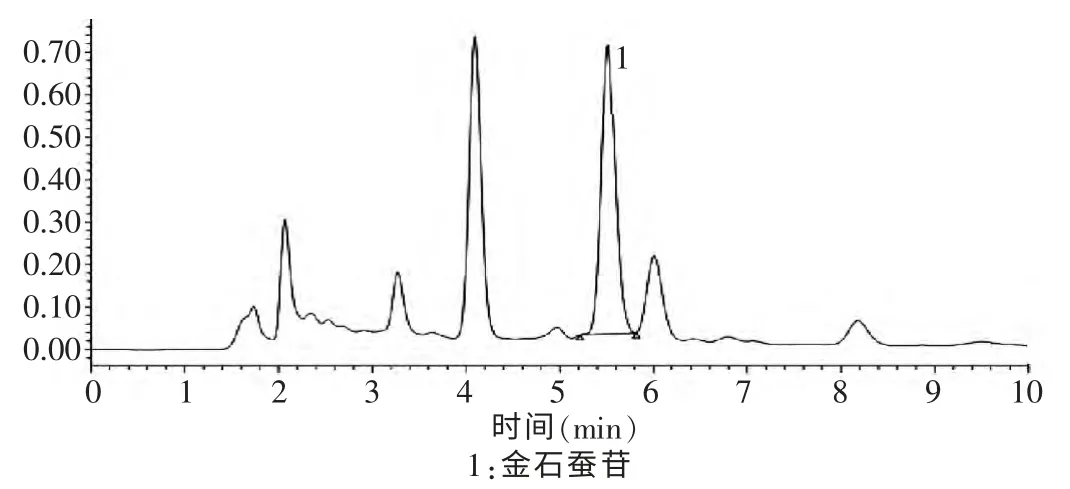
图4 抗宫炎凝胶剂供试品高效液相色谱图
3 讨论
3.1 薄层色谱定性鉴别研究
本实验探讨了抗宫炎凝胶剂成品中主要成分乌药、益母草的薄层色谱定性鉴别研究,结果表明,薄层色谱中具有益母草和乌药的显著鉴别特征,各检出成分不受处方中其他药的干扰,方法稳定,斑点清晰,可作为抗宫炎凝胶剂的有效定性鉴别方法。
3.2 高效液相定性鉴别研究
3.2.1 供试品制备方法考察
本实验探讨了超声提取法和加热回流提取法两种方法,根据结果显示加热回流提取的效果明显优于超声提取,故本实验选用加热回流提取方法。
3.2.2 提取时间的选择
本实验分别考察了加热回流提取0.5、1、1.5 h,结果表明提取时间为1 h 时,样品的含量最高,故本实验采取回流1 h 的提取时间,最终确定样品的最佳提取工艺为加热回流1 h。
3.3 研究意义
抗宫炎凝胶剂作为治疗慢性宫颈炎外用药新剂型[15],是近几年局部用药的研究热点[16],应用于阴道给药的凝胶主要为水溶性凝胶[17-18],具有与吸附处的黏膜紧密结合,具有制备工艺简单、形状美观、易于涂布使用、易清洗、不污染衣物、稳定性较好等特点[19-20],因患者使用无异物感,顺应性强,能充盈整个阴道[21],是阴道给药治疗宫颈疾病的一种理想剂型。所以抗宫炎凝胶剂临床疗效好,尤其与物理治疗、手术治疗相结合使用时,对慢性宫颈炎的治愈率更高,本研究为治疗妇科疾病临床用药的剂型发展开辟了新道路。
综上所述,本研究对抗宫炎凝胶剂成品中的主要成分广东紫珠进行的高效液相定性鉴别研究,结果表明,广东紫珠在供试品色谱中呈现出与对照品色谱中保留时间相同的色谱峰,所以本方法可作为抗宫炎凝胶剂的有效鉴别方法。
[1] 孙雅平.抗宫炎软胶囊联合金刚藤颗粒应用于治疗慢性盆腔炎疗效观察[J].新中医,2014,46(6):133-134.
[2] 杨燕玲.应用利普刀治疗慢性宫颈炎的临床疗效观察[J].中国医药导报,2012,9(3):61-62.
[3] 国家药典委员会.中国药典[S].北京:中国医药科技出版社,2010.
[4] 孔令芳.宫颈糜烂应用宫颈炎康栓加微波及抗宫炎片治疗的临床分析[J].中国实用医药,2013,24(8):172-173.
[5] 孔爱姣.中药内服外用治疗慢性宫颈炎临床观察[J].中国医药导报,2010,7(6):94.
[6] 林川,熊希,杨君,等.慢性宫颈炎定义与治疗方法的历史沿革[J].临床医学,2010,18(9):1330-1332.
[7] 李琳.慢性宫颈炎的治疗进展[J].中国医药指南,2013,11(9):67-68.
[8] 刘玠,翟春梅,褚利娟.中药凝胶剂在宫颈炎中的应用进展[J].中医药学报,2011,39(5):88-90.
[9] 孙淑花.中西医结合治疗慢性宫颈炎的临床效果分析[J].中国现代药物应用,2014,8(7):144-145.
[10] 钟雪.慢性宫颈炎治疗新进展[J].基层医学论坛,2014,18(4):516-518.
[11] 刘玠,韩雪,席珊珊.治糜灵凝胶剂制备工艺研究[J].中成药,2010,32(10):1822-1823.
[12] 刘玠,褚丽娟.治糜灵凝胶剂提取工艺研究[J].中医药信息,2011,28(2):36-37.
[13] 洪燕龙.妇炎康泡腾片的制剂工艺,质量标准和广东紫珠化学成分的研究[D].北京:北京中医药大学,2010.
[14] 张青青,蓝日春,黄锦威,等.壮药香花护乳凝胶剂提取工艺的研究[J].广西医科大学学报,2013,30(5):667-668.
[15] 谢谊,李跃辉,唐纯玉,等.HPLC 法测定喉咽清口服液中齐墩果酸的含量[J].中国医药导报,2014,11(20):110-113.
[16] 李智红.中西医治疗慢性宫颈炎进展[J].实用中医药杂志,2010,26(6):443-444.
[17] 杨柳,王爱武,刘帅.凝胶剂研究概况及临床应用[J].辽宁中医药大学学报,2014,16(7):147-149.
[18] 朱占永,余墨声,刘思洋,等.蝎肽抗菌凝胶对痤疮丙酸杆菌的抑制作用[J].中国医药导报,2014,11(4):43-45.
[19] 邱璐.慢性宫颈炎的预防与治疗[J].中国医药指南,2014,12(14):398-399.
[20] 祁丽亚.宫颈炎病原学及影响因素探讨[J].中国妇幼保健,2014,29(6):855-856.
[21] 郭红叶,伊博文,闫小平,等.新型辅料卡波姆在凝胶剂中应用现状[J].中国实验方剂学杂志,2013,19(17):371-374.

