臭氧对剩余污泥的破解效果研究*
史锦芳,金 辉,游思琴,李 彪
(1.中山大学环境科学与工程学院,广东 广州510275;2.广东省环境污染控制与修复技术重点实验室,广东 广州 510275)
剩余污泥的处理已成为城市污水处理厂面临的一个重要的问题,各种减量化技术备受人们关注。目前,国内外研究者采用了各种物理(热预处理、微波预处理、超声波预处理、机械预处理)、化学(碱预处理、臭氧预处理)和生物法(酶预处理)对污泥进行减量化。
金瑞洪等[1]研究发现臭氧具有强的氧化性,不仅能破坏细胞壁,释放出细胞中易降解的有机物,同时还能将难降解的大分子物质分解为易降解的小分子物质,从而提高污泥的破解效果,是一种有效对污泥中细胞的破裂和溶解的方法。 何楚茵等[2-4]的研究也表明直接利用臭氧对剩余污泥进行处理,可获得良好的减量化效果。因此将臭氧用于剩余污泥的破解,是一种行之有效且有着良好前景的新工艺。欧洲许多国家都有将臭氧应用于污泥的处理中,而我国才刚刚起步,应用还不够普遍。目前仍待解决的问题主要有臭氧设备成本高、寿命较短、操作条件有待优化等。
为探讨臭氧对剩余污泥的溶胞技术,优化臭氧处理污泥的条件,实验对不同臭氧投加时间下污泥溶胞效果和破解机理进行研究,并探索臭氧对污泥量和污泥形态的改变。
1 材料与方法
1.1 材料
试验用剩余污泥采自广州市沥滘污水处理厂二沉池的回流管路上,污泥呈黑褐色,在显微镜观察下有大量原生生物,菌胶团结构紧密,初始污泥浓度10.8 g/L。
取样后装入塑料桶内,并于4 ℃下储存到冰箱内,实验时间均控制在3 d内完成。实验各指标各设三组平行样。
臭氧发生器采用武汉康桥环保设备有限公司所生产的ECO-09100型电解式臭氧发生器,利用质子交换聚合物膜电解法(PEM)电解母液(电导率≤5 μS/cm)来制备臭氧和氧气混合气体,常规下臭氧浓度可达20%。当室温为25 ℃时,经碘量法测定臭氧浓度,臭氧的最大产量为4.8 g/h。
1.2 实验装置与方法
臭氧处理污泥的实验流程如图1所示,臭氧发生器电解母液产生臭氧,经微型气泵增压(微型气泵流量为4 L/s),通入臭氧反应器,尾气用碘化钾溶液吸收。实验通过控制臭氧破解时间来控制臭氧浓度.处理完成后,取适量臭氧处理后的污泥进行处理并分析测定其中蛋白质的含量、UV254值、pH,观察污泥形态和污泥粒径。

图1 实验流程图Fig.1 Schematic diagram of the test1,臭氧发生器;2,微型气泵;3,臭氧反应器;4,尾气收集装置
1.3 测定方法
pH值测定方法:用上海精密科学仪器有限公司所生产的pH计(pHSJ-3F)测定。
蛋白质测定方法:取适量破解后的污泥混合液10 000 r/min离心30 min,取其上清液,采用考马斯亮蓝法测定蛋白质的值。
UV254的测定:采用紫外分光光度计测定上清液在254 nm下的吸光度。
污泥形态观察:吸取适量污泥样品,均匀分布在显微镜载玻片上,放大倍数为 100 倍,在 Nikon Eclipse 50i上观察,拍照絮体结构。
污泥的粒径测定方法:采用 LS-POP(Ⅲ)激光粒度分析仪(珠海欧美克公司)测定,粒径结果按4种削减直径(cut diameter): D25、D50、D75 及 D90来划分。
2 结果与讨论
2.1 臭氧处理对pH的影响
不同臭氧投加时间下,污泥溶液PH的变化情况如图2所示。随着臭氧投加时间的增加,污泥溶液的pH逐渐降低,从处理前的6.9降到投加臭氧60 min时的5.2。
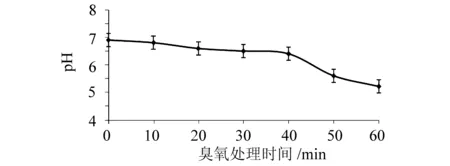
图2 pH随臭氧处理时间的变化Fig.2 Change of pH by oxidizing time
根据王琳等[5]和Weemaes等[6]的研究,臭氧破解了污泥中微生物,并将胞内释放出来的大分子有机物水解成较小的有机物,而这些小分子有机物被臭氧继续氧化,形成以羧酸为主的最终产物。且污泥液相中还会出现多种挥发性脂肪酸,如乙酸、丙酸、丁酸、乳酸以及其它一些低分子量有机物[7],使溶液呈弱酸性,从而使pH值略微降低。
2.2 臭氧处理对污泥液相中蛋白质的影响
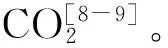

图3 蛋白质随臭氧处理时间的变化Fig.3 Change of protein with oxidizing time
由图3可知,随着臭氧投加时间从0 min增加到60 min, 蛋白质含量由破解前的8.3 mg/L增加到56.3 mg/L。尤其在臭氧投加时间为0~30 min时,蛋白质含量的增加较为明显,溶胞处理后蛋白质浓度从8.3 mg/L增加到37.5 mg/L,增幅约为4.52倍,而30~60 min时增幅为1.5倍。这是由于臭氧与污泥反应时,臭氧首先破坏了微生物的细胞壁和细胞膜,改变细胞通透性,使得细胞内的蛋白质、氨基酸、多糖等物质释放出来,从而使污泥上清液中的蛋白质含量增加。而随后蛋白质含量的增加速率变慢,这是由于在此过程中,蛋白质的释放与分解同时存在。随着臭氧投加时间的增加,蛋白质被臭氧氧化分解的速率变快,使得上清液中蛋白质含量的增加速率变缓[10-11],但是在上清液中仍可检测出蛋白质的含量。同时说明一定臭氧处理时间下,污泥存在最大破解率。
2.3 臭氧处理对污泥液相UV254的影响
UV254是衡量水中有机污染物指标的一项重要控制参数,它表征在254 nm波长下,对紫外光有较强吸收的芳香族化合物或者含不饱和键的有机物的吸光度。国内外许多文献表明UV254与TOC、DOC、COD等有一定相关性,可间接反映有机物的污染程度[12-13]。但检测TOC的设备昂贵且成本高,检测COD耗时长且药品消耗量大,将这两项指标用于实际工业中比较困难。日本早在1978 年就将UV254值列为水质监测正式指标,欧洲也将其作为水厂的去除有机物效果的监测指标[12]。且该方法的测定速度快,操作方便,成本低,重复性好,对特定的水体,用UV254考察有机污染物浓度具有很大的推广意义[14]。 且有研究发现UV254和COD回归分析的相关系数达0.997 8[15]。


图4 UV254随臭氧处理时间的变化Fig.4 Change of UV254 with oxidizing time
2.4 臭氧处理对污泥形态的影响
采用显微镜对臭氧破解前后污泥进行形态观察,可以清晰直观地表现污泥经臭氧处理后絮体结构的变化。图5是不同臭氧处理时间下污泥结构放大100倍的镜检照片。

图5 不同氧化时间下污泥的100倍显微镜照片Fig.5 Photomicrographs of sludge under different oxidizing time (100×)
由图5中的(a)可见,污泥在臭氧破解前,在显微镜观察下,污泥颗粒较大,絮体结构较完整,菌胶团细菌占优势,并且可以观察到鞭毛虫、钟虫等活跃的微生物。而由图5中的(b)、(c)、(d)可以看出,污泥在臭氧破解后,污泥颗粒变小,原来紧密的絮体结构遭到破坏,污泥絮体趋于松散。且随着臭氧处理时间的增加,污泥破碎化程度越来越严重,丝状菌大量减少,絮体分离越来越明显。其中污泥减少最快的是在臭氧氧化时间为30 min。
通过显微镜镜检照片可以看出,臭氧可以促进污泥絮体的破坏,丝状菌的减少,从而使絮体颗粒变小、变分散;且随着臭氧处理时间的增加,污泥破碎越来越严重。这是由于臭氧具有强氧化性,它通过作用于污泥微生物的细胞壁和细胞膜,使其破裂,改变其结构和成分,继而臭氧渗透到细胞内,破坏膜内物质,改变细胞通透性,从而使整个细胞发生失活、死亡并溶解的现象[11]。从以上结果可以知道,要达到臭氧减量化污泥的目的,臭氧处理时间控制在30 min左右比较合适,此时臭氧浓度为每克SS中含O30.088 g。
2.5 臭氧处理对粒径分布的影响
图6是在不同的臭氧处理时间下,污泥的消减直径变化。从图6看出原污泥的D90<65.2 μm, 臭氧处理时间为10 min时D90<61.89 μm,20 min时D90<56.77 μm,30 min时D90<52.65 μm,随着通臭氧时间的增加,D90明显下降,其下降率与原污泥相比分别为5.77%、12.93%、19.25%,30 min时臭氧处理的效果比10 min和20 min的处理效果更显著。表明通臭氧时间的增加,污泥微分粒径有不同程度的改变,更多的污泥被破坏。而污泥其它颗粒的D25、D50、D75变化规律也与D90一致。其中通臭氧30 min时,污泥D25、D50、D75的值与原污泥相比,下降率分别为28.7%、18.72%、34.5%。表明臭氧可以很有效地破解污泥,使絮体颗粒分散,降低大颗粒的数量,增加小颗粒的数量,同时也增加了污泥的比表面积。
结合图5和图6可以知道,臭氧利用其强氧化性,能够大幅度破坏污泥絮体结构,分散菌胶团,破裂细胞,释放絮体及细胞内的空隙水、吸附水、结合水和毛细水,以减少污泥絮体的尺寸大小,增加小颗粒的数量,从而达到减量化污泥的目的。
3 结 论
1)随着臭氧破解时间的增加,污泥溶液的pH呈下降趋势,这是由于污泥破解后产生一些羧酸和挥发性脂肪酸,使溶液呈弱酸性。
(2)臭氧的强氧化性可以使活性污泥中的微生物体内的蛋白质释放,释放的蛋白质浓度最高约56.3 mg/L,尤其在臭氧投加时间为30 min,即液相臭氧浓度为每克SS中含O30.088 g时,蛋白质含量的增加较为明显,增幅约为4.52倍,30 min后蛋白质含量缓慢增加。
(3)随着的增加,UV254逐步增加,臭氧破解时间为30 min时,UV254的增加斜率最大,达到46.21%,说明臭氧能有效地实现污泥的减量化,臭氧首先破坏了微生物的细胞壁和细胞膜,使内含物释放出来,上清液中有机物的含量增多,臭氧进而将大分子有机物质分解为小分子,从而提高了污泥可生化降解性。
(4)从污泥镜检结果和粒径测定结果可以发现,臭氧可以促进污泥絮体的破坏,使絮体颗粒变小、变分散,减少大颗粒的数量,增加小颗粒的数量,进而使微生物细胞发生失活、死亡并溶解的现象,由此说明经臭氧处理后的污泥减量化效果明显。
(5)综上分析,从蛋白质、U254、粒径等随臭氧浓度的变化规律可以看出,要达到臭氧减量化污泥最佳效果,在室温下当污泥初始污泥浓度为10.8 g/L,臭氧处理时间控制在30 min左右最好,此时臭氧浓度为每克SS中含O30.088 g。
[1] 金瑞洪, NG Wun Jern. 臭氧对活性污泥特性影响研究[J].环境污染治理技术与设备,2004,5(9):48-50.
[2] 何楚茵, 金辉, 卜淳炜,等.臭氧处理剩余污泥的减量化实验研究[J].环境工程学报,2012,6(11):4228-4234.
[3] 贾舒婷,张栋,赵建夫,等.不同预处理方法促进初沉/剩余污泥厌氧发酵产沼气研究进展[J].化工进展,2013,32(1):193-198.
[4] 何楚茵,金辉,黄宋彬,等. 臭氧与酸碱耦合对剩余污泥的溶胞减量研究[J]. 中国给水排水, 2013, 29(21):122-127.
[5] 王琳,王宝贞.污泥减量技术[J].给水排水,2000,26(10):28.31.
[6] WEEMAES M, GROOTAERD H, SIMOCNS F. Anaestion digestion of ozonized biosolids [J]. Water Research, 2000, 34(8): 2330-2336.
[7] SONG K G, CHUONGY Y K, AHNK H. Performance of membrane bioreactor system with sludge ozonation process for minimization of excess sludge production [J].Desalination, 2003, 157:353.
[8] CUI R, JAHNH D. Nitrogen control in AO process with recirculation of solubilized excess sludge[J]. Water Res, 2004, 38(5): 1159-1172.
[9] YU L. Chemically reduced excess sludge production in the activated sludge process[J]. Chemosophere, 2003, 50(1):1-7.
[10] 尹军,王剑寒,赵玉鑫,等. 臭氧投量对活性污泥特性参数的影响[J]. 中国给水排水, 2009, 25(1): 18-21.
[11] SCHEMINSKE A, KRULL R, HEMPEL D C. Oxidative treatment of digested sewage sludge with ozone[J].Water Science and Technology, 2000, 42(9):151-158.
[12] EATONAD.Measuring UV-absorbing organics:a standard method[J]. J AWWA, 1995, 87(2):86-90.
[13] EDZWALD J K. Coagulation in drinking water treatment: particles, organics and coagulants control of organic material by coagulation and F loc separation process[M]. Water Science &Technology. Oxford Pergamon Press, 1993: 21-35.
[14] 蒋绍阶, 刘宗源. UV254作为水处理中有机物控制指标的意义 [J]. 重庆建筑大学学报, 2002, 24(2):61-65.
[15] 林星杰, 杨慧芬, 宋存义. UV254在水质监测中应用的研究[J].能源与环境,2006,25(1):22-24.
[16] YASUI H, NAKAMURA K, SAKUMA S, et al. A full scale operation of a novel activated sludge process without excess sludge production [J] .Wat Sci Tech, 1996, 34 (3/4): 395-404.
[17] 焦阳, 李军, 董文艺, 等. 臭氧对二沉池出水的氧化特性研究[J].中国给水排水, 2010, 26(5): 124-130,126.
[18] 金伟,范瑾初.紫外吸光值(UV254)作为有机物替代参数的探讨[J].工业水处理,1997,17(6):30-33.

