右美托咪定联合格拉司琼预防妇科腹腔镜手术术后恶心呕吐的临床观察
刘晓捷 罗富荣 冯宝莹(广东省佛山市中医院麻醉科,528000)
右美托咪定联合格拉司琼预防妇科腹腔镜手术术后恶心呕吐的临床观察
刘晓捷 罗富荣 冯宝莹
(广东省佛山市中医院麻醉科,528000)
目的 探讨右美托咪定联合格拉司琼预防妇科腹腔镜手术术后恶心呕吐的效果。方法 60例腹腔镜手术患者随机分成诱导组(Ⅰ组)、术毕组(EOS组)和格拉司琼组(G组)各20例。Ⅰ组于诱导前10 min静脉泵注右美托咪定,EOS组于手术结束前30 min静脉泵注相同剂量右美托咪定,所有患者手术结束前30 min均静脉注射格拉司琼3 mg。记录术毕至拔气管导管、听从指令时间,麻醉恢复期内患者呼吸抑制、躁动等不良反应发生情况,术后24 h内恶心呕吐发生率及严重程度。结果 Ⅰ组拔管时间、听从指令时间,术后0~1 h、1~2 h恶心呕吐评分,在麻醉后恢复室内止吐药给药人次数均小于EOS组和G组。EOS组术后0~1 h、1~2 h恶心呕吐评分和在麻醉后恢复室内止吐药给药人次数均小于G组(P<0.05)。EOS组和G组拔管时间、听从指令时间无明显差异(P>0.05)。术后2~4 h、4~12 h、12~24 h各组间恶心呕吐评分无明显差异(P>0.05)。所有患者均未见麻醉恢复期内呼吸抑制、躁动等不良反应。结论 右美托咪定联合格拉司琼预防妇科腹腔镜手术术后恶心呕吐效果较单用格拉司琼更好,诱导前10 min使用为佳。
腹腔镜手术;并发症;恶心;呕吐;预防;右美托咪定;格拉司琼
根据美国麻醉师协会(ASA)的最新调查,患者对麻醉最为担心的问题是失去记忆、术中知晓、术后疼痛、术后恶心呕吐(PONV)和死亡等[1]。据文献报道,术后呕吐的发生率为30%,高危患者术后恶心的发生率为50%,PONV的发生率更是高达80%[2]。因此,预防PONV的发生是降低PONV发生率、减轻其严重程度的重要环节。右美托咪定(DEX)具抗焦虑、镇静、镇痛和抗交感神经活性作用,围手术期使用可明显减少麻醉药用量[3],还可预防PONV[4]。本研究旨在观察DEX联合格拉司琼对妇科腹腔镜手术PONV的预防作用和安全性。
1 资料与方法
1.1 一般资料 选取2014年1—4月我院收治的拟行妇科腹腔镜手术患者60例,ASA分级均为Ⅰ~Ⅱ级,年龄
18~50岁;经医院伦理委员会批准,患者愿意签署麻醉知情同意书,排除吸烟史、晕动病史、PONV史、心脏传导阻滞或心率<65次/min的患者。所有患者均无术后镇痛要求,采取随机数字表方法分为诱导组(Ⅰ组)、术毕组(EOS组)和格拉司琼组(G组)各20例。
1.2 麻醉和监测方法 患者入室后给予开放面罩吸氧(3 L/min),静卧5 min后采用多功能监护仪监测心电图(ECG)、脉搏血氧饱和度(SpO2)和心率(HR)。
Ⅰ组于诱导前10 min使用0.9%氯化钠溶液稀释浓度为4 μg/mL的DEX以0.5 μg/kg静脉泵注。EOS组于手术结束前30 min静脉泵注相同剂量的DEX。所有患者在手术结束前30 min静脉注射格拉司琼3 mg。
插管前予咪唑安定0.04 mg/kg、丙泊酚3 mg/kg、舒芬太尼0.15 μg/kg、罗库溴铵0.6 mg/kg快速诱导,插管成功后机械通气,潮气量8~10 mL/kg,呼吸频率10~12次/min。监测潮气量(TV)、分钟通气量(MV)、呼吸频率(f)、呼气末二氧化碳分压(PETCO2)等。调整潮气量和通气频率,维持PETCO2在30~40 mm Hg之间,SpO2>99%。术中给予瑞芬太尼靶控输注(TCI)(血浆浓度4 ng/mL)和七氟醚(O2流量1.5 L/min,浓度据术中血压调节,使术中平均动脉压维持在高于或低于术前25%以内),并按需追加罗库溴铵维持肌肉松驰。术中患者心率<45 次/min时,给予阿托品0.25 mg/次,总量≤1 mg。
术毕前15 min停用七氟醚,O2流量调至6 L/min。术毕停用瑞芬太尼,手控呼吸直到恢复自主呼吸。静脉注射新斯的明0.03 mg/kg、阿托品0.02 mg/kg后,拔出气管导管置入口咽通气道。拔管后患者进入麻醉后恢复室(PACU),继续监测生命体征并处理、记录可能发生的不良反应。如患者出现中度恶心或呕吐,给予静脉注射氟哌利多1 mg,如未能缓解,再静脉注射地塞米松5 mg。如果患者主诉疼痛,给予舒芬太尼5 μg,总量≤10 μg。患者至少观察60 min,达到出室标准后送回病房。
1.3 观察指标 ①患者年龄、体重、手术历时、术中入液量和出血量。②术毕至拔气管导管时间、术毕至听从指令时间。③患者麻醉恢复期间呼吸抑制、躁动等不良反应。④患者在PACU发生心率<45次/min的次数。⑤术后24 h内(分0~1 h、1~2 h、2~4 h、4~12 h、12~24 h五个时间段)进行恶心、呕吐严重程度评分(NVS),在PACU停留时间及止吐药使用人次数。恶心、呕吐严重程度评分标准:无恶心、呕吐0分;轻微恶心1分;中度恶心、呕吐(<4次)2分;频繁呕吐(≥4次)3分;严重呕吐(持续)4分。
1.4 统计学分析 数据使用SPSS 19.0软件进行统计分析,计量资料以均数±标准差表示,采用t检验;等级资料采用秩和检验(Kruskal-Wallis Test);术后24 h内使用止吐药人次采用χ2检验;P<0.05为差异有统计学意义。
2 结果
三组患者年龄、体重、手术历时、术中入液量和出血量比较,差异均无统计学意义(P>0.05),见表1。Ⅰ组拔管时间、听从指令时间较EOS组和G组短(P<0.05),后两组间无明显差异(P>0.05),见表2。所有患者在麻醉恢复期间未观察到呼吸抑制、躁动及心率<45次/min的情况发生。术后24 h内,Ⅰ组0~1 h、1~2 h期间NVS评分低于EOS组和G组(P<0.05),同时期EOS组NVS评分低于G组(P<0.05);其余时间段三组间NVS评分无明显差异(P>0.05),见表3。三组患者在PACU内停留时间无明显差异(P>0.05)。PACU内止吐药使用人次数Ⅰ组(1人次)少于EOS组(6人次)和G组(11人次),EOS组少于G组,差异均具有统计学意义(P<0.05)。

表1 三组患者年龄、体重、手术历时、入液量和出血量比较

表2 三组患者拔管时间、听从指令时间比较 (min)
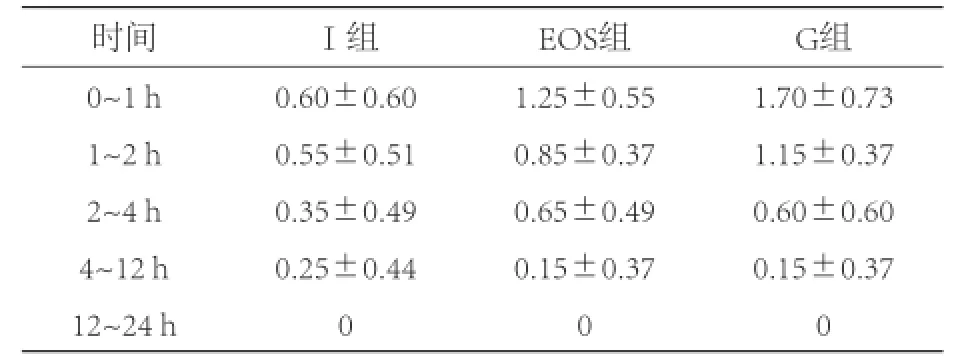
表3 三组患者术后24 h内NVS比较 (分)
3 讨论
影响PONV发生的因素较多,根据ASA发布的最新“PONV管理指南”,在与患者自身有关的因素中,女性为最强的PONV预测因素,随后依次为PONV史、不吸烟、晕动病史、年龄(<50岁)。在与麻醉相关的因素中,应用挥发性麻醉药为最强预测因素,随后依次为麻醉时间、术后应用阿片类药物及氧化亚氮。胆囊切除术、妇科手术及腹腔镜检查PONV发生风险较高[5]。
DEX是新型、高选择性α2肾上腺素受体激动剂,除具有抗焦虑、抗交感、镇静、镇痛作用外,还有微弱并且短效的抗恶心、呕吐作用[6]。DEX主要给药方式有两种:①总量控制0.5~1.0 μ g/kg、持续泵注10~15 min;②根据
临床需要,以0.1~0.7 μg/(kg・h)的速度持续泵注[7]。DEX的分布半衰期(t1/2α)为6 min,消除半衰期(t1/2β)约2 h,其持续输注半衰期(t1/2CS)随输注时间增加而显著延长。
本研究中的患者存在PONV中度风险,且行妇科腹腔镜手术,发生PONV的风险较高,故没有设立空白对照组,而是将只接受格拉司琼的G组患者作为对照。为获得更好的麻醉复苏效果,避免DEX引起心动过缓的不良反应,本研究选择0.5 μg/kg、静脉泵注10 min的给药方式,结果显示,使用DEX 0.5 μg/kg预防PONV,其效果仅体现在术后2 h内,这与国外学者的研究结果一致。但是笔者发现,诱导前给药的Ⅰ组比术终前30 min给药的EOS组预防作用更强。Ⅰ组患者诱导前使用DEX,能节省术中七氟醚用量,而吸入麻醉药正是引起PONV的最强麻醉相关因素。因此,笔者认为,DEX预防PONV的作用机制,除具有降低交感神经系统张力的直接作用外,还与DEX节省吸入麻醉药的间接作用有关。另外,本研究中的患者术中未出现心率<45次/min的情况,说明DEX的给药剂量及方式是安全的。但对术前即有窦性心律过缓或各种传导阻滞、肝肾功能不全、糖尿病患者,DEX应慎用。
本研究不足:①病例数量较少,未能做到双盲,NVS评分存在主观因素;②DEX只使用0.5 μg/kg静脉泵注10 min的给药方式。而DEX预防PONV是否存在量效关系及其最有效安全剂量,尚需进一步研究。
[1] 吴新民,于布为,叶铁虎,等.术中知晓预防和脑功能监测快捷指南[J].中国继续医学教育,2011,3(10):139-140.
[2] Apfel CC, L☒☒r☒ E, Koivuranta M, et al. A simplified risk score for predicting postoperative nausea and vomiting: conclusions from cross-validations between two centers[J]. Anesthesiology, 1999, 91(3): 693-700.
[3] Gerlach AT, Murphy CV, Dasta JF. An updated focused review of dexmedetomidine in adults[J]. Ann Pharmacother, 2009, 43(12): 2064-2074.
[4] Tufanogullari B, White PF, Peixoto MP, et al. Dexmedetomidine infusion during laparoscopic bariatric surgery: the effect on recovery outcome variables[J]. Anesth Analg, 2008, 106(6): 1741-1748.
[5] Gan TJ, Diemunsch P, Habib AS, et al. Consensus guidelines for the management of postoperative nausea and vomiting[J]. Anesth Analg, 2014, 118(1): 85-113.
[6] Blaudszun G, Lysakowski C, Elia N, et al. Effect of perioperative systemic alpha-2 agonists on postoperative morphine consumption and pain intensity: systematic review and metaanalysis of randomized controlled trials[J]. Anesthesiology, 2012, 116(6): 1312-1322.
[7] 中华医学会麻醉学分会.右美托咪定临床应用指导意见(2013)[J].中华麻醉学杂志,2013,33(10):1165-1167.
Dexmedetomidine Combined with Granisetron in Preventing Postoperative Nausea and Vomiting after Gynecological Laparoscopic Surgery
Liu Xiaojie Luo Furong Feng Baoying
(Department of Anesthesiology, Foshan Hospital of Traditional Chinese Medicine, Guangdong 528000)
ObjectiveTo investigate the effect of dexmedetomidine combined with granisetron in preventing postoperative nausea and vomiting after gynecological laparoscopic surgery.Methods60 patients underwent gynecological laparoscopic surgery were randomly divided into the induction group(Ⅰ group, 20 cases), the end of surgery group(EOS group, 20 cases), and the granisetron group(G group, 20 cases). Dexmedetomidine was administered 10 min before induction in the Ⅰ group patients, or 30 min before the end of surgery in the EOS group patients. All patients received 3 mg of granisetron 30 min before the end of surgery. The time to extubation and response to verbal command, respiratory depression, dysphoria in the postanesthesia intensive care unit, incidence and severity of nausea and vomiting for postoperative 24 h were recorded.ResultsThe time to extubation and response to verbal command, nausea and vomiting scores in postoperative 0~1 h and 1~2 h, antiemetics given in the postanesthesia intensive care unit in the Ⅰ group were less than those in the EOS group and the G group(P<0.05). Nausea and vomiting scores within postoperative 0~1 h and 1~2 h, antiemetics given in the postanesthesia intensive care unit in the EOS group were less than those in the G group(P<0.05). Time to extubation and response to verbal command between the EOS group and the G group had no signifi cant difference(P>0.05); The nausea and vomiting scores of the three groups within postoperative 2~4 h, 4~12 h, and 12~24 h had no signifi cant difference(P>0.05).ConclusionDexmedetomidine combined with granisetron in preventing postoperative nausea and vomiting after gynecological laparoscopic surgery was more effective than using granisetron lonely, and it’s better by administered 10 min before induction.
gynecological laparoscopic surgery; complication; nausea and vomiting; prevention; dexmedetomidine; granisetron
1672-7185(2014)15-0043-03
10.3969/j.issn.1672-7185.2014.15.025
刘晓捷
2014-06-03)
R614
A

