蛛网膜下腔出血患者继发症状性脑血管痉挛的相关危险因素分析
张铃铛,宋毅,冯清林,刘明冬,范仕兵,杜江峰,张鹏,冯梅
症状性脑血管痉挛(symptomatic cerebral vasospasm,SCVS),可引起严重的脑组织局部缺血缺氧,是导致蛛网膜下腔出血(subarachnoid hemorrhage,SAH)患者预后不良的主要原因之一[1],其发生率为10%~60%[2]。到目前为止对SCVS没有可靠的预警方法[3],明确SCVS的相关危险因素对提高SAH患者疾病预后有重要意义。本文通过回顾性分析96例SAH患者临床资料,探讨SCVS的相关危险因素,以期为SCVS的防治提供参考。
1 对象和方法
1.1 研究对象 回顾分析2008年5月~2013年5月我院收治的动脉瘤性SAH患者的临床资料。纳入标准:①患者符合全国第四次脑血管会议制定的《脑血管疾病分类(1995)》中蛛网膜下腔出血诊断标准[4];②数字减影血管造影(digital subtraction angiography,DSA)检查表现为动脉瘤,临床考虑为此次SAH的责任病灶;③自发病至住院时间≤14 d;④年龄≥12岁。排除标准:排除脑实质出血破入蛛网膜下腔者、颅内感染、瘤卒中和血液系统疾病继发SAH者。本次研究共收集109例患者资料,有13例在入院24 h内死亡,未纳入分析范围,实际分析例数为96例,其年龄范围为20~78岁。所有患者在入院48 h内进行全脑DSA以确定动脉瘤位置,根据患者病情评估,选择手术时机。在治疗上,有45例患者自入院开始持续予以静脉微泵入尼莫地平1 mg/h,以预防SCVS的发生。其余治疗为常规对症支持治疗,必要时给予静脉输入脱水剂如甘露醇、呋塞米、高渗葡萄糖等。
1.2 方法
1.2.1 资料收集 本研究采用自行设计的调查表收集患者人口学资料、行为习惯、临床资料,根据国内外相关资料并结合病历记录项目,共有16个指标纳入研究,包括性别、年龄、高血压史[5]、糖尿病史[6]、吸烟、饮酒、手术时机、颅内血肿、动脉瘤位置、脑室内积血、Hunt-Hess分级[7](Ⅰ~Ⅴ级)、Fisher分级[8](Ⅰ~Ⅳ级)、血管痉挛程度、发热、预防性尼莫地平使用、脱水剂使用,对其进行统计分析。
1.2.2 危险因素相关界定 吸烟史:吸烟≥3支/日或18支/周,持续超过1年;饮酒史:连续饮酒>100 g/d超过1年[9];发热:入院时体温≥38℃;
1.3 统计方法 所有数据由双人双份平行录入,以SPSS 16.0统计软件进行分析。符合正态分布的计量资料以s表示,计数资料用百分比表示;组间比较计数资料采用χ2检验、等级资料采用秩和检验。对单因素分析中P<0.05的因素进行Logistic回归分析,确定SCVS发生的危险因素和保护因素。以α=0.05为检验水准,P<0.05为差异有显著性。血管痉挛程度[10]:颅内大动脉严重痉挛定义为DSA显示动脉管径缩小>50%,中度痉挛为25%~50%,轻度为<25%。
1.2.3 SCVS判定标准[11]①SAH症状经治疗好转或稳定后,又出现恶化或进行性加重,伴发热、血象高且无感染迹象;②意识由清醒转为嗜睡、昏迷,或由原来昏迷转为清醒后又发生昏迷;③依据脑血管痉挛部位的不同产生相应的局灶体征,如偏瘫、失语、失认和失用症。神经系统局部损害症状可在数周内逐渐出现,也可在突然发生后数分钟至l h达高峰;④出现头痛、呕吐、视乳头水肿等颅内压增高症状;⑤入院后DSA、磁共振血管造影(magnetic resonance angiography,MRA)或CT血管造影(CT angiography,CTA)显示CVS;⑥经颅多普勒(transcranial Doppler,TCD)发现脑血流速增快,并可见频谱异常,出现湍流现象。符合上述标准的一项或一项以上,且排除再出血、颅内血肿、脑积水和电解质紊乱等其他原因导致者可诊断为CVS。
2 结果
2.1 SCVS患病情况 本次调查的96例SAH患者中,发生SCVS的患者39例(40.63%),其中男性26例,女性13例,平均年龄(50.32±12.52)岁,SAH后出现SCVS症状的时间范围为1~5 d;未发生SCVS的患者57例(59.37%),男性41例,女性16例,平均年龄(62.53±14.06)岁。
2.2 SCVS影响因素单因素分析 单因素分析结果显示,SCVS组与非SCVS组在年龄、高血压、吸烟、脑室内积血、Hunt-Hess分级、Fisher分级、血管痉挛程度、尼莫地平预防性使用等8个方面差异有显著性;而在性别、糖尿病、饮酒、颅内血肿、动脉瘤位置、手术时机、发热、脱水剂使用等方面差异无显著性。详细数据见表1。
2.3 SCVS影响因素多因素Logistic回归分析结果 将患者SCVS有无发生与其影响因素做二分类Logistic回归,其中自变量为单因素分析基础上所筛选的具有显著差异的影响因素,因变量为SCVS的发生状况。因变量赋值:0=未发生SCVS,1=发生SCVS。对影响因素赋值如下:①年龄:1=<30岁,2=30~60岁,3=≥60岁;②高血压:0=无,1=有;③吸烟:0=无,1=有;④脑室内积血:0=无,1=有;⑤Hunt-Hess分级:0=Ⅰ~Ⅱ级,1=Ⅲ~Ⅴ级;⑥Fisher分级:0=Ⅰ~Ⅱ级,1=Ⅲ~Ⅳ级;⑦DSA显示血管痉挛程度:1=无痉挛,2=轻中度痉挛,3=重度痉挛;⑧尼莫地平预防性使用:0=未使用,1=使用。
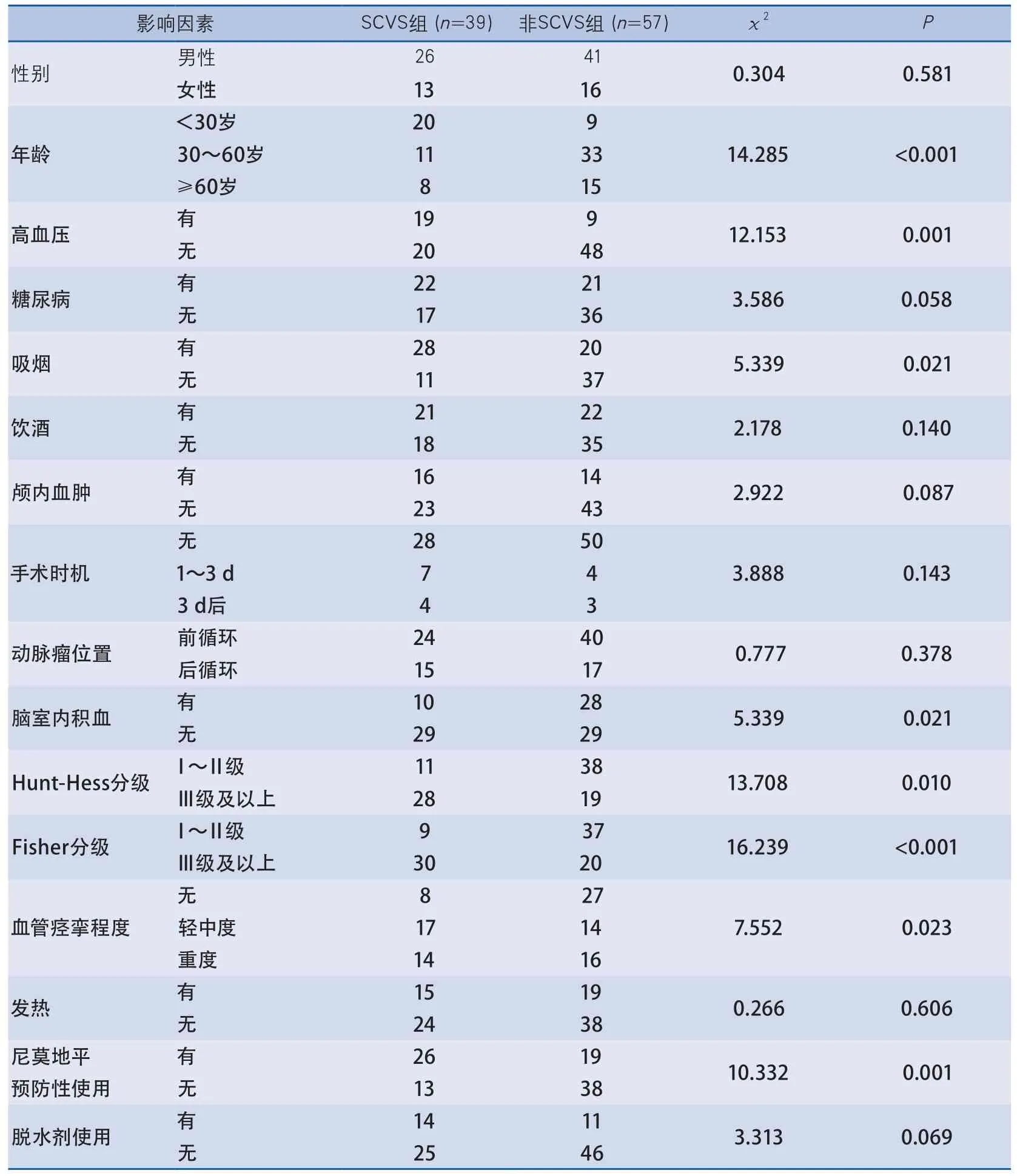
表1 SCVS组与非SCVS组影响因素的单因素分析结果
采用逐步法筛选自变量,最终进入方程的因素包括:年龄、高血压史、Fisher分级、尼莫地平的使用。其余在单因素分析时有统计学差异的因素,最终未能进入方程。结果见表2。
3 讨论
SCVS是SAH的严重并发症之一,若处理不当或不及时常造成脑组织严重缺血或诱发迟发型缺血性脑损伤而加重病情[12]。SCVS的发生机制尚不清楚,由于SCVS与SAH患者的预后相关[13],因此及早评估病情,明确SCVS的危险因素,预测SCVS的发生,有利于降低SAH的病死率与致残率。
有研究者[14-15]认为低龄SAH患者SCVS发生率高,而Fetch和李照凯[16-17]的研究表明年龄增长是SCVS的独立危险因素,Reilly及Mclaughlin[18-19]则发现中年人更易发生SCVS。本组研究资料结果显示低龄是SCVS发生的独立危险因素。Torbey等研究者认为低龄SAH患者脑动脉血管内膜完整,对血液释放的某些缩血管物质更敏感[15],相对老龄患者更易出现脑血管痉挛;而持相反看法者则认为老年人血管硬化程度重,自我调节能力降低,侧支循环代偿能力不足,脑组织对缺血的耐受性下降,更容易发生痉挛[20]。目前,年龄与SCVS的关系尚存争议,但可以肯定的是脑血管壁结构伴随年龄增大而改变,此关系需要更大样本研究的循证医学证据支持和基础医学研究来进行解释。
有研究认为高压病史是SCVS独立危险因素,其病理生理基础之一就是长期血压升高可使血管产生器质性改变,导致脑血管自身调节能力受损,脑血流下降,在SAH后更易发生SCVS[21-22]。但在有的研究结果中[11,17,23],高血压未能在多元回归分析中被证实为SCVS的独立危险因素。本研究的结果支持高血压是SCVS的独立危险因素。诸多研究结果不一致的原因可能在于样本例数受限、抽样误差等所致,有待进一步研究。
改良Fisher分级是以蛛网膜下腔的积血厚度为基础的,可较准确地反映蛛网膜下腔和脑室内出血量与SCVS发生的相关性[24],改良Fisher分级已被公认为脑血管痉挛的独立危险因素[25]。本研究结果也显示改良Fisher分级越高,症状性脑血管痉挛的发生率越高。改良Fisher分级的基础是蛛网膜下腔的积血厚度,而相关动物与临床观察均证实积血厚度及分布范围在一定程度上决定血管痉挛累及的严重程度和范围[26-27],因此,改良Fisher分级是一个较好的SCVS预警因子。
尼莫地平可以降低迟发性神经功能障碍的风险和不良结局的发生,这已经得到Ⅰ级证据的支持[28],大量的前瞻性临床试验已经验证了口服尼莫地平的有效性,预防性应用尼莫地平,可以明显地有效改善临床结果[28]。本研究中使用尼莫地平组患者与未使用者SCVS的发生率有显著差异,回归分析显示尼莫地平的使用是SCVS的保护因素。
总之,SCVS的发生是多种因素共同作用的结果,临床上应针对相关因素给予适当处理,对改善患者预后具有重要意义。但本研究不足之处在于样本量偏小,某些相关因素如血生化指标,意识障碍程度,动脉瘤类型等未纳入研究,有待进一步研究。
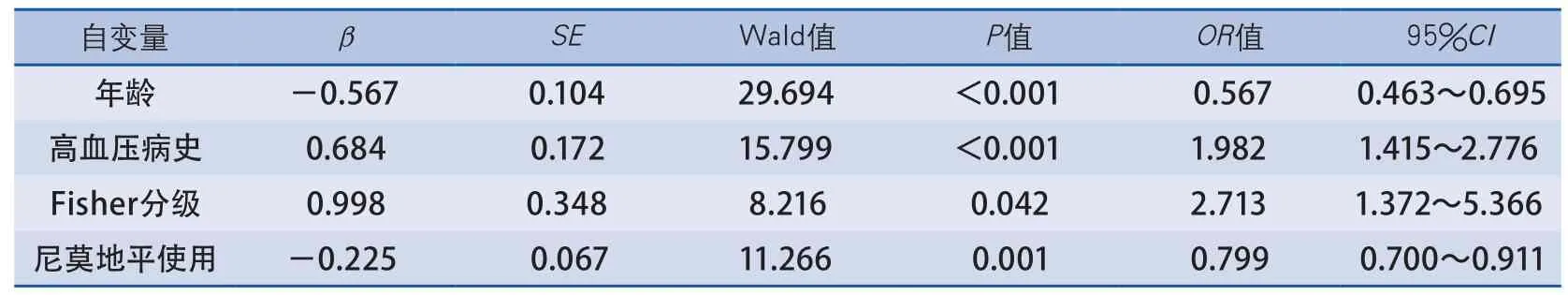
表2 SCVS影响因素多因素Logistic回归分析结果
1 刘飞, 袁文, 廖达光, 等. 动脉瘤夹闭术对蛛网膜下腔积血量的影响[J]. 南方医科大学学报, 2013, 33:1041-1044.
2 刘承基. 脑血管外科学[M]. 南京; 江苏科学技术出版社,1999:39-41.
3 Ko NU, Rajendran P, Kim H, et al. Endothelial nitric oxide synthase polymorphism and increased risk of angiographic vasospasm after aneurismal subarachnoid hemorrhage[J]. Stroke, 2008, 39:1103-1108.
4 中华神经科学会. 各类脑血管疾病诊断要点[J]. 中华神经科杂志, 1996, 29:379.
5 Mancia G, De Backer G, Dominiczak A, et al.2007 Guidelines for the management of arterial hypertension;The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC)[J]. J Hypertens, 2007, 25:1105-1187.
6 World Health Organizanion; Def i nition and diagnosis of diabetes mellitus and intermediate hyperglycemia;Report of a WHO/IDF consultation[D]. Geneva,World Health Org., 2006.
7 Hunt WE, Hess RM. Surgical risk as related to time of intervention in the repair of intracranial aneurysms[J].J Neurosurg, 1968, 28:14-20.
8 Fisher CM, Kistler JP, Davis JM. Relation of cerebral vasospasm to subarachnoid hemorrhage visualized by computerized tomographic scanning[J]. Neurosurgery,1980, 6:1-9.
9 刘光健, 陈俊, 王云甫, 等. 蛛网膜下腔出血患者脑血管痉挛相关危险因素回顾性研究[J]. 中国神经精神疾病杂志, 2010, 36:554-556.
10 赵一平, 张贺, 李松柏, 等. 蛛网膜下腔出血后脑血管痉挛常规影像诊断方法的研究[J]. 临床放射学杂志, 2013,32:469-474.
11 黄佳. 蛛网膜下腔出血后脑血管痉挛的危险因素[J]. 中华神经精神疾病杂志, 2009, 35:368-370.
12 廖建平. 尼莫地平治疗蛛网膜下腔出血脑血管痉挛疗效观察[J]. 中国实用神经疾病杂志, 2013, 16:62-63.
13 Kincaid MS, Souter MJ, Treggiari MM, et a1. Accuracy of transcranial Doppler ultrasonography and singlephoton emission computed tomography in the diagnosis of angiographically demonstrated cerebral vasospasm[J]. J Neurosurg, 2009, 110:67-72.
14 陈高, 张建民, 李珉, 等. 动脉瘤性SAH继发重度脑血管痉挛相关因素研究[J]. 中华神经外科杂志, 2005,21:665-667.
15 Torbey MT, Hauser TK, Bhardwaj A, et al. Effect of age on cerebral blood flow velocity and incidence of vasospasm after aneurismal subarachnoid hemorrhage[J]. Stroke, 2001, 32:2005-2011.
16 Fetch R, Pasqualin A, Pinna G, et al.Temporary arterial occlusion in the repair of ruptured intracranial aneurysms;an analysis of risk factors for stroke[J]. J Neurosurg, 2002, 97:836-842.
17 李照凯, 姜长斌, 尹琳, 等. 蛛网膜下腔出血后症状性脑血管痉挛的危险因素分析[J]. 中国实用神经疾病杂志,2009, 12:3-5.
18 Reilly C, Amidei C, Tolentino J, et al. Clot volume and clearance rate as independent predictors of vasospasm after aneurismal subarachnoid hemorrhage[J]. J Neurosurg, 2004, 101:255-261.
19 Mclaughlin N, Bojanowski MW. Ealy surgey-related complications after aneurysmclip placement :an analysis of causes and patient outcomes[J]. J Neurosurg,2004, 101:600-606.
20 朱建新, 李丽, 耿凤阳, 等. 颅脑损伤后症状性脑血管痉挛的危险因素分析[J]. 中华神经外科疾病研究杂志,2009, 8:268-269.
21 Tabuchi S, Hirano N, Tanabe M, et al. Relationship of hypotension and cerebral vasospasm in patients with aneurismal subarachnoid hemorrhage[J]. Neurol Res,2006, 28:196-199.
22 Macdonald RL, Rosengart A, Huo D, et al. Factors associated with the development of vasospasm after planned surgical treatment of aneurismal subarachnoid hemorrhage[J]. J Neurosurg, 2003, 99:644-652.
23 何育生, 赵丽娟, 潘有贵, 等. 蛛网膜下腔出血后症状性脑血管痉挛危险因素的多元分析[J]. 中风与神经疾病杂志, 2007, 10 24:603-605.
24 Frontera JA, Claassen J, Schmidt JM, et al. Prediction of symptomatic vasospasm after subarachnoid hemorrhage:the modif i ed Fisher scale[J]. Neurosurgery,2006, 59:21-27.
25 Qureshi AI, Sung GY, Razumovsky AY, et al. Early identification of patients at risk for symptomatic vasospasm after aneurysmal subarachnoid hemorrhage[J]. Crit Care Med, 2000, 28:984-990.
26 王文娟, 赵性泉, 王伊龙. 脑血管痉挛的管理[J]. 中国卒中杂志, 2006:352-360.
27 Dorsch NWC, King MT. A review of cerebral vasospasm in aneurismal subarachnoid hemorrhage.Part I:Incidence and effects[J]. Clin Neurosci, 1994,1:19-26.
28 Dreier JP, Woitzik J, Fabricius M, et al. Delayed ischaemic neurological deficits after subarachnoid haemorrhage are associated with clusters of spread in depolarizations[J]. Brain, 2006, 129 :3224-3237.
28 祝源. 颅内动脉瘤术后症状性脑血管痉挛的预测因子分析[D]. 湖北省:华中科技大学, 2012:26-27.

