脑出血模型大鼠脑组织胰岛素样生长因子-1表达的实验研究
严永兴 梁丽贞 袁艳蓉 沈咏慧 陈 涛 吴春丽 刘慧丽
杭州市第三人民医院神经内科 杭州 310009
胰岛素样生长因子-1(insulin-like growth factor-1,IGF-1)是一种非选择性神经营养因子,具有调节神经组织的生长、分化、修复、再生等作用。在脑损伤等病理状态下,IGF-1对中枢神经细胞起到营养保护作用,可有助于神经细胞受损后的功能恢复[1]。既往较多文献报道IGF-1在缺血性脑损伤中的作用[2-3],但有关IGF-1在脑出血后的作用研究较少。本实验通过观察大鼠脑出血后脑内IGF-1的表达及其与细胞凋亡的关系,探讨其在脑出血后继发性脑损伤的作用。
1 资料与方法
1.1 动物和分组 健康雄性SD大鼠105只,体质量240~320g,清洁级Ⅱ度,由浙江中医药大学动物实验中心提供,动物合格证号:SYXK(浙)2013-0184,于屏障环境饲养。105只大鼠依次编号为1~105号,应用随机数字表法完全随机分为正常对照组5只,脑出血组50只和假手术组50只。脑出血组和假手术组动物在模型建立后依旧按随机数字表法再次完全随机按6、24、48、72h和1周5个时间点分为5个亚组,每个亚组10只大鼠。
1.2 脑出血动物模型的建立 参照文献[4]建立大鼠自体动脉血脑出血动物模型。大鼠用10%水合氯醛腹腔注射麻醉(3.0ml/kg),取尾动脉血50μL,应用脑立体定向技术注入大鼠脑内右侧尾状核。假手术组在右侧尾状核注入50μL生理盐水,其它条件与脑出血组完全一致。术中保持无菌操作,术后观察神经系统症状,在不同时间点处死动物。建模是否成功根据Bederson 法[5]判定。
1.3 标本制备 各组大鼠分别在6、24、48、72h和1周时间点给予水合氯醛深度麻醉,迅速打开胸腔,剪开右心耳,自左心室灌注生理盐水,致流出液清亮为止,再断头,迅速取脑。各亚组随机取5只大鼠脑组织迅速置于液氮保存(用于荧光定量RT-PCR检测IGF-1mRNA),另5只大鼠脑组织置于中性福尔马林固定24h,沿针孔处作冠状切开,有明显血肿且无蛛网膜下腔出血,未破入脑室者为模型制作成功。沿针孔处冠状面前后各取厚约2.5mm的脑组织,做连续冠状切片,厚5μm,分别作末端脱氧核苷酸酶转移酶介导的dUTP缺几末端标记法(TUNEL)染色及IGF-1免疫组化染色。
1.4 TUNEL法检测脑组织细胞凋亡 采用TUNEL试剂盒(武汉博士德生物工程有限公司)检测凋亡细胞。按试剂盒提供的步骤进行,苏木精轻度复染,镜下细胞核染色呈棕黄色为TUNEL阳性细胞,每只大鼠均取3张切片,在每张脑切片的脑出血部边缘随机选取5个高倍镜(400倍)不重叠视野,在图像分析仪下,计数阳性细胞数。
1.5 RT-PCR检测IGF-1 mRNA 总RNA提取按照TaKaRa RNAiso Plus(Total RNA提取试剂)说明书进行。反转录按TaKaRa逆转录试剂盒Prime-ScriptTM RT reagent要求,将已提取的总RNA反转录为 cDNA,反转录反应条件:37°C 15min,85°C 5s。实时荧光定量PCR按照TaKaRa荧光定量试剂盒SYBR Premix Ex Taq TMⅡ进行,荧光定量PCR引物序列由生工生物工程(上海)有限公司设计并合成,各引物序列如下:IGF-1:上游引物:5′-TACTTC AACAAGCCCACAGG-3′,下游引物:5′-ACATCTCC AGCCTCCTCAGA-3,GAPDH:上游引物:5′-GGCAC AGTCAAGGCTGAGAATG-3′,下游引物:5′-ATGGTGGTGAAGACGCCAGTA-3。扩增反应条件如下:预变性:95℃ 3min;48 个循环(95℃ 10s,60℃ 30s);溶解曲线:从55°C开始,每30s升高0.5°C,直到95℃,循环1次。所有反应信息资料由Bio-Rad iQ5 PCR仪收集,Ct值通过计算机软件来测量和计算,转录水平通过公式2-△△CT计算。
1.6 免疫组化染色检测IGF-1表达相对含量 按兔鼠通用二步法免疫组化试剂盒(生工生物工程(上海)有限公司)步骤进行操作。常规脱蜡至水,3%H2O2溶液阻断过氧化物酶,10min;各步骤间以PBS冲洗5min×3次,滴加一抗,37℃孵育60min;PBS洗5min×3次;滴加二抗,37℃孵育 60min;PBS洗 5min×3次;DAB显色1~2min然后脱水、透明、封片。阴性对照用PBS代替一抗。图像分析采用荧光显微镜系统(Olympus BX-60型)及显微镜数码相机系统(Olympus DPIO型)进行图像采集。各切片选择4个不同的视野照相(放大200倍),各切片选择视野的位置保持一致。将照片输入计算机后,使用Image J图像分析软件进行分析。照片经过灰度转换和二值化处理后,由软件标记并计算出每张照片中阳性细胞的数量。
1.7 统计学方法 应用SPSS10.0软件,计量资料以(x±s) 表示,两样本均数比较采用t检验;多个均数比较采用单因素重复测量资料方差分析,两两比较采用LSD检验;两变量之间采用直线相关分析,P<0.05为有统计学意义。
2 结果
2.1 TUNEL染色 正常对照组见少量TUNEL阳性细胞;假手术组各时间段均可检测到TUNEL阳性细胞;脑出血组6h后血肿周围脑组织可见TUNEL阳性细胞,72h达高峰,1周开始下降,与正常对照组、假手术组比较,差异有统计学意义(P<0.01)。见表1。
2.2 免疫组化检测 各组脑切片均可见IGF-1免疫反应阳性细胞表达,脑出血组IGF-1阳性细胞数量较正常对照组和假手术组明显增多,染色较强。图像分析结果显示,与正常对照组和假手术组比较,脑出血组IGF-1表达显著升高,差异有统计学意义(P<0.01),表达于24h达高峰,48h下降。见表2。
2.3 RT-PCR定量分析 与正常对照组、假手术组比较,脑出血组IGF-1 mRNA表达显著升高(P<0.05,P<0.01),24h 达高峰。见表 3。
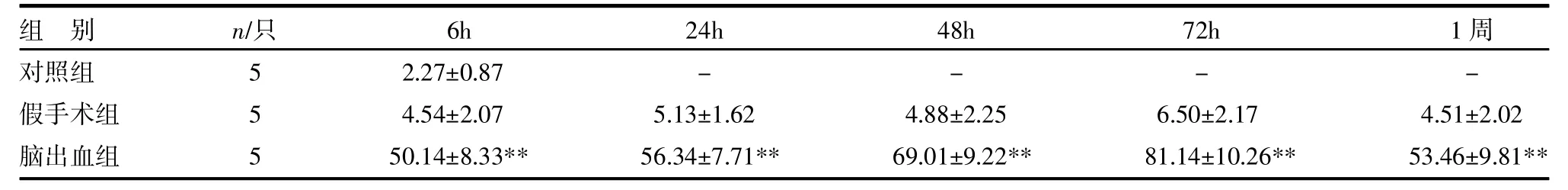
表1 各组大鼠脑组织细胞凋亡水平比较(x±s)
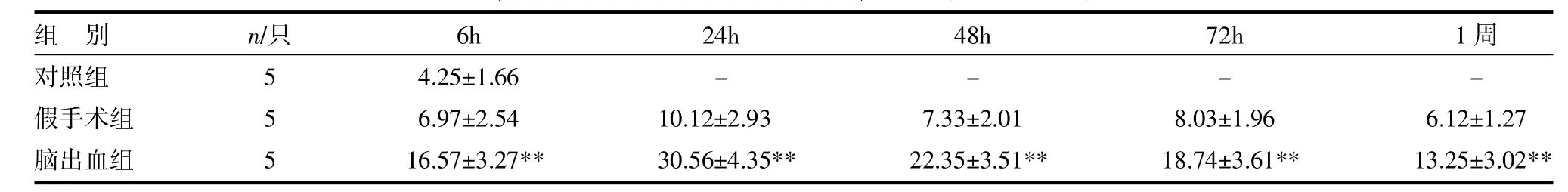
表2 各组大鼠脑组织IGF-1表达水平比较(x±s)

表3 各组大鼠脑组织IGF-1mRNA表达水平比较(x±s)
2.4 相关性分析 脑出血后血肿周围脑组织IGF-1阳性细胞数与TUNEL阳性细胞数呈正相关(r=0.62,P=0.027)。
3 讨 论
脑出血由于其高发病率、高致残率和高死亡率而严重威胁人类健康。但脑出血的病理生理机制目前尚未明确,脑出血后除血肿的占位效应和直接损伤外,继发性损伤也是脑组织损伤的一个重要原因。而各种原因导致的细胞凋亡则是继发性损伤的主要机制之一,研究表明,细胞凋亡参与了脑出血后继发性损伤[6-7],抑制细胞凋亡可以改善脑出血的预后。本实验发现,脑出血6h后血肿周围脑组织可见TUNEL阳性细胞,且72h达高峰,与正常对照组、假手术组比较有明显差异(P<0.01)。因此,细胞凋亡机制不仅参与了出血性脑损伤的病理生理过程,而且持续时间较长。脑出血后细胞凋亡既可能由脑出血后血肿占位直接导致,也可能由脑出血后血肿周围血流量下降,血管损伤后血液中的多种活性蛋白激活等因素所致。
研究表明,脑出血后造成的继发性损伤除了存在如细胞凋亡、自由基损伤、氧化应激、血红蛋白毒性等多种损害机制外,但亦存在重要的神经元保护机制[6,8]。其中IGF-1是一种与机体组织分化、增殖和成熟有关的重要细胞因子,因其与胰岛素具有结构同源性、且在机体许多组织中具有类似于胰岛素的作用而得名。近年研究发现,IGF-1是一种重要的调节神经生长的生物活性物质,它不仅是大脑发育所必需,而且能够在脑出血/脑缺血等多种病理状态下减轻对中枢神经系统造成的损伤,有助于神经细胞损伤后功能恢复,对神经组织生长发育起到非常重要的作用[9]。本实验结果显示,脑出血后IGF-1表达水平升高,24h达高峰,48h开始下降,表达水平均明显高于假手术组和正常对照组(P<0.05,P<0.01),且IGF-1阳性细胞数与TUNEL阳性细胞数呈正相关,既往研究也发现细胞凋亡促使IGF-1的高表达,两者密切相关[10],IGF-1的脑保护机制可能与抑制神经细胞凋亡,对抗兴奋性氨基酸毒性,调节一氧化氮酶活性,抑制一氧化氮的细胞毒性等有关[11]。
本实验结果显示,脑出血后IGF-1表达上调,参与脑出血的病理生理过程,可能对脑出血继发神经损伤起重要的保护作用。
[1]高丽丽,吴成翰.胰岛素样生长因子-1与脑出血[J].国际脑血管病杂志,2007,15(9):690-692.
[2]马莉.胰岛素样生长因子1对局灶性脑缺血大鼠的神经功能及神经细胞凋亡的影响[J].中国老年学杂志,2012,32(8):3469-3471.
[3]De Geyter D,Stoop W,Sarre S,et al.Neuroprotective efficacy of subcutaneous insulin-like growth factor-Iadministration in normotensive and hypertensive ratswith an ischemic stroke[J].Neuroscience,2013,250(10):253-262.
[4]李春岩,刘瑞春,胡书超,等.大鼠自体动脉血脑出血动物模型的建立[J].脑与神经疾病杂志,2003,11(6):341-344.
[5] Bederson JB,Pitts LH,Tsuji M,et al.Rat middle cerebral artery occlusion:evaluation of the model and development of a neurologic examination[J].Stroke,1986,17(3):472-476.
[6]刘宝华,王小同.急性期脑出血神经损伤机制的研究进展[J].温州医学院学报,2012,42(5):499-502.
[7]程娟,柯开富.脑出血后继发性脑损伤机制[J].国际脑血管病杂志,2010,18(10):787-791.
[8]缪星宇,刘晓斌,岳青,等.去铁胺对大鼠脑出血后小胶质细胞活化的抑制及其继发性神经损伤的保护作用[J].南方医科大学学报,2012,32(7):970-975.
[9]刘薇,张祥建.胰岛素样生长因子-1神经保护作用的研究进展[J].中国卒中杂志,2008,3(8):587-602.
[10]Tang M,Wang Q,LiHD,etal.Study on the anti-apoptosis effect of insulin-like growth factor I on the regulation of neural precursor cells survival[J].Sichuan Da Xue Xue Bao Yi Xue Ban,2014,45(1):15-18.
[11]王新平,曹国辉,宋洪波.胰岛素样生长因子-1在急性脑缺血中的作用[J].临床荟萃,2009,24(14):1282-1284.

