148例药品不良反应报告分析
黄惠红


摘 要 目的:了解药品不良反应的发生情况及产生原因,为临床合理用药提供参考。方法:对奉贤区中医医院2011年1月-2013年12月收集到的148例药品不良反应报告进行回顾性分析。结果:抗感染药物的不良反应发生率最高,占总数的62.8%(93例);其次为中成药,占总数的21.6%(32例)。静脉给药引发的药品不良反应占95.9%(142例),药品不良反应的临床表现以皮疹、瘙痒等皮肤及其附件损害最为常见。结论:应充分重视药品的不良反应,加强对药品不良反应的监测和管理力度,指导临床合理使用抗感染药及中药注射剂,避免或减少药品不良反应的重复发生。
关键词 药品不良反应 抗感染药 分析
中图分类号:R97; R969.3 文献标识码:A 文章编号:1006-1533(2014)03-0031-03
Report on the analysis of 148 cases of adverse drug reactions
HUANG Huihong
(Chinese Medicine Hospital of Fengxian District, Shanghai 201499, China)
ABSTRACT Objective: To understand the adverse drug reactions (ADR) occurred and their reasons, and provide a reference for clinical rational drug use. Methods: The data of 148 cases of ADR occurred from Jan. 2011 to Dec. 2013 were retrospectively analyzed. Results: Incidence of ADR of anti-infective drugs was the highest, accounting for 62.8% (93 cases), followed by Chinese medicine 21.6% (32 cases). ADR caused by intravenous administration accounted for 95.9% (142 cases). Skin rashes and itching and other skin damage are the most common in clinical manifestations of ADR. Conclusion: Sufficient attention should be paid to ADR, and the monitoring and management of ADR should be strengthened so as to guide the clinical rational use of anti-infective drugs and traditional Chinese medicine injection and to avoid or reduce the recurrence of ADR.
KEY WORDS adverse drug reaction; anti-infective drugs; analysis
药品不良反应 (Adverse Drug Reaction, ADR)是指合格药品在正常用量、用法下出现的与用药目的无关或意外的有害反应[1]。为了全面了解ADR发生的情况和上报质量,探讨ADR发生的易感因素,本文回顾性分析奉贤区中医医院2011年1月-2013年12月收集的148例ADR报告的资料,探讨ADR的特点,以促进临床合理用药。
1 资料与方法
1.1 资料来源
2011年1月-2013年12月由本院医护人员在临床工作中发现的ADR,以自发呈报方式上报到药剂科,经审定筛选后上报到上海市ADR监测中心,经确认的ADR报告148例。
1.2 方法
将呈报的148例ADR报告,按患者性别、年龄、药品种类、ADR临床表现、因果关系评价等进行统计分析。
2 结果
2.1 发生ADR患者的性别与年龄分布
148例ADR报告中,男性患者69例,占46.6%,女性患者79例,占53.4%,年龄最小5岁,最大93岁,60岁以上所占比例最高,发生ADR患者的性别与年龄分布见表1。
2.2 给药途径
148例ADR报告中,静脉给药引发ADR的发生率最高,有142例,占95.9%,口服给药4例,占2.7%,静脉注射1例,占0.7%,肌肉注射1例,占0.7%。
2.3 引发ADR的种类及构成比
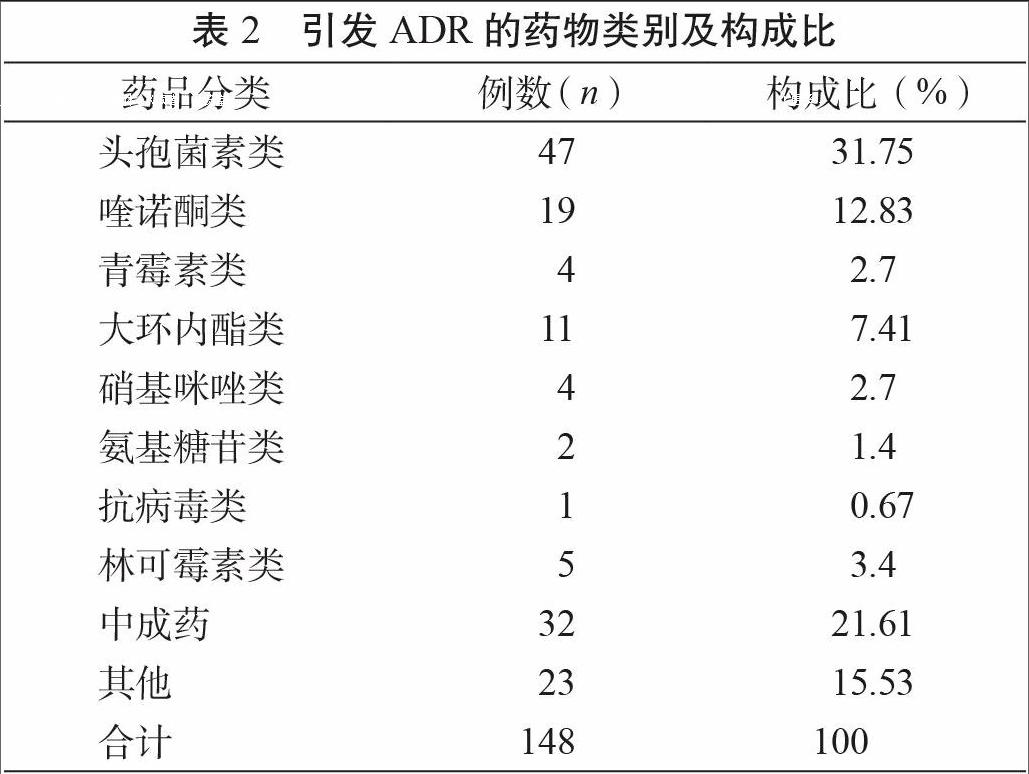
148例ADR报告中,引发ADR的药物共涉及8个类别,其中以抗菌药物和中成药为主,结果见表2。
2.4 ADR涉及的器官、系统分类及临床表现
在148例ADR报告中,涉及9个系统和器官,主要为皮肤及其附件损害,共36例,占总数的43.9%,消化系统损害16例,占 19.5% ,结果见表3。
2.5 引发严重ADR的药品、例数及临床表现
在148例ADR报告中,严重ADR报告有8例,占6%,涉及药品品种8种,结果见表4。
2.6 转归
上报的148例ADR在停用可疑药品或同时给予对症治疗后均治愈或好转,其中治愈124例,占84%,好转24例,占16% 。
3 讨论
3.1 性别、年龄对ADR的影响
从表1的数据来看,年龄构成比显示,148例ADR报告中患者年龄最小为5岁,因儿童处于生长发育过程,对药物具有特殊的反应性和敏感性,因此,控制儿科患者的输液量,提倡能口服尽量不注射的理念对降低10岁以下患者的ADR发生率很关键。60岁以上年龄组ADR的构成比最高,占41.2% ,老年人是一个特殊的用药群体,人体器官功能随着年龄的增长而衰退,肾脏的排泄功能、肝脏的代谢功能及血浆蛋白含量均降低,血浆蛋白与药物的结合力下降,易发生ADR;而且超过60岁的老年人因药物治疗而发生ADR的危险性是一般人的2.5倍。148例ADR报告中有1例老年人使用依达拉奉治疗急性脑梗死而出现急性肾功能衰竭,依达拉奉用于改善急性脑梗死所致的神经症状,不包括出血性脑血管病、颅脑外伤等疾病。本病例老人在用药前肾功能处于临界状态,用药5 d后尿素氮和肌酐急剧升高致急性肾衰,经停药治疗后好转。日本厚生省曾对依达拉奉发出警报,发现有致急性肾功能衰竭的报道[2],要求限制在无肾功能障碍患者中使用,对应用依达拉奉的老年患者要进行严格肾功能方面的监测,因此,临床用药时需慎重评估老年患者的肝、肾功能,谨慎选择药物及用法用量。
3.2 给药途径与ADR
导致ADR的主要给药途径是静脉给药,148例ADR中,静脉注射引起的有142例,占95.9%。静脉给药途径相对其它途径给药,发生ADR的频率最高。首先,这是由于静脉滴注时药物直接进入人体,无首过效应,作用及ADR较口服迅速而强烈。其次,静脉注射液的浓度,pH、渗透压、药物微粒和内毒素等均可成为引发ADR的因素[3]。同时,药物配制、药物的浓度、药液放置时间、滴速等也是引发ADR的因素。所以,要控制输液,加强输液配制的无菌操作,减少放置时间,避免不合理配伍等,以有效降低ADR的发生。因此,建议临床医生根据患者病情,能口服给药达到治疗目的的,原则上不使用静脉给药,能以小剂量分次给药的,不要以大剂量一次性给药,从而减少不必要的ADR发生。
3.3 抗菌药物类别及其ADR
从表2可见, 抗菌药物引起的ADR最多,可能与抗菌药物的广泛使用有关,其中以头孢类居首,其次是喹诺酮类。近年喹诺酮类药物因广谱、高效、安全而广泛用于临床,喹诺酮类药物除会引起常见的恶心、呕吐、上腹部不适外,可能会引起变态反应,如皮疹、红斑、瘙痒、光敏反应等,还须注意少见的严重ADR——癫痫发作。其作用机制为喹诺酮类具有脂溶性,组织渗透力强,并且可以透过血脑屏障,颅内脑脊液中浓度高,抑制递质γ-氨基丁酸(GABA)与其受体结合的作用,从而引起中枢神经系统疾病 [4],因此,在临床应用时要询问患者有无癫痫病史及中枢神经系统疾病史。中药注射剂ADR报告较多与我院是一家中医医院,使用中药注射剂频率高有关, 148例ADR报告中有2例血塞通注射液和热毒宁注射液引起的过敏性休克,可能与中药制剂成分复杂、作用机制不明、药材质量参差不齐、质量标准不高、生产工艺不稳定有关。因此,临床使用中药注射剂须遵循中成药临床使用基本原则,严格掌握适应证、辨证用药、严格掌握用法用量、严禁混合配伍等,特别是要加强用药监护。
3.4 ADR涉及的系统或器官及临床表现
从表3可见, ADR引起的各系统、器官症状,以皮肤及其附件损害最多,有81例次,占54.7%,可能是由于皮肤损害的临床表现易于观察和诊断,而且不易与其他疾病相混淆。148例ADR报告中,皮肤损害有一个严重的ADR,由口服醋甲唑胺片引起表皮松解剥脱, 醋甲唑胺是含有磺酰胺基的碳酸酐酶抑制剂,临床上以口服给药用于治疗青光眼及眼科术后降眼压,醋甲唑胺说明书中提到对磺胺少见的严重ADR会造成死亡,包括Stevens-Johnson综合征、表皮溶解坏死[5]。因此,临床应重视用药前详细询问药品过敏史, 一般在发生ADR后的处理过程中,应停药或给予抗组胺药物、激素等药物处理。
4 结语
从以上分析可以看出,加强ADR监测是临床必不可少的工作,尽管一部分ADR具有不可预测性,但是大多数的ADR是可以避免的,要加强对临床医生的宣传,药师严格审方,同时把ADR反馈给医生,还须加强对临床医生进行药物知识的培训,全面了解药物的药理机制及其ADR, 做到及时发现、及时治疗、及时上报,从而真正确保患者的用药安全。
参考文献
[1] 邵家荣. 社区卫生服务中心254份药品不良反应报告分析[J]. 上海医药, 2012, 33(3): 19-20, 25.
[2] 彭涛, 王林. 日本厚生省对依达拉奉发出警报[J]. 国外医学: 药学分册, 2003, 20(2): 126.
[3] 何娟, 方洁, 陈冰, 等. 我院187例年药品不良反应报告分析[J]. 中国药房, 2011, 22(14): 1312-1313.
[4] 吴子杰. 药品不良报告分析[J]. 现代医院, 2011, 11(14): 64-65.
[5] 闫成, 蔡长春, 薛洪源. 醋甲唑胺致Stevens-Johnson综合症及中毒性表皮坏死溶解症文献分析[J]. 医药导报, 2013, 32(2): 270-271.
(收稿日期:2013-11-11)

