饲料中亚油酸和亚麻酸含量对团头鲂幼鱼生长、体成分和消化酶活性的影响
王煜恒,刘文斌,王会聪,陈军,骆桂兰,邢军
(1.江苏农林职业技术学院 畜牧兽医系,江苏 镇江212400;2.南京农业大学 动物科技学院 江苏省水产动物营养重点实验室,江苏南京210095)
鱼类的必需脂肪酸(essential fatty acid,EFA)是一些不能由鱼体自身合成而只能由食物提供的满足其正常生长发育及维持细胞组织功能所必需的多不饱和脂肪酸。必需脂肪酸缺乏或者相互之间组成不平衡,均会导致鱼类生长速度及饲料转化率下降,肌肉中水分和肝脏中脂肪含量显著增加,并引发多种病理缺乏症[1-3]。淡水鱼和海水鱼在EFA需求上存在较大差异,淡水鱼能利用18 碳脂肪酸合成20 碳或22 碳脂肪酸,因此,它的EFA 主要是C18:2n-6(linoleic acid,LA)和C18:3n-3(α- linolenic acid,ALA),而海水鱼主要对高不饱和脂肪酸如C20:5n-3(EPA)和C22:6n-3(DHA)需求比较大[4]。
以往研究EFA 需要量的试验都采用单因素设计,即在饱和或单不饱和脂肪酸的基础上添加单一的EFA,最近有学者开始通过在脂肪中添加两种或更多的EFA 来研究各种EFA 之间的交互作用。Smith等[5]通过4 ×4 双因子试验发现,砂鲈Bidyanus bidyanus 对LA 的最适需要量为1.7 g/kg;斑节对虾Penaeus monodon 饲料中n -3和n -6 系列EFA 的比例为2.5 ~1.0 时,其生长效果最佳[6];黄颡鱼Pelteobagrus fulvidraco日粮中ALA 与LA 的比例为1.17和2.12 时,其增重率最高且饲料系数最低[7]。但EFA 之间交互作用的机理目前尚不清楚,推测可能与其改变细胞膜结构,或者其变构效应对脂肪酸去饱和酶和竞争性底物的影响有关[8]。
团头鲂Megalobrama amblycephala是中国主要的淡水养殖品种之一。目前关于团头鲂对EFA 需要量的研究尚未见报道,刘玮等[9]在不同脂肪源对团头鲂幼鱼生长影响的研究中发现,团头鲂的EFA 应同时包含LA和ALA,且对LA 的需求要比对ALA 更大。Takeuchi等[10]认为,鲤Cyprinus carpio 的EFA 应包括1%的LA和1%的ALA,草鱼Ctenopharyngodon idella[11]的EFA 与 鲤 相 似,为0.5% ~1.0%的ALA和1.0%的LA。鉴于团头鲂同属鲤科鱼类,对EFA 的需要量应该比较相近,因此,本试验在前人研究的基础上[12],通过在含35%蛋白质和7%脂肪的基础日粮中添加LA(3 个水平)和ALA(3 个水平),探讨LA和ALA 的不同含量对团头鲂幼鱼生长性能、形体指标、体成分和消化酶活性的影响,从而确定团头鲂幼鱼对这两种EFA 的最适需要量,以期为团头鲂的脂肪酸需求研究和饲料油脂的选择提供参考。
1 材料与方法
1.1 材料
试验在南京农业大学水产动物营养和生态实验室进行。试验用鱼为购自上海松江浦南水产良种场的团头鲂“浦江1 号”夏花。
1.2 方法
1.2.1 试验设计与试验饲料 试验设3 个LA 水平(0.5%、1.0%、1.5%,占饲料质量比)和3个ALA 水平(0.5%、0.9%、1.3%),采用3 ×3双因子设计方法配制成9种饲料,记为L0.5A0.5、L0.5A0.9、L0.5A1.3、L1.0A0.5、L1.0A0.9、L1.0A1.3、L1.5A0.5、L1.5A0.9、L1.5A1.3,分别投喂9 组鱼,每组设4 个重复。以酪蛋白和明胶为主要蛋白源,玉米淀粉为糖源,羧甲基纤维素为黏合剂,并填充微晶纤维素、矿物质等制成等氮等能的基础日粮。基础日粮配方(均为质量分数,%)为:酪蛋白32.00、明胶8.00、玉米淀粉30.00、微晶纤维素15.50、羧甲基纤维素3.00、预混料1.00、磷酸二氢钙1.90、沸石粉2.00、抗氧化剂0.10、氯化钠0.50、油脂6.00。以鱼油、豆油、花生油、亚麻油、油酸和棕榈酸为脂肪源,通过几种油脂的不同配比来调节日粮中LA和ALA的水平。饲料营养组成及油脂配制见表1,饲料脂肪酸组成见表2。将各组饲料逐级混合均匀,再加水拌匀,用QRLS-150Ⅱ型电动绞肉机制成颗粒,成型后先进行破碎再经20 ~40 目(粒径为380 ~830 μm)筛两次筛分,25 ℃下风干,置于冰箱(-20 ℃)中保存备用。
1.2.2 饲养管理 试验前先于试验环境下投喂商品料暂养,驯化10 d 后,选取体格健康、无畸形体质量为(0.80 ±0.02)g 的团头鲂鱼苗720 尾,随机投放36 个水族箱(直径为52 cm,水深为50 cm)中,每箱20 尾。试验期间,每3天换水一次,每次换水量为总水量的30%。每天7:00、12:00、17:00 投饲,日投饲率为鱼体质量的3% ~5%,投喂之前吸出粪便,饲料投喂持续20 min,投喂结束后30 min,捞出残饵烘干称重。试验周期为56 d。试验用水为曝气自来水,水温为(27 ±3)℃,pH 为6.8 ~8.0,溶解氧>5 mg/L。
1.2.3 指标的测定与计算
(1)生长性能与营养成分。试验鱼养殖56 d后,停饲24 h,测定总质量,计算增重率、特定生长率、饲料系数、蛋白质效率,并随机从每箱取6尾鱼测量体长、体质量,解剖取其肝胰脏及全部内脏称重,计算肥满度、肝胰脏指数和脏体指数。同时取肠道,并将剩余的所有幼鱼用4 ℃预冷的盐度为8.6 的生理盐水冲洗,然后用滤纸吸干水分,于-20 ℃下保存备用。参照AOAC[13]的方法测定饲料和鱼体中的水分、粗蛋白质和灰分含量,干物质烘干(105 ℃)至恒重,通过失重法测定;用凯氏定氮仪(2300Kjeltec Analyzer Unit,FOSS TECATOR,Sweden)测定粗蛋白含量;用马福炉(550 ℃)燃烧失重法测定灰分含量;参照Folch等[14]的方法测定粗脂肪含量。每个样品至少测定3 个平行。增重率(WG)、特定生长率(SGR)、饲料系数(FCR)、蛋白质效率(PER)、肥满度(CF)、肝体指数(HSI)、脏体指数(VSI)的计算公式为

表1 饲料营养组成及油脂配制Tab.1 Approximate composition of the experimental diets and preparation of the dietary fat

(2)消化酶。将肠道解冻之后准确称重,使用去离子水按质量比为1∶ 9 进行冰浴匀浆,以3000 r/min 离心10 min,收集上清液标号分装待测,于4 ℃下保存,24 h 内测定完毕。采用福林-酚法测定总蛋白酶[15]。采用南京建成公司的试剂盒测定各种消化酶活性。蛋白酶活力单位定义为:在27 ℃条件下,每分钟水解酪素产生相当于1 μg酪氨酸所需的酶量为1 个酶活力单位。脂肪酶活力单位定义为:在27 ℃条件下,每克组织蛋白在本反应体系中与底物反应1 min,每消耗1 μmol 底物为1 个酶活力单位。淀粉酶活力单位定义为:每毫克蛋白在27 ℃下与底物作用30 min,水解10 mg淀粉定义为1 个酶活力单位。
(3)脂肪酸。饲料样品中脂肪的提取参照Folch等[14]的方法。油脂的皂化及甲酯化方法参照Christie[16]的方法,略有改进。样品皂化甲酯化后,用气相色谱-质谱仪进行分析。分析仪器为岛津GCMS-QP2010 Plus 气质联用仪,色谱柱为HP -5MS(30 m×0.25 mm×0.25 μm);色谱柱升温程序为初温50 ℃,以10 ℃/min 升至150 ℃并保持3 min,以3 ℃/min 升至230 ℃保持3 min;进样方式为分流进样,分流比为10∶ 1,进样量为1 μL,载气为高纯氮气,气流为1.3 mL/min。检索NIST质谱图库,比较样品质谱图与图库中标准质谱图,即可确定样品中脂肪酸种类,采用面积归一化法计算各脂肪酸的相对含量。
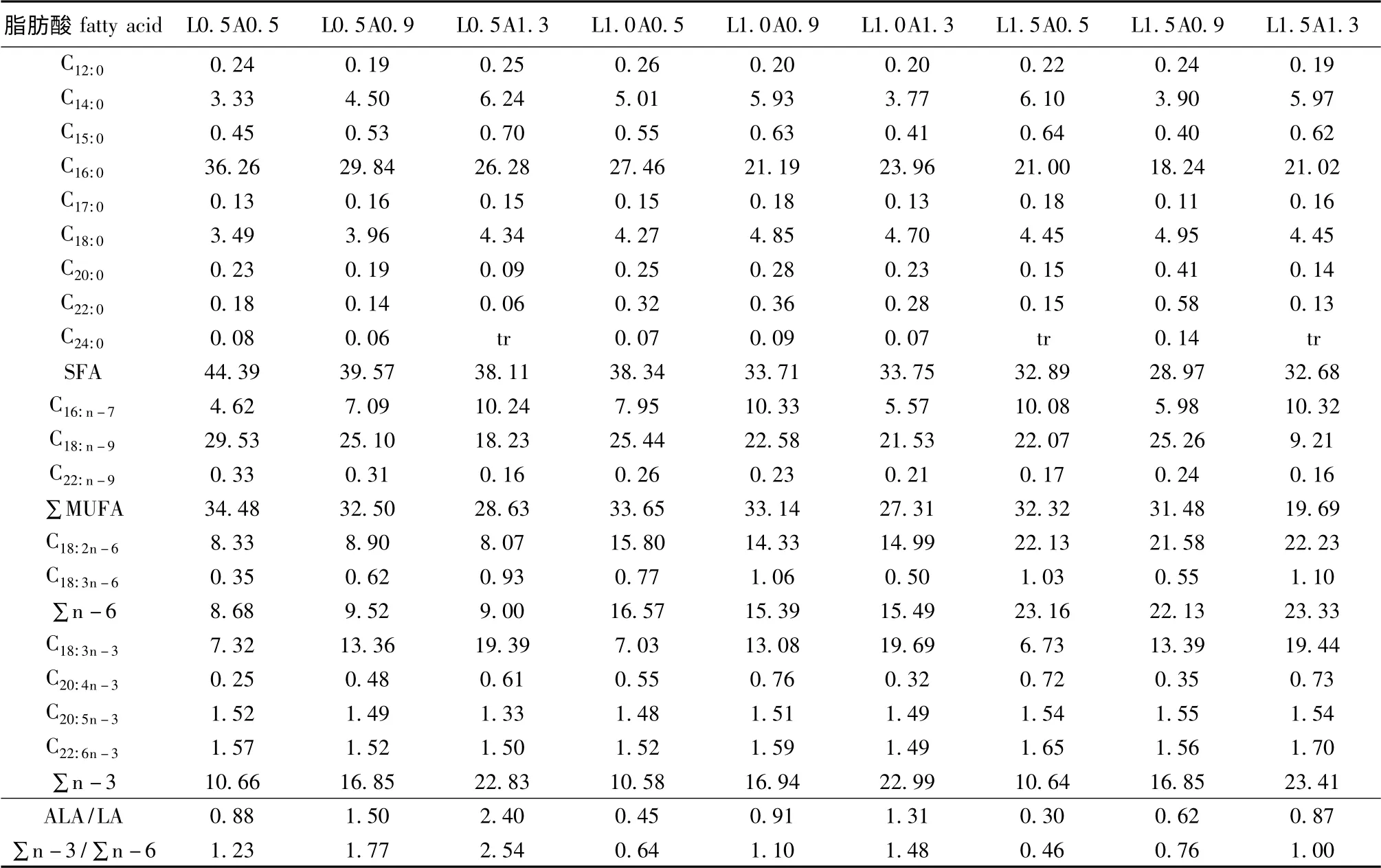
表2 各组试验饲料脂肪酸的组成Tab.2 The fatty acid composition of the experimental diets w/%
1.3 数据处理
试验数据均用平均值± 标准误(means ±S.E.)表示。采用SPSS 18.0 软件进行单因素方差分析(One-Way ANOVA)。当差异显著时,以饲料LA和ALA 添加水平为主要影响因子,进行双因素方差分析,采用Duncan 法进行组间多重比较。
2 结果与分析
2.1 LA和ALA 含量对幼鱼生长性能的影响
养殖试验期间,各试验组幼鱼肉眼未发现组织病变。从表3可见:饲料中LA和ALA 含量对团头鲂幼鱼WG和SGR 的影响极显著(P<0.01);当饲料中LA 的添加量为0.5%时,幼鱼的WG、SGR和PER 均显著低于其他两个LA 组(P<0.05);而当ALA 添加量为0.9%时,幼鱼的WG、SGR和PER 均显著高于1.3%组(P<0.05),但与0.5%组无显著性差异(P >0.05)。同时发现:LA 与ALA 之间存在交互作用,当饲料中LA 含量为1.0%且ALA 的含量为0.9%时,其WG和SGR 均达 到 最 高,显 著 高 于L0.5A0.5、L0.5A1.3和L1.5A1.3 组(P<0.05),但与其他组无显著性差异(P >0.05);L1.0A0.5 组PER 为各组最高且与L1.0A0.9、L1.5A0.5和L1.5A0.9 组无显著性差异(P >0.05),但显著高于其他组(P<0.05)。观察FCR 发现,当饲料中ALA 为1.3%时,显著高于其他两个ALA 组(P<0.05),而LA 添加量对其无显著影响(P >0.05)。各试验组存活率无显著性差异(P >0.05)。通过二次回归分析得到增重率(y)与LA(x)的关系式为y=-96.043x2+208.88x+265.3(R2=0.3337),当增重率最高时LA 为1.09%,其回归曲线见图1。同时建立增重率(y)与ALA(x)的关系式为y=-154.77x2+260.08+269.93(R2=0.3293),当增重率最高时ALA 为0.84%,其回归曲线见图1。

表3 饲料中亚油酸和亚麻酸含量对团头鲂幼鱼生长性能的影响Tab.3 Effect of dietary linoleic acid and linolenic acid levels on growth performance in juvenile blunt snout bream
2.2 LA和ALA 含量对幼鱼形体指标的影响
从表4可见:饲料中LA和ALA 含量对团头鲂HSI和VSI 无显著影响(P >0.05),但随着饲料中LA和ALA 含量的增加HSI 均呈下降趋势,L0.5A0.5 组的HSI 达到2.80,为各组最高;LA为1.0%组的VSI 略小于其他两个LA 组,而ALA为1.3%组的VSI 略高于其他两个ALA 组;团头鲂幼鱼的CF 受LA 的影响显著(P<0.05),LA 为1.0%组的CF 显著高于其他两个LA 组(P<0.05),ALA 对CF 影响不显著(P >0.05),但0.9%组的CF 略高于其他两个ALA 组。
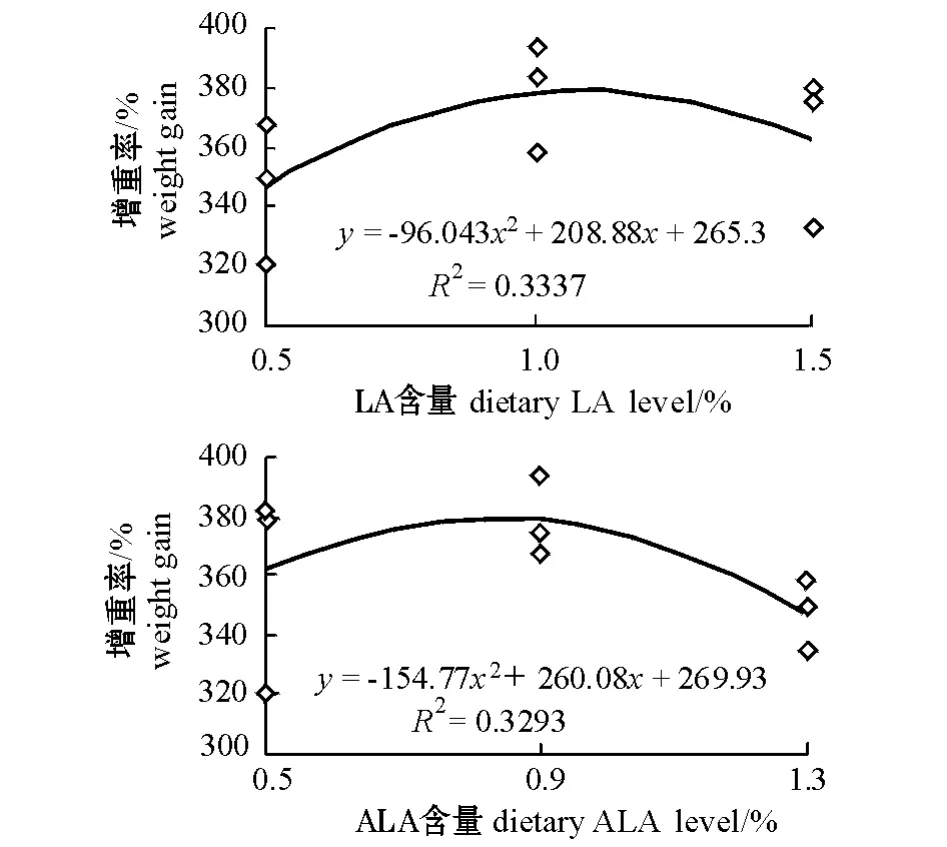
图1 饲料中亚油酸和亚麻酸含量与增重率的关系Fig.1 Effect of dietary LA,and ALA levels on weitght gain of blunt snout bream

表4 饲料中亚油酸和亚麻酸含量对团头鲂幼鱼形体指标的影响Tab.4 Effect of dietary LA and ALA levels on morphometric index of juvenile blunt snout bream
2.3 LA和ALA 含量对幼鱼体组成的影响
从表5可见,饲料中LA和ALA 对全鱼的粗蛋白质与粗灰分含量均无显著影响(P >0.05)。LA为1.0%组的全鱼粗蛋白质含量略高于其他两个LA 组,但粗蛋白质含量随ALA 添加量的增加呈下降趋势;LA 为0.5%组的全鱼水分含量显著高于其他两个LA 组(P<0.05);LA 为0.5%组的全鱼粗脂肪含量显著低于其他两个LA 组(P<0.05);ALA 对全鱼水分和粗脂肪含量均无显著影响(P >0.05);LA和ALA 均对肝胰脏脂肪含量的影响显著(P<0.05),LA 为0.5%组显著高于其他两个LA 组(P<0.05),ALA 为0.9%组显著低于其他两个ALA 组(P<0.05),但LA和ALA对肝胰脏脂肪含量不存在交互作用,L0.5A0.5 组的肝胰脏脂肪含量为各组最高。
2.4 LA和ALA 含量对幼鱼消化酶活性的影响
从表6可见:饲料中LA和ALA 对团头鲂肠道淀粉酶活性无显著影响(P >0.05);LA 为1.0%组的肠道脂肪酶活性显著高于LA 为0.5%组(P<0.05),但与1.5%组无显著性差异(P >0.05),ALA 为1.3%组显著低于其他两个ALA 组(P<0.05),此外两种EFA 对脂肪酶存在交互作用,L0.5A0.5和L1.5A1.3 组显著低于L1.0A0.5和L1.0A0.9 组(P<0.05),其他组之间无显著性差异(P >0.05);LA 为0.5%组的肠道蛋白酶活性显著低于其他两个LA 组(P<0.05),ALA 为1.3%组的蛋白酶活性显著低于其他两个ALA 组(P<0.05)。
3 讨论
本试验中通过在等氮等能的纯合饲料基础上添加不同水平的LA和ALA,在各组饲料中提供等量的EPA和DHA 来研究团头鲂幼鱼对这两种脂肪酸的需求量,由于饲料中EFA 过量或缺少时都会对鱼类的增重率产生影响[17],所以本试验中以团头鲂幼鱼的增重率作为主要评判指标来研究幼鱼对这两种脂肪酸的适宜需求量。结果表明:增重率随LA 含量的增加而逐渐升高,当LA 添加量为1.0%时达到最高,而LA 增加到1.5%时增重率有所下降但不显著;当ALA 添加量为0.5%和0.9%时,增重率无显著差异,但当ALA 达到1.3%时对团头鲂生长有一定的阻碍作用。Glencross等[18]研究表明:斑节对虾的增重率随饲料中ALA 含量的增加而升高,当ALA 达到2.6%时其增重率最高,再增加时就对其生长产生消极影响;LA 对生长虽有促进作用,但过量时对生长的抑制作用可能与ALA的交互作用有关。Smith等[5]研究砂鲈对LA和ALA 的需要量时发现,随LA 含量的增加其增重率升高,最适添加量为1.8%,当添加量为2.3%时增重率明显下降,但ALA 对增重率影响不显著。本试验结果与上述研究相似,团头鲂幼鱼同样对LA和ALA 的需要量有一个适宜范围,添加量过多或过少都会影响其生长,参照Zuridah等[19]的方法进行二次回归分析,得出当LA 为1.09%和ALA为0.84%时可使增重率分别达到最高。本试验中发现,LA和ALA 对增重率的影响存在一定的交互作用,Glencross等[18]认为,饲料中LA和ALA 的交互作用对增重率的影响与这两种EFA在饲料中的平衡(即饲料中LA和ALA 应保持适宜水平和比例)密切相关,这种平衡性主要体现在LA和ALA在体内进行生物合成HUFA 过程中两者对△6和△5 去饱和酶系统底物的竞争性抑制[20]。本试验中发现,各组饲料系数普遍偏高,推测可能与纯合饲料适口性较差和消化吸收率低有关;LA 对饲料系数影响不大,但当ALA 添加过量后会导致饲料系数升高,这可能与过量ALA 会阻碍团头鲂幼鱼生长有关。
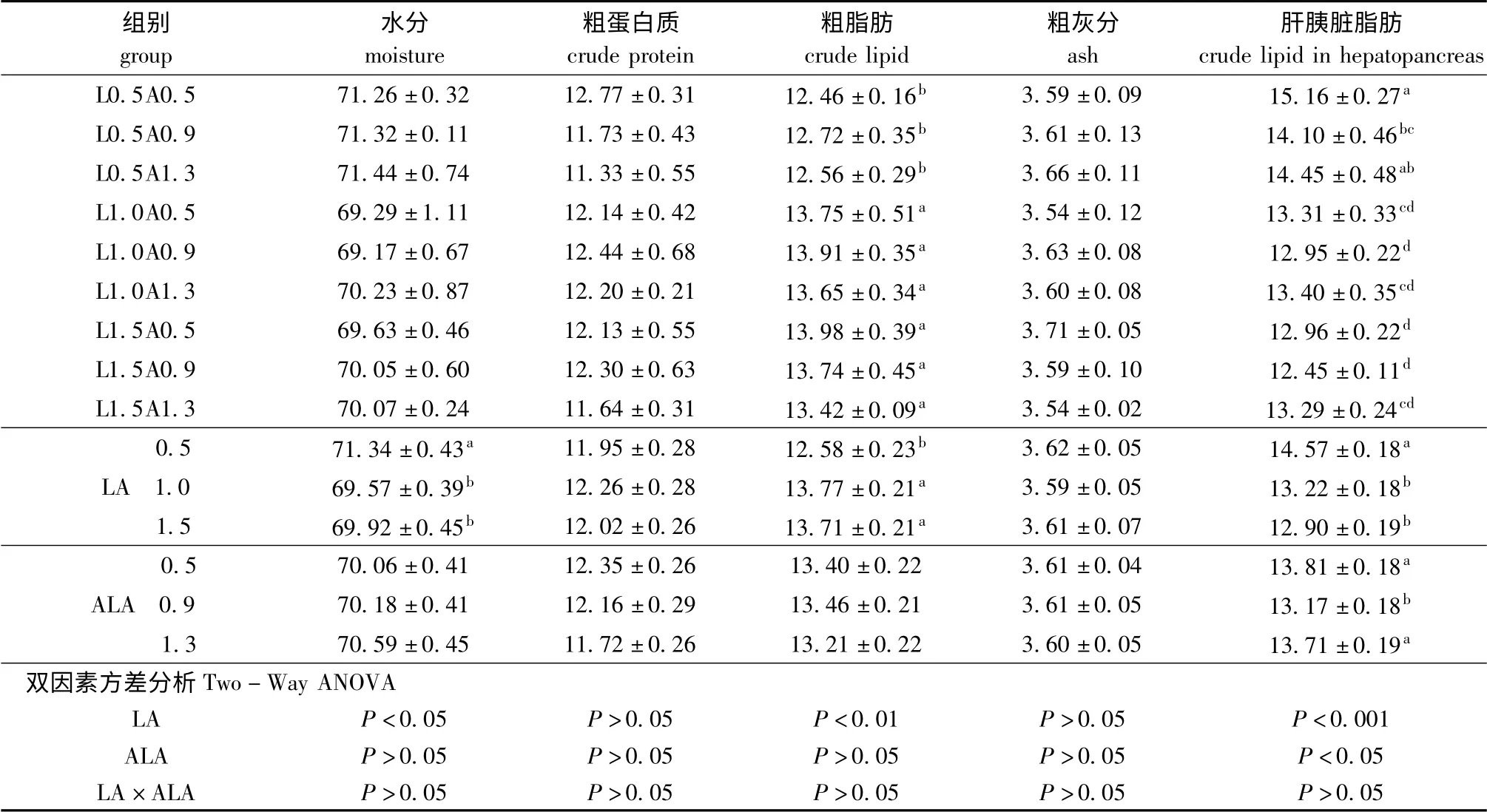
表5 饲料中亚油酸和亚麻酸含量对团头鲂幼鱼全鱼体组成的影响(湿质量)Tab.5 Effect of dietary LA and ALA levels on whole body composition(wet weight basis)of juvenile blunt snout bream w/%
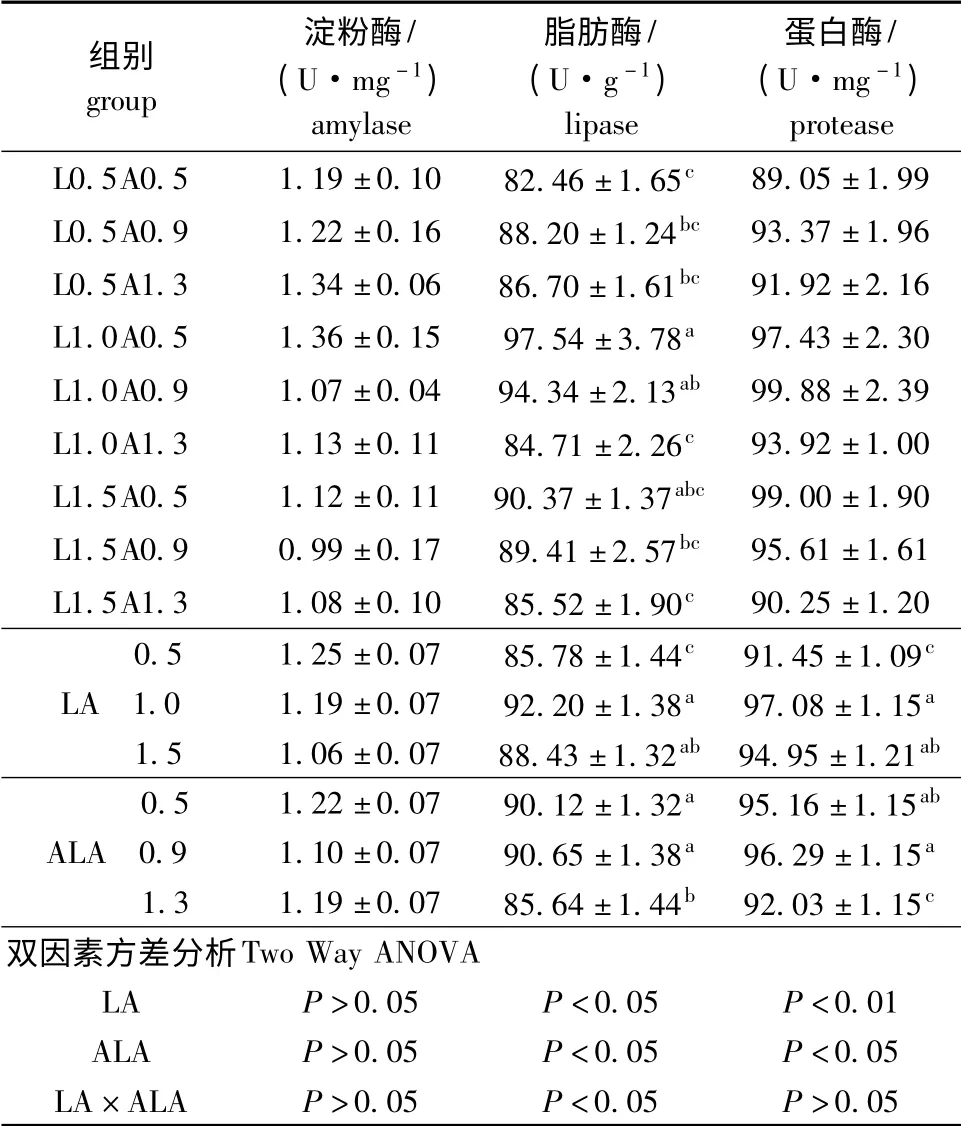
表6 饲料中亚油酸和亚麻酸含量对团头鲂幼鱼肠道消化酶活性的影响Tab.6 Effect of dietary LA and ALA levels on activities of intestinal digestive enzymes in juvenile blunt snout bream
Takeuchi等[21]研究了EFA 对虹鳟Oncorhynchus mykiss 的营养功能,发现EFA 缺乏可使该鱼肝脏脂质特别是中性脂肪大量积累,而磷脂含量大幅降低。其他学者在大菱鲆Scophthalmus maximus[22]和鲑鱼Oncorhychus keta[23]等鱼类中也观察到,缺乏EFA 时鱼类肝脏中脂质积累增加并且肝质量相对增大。本试验结果表明,LA 为0.5%组的鱼体肝胰脏脂肪含量显著高于其他两个LA 组,LA 对鱼体肝体指数的影响虽不显著但趋势相似,这些表明,当LA 添加量为0.5%时不能满足鱼体需要,导致EFA 缺乏。饲料中ALA 对鱼体肝胰脏脂肪含量和肝体指数的影响结果显示,添加0.9%的ALA时团头鲂幼鱼肝脏表现的更为健康。Lee等[24]对星斑川鲽Platichthys stellatus 的研究发现,当EFA 缺乏时全鱼的粗脂肪含量也有所降低。本试验中发现:LA 为0.5%组的全鱼粗脂肪含量显著小于LA为1.0%和1.5%组;ALA 对全鱼粗脂肪含量的影响虽不显著,但ALA 为0.9%组还是要稍高于其他两个ALA 组,由此认为,LA 为1.0%和ALA 为0.9%时,更能满足鱼体EFA 的需要。
本试验中发现:LA 为1.0%时团头鲂幼鱼的肥满度显著高于0.5%和1.5%组,LA 对全鱼粗蛋白质含量的影响无显著性差异,但1.0%组粗蛋白质含量稍高于其他两个LA 组;ALA 对肥满度无显著影响,但ALA 为0.9%时为3 组中最高。薛敏等[25]认为,鱼类的生长效果和鱼体品质与饲料中EFA 的适宜含量和比例密切相关。结合本试验中当LA 为1.0%和ALA 为0.9%时,鱼体肥满度、全鱼粗蛋白质、粗脂肪含量较高,肝胰脏脂肪含量较低,说明此时饲料中EFA 的含量是适宜的。
当考虑LA 与ALA 的交互作用影响时,L1.0A0.9、L1.5A0.5、L1.5A0.9 组的相关指标均较好,而L1.0A0.5、L1.0A1.3、L1.5A1.3 组也未表现出 EFA 极度缺乏或者过量症状,仅L0.5A0.5、L0.5A0.9、L0.5A1.3 组表现 出EFA不足的可能症状,故从对形体指标和机体成分的影响综合分析,团头鲂幼鱼对LA、ALA 均需要,但对LA 的需求更大,当LA 为0.5%时可能会产生EFA 缺乏,当LA 为1.5%和ALA 为1.3%时也能耐受。
鱼类消化酶活性的高低能直接反映对营养物质的消化吸收能力,提高鱼体的消化酶活性就能提高鱼对营养物质的消化能力,鱼类对营养物质的吸收也会随之增加[26]。本试验结果显示:当LA 的添加量为1.0%时,肠道脂肪酶活性最大;ALA 添加水平为1.3%时能显著降低脂肪酶活性。作者推测,这两种EFA可能通过消化酶影响鱼体消化吸收,从而造成对鱼体体脂沉积的改变,但有待进一步试验验证。饲料中LA和ALA 对蛋白酶的影响显著,当LA 过低和ALA 过高时都会导致蛋白酶活性降低,虽然EFA 对蛋白酶活性的影响未显著改变鱼体组织中蛋白质的积累,但是可以通过提高团头鲂对蛋白质的利用率,促进鱼体生长。
综上所述,从团头鲂幼鱼的生长性能、形体指标、体成分和消化酶数据来看,团头鲂幼鱼对LA的需要量为1.0% ~1.5%,对ALA 的需要量为0.5% ~0.9%。通过二次回归方程分析得出,当LA 为1.09%和ALA 为0.84%时,团头鲂幼鱼生长较好,各项生理机能指标正常。
[1]Watanabe T,Ogino C,Koshiishi Y,et al.Requirement of rainbow trout for essential fatty acids[J].Bulletin of the Japanese Society of Scientific Fisheries,1974,40:493 -499.
[2]刘穗华,曹俊明,黄燕华,等.饲料中不同亚麻酸/亚油酸比对凡纳滨对虾幼虾生长性能和脂肪酸组成的影响[J].动物营养学报,2010,22(5):1413 -1421.
[3]Glencross B D,Smith D M.The dietary linoleic and linolenic fatty acids requirements of the prawn Penaeus monodon[J].Aquaculture Nutrition,1999,5(1):53 -63.
[4]Sargent J,Henderson R J,Tocher D R.The lipids[M]//Halver J E.Fish Nutrition.2nd ed.New York:Academic Press,1989:153-218.
[5]Smith D M,Hunter B J,Allan G L,et al.Essential fatty acids in the diet of silver perch(Bidyanus bidyanus):effect of linolenic and linoleic acids on growth and survival[J].Aquaculture,2004,236:377 -390.
[6]Blanchard G,Makombu J G,Kesternont P.Influence of different dietary 18:3n-3/18:2n-6 ratio on growth performance,fatty acid composition and hepatic ultrastructure in Eurasian perch,Perca fluviatilis[J].Aquaculture,2008,284(1/4):144 -150.
[7]Tan X Y,Luo Z,Xie P,et al.Effect of dietary linolenic acid/linoleic acid ratio on growth performance,hepatic fatty acid profiles and intermediary metabolism of juvenile yellow catfish Pelteobagrus fulvidraco[J].Aquaculture,2009,296:96 -101.
[8]Garg M L,Sebokava E,Thomson A B R,et al.Δ6 -desaturase activity in liver microsomes of rats fed diets enriched with cholesterol and/or ω3 fatty acids[J].Biochem J,1988,249:351 -356.
[9]刘玮,戴年华,任本根,等.不同脂肪源饲料对团头鲂稚鱼生长的影响[J].水产学报,1997,21(1):44 -48.
[10]Takeuchi T,Watanabe T.Requirement of carp for essential fatty acids[J].Bulletin of the Japanese Society of Scientific Fisheries,1977,43(4):541 -551.
[11]Takeuchi T,Watanabe K,Yong W Y,et al.Essential fatty acids of grass carp Ctenopharyngodon idella[J].Bulletin of the Japanese Society of Scientific Fisheries,1991,57:467 -473.
[12]Li X F,Liu W B,Jiang Y Y,et al.Effects of dietary protein and lipid levels in practical diets on growth performance and body composition of blunt snout bream(Megalobrama amblycephala)fingerlings[J].Aquaculture,2010,303:65 -70.
[13]AOAC.Official Methods of Analysis[M].15th ed.Arlington:Association of Official Analytical Chemists,1990:684.
[14]Folch J,Lees M,Stanley G H S.A simple method for the isolation and purification of total lipids from animal tissues[J].The Journal of Biological Chemistry,1957,226(1):497 -509.
[15]Lowry O P,Rosebrough N J,Farr A L,et al.Protein measurement with the folin - phenol reagent[J].The Journal of Biological Chemistry,1951,193(1):265 -275.
[16]Christie W W.A simple procedure for rapid transmethylation of glycerolipids and cholesteryl esters[J].Journal of Lipid Research,1982,23:1072 -1075.
[17]Zeitoun I H,Ullrey D E,Magee W T,et al.Quantifying nutrient requirements of fish[J].J Fish Res Board Can,1976,33:167 -172.
[18]Glencross B D,Smith D M,Thomas M R,et al.The effect of dietary n-3 and n-6 fatty acid balance on the growth of the prawn Penaeus monodon[J].Aquaculture Nutrition,2002,8(1):43-51.
[19]Zuridah O,Shim M K F.Quantitative requirements of linolenic and docosahexaenoic acid for juvenile Penaeus monodon[J].Aquaculture,1997,157:277 -295.
[20]Henderson R J,Tocher D R.The lipid composition and biochemistry of freshwater fish[J].Progress in Lipid Research,1987,26(4):281 -347.
[21]Takeuchi T,Watanabe T.Effects of various polyunsaturated fatty acids on growth and fatty acid composition of rainbow trout,Oncorhynchus keta[J].Bulletin of the Japanese Society of Scientific Fisheries,1982,48:1745 -1752.
[22]Cowey C B,Owen J M,Adron J W,et al.Studies on the nutrition of marine flatfish[J].Bri J Nutr,1986,36:479 -486.
[23]Takeuchi T,Watanabe T,Nose T.Requirement for essential fatty acids of chum salmon(Oncorhynchus keta)in fresh water environment[J].Bulletin of the Japanese Society of Scientific Fisheries,1979,45:1319 -1323.
[24]Lee S M,Lee J H,Kim K D.Effect of dietary essential fatty acids on growth,body composition and blood chemistry of juvenile starry flounder(Platichthys stellatus)[J].Aquaculture,2003,225:269 -281.
[25]薛敏,李爱杰,张显娟.牙鲆幼鱼对EPA和DHA 的营养需求[J].水产学报,2004,28(3):285 -291.
[26]李卫芬,沈涛,陈南南,等.饲料中添加枯草芽孢杆菌对草鱼消化酶活性和肠道菌群的影响[J].大连海洋大学学报,2012,27(3):31 -35.

