血府逐瘀汤对大鼠后肢缺血模型血管新生的影响❋
施伟丽,苏晓艳,庄淑美,胡雅琼,高 冬△,宋 军
(1.中国中医科学院医学实验中心,北京 100700;2.北京市海淀医院,北京 100080;3.福建中医药大学中西医结合学院,福州 350122)
缺血模型的建立是缺血性疾病及血管再生研究的一种有效途径,成功建立一种效果确切、简单可靠的肢体缺血模型是保证后续实验顺利进行的关键。动物后肢动脉表浅的特点,使后肢缺血模型的制作相对简单,也就使得后肢缺血模型在血管新生的研究中颇为多用。本实验用白及微球栓塞法制作SD大鼠后肢缺血模型,并观察不同剂量血府逐瘀汤对该模型缺血组织血管新生的影响,为血府逐瘀汤促血管新生的研究提供进一步的实验依据。
1 材料与方法
1.1 动物
无特定病原体(Specific pathogen Free,SPF)4周龄雄性SD大鼠18只,体质量300±20 g,由上海斯莱克实验动物有限责任公司提供(合格证号2007000542160,生产许可证号SYXK(沪)2012-0002)。经福建中医药大学动物实验中心SPF级动物房饲养,自由饮水,普通高压饲料喂养。
1.2 药物及栓塞剂
1.2.1 血府逐瘀汤 采用胶囊制剂,购于天津宏仁堂药业有限公司(产品批号A03149),主要成分为柴胡、当归、甘草、川芎、牛膝、桔梗、地黄、赤芍、红花、炒桃仁、麸炒枳壳,每粒装0.4 g。成人口服1次6粒,每日2次。
1.2.2 戊巴比妥钠 购于贝尔曼生物技术有限公司,德国分装进口。生理盐水按质量/体积比配置成2%溶液,冰箱储存容易结晶,影响麻醉效果,需常温保存。
1.2.3 白及微球栓塞剂制作 白及胶的抽提:中药白及50 g于蒸馏水1000 ml中浸泡2 h后,60 ℃水浴4 h,过滤收集滤液;将固体加入800 ml蒸馏水于60 ℃水浴4 h,过滤收集滤液,依次同上经过70 ℃、80 ℃后,合并4次滤液,真空抽滤滤液,将滤液浓缩后以无水乙醇沉淀,可得白色絮状沉淀,干燥后即得白及胶。
栓塞剂白及微球的制作:取干燥好的白及胶配制20%胶液20 ml,以1∶9比例加入含6%司班80的液体石蜡中,50 ℃搅拌30 min后于0 ℃冷却1 h,室温搅拌加入乙二胺至3%固化交联,可见微球悬浮于液体中,0 ℃静置2 h,加入异丙醇静置,弃上层油相,加入异丙醇重复洗去油相,加入无水乙醇洗去异丙醇,60 ℃干燥,过200目筛,所得即为直径为小于75 μm的白及微球栓塞剂。
1.3 仪器
恒温箱GHP-9050、YB-7LF石蜡包埋机(湖北省孝感市亚光医用电子技术有限公司),HM340E石蜡切片机(德国制造),YT-7FB型摊烤片机(湖北省孝感市亚光医用电子技术有限公司),ECLIP SE55I型生物显微镜(日本Nikon公司)。
1.4 方法
1.4.1 大鼠下肢缺血模型的制作 SD大鼠固定后用2%戊巴比妥钠以3 mL/kg剂量麻醉,完全肌松后从腹股沟处纵向钝性分离皮下组织,暴露血管神经束,分离股动脉约0.5 cm,近心端结扎,用5 mL注射器将无菌生理盐水配置的4%白及微球栓塞剂悬液0.2 mL推入股动脉远心端,作无菌外科缝合,术后第3天于小腿近心端约1/3处行无菌截肢术。
1.4.2 分组及给药方法 术后第2天将大鼠随机分为生理盐水组和药物组,预实验时低剂量的药物未见明显效果,故药物组又分血府逐瘀汤常规剂量和高剂量2组,每组6只。常规剂量组大鼠每天给药剂量是正常成人剂量的6倍,即0.48 g/kg/d,高剂量组是常规剂量组的2倍,分早晚2次灌胃给药。
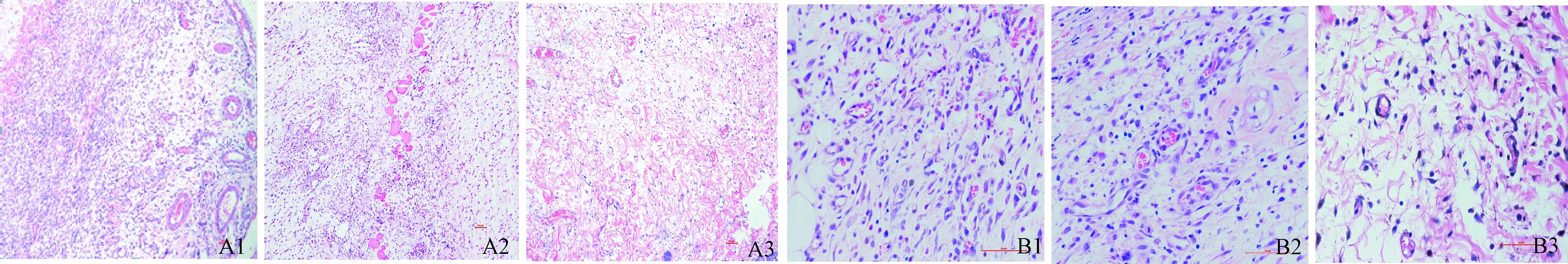
图2 A1-3分别为截肢术后36、48 h和72 h 100倍镜下HE表现,B1-3分别为截肢后36、48 h和72 h 400倍镜下HE表现
1.4.3 取材及HE染色 分别在截肢术后36 h、48 h和72 h灌药2 h后用戊巴比妥钠麻醉,取材肉芽组织,生理盐水清洗后于中性甲醛固定12 h,经石蜡包埋、切片、烤片、二甲苯脱蜡、不同浓度酒精复水、苏木素染色、自来水蓝化、1%浓盐酸乙醇分化液褪色、伊红染色后封片、晾干。
1.4.4 病理观察及血管计数 100倍镜下观察截肢术后36 h、48 h和72 h缺血组织的形态,并选择血管数量较多的时间点400倍镜下随机选取6个视野进行血管数量统计。
2 结果
2.1 一般情况观察
图1显示,术后造模肢体与正常肢体相比明显苍白;术后第1天术侧轻度瘀血,颜色呈浅黑色,跛行;第2、3天精神欠佳,缺血加重,肢体毛发脱落,拖拽或跛行,趾甲瘀血呈黑色或暗红色,脚掌可呈深黑色或伴水肿,尤以脚底明显,或伴指端坏死甚至脱落,或下肢皮肤溃烂伴渗出液;从背部抓起大鼠患侧肢体脚趾不成扇形展开,提起大鼠尾巴时与正常肢体对比无趾曲,用Eugenio Stabile半定量评分法[6]对肢体功能和缺血损伤评分发现这两项评分均大于或等于2分。
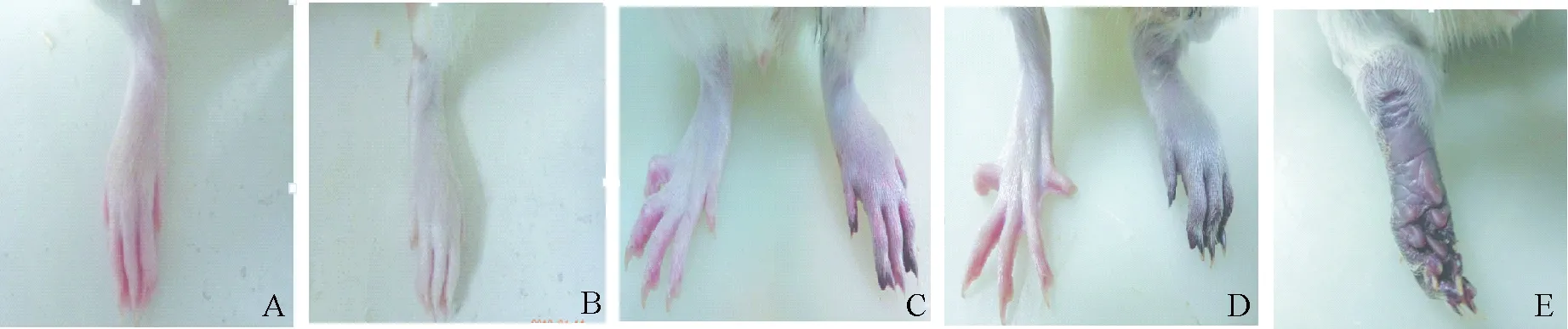
图1 A.术后正常侧肢体,红润;B.白及微球栓塞侧肢体,呈苍白色;C.术后第1天术侧肢体轻度瘀血;D.术后第2天患肢肿胀瘀血加重,呈灰黑色,且与正常侧肢体比较患侧足趾不成扇形展开;E.患肢足底
2.2 缺血坏死区肉芽组织修复的病理观察
肉芽组织的生长时间及形态特征使其成为早期组织缺血损伤修复的重要观察对象,其介导的损伤修复过程包括炎症反应、组织增生和肉芽形成、伤口收缩与瘢痕形成3个阶段,3个阶段彼此重叠,没有明显界限。缺血组织3个时间点的镜下观察发现,截肢术后72 h胶原纤维增粗并互相融合,呈均质红染的波浪状、带状或片状结构,纤维细胞和毛细血管少,肉芽组织成熟为纤维结缔组织,并逐渐老化为瘢痕组织(图A3、B3)。48 h(图A2、B2)可见,成纤维细胞向纤维细胞转变,胞核变细长而深染,胞质染色也加深;部分毛细血管管腔闭塞,或改建为小动脉小静脉;胶原纤维等细胞外基质成分增加,肉芽组织有纤维化趋势。36 h(图A1、B1)各组镜下均可见新鲜肉芽组织,表现为内皮细胞增多及大量毛细血管管腔形成;成纤维细胞活跃,呈梭形、核椭圆,染色质浅,可伴有炎性细胞浸润。
由上述病理切片结果可知,72 h成纤维细胞分泌的胶原纤维增粗并逐渐融合,血管数量少,已处于修复的第三阶段;36 h表现为新鲜肉芽组织,新生血管丰富;虽然48 h胶原纤维开始形成,但处于肉芽组织向瘢痕组织过渡的早期纤维化阶段,与36 h肉芽组织没有明显的界线,两者具有可比性。综上,我们选择36 h和48 h时间点对血管数量进行统计比较。
2.3 药物对缺血坏死区血管新生数量的影响
表1显示,通过血管计数结果可知,48 h的血管数量较36 h减少,符合肉芽组织的生长特点。其中36 h两个剂量药物组的血管数量均比对照组显著升高,且高剂量药物组的血管数量也明显高于常规剂量组。随着药物作用时间延长至48 h,常规剂量组的药效消失,但高剂量药物组保持其药效作用,血管数量仍明显高于对照组。
表1 血府逐瘀汤对肉芽组织中血管数量的影响
注:与生理盐水组比较:#P<0.05,*P<0.001,与常规剂量组比较:△P<0.001
3 讨论
后肢缺血模型是研究缺血性疾病及血管新生的重要手段。从制作方法来看,多数研究采用结扎或切断股动脉或髂动脉及其分支的方法制造缺血状态[1~5],但由于鼠科动物侧枝循环丰富,修复能力强,模型的缺血状态多不能持久,且机械性急性阻断动脉导致的缺血,不符合由慢性血管内皮损伤引发缓慢阻塞所形成的缺血性疾病的发生发展进程。相比较而言,白及微球由白及胶经过乳化、冻凝、化学交联而成,直径小于75 μm,在血流的冲击下可迁徙阻塞末梢小动脉甚至微动脉,并在血液中缓慢膨胀不被降解吸收,使缺血效果持续稳定;且白及尤其是白及多糖能促进局部血小板凝集、缩短凝血时间[7],从而促进继发性血栓形成,有效模拟内皮损伤及动脉慢性阻塞过程,更接近此类缺血性疾病的病理状态。但是实验中我们发现,动物侧支循环建立能力不一,使得缺血组织坏死溃烂程度不均一,不利于取材点的统一。另外,以该方法造模可取用的肉芽组织样本量较少,给血管新生的药物研究带来不便。为解决这个问题,本实验在白及栓塞法造模的基础上,于造模后的第3天对缺血肢体进行低位截肢,既保持肢体的缺血状态,又能在统一部位取材,而且由于截肢使得损伤位置上移,增加了可取材肉芽组织的样本量,通过二次造模克服单纯栓塞法造模的局限性,有利于后续各项实验的开展。
缺血损伤修复的关键在于早期血供的建立,肌肉组织再生性修复能力弱,需靠新生的、富含毛细血管的肉芽组织进行瘢痕修复,肉芽组织一般在损伤后第2~3天出现,7 d成熟,该组织的生长时间点和形态特征使其成为早期改善缺血、修复损伤的重要观察对象。本实验通过观察缺血组织的病理表现,发现低位截肢术后36 h和48 h肉芽组织新鲜,血管数量丰富,是观察血管新生的较好时机。国内外极少见到将肉芽组织应用于血管新生的研究,本项目组突破常规做法,以病理切片直接计数血管数量,为筛选血管新生药物提出了一个较好的在体模型。通过计数最佳观察时间点的新生血管数量,本实验证实血府逐瘀汤能促进两个时间点肉芽组织的血管生长。本项目组曾单纯采用栓塞剂造模观察药物对肉芽组织血管生长的影响[8],虽然与本实验的药物制剂不同,给药时间长短不同,但两次实验的结论一致,均通过在体实验进一步证实了该方剂具有促血管新生的功效,为药物临床治疗缺血性疾病疗效显著提供实验依据。另外,本实验从两个时间点的血管数量比较结果可知,随着作用时间延长至48 h,常规剂量的药物已失去促血管生长的作用,且高剂量药物组的血管数量较其他两个组的差异缩小,提示药物的作用逐渐消退。说明药物促血管生长的作用存在有效时间范围,与本项目组其他细胞模型的体外实验结果相符[9,10],为本项目组提出的血府逐瘀汤促血管适度生长提供了又一佐证。
本项目组的实验研究已从不同角度、不同层次说明血府逐瘀汤具有避免血管过度生长的作用特点,由于血管新生的调控因子众多,调控机制复杂,药物如何能够调控血管适度生长,尚需大量深入的研究,这也为本项目组今后的工作指明了方向。
[1] Pu LQ, Jackson S, Lachapelle KJ, et al. A persistent hindlimb ischemia model in the rabbit[J]. J Invest Surg,1994 ,7(1):49-60.
[2] Hendricks DL, Pevec WC, Shestak KC, et al. A model of persistent partial hindlimb ischemia in the rabbit[J]. J Surg Res,1990 ,49(5):453-457.
[3] Westvik TS, Fitzgerald TN, Muto A, et al. Limb ischemia after iliac ligation in aged mice stimulates angiogenesis without arteriogenesis[J]. J Vasc Surg, 2009 ,49(2):464-473.
[4] Brenes RA, Jadlowiec CC, Bear M, et al. Toward a mouse model of hind limb ischemia to test therapeutic angiogenesis[J]. J Vasc Surg, 2012 ,56(6):1669-1679.
[5] Yang Z, von Ballmoos MW, Diehm N, et al. Call for a reference model of chronic hind limb ischemia to investigate therapeutic angiogenesis[J]. Vascul Pharmacol, 2009 ,51(4):268-274.
[6] Stabile E, Burnett MS, Watkins C, et al. Impaired arteriogenic response to acute hindlimb ischemia in CD4-knockout mice[J]. Circulation,2003,108(2):205-210.
[7] 孙剑涛,张峻峰,王春明. 新型血管内液体栓塞剂中有效组分的体外促凝血作用研究[J]. 实用临床医药杂志,2006,10(4):59-61.
[8] 高冬, 焦雨欢, 武一曼, 等. 血府逐瘀汤诱导内皮祖细胞参与缺血区血管新生的实验研究[J]. 中国中西医结合杂志, 2012,32 (2):239-243.
[9] Song J, Chen WY, Gao D, et al. A microarray analysis of angiogenesis modulation effect of Xuefu Zhuyu decoction on endothelial cells[J]. Chin J Integr Med, 2012,18(7):502-506.
[10] 高冬, 陈文元, 吴立娅, 等. 血府逐瘀汤诱导内皮细胞促血管新生的基因调控研究[J]. 中国中西医结合杂志, 2010,30(2):153-156.

