取向型LiFePO4材料合成的研究进展
陈明鸣,马倩倩,王成扬,陈 松
(1.天津大学化工学院 绿色合成与转换教育部重点实验室,天津300072;2.天津化学化工协同创新中心,天津300072)
聚阴离子型正极材料LiFePO4自1997年由Goodenough团队首次提出[1-2],便由于原料储量丰富、成本低廉、环境友好、比容量高、安全性能和稳定性好等优点,被认为是极有应用前景的锂离子电池正极材料,并成为电动汽车用动力电池的首选。然而,由于受其自身结构的限制,LiFePO4存在电子电导率低(10_10~10_9S/cm)和 Li+扩散速率慢(_1.8×10_14cm2/S)等缺点,使得材料的容量性能、快速充放和倍率性能难以满足新一代锂离子动力电池的要求。为了在上述电化学性质方面进行改善,科研人员进行了大量的研究。近几年的研究主要采用纳米化[3-4]、表面导电物质包覆[5-7]、金属离子掺杂[8-9]等方法来提高 LiFePO4材料的电化学性能。进一步的研究表明,LiFePO4晶体作为锂电正极材料,在充/放电(Li+的脱出/嵌入)过程中 Li+主要沿 LiFePO4的 b轴([010])方向进行一维扩散[10-13],而电荷的传输主要发生在其 ac面上[14-15]。因此,针对LiFePO4电化学储能特性的提高,近几年的研究工作已经开始集中关注到晶体取向生长的研究。Maier等[13]的研究结果表明,在 b轴和 c轴上Li+的扩散速率要比电子电导率低4个数量级,而在a轴上就更低,所以提高Li+的传输性能对于提高LiFePO4的动力学性能至关重要。综上,可控合成具有较短b轴的LiFePO4颗粒将有利于缩短Li+的传输距离,使得 Li+的嵌入脱出变得更加容易,从而提高LiFePO4材料的电化学性能。
本论文首先综述了LiFePO4的晶体结构以及Li+在其中的扩散方向的理论研究,总结了LiFePO4晶体取向的表征与评价方法,并着重介绍了近年来国内外关于取向型LiFePO4晶体的研究进展。
1 LiFePO 4的晶体结构和Li+扩散方向的理论研究
LiFePO4晶体为橄榄石结构,属于正交晶系,空间群为Pmna,晶胞参数a=1.033 2 nm,b=0.601 0 nm,c=0.469 2 nm,其结构示意图如图1所示。在LiFePO4中,氧原子以稍微扭曲的六方紧密堆积方式排列,P占据了氧原子四面体的4c位置,形成PO4四面体。Fe和Li分别位于氧原子八面体中心位置,形成FeO6和LiO6八面体。交替排列的FeO6八面体、LiO6八面体和 PO4四面体形成层状结构。Li+在4a位形成平行于c轴的共棱的连续直线链,从而使Li+具有可移动性,可以在充/放电过程中可逆的脱出和嵌入[16-17]。

图1 橄榄石L iFePO 4结构[16],P占据四面体的4c位(深色四面体),Fe占据八面体的4c位(浅色八面体)Fig.1 The crystal structure of LiFePO 4 viewed along the c-axis[16].The P atom s occupy tetrahed ral(4c)sites(dark shading)and the Fe atom s occupy octahedral(4c)sites(light shading)
Thomas等[18]曾认为 Li+可以沿着 c轴形成二维扩散运动,自由的脱嵌。于是在2001年提出两种经典的 LiFePO4充放电模型,一个是辐射模型(shinking core),另一个是马赛克模型(mosaic model)。但是,这两种模型的提出只是凭借想象,没有可靠的实验数据证明。2004年,Ceder等[10]首次应用第一性原理研究了 Li+在 LiFePO4中的扩散方向。研究结果证明,Li+主要沿 b轴运动。Li+沿[010]方向扩散的速率是[001]方向的好几倍。2005年,Islam等[11]运用原子建模技术对 LiFePO4的“Li-Fe”反位缺陷等方面的研究进一步证实了Ceder等的研究结果。Yamada等[12]在2008年运用高温粉末中子衍射技术和最大熵方法进一步证实了Li+沿[010]方向进行一维扩散。
2 LiFePO4晶体取向的表征与评价方法
LiFePO4的晶体取向特征可以通过TEM表征和XRD图谱表征手段获得。
2.1 TEM表征
高倍透射电镜(HRTEM)可以观察到 LiFePO4的晶格条纹图像,将条纹间距与标准PDF卡片的d值进行对比,从而可以判断相应的晶面[19-31];对LiFePO4样品做选区电子衍射(SAED),根据式(1):

(其中,R为衍射斑距透射斑长度,L为相机长度,λ为电子波长)可以求出衍射斑对应的晶面间距d,与PDF卡片的d值进行对比,从而获得LiFePO4样品的晶体取向[19-25,27,29-38]特征。
2.2 XRD表征
XRD图谱中衍射峰的相对强度代表了LiFePO4的晶体取向。(020)峰强度较高说明LiFePO4晶体沿ac面取向生长,如果(200)峰强度较高说明LiFe-PO4晶 体 沿 bc面 取 向 生 长[21,31,34,36,39-40]。 Yan等[30]、Kanumara等[32]和 He等[37]认为 I(020)/I(200)的比值若比标准卡片比值[I(020)/I(200)=2.1]高,则认为LiFePO4晶体沿ac面取向生长,若低于标准卡片比值则认为LiFePO4晶体沿bc面取向生长。在此基础上,(020)峰强度越高说明晶体沿[010]方向取向度越高[27,29,41-42]。
2.3 Li+表观扩散系数的测定
可控合成沿ac面取向生长的LiFePO4颗粒将有利于缩短Li+的传输距离,提高Li+的扩散速率。扩散系数越大,电极的大电流放电能力越好,材料的功率密度越高,高倍率性能越好。所以Li+的表观扩散系数的测量也是一种评价材料性能的重要手段。Li+表观扩散系数的测定方法主要有以下2种。
2.3.1 循环伏安法
材料在不同的扫描速度下会表现出不同的循环伏安响应曲线,根据Randles-Sevcik公式[43]

(其中Ip为峰电流的大小,A为浸入溶液中的电极面积,C为反应前后 Li+浓度的变化,DLi+为 Li+在电极中的扩散系数,n为参与反应的电子数,ν为扫描速率),将不同扫描速率下的峰值电流 Ip对扫描速率ν的平方根作图,求得直线斜率即可求得Li+在电极中的表观扩散系数。
2.3.2 交流阻抗法
根据锂电的交流阻抗特性测定Li+扩散系数的公式如式(3)、(4)和(5)所示[44]:
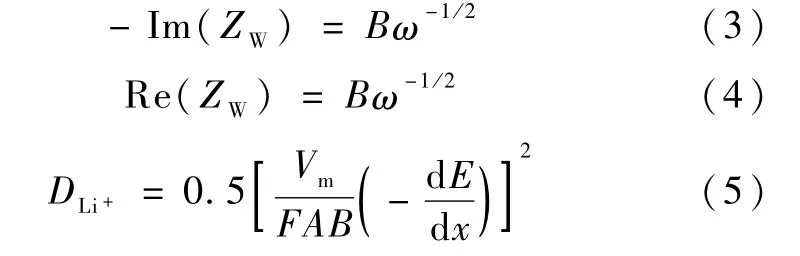
其中:ω为角频率,B为 Warburg系数,DLi+为 Li+在电极中的扩散系数,Vm为活性物质的摩尔体积,F为法拉第常量,A为浸入溶液中的电极面积,(d E)/(d x)为库仑滴定曲线的斜率,即为开路电位对电极中Li+浓度曲线上某浓度处的斜率。
具体计算方法为:从Nyquist图上取出扩散控制部分,根据公式(3)或(4),用 ZW的实部或虚部对ω_1/2作图,即可求得系数 B,将 B代入公式(5),即可求得Li+扩散系数。
3 取向型LiFePO4晶体的制备方法及其电化学性能
目前LiFePO4晶体取向生长的制备方法主要为液相合成方法,包括水热合成法和溶剂热合成法。水热/溶剂热合成法是指在密封的压力容器中,以水/有机溶剂为反应介质,对反应容器加热,创造一个高温、高压的反应环境,使通常难溶或不溶的物质溶解并重结晶。其过程相对简单而且易于控制,溶液条件下有利于生长极少缺陷、取向好、完美的晶体,而且产物的分散性较好。由于Li+主要沿b轴方向进行一维扩散,LiFePO4晶体沿ac面(垂直于b轴)择优生长显得尤为有意义,所以本论文主要综述LiFePO4晶体沿ac面择优生长的制备和合成方法。
3.1 水热合成法
从近几年的研究成果来看,水热合成过程中调控LiFePO4晶体取向主要是通过调节反应体系的pH值[32-33,39],或者调节反应体系中 Fe前驱体的浓度[42]或在反应体系中加入添加剂[34]。
2007 年,Kanamura等[32]以 FeSO4·H2O为铁源,LiOH·H2O和 Li2SO4为锂源,(NH4)2HPO4和 H3PO4为磷源。通过调节锂源与磷源的比例来控制水热合成过程中前驱体溶液的pH值。研究发现,不同pH值条件下可以得到不同晶体取向的LiFePO4颗粒。当pH值在4.0~6.5之间时,可以得到沿ac面择优生长的片状LiFePO4颗粒,片层平均厚度为0.25μm。当pH值大于7.2时,得到沿bc面择优生长的针状LiFePO4颗粒。沿ac面择优生长的片状LiFePO4颗粒表现出最优异的电化学性能,当电流密度为17 mA/g时放电比容量达到 163 mA·h/g。Wang等[45]认为微米级大小的晶体的形态主要受晶核表面能的各向异性控制,具有高表面能的晶核表面对离子具有更大的吸附能力。因此,随着反应的进行,LiFePO4的晶粒沿着具有高表面能的晶核表面的垂直方向生长的更快。而相比于其他晶面,[010]面具有最低的表面能[46],所以垂直于[010]面的方向晶体生长速度最慢。Kanamura等[32]推断,当水热条件为中性或弱酸性时,ac面的表面能要低于其他晶面。在酸性pH值范围内,LiFePO4晶面的沉积速率顺序为:ab面>ac面>bc面。
2008年,Kanamura小组[39]通过改变锂源来控制溶液的pH值。当锂源为醋酸锂时,pH值为5.15,得到沿[020]面择优生长的片状 LiFePO4颗粒;当锂源为氯化锂时,pH值为3.44,得到沿[200]面择优生长的片状LiFePO4颗粒。同年,Kanamura等[33]又以 LiOH、FeSO4、(NH4)2HPO4、H3PO4为原料,抗坏血酸为碳源原位加入反应体系中,将溶液的pH值控制在5.00,经过在190℃下5 h的水热反应及在700℃下1 h的高温热处理后,得到沿ac面择优生长的板状LiFePO4颗粒,颗粒表面均匀包覆约5 nm厚的炭层。将该样品组装成锂离子电池后,在10 C电流密度下放电比容量达到104 mA·h/g。组装成锂离子聚合物电池后,30℃时在0.5 C电流密度下放电比容量为122 mA·h/g。
Nazar等[42]以(NH4)2Fe(SO4)2·6H2O、H3PO4、LiOH·H2O为原料,按1∶1∶3的比例进行反应。 作者发现,Fe前驱体的浓度会影响LiFePO4材料的晶体取向度,低浓度(0.25 mol/L)时所得样品的[020]峰值较高浓度(0.75 mol/L)下获得的样品的峰值高(如图2),说明低浓度下制得的 LiFePO4晶体在[020]轴方向上的取向度更高。

图2 不同浓度下合成的LiFePO 4样品的SEM图[42]Fig.2 SEM micrographs of carbon-free LiFePO 4 crystallized at different concen trations[42]
Mustarelli等[34]在水热过程中加入聚乙烯吡咯烷酮(PVP),一方面,PVP可以作为抑制 Fe2+被氧化的碳源;另一方面,它可以抑制LiFePO4晶体的长大及控制晶体沿ac面择优取向生长。如图3a)所示,LiFePO4颗粒为厚0.5~1.0μm的纳米片。电化学测试发现[图3c)和图3d)],在低电流密度(C/20和C/10)下,电化学性能主要受晶体取向影响;而在大电流密度下,小尺寸、无取向的颗粒要比大尺寸、ac面取向的颗粒的电化学性能要好。
3.2 溶剂热合成法
溶剂热合成是水热合成的发展,采用类似于水热合成法的原理,只是将水热法中的水换成有机溶剂。有机溶剂具有沸点低、介电常数小和黏度较大等特点,常用的有机溶剂有甲醇、乙醇、乙二醇、乙二胺、苯、四氯化碳以及聚醚等。
从近年的文献来看,溶剂热合成LiFePO4晶体的方法中,多采用醇类作为溶剂。由于醇类具有弱还原性,在溶剂热反应过程中,除作为溶剂外还可以作为还原剂抑制Fe2+被氧化成Fe3+;醇类上的羟基之间相互连接形成氢键,从而醇类可以作为软模板剂促使LiFePO4晶体取向生长;另外,醇类的黏度比水的黏度大,可以有效控制颗粒的长大,从而制得纳米尺寸的颗粒。
3.2.1 乙醇作为反应介质
Ren 等[19]将乙醇作为溶剂,LiI作为锂源,FeCl3·6H2O作为铁源,H3PO3作为磷源,PVP(聚乙烯吡咯烷酮)作为碳源和模板剂,在180℃下反应48 h,制得沿b轴方向具有层层堆叠结构的 LiFePO4微米束,如图4所示。

图3 以PVP为添加剂制得LiFePO 4样品的SEM图和球磨之后的SEM图及球磨前后样品的首次充放电曲线对比[34]Fig.3 a)SEM image of LiFePO 4 sample with PVP as the additive;b)SEM image of the sample in figure a)after ball-milling.The first charge-discharge curves of the samples before and after ball-milling:c)first cycle at C/20 and d)first cycle at 2 C[34]

图4 LiFePO 4样品的 SEM图 a),TEM图 b),图c)和SAED图谱d)[19]Fig.4 SEM image of LiFePO 4 a);TEM images of LiFePO4[b)and c)]and SAED pattern of LiFePO4 d)[19]
Yan等[30]采用液相剥离法结合高温高压溶剂热(乙醇为溶剂)锂化过程制备炭包覆LiMPO4(M=Fe,Mn,Co,Ni)超薄纳米片,制得的纳米片在 b轴方向厚度为3.7~4.6 nm。LiFePO4超薄纳米片的具体制备过程如图5a)所示,作者通过将甲酰胺分子插入NH4FePO4·H2O块状颗粒的层与层之间使其膨胀,之后采用超声方法将其剥离成厚约1.9 nm的NH4FePO4·H2O纳米片,然后将纳米片表面包覆一层PVP之后加入锂源 CH3COOLi·H2O,采用超临界溶剂热法将表面包覆有 PVP的 NH4FePO4·H2O纳米片锂化转变成LiFePO4/C纳米片。合成的LiFePO4/C纳米片拥有128.5 m2/g的比表面积,从而有利于与电解液的充分接触;通过公式t=L2/D计算得Li+沿 LiFePO4/C纳米片的[010]面进行扩散的扩散时间小于25μs,比相应的块状LiFePO4颗粒中Li+的扩散时间低5个数量级。因此,这种超薄LiFePO4/C纳米片表现出优异的大倍率性能[如图5c)]:在10、20和50 C下的放电比容量分别能够达到139、121和 100 mA·h/g,甚至在 80 C的大倍率下仍保持有70 mA·h/g的放电比容量。

图5 a)液相剥离法结合高温高压溶剂热锂化过程制备炭包覆LiFePO 4纳米片的示意图;b)LiFePO 4/C样品的首次恒流充放电曲线(电流密度为0.2 C);c)LiFePO 4/C样品的倍率性能[30]Fig.5 a)Schematic illustration of the preparation of carbon-coated LiFePO 4 nanosheets through a liquid-phase exfoliation approach combined with a HPHT solvothermal lithiation process;b)The initial galvanostatic charge-discharge voltage profiles of LiFePO 4/C at a rate of 0.2 C;c)Rate capabilities of LiFePO 4/C[30]
3.2.2 乙二醇作为反应介质
反应介质乙二醇对合成取向型LiFePO4纳米材料起着至关重要的作用:1)乙二醇具有弱还原性,溶剂热过程中可以抑制Fe2+被氧化成Fe3+,从而保证合成材料的纯度;2)乙二醇具有比水、乙醇等常规溶剂更大的黏度,有利于降低反应介质中的离子扩散速率,从而有效抑制颗粒长大;3)乙二醇上的羟基之间相互连接形成氢键,使乙二醇连接成长链,如图6所示。乙二醇与[010]面上的Fe2+有很强的螯合作用,连成长链的乙二醇吸附在[010]面上,抑制晶体在[010]面上的生长,使晶体各个面的生长速率不同,从而有利于沿ac面取向的薄片状LiFePO4的形成。

图6 原理示意图[21]Fig.6 Schematic illusion[21]
Vittal等[35-36]采用乙二醇作为反应介质,以LiH2PO4为锂源和磷源,FeC2O4·2H2O、Fe(acac)3、Fe(PMIDA)、Fe(gluconate)2为铁源,在 250~270℃下合成出沿ac面择优取向生长的LiFePO4颗粒。铁源不同,所得LiFePO4样品的形貌也有所差别,如图7。但是所有样品均沿 ac面择优取向生长。除此之外,作者以葡萄糖酸内酯作为原位包覆的碳源。反应过程中,葡萄糖酸内酯水解为葡萄糖酸,葡萄糖酸对铁离子具有很强的螯合作用,可以很好的吸附在LiFePO4颗粒表面,经过高温热处理后可以在颗粒表面形成一层均匀的炭包覆层,从而提高材料的电化学性能。其中,以草酸亚铁为铁源制得的层层堆叠的LiFePO4纳米片(纳米片厚30~40 nm)的电化学性能最好,0.1 C下放电比容量达到167 mA·h/g,接近LiFePO4的理论比容量。

图7 不同铁源合成的LiFePO 4纳米片的FESEM图[36]Fig.7 FESEM images of LFP/C nanop lates from various precu rsors at two different magnifications[36]
He等[37]以乙二醇为反应介质,以 LiOH·H2O、FeSO4·H2O和 H3PO4为原料。通过改变原料的加入顺序,可以得到沿不同晶面择优取向生长的LiFe-PO4纳米颗粒。如图8中的透射电镜图与选区电子衍射图所示,先将 LiOH·H2O与H3PO4混合反应再加入FeSO4·H2O可以得到沿ac面择优取向生长的LiFePO4纳米片;而先将 FeSO4·H2O与 H3PO4混合反应再加入LiOH·H2O可以得到沿bc面择优取向生长的LiFePO4纳米片。充放电性能测试表明[图8(c,d)],两种取向的样品在低电流密度下(0.1 C~1.0 C)的放电比容量相当,但是在大电流密度下,沿ac面择优取向生长的样品的放电比容量更高,5 C下为 156 mA·h/g,10 C下为 148 mA·h/g。

图8 沿ac面取向生长的LiFePO 4样品S1(a)和沿bc面取向生长的LiFePO 4样品S2(b)的TEM图(内含SAED图);S1/C和S2/C样品对应的倍率性能(c,d)[37]Fig.8 TEM images(SAED inside)of(a)S1 and(b)S2.The exposu re facet is[010]for S1,while crystal grow th orientations along the bc p lane are prominent for S2.Performance of rate capability of S1/C(c)and S2/C(d)[37]
Li等[26]以乙二醇为反应介质,LiOH·H2O、Fe-SO4·H2O和 H3PO4为原料,按 2.7∶1.0∶1.0 的比例配料,通过溶剂热合成法制得厚30 nm、宽100 nm、长200 nm,并且沿ac面择优取向生长的LiFePO4纳米片。LiFePO4样品的透射电镜图和选区电子衍射图如图9a)和b)所示。电化学性能测试表明[图9(c,d)],LiFePO4纳米片及炭包覆 LiFePO4纳米片极化值均很低,炭包覆 LiFePO4纳米片在0.1 C时的放电比容量为165 mA·h/g,5 C时的放电比容量为140 mA·h/g,表现出良好的电化学性能。Ma等[38]同样以乙二醇为反应介质,LiOH·H2O、FeSO4·H2O和H3PO4为原料,制得沿 ac面择优取向生长的LiFePO4纳米片后,通过乙二醇与柠檬酸之间的酯化反应在LiFePO4纳米片表面包覆一层厚约1.8 nm的炭层。_20℃的低温条件下0.1 C倍率时放电比容量达到116 mA·h/g。
Cui等[27]以 CH2COOLi·2H2O、H3PO4、FeC2O4·2H2O为原料,在反应介质乙二醇中加入TiN。实验结果发现TiN的加入促进了LiFePO4晶体沿ac面择优取向生长,TiN黏附在[010]面上促使 LiFePO4纳米片的形成,为了进一步降低表面能纳米片层层堆叠在一起;另外,TiN的加入量会影响LiFePO4的形貌,随TiN加入量的增大,LiFePO4的形貌由自组装纳米片逐渐变成自组装纳米球。研究也发现TiN的加入可以提高材料的导电性。
Wang等[28]以乙二醇为反应介质,LiOH·H2O、FeSO4·H2O和H3PO4为原料,在反应体系中原位加入氧化石墨烯(GO)。首先,阳离子Li+和Fe2+被吸附在带负电的氧化石墨烯纳米片的表面;之后,由于乙二醇溶剂的作用,沿 ac面择优取向生长的LiFePO4纳米片在氧化石墨烯片上生成;另外,由于乙二醇的弱还原性,将GO还原成石墨烯片,并且阻止Fe2+被氧化成 Fe3+;最终合成 LFP@GNs复合物。厚度为10~30 nm的LiFePO4纳米片在GNs表面分散均匀,如图10a)和图10b)所示。LFP@GNs复合材料表现出优异的倍率性能和循环性能[图10c)],20 C倍率下放电比容量达到126 mA·h/g,10 C倍率下循环600次之后容量无衰减。LFP@GNs优异的电化学性能一方面归功于材料沿ac面取向的纳米片结构,使得Li+嵌入脱出的距离缩短;另一方面,原位加入的石墨烯与LFP纳米片形成交联结构,有效的抑制了纳米片的聚合,促进了电解质的渗透,扩大了载流子的传输表面积。
离子液体具有很高的溶解性和热稳定性、蒸汽压值很小,并且环境友好。Wei等[29]将离子液体氯化胆碱(ChCl)与乙二醇(EG)按体积比1∶2的比例混合作为LiFePO4溶剂热合成的反应介质。实验结果发现,离子液体氯化胆碱可以控制晶体取向生长和颗粒尺寸。离子液体具有很高的黏度,减缓了反应体系中两个晶面之间的聚合速度,给予足够的时间去调整晶体取向。XRD、SEM与TEM测试结果表明,在离子液体溶剂热反应体系(ChCl+EG)中可以制得沿ac面择优取向生长的纳米片层层堆叠形成的的弓状LiFePO4颗粒,如图11(a,b)的透射电镜图片所示。如图11(c,d),以10%(质量分数)蔗糖为碳源进行碳包覆后,材料在20 C倍率下进行充放电1 000次后,容量保持率为95%,表现出优异的倍率性能和循环性能。

图10 a),b)LFP@GNs样品的 TEM图;c)LFP@GNs样品在10 C倍率时的循环性能;d)LFP@GNs样品充放电过程示意图[28]Fig.10 a),b)TEM images of LFP@GNs;c)long cycling stabilities with cou lom bic efficiency at 10 C of LFP@GNs;d)schematical illustration of the charge/d ischarge process of LFP@GNs[28]
3.2.3 其他多元醇类作为反应介质
2006年,Kim小组[47]开发了一种常压高温下合成LiFePO4材料的新方法。Kim等采用四甘醇(TTEG)回流体系,于335℃高温下在圆底烧瓶中进行溶剂热反应,合成宽20 nm,长50 nm并且沿ac面择优取向生长的LiFePO4纳米颗粒。样品不经过进一步的高温热处理便表现出很好的电化学性能,0.1 mA/cm2的电流密度下放电比容量为166 mA·h/g,在30和60 C的大电流下仍有58%和47%的容量保持率。2012年,Kim小组[40]又以二甘醇为溶剂,金属铁为铁源,在高压反应釜中与230℃高温下制备出沿[010]面和[101]面择优取向生长的LiFe-PO4纳米片。SEM结果显示,纳米片厚20 nm,长宽均为100 nm。材料在16 C时的放电比容量为125 mA·h/g,电化学性能优异。文章中也对二甘醇、三甘醇、四甘醇的化学性质做了对比。作者认为,3种醇类会营造不同的反应环境,从而影响纳米颗粒的形貌与尺寸,其中,与三甘醇、四甘醇相比,二甘醇具有更低的黏度和沸点,还有自身特殊的分子结构,正是二甘醇的这些物化特性影响了最终LiFe-PO4的晶体结构,使其沿[010]面和[101]面取向生长。

图11 a),b)LiFePO 4样品的 TEM图;c)LFP/C样品的充放电曲线;d)LFP/C样品的循环性能[29]Fig.11 a),b)TEM images of the LiFePO 4 sample;c)charge-d ischarge profiles and d)cycling performance of LFP/C composite.The inset:Coulombic efficiency[29]
3.2.4 多元醇类和水二元混合溶剂作为反应介质
Shen 等[20],Zhang等[21],Wang等[22],Ye等[31]和Yuan等[41]均将乙二醇和水混合作为二元混合溶剂,在170~180℃温度范围内制备出沿ac面择优生长的纳米片状或纳米棒状的LiFePO4。二元混合溶剂中的乙二醇对晶体的取向生长起了主导作用,与将乙二醇作为单一的反应介质的作用相同。其中,Yuan等[41]通过调节乙二醇与水的比例制得不同形貌的LiFePO4颗粒。XRD数据结果显示,随着乙二醇与水的体积比增加(1∶4、2∶3、3∶2),2θ=30°处的(020)峰变得更强;并且SEM图谱(图12)显示LiFePO4的形貌由微米片变成纳米棒。充放电性能测试(图12)表明,纳米棒状的LiFePO4样品表现出最好的电化学性能,5 C时的放电比容量为141 mA·h/g,循环100次后仍能保持120 mA·h/g的容量。这一结果说明晶体取向与晶体尺寸共同决定样品的电化学性能,尽管微米片具有[010]面的晶体取向,但是微米数量级的尺寸偏大仍然会阻碍Li+的有效扩散。Zhang等[21]制得的 LiFePO4纳米片比 LiFe-PO4纳米颗粒表现出更好的大倍率性能,在10和20 C下的放电比容量分别为113.4和85.6 mA·h/g。

图12 EG与H 2 O不同体积比的条件下制备所得的LiFePO 4颗粒的SEM图(a1)L14(EG:water=1:4);(b1)L23(EG:water=2:3);(c1)L32(EG:water=3:2)和倍率循环性能图(a2)L14/C;(b2)L23/C;(c2)L32/C[41]Fig.12 SEM images of LFP par ticles prepared by solvothermal process with different volume ratio of EG to water:(a1)L 14(EG:water=1:4),(b1)L23(EG:water=2:3),and(c1)L32(EG:water=3:2).Cycle performance at various rates for(a2)L14/C,(b2)L23/C,and(c2)L32/C electrodes[41]
Teng等[23]也采用将乙二醇和水混合(体积比为2∶1)作为二元混合溶剂,不同的是在溶剂中加入了添加剂十二烷基苯磺酸钠(SDBS),最终得到层层堆叠的纺锤体形 LiFePO4颗粒。如图13a)和图13b),纺锤体是由垂直于b轴方向的纳米片层层堆叠而成,纺锤体长约10μm,宽4~5μm,片层厚度约几十纳米。Chen等认为反应介质(乙二醇和水)和表面活性剂SDBS的加入共同导致了最终形貌的形成。LiFePO4不同晶面对SDBS的吸附力大小是不同的,[010]面对 SDBS的吸附力最大,所以在[010]面上聚集最多的 SDBS,导致[010]面生长速度最慢,从而形成 LiFePO4纳米片。又因为 SDBS上的疏水端之间范德华力的存在而将形成的纳米片相互连接,最终形成层层堆叠结构,形成机理如图13c)所示。电化学测试表明,层层堆叠纺锤体形LiFePO4颗粒的大倍率性能和循环性能要优于在水溶液中制得的不规则形貌 LiFePO4颗粒。在1,2,3和4 C倍率下的放电比容量分别为146,143,138和135 mA·h/g,循环40次后容量没有衰减。然而,在水溶液中制得的LiFePO4样品在1,2,3和4 C倍率下的放电比容量分别为125,117,112和105 mA·h/g,循环40次后容量有明显衰减。

图13 a),b)L iFePO 4样品的SEM图;c)具有分层结构LiFePO 4的形成机制:红色―表面活性剂分子;灰色―LiFePO 4晶体[23]Fig.13 a),b)SEM micrographs of the L iFePO 4 samples;c)The proposed form ation mechanism of the hierarchical LiFePO 4:red,surfactant m olecu les;gray,LiFePO 4 crystals[23]
Liu等[24]将聚乙二醇(PEG400)与水按一定体积比混合作为反应介质,LiOH·H2O、FeSO4·H2O和H3PO4为原料,考察了PEG400与水的比例、反应温度、反应物浓度、加料顺序对产物 LiFePO4的形貌、颗粒尺寸的影响。最终得到纳米颗粒、纳米片和微米片3种形貌的LiFePO4样品。无论是纳米颗粒、纳米片、还是微米片,3种形貌的样品的晶体取向一致,均为沿ac面择优取向生长。其中,纳米颗粒和纳米片表现出较好的电化学性能,并且测得颗粒在b轴方向越短Li+的扩散系数越大。
Kisailus等[25]将三甘醇与水按一定比例混合作为反应介质,系统的研究了在这种介质中 LiFePO4的晶体成核机制和形态演变过程。研究结果认为,LiFePO4首先在拥有高能量的 Fe3(PO4)2·8H2O薄片表面生成;初级粒子形成后,反应介质的pH值降低,LiFePO4初级粒子的表面电荷减少;表面电荷的减少促使初级粒子相互靠近并按有序的方向结合成二次粒子,形成沿[010]面择优取向生长的菱形多晶LiFePO4颗粒,如图14a)和图14b);随着反应时间的延长,pH值继续降低,LiFePO4继续结晶并由于奥斯特瓦尔德熟化晶体变得更致密,最终形成单晶LiFePO4纳米颗粒,如图14c)和图14d)。电化学性能测试表明,与单晶颗粒相比,拥有较小初级晶粒尺寸的多晶颗粒具有更好的电化学性能和动力学性能。

图14 160℃下反应10 min得到的多晶LiFePO 4样品(a,b)与160℃下反应900 min得到的单晶LiFePO 4样品的 SEM图和 TEM图(c,d)[25]Fig.14 SEMand TEM micrographs of polycrystalline crystalline L iFePO 4 synthesized at 160℃for 10 min(a,b)and single crystalline LiFePO 4 synthesized at 160 ℃ for 900 min(c,d)[25]
[010]面取向的LiFePO4晶体的制备方法、制得LiFePO4晶体的形貌及其电化学性能如表1所示。
4 结论和展望
LiFePO4作为动力电池中最有潜力的正极材料,其大倍率性能的好坏直接影响了材料的应用价值与前景。其中,锂离子在正极材料LiFePO4中的扩散性能是制约锂离子电池大电流充放电性能的一个重要因素,锂离子扩散过程与电子移动速度相比要慢几个数量级,因此提高锂离子的扩散速度有利于提高LiFePO4的大倍率性能。取向型LiFePO4材料的合成研究大大改善了材料在锂离子扩散方面的不足,推进了LiFePO4材料的实用化进展。随着取向型LiFePO4材料的不断深入研究和发展,会进一步推动锂离子动力电池的大规模应用。

表1 [010]面取向的LiFePO 4晶体的制备方法及其电化学性能Table 1 Various approaches to synthesis LiFePO 4 crystals with[010]orientation and its electrochemical performance.
[1]Padhi A K, Nanjundaswamy K S, Goodenough J B.Phospho-Olivines as positive-electrode materials for rechargeable lithium batteries[J].Journal of The Electrochemical Society, 1997, 144(4):1 188_1 194
[2]Padhi A K,Nanjundaswamy K S,Goodenough J B,et al.Effect of structure on the Fe3+/Fe2+redox couple in iron phosphates[J].Journal of the Electrochemical Society, 1997, 144(5):1 609_1 613
[3]Wang Y, Wang Y, Zhou H, et al.The design of a LiFePO4/carbon nanocomposite with a core-shell structure and its synthesis by an in situ polymerization restriction method [J].Angewandte Chemie International Edition,2008,47:7 461_7 465
[4]刘晓亮,单忠强,张磊,等.制备条件对磷酸铁锂电化学性能的影响[J].化学工业与工程,2008,25(6):471_474 Liu Xiaoliang, Shan Zhongqiang, Zhang Lei, et al.Effects of experiment conditions on electrochemical performance of lithiumiron phospho-olivine[J].Chemical Industry and Engineering, 2008, 25(6):471_474(in Chinese)
[5]Zhou N,Uchaker E,Liu Y,et al.Effect of carbon content on electrochemical performance of LiFePO4/C thin film cathodes[J].International Journal of Electrochemical Science, 2012, 7:12 633_12 645
[6]Su C, Bu X, Zhang C, et al.A novel LiFePO4/graphene/carbon composite as a performance-improved cathode material for lithium-ion batteries[J].Electrochimica Acta, 2012, 64:190_195
[7]Fedorkova A, Orinakova R, Orinak A, et al.PPY doped PEG conducting polymer films synthesized on LiFePO4particles[J].Journal of Power Sources, 2010,195:3 907_3 912
[8]Lin Y,Lin Y,Zhou T,et al.Enhanced electrochemical performances of LiFePO4/C by surface modification with Sn nanoparticles[J].Journal of Power Sources, 2013,226:20_26
[9]Ma Z,Shao G,Wang G,et al.Effects of Nb-doped on the structure and electrochemical performance of LiFe-PO4/C composites[J].Journal of Solid State Chemistry, 2014, 210:232_237
[10]Morgan D, Vanderven A, Ceder G.Li conductivity in LixMPO4(M=Mn, Fe, Co, Ni)olivine materials[J].Electrochemical and Solid-State Letters, 2004, 7(2):A30_A32
[11]Islam M S, Driscoll D J, Fisher C A J, et al.Atomic-Scale investigation of defects, dopants, and lithium transport in the LiFePO4olivine-type battery material[J].Chemistry of Materials, 2005, 17:5 085_5 092
[12]Nishimura S I, Kobayashi G, Yamada A, et al.Experimental visualization of lithium diffusion in LixFePO4[J].Nature Materials, 2008, 7:707_711
[13]Amin R, Balaya P, Maier J.Anisotropy of electronic and ionic transport in LiFePO4single crystals[J].Electrochemical and Solid-State Letters, 2007, 10(1):A13_A16
[14]Chen G, Song X, Richardson T J.Electron microscopy study of the LiFePO4to FePO4phase transition[J].Electrochemical and Solid-State Letters, 2006, 9(6):A295_A298
[15]Yu D Y W, Fietzek C, Weydanz W, et al.Study of LiFePO4by cyclic voltammetry[J].Journal of The Electrochemical Society, 2007, 154(4):A253_A257
[16]于文志.锂离子电池正极材料 LiFePO4的金属离子掺杂改性研究[D].湖南:湖南大学,2007 Yu Wenzhi.Research on themetallic ions dopingmodification of LiFePO4cathode materials[D].Hunan:Hunan University,2007
[17]Zhang W.Structure and performance of LiFePO4cathode materials:A review[J].Journal of Power Sources,2011,196(6):2 962_2 970
[18]Andersson A S, Thomas JO.The source of first-cycle capacity loss in LiFePO4[J].Journal of Power Sources,2001,97/98:498_502
[19]Su J, Wei B, Ren L, et al.A general solution-chemistry route to the synthesis LiMPO4(M=Mn, Fe, and Co)nanoparticle with [010]oritention for lithiumion batteries[J].Journal of Solid State Chemistry, 2011,184:2 909_2 919
[20]Kang W,Zhao C,Shen Q,et al.Ethylene glycol-assisted nanocrystallization of LiFePO4for a rechargeable lithium-ion battery cathode[J].Cryst Eng Comm,2012,14:2 245_2 250
[21]Mei R, Song X, Zhang J, et al.Plate-Like LiFePO4crystallite with preferential growth of(010)lattice plane for high performance Li-ion batteries[J].RSC Advances, 2014, 4:5 746_5 752
[22]Qin X, Wang J, Wang X, et al.Hydrothermally synthesized LiFePO4crystals with enhanced electrochemical properties:Simultaneous suppression of crystal growth along[010]and antisite defect formation[J].Physical Chemistry Chemical Physics, 2012, 14:2 669_2 677
[23]Chen M,Teng F, Li G, et al.Self-Assembly of highly uniform LiFePO4hierarchical nanostructure by surfactant molecules in a new mixture medium[J].Ionics, 2012,18:541_547
[24]Yang S, Zhou X, Liu Z, et al.Morphology-Controlled solvothermal synthesis of LiFePO4as a cathode material for lithium-ion batteries[J].Journal of Materials Chemistry, 2010, 20:8 086_8 091
[25]Zhu J, Fiore J, Kisailus D, et al.Solvothermal synthesis, development, and performance of LiFePO4nanostructures[J].Crystal Growth&Design, 2013, 13:4 659_4 666
[26]Nan C, Lu J, Li Y, et al.Solvothermal synthesis of lithiumiron phosphate nanoplates[J].Journal of Materials Chemistry, 2011, 21:9 994_9 996
[27]Zhang C, He X, Cui G, et al.A novel assembly of LiFePO4microspheres from nanoplates[J].Cryst Eng Comm,2012,14:4 344_4 349
[28]Wang B, Wang S, Wang D, et al.Growth of LiFePO4nanop lates with orientated(010)facets on grapheme for fast lithium storage[J].Materials Letters, 2014, 118:137_141
[29]Guo B, Ruan H, Wei M, et al.Hierarchical LiFePO4with a controllable growth of the(010)facet for lithiumion batteries[J].Scientific Reports, 2013, 3(2788):1_6
[30]Rui X,Zhao X,Yan Q,et al.Olivine-Type nanosheets for lithiumion battery cathodes[J].ACS Nano, 7(6):5 637_5 646
[31]Long Y,Shu Y,Ye M,et al.In-Situ synthesizing superior high-rate LiFePO4/C nanorods embedded in grapheme matrix[J].Electrochimica Acta, 2014, 117:105_112
[32]Dokko K,Koizumi S,Kanamura K,et al.Particlemorphology, crystal orientation, and electrochemical reactivity of LiFePO4synthesized by the hydrothermal method at 443 K[J].Journal of Materials Chemistry, 2007,17:4 803_4 810
[33]Nakano H,Dokko K,Kanamura K,et al.Hydrothermal synthesis of carbon-coated LiFePO4and its application to lithium polymer battery[J].Journal of the Electrochemical Society, 2008, 155(12):A909_A914
[34]Ferrari S, Lavall R L, Mustarelli P, et al.Influence of particle size and crystal orientation on the electorchemical behavior of carbon-coated LiFePO4[J].The Journal of Physical Chemistry C,2010,114:12 598_12 603
[35]Saravanan K, Reddy M V, Vittal J J, et al.Storage performance of LiFePO4nanoplates[J].Journal of Materials Chemistry, 2009, 19:605_610
[36]Saravanan K, Balava P, Vittal J J, et al.Morphology controlled synthesis of LiFePO4/C nanoplates for Li-ion batteries[J].Energy&Environmental Science, 2010,3:457_464
[37]Wang L, He X, Sun W, et al.Crystal orientation tuning of LiFePO4nanoplates for high rate lithium battery cathode materials[J].Nano Letters, 2012, 12:5 632_5 636
[38]Ma Z, Shao G, Wang X, et al.Solvothermal synthesis of LiFePO4nanoplateswith(010)p lane and the uniform carbon coated on their surface by esterification reaction[J].Materials Chemistry and Physics, 2014, 143:969_976
[39]Kanamura K, Koizumi S, Dokko K.Hydrothermal synthesis of LiFePO4as a cathode material for lithium batteries[J].Journal of Materials Science, 2008, 43:2 138_2 142
[40]Kim D, Lim J, Kim J, et al.Low-Cost LiFePO4using Fe metal precursor[J].Journal of Materials Chemistry,2012,22:2 624_2 631
[41]Wu M, Wang Z, Yuan L, et al.Morphology-Controllable solvothermal synthesis of nanoscale LiFePO4in a binary solvent[J].Chinese Science Bulletin, 2012, 57(32):4 170_4 175
[42]Ellis B,Kan W H,Nazar L F,et al.Synthesis of nanocrystals and morphology control of hydrothermally prepared LiFePO4[J].Journal of Materials Chemistry,2007,17:3 248_3 254
[43]Das S R, Majunder S B, Katiyar R S.Kinetic analysis of the Li+ion intercalation behavior of solution derived nano-crystalline lithium manganate thin films[J].Journal of Power Sources, 2005, 139:261_268
[44]Zhang D, Popov B N, White R E.Electrochemical investigation of CrO2.65doped LiMn2O4as a cathode material for lithium-ion batteries[J].Journal of Power Sources, 1998, 76:81_90
[45]Qin X,Wang X,Xiang H,et al.Mechanism for hydrothermal synthesis of LiFePO4platelets as cathodematerial for lithium-ion batteries[J].The Journal of Physical Chemistry C,2010,114:16 806_16 812
[46]Fisher C A J, Islam M S.Surface structures and crystal morphologies of LiFePO4:Relevance to electrochemical behavior[J].Journal of Materials Chemistry, 2008,18:1 209_1 215
[47]Kim D, Kim J.Synthesis of LiFePO4nanoparticles in polyolmedium and their electrochemical properties[J].Electrochemical and Solid-State Letters, 2006, 9(9):A439_A442

