二氧化碳和水对低温氧化铁脱硫的影响
张振荣,樊惠玲
(1.山西省应用化学研究所,山西太原030027;2.太原理工大学煤化所,山西太原030024)
硫普遍存在于各种化石能源中.在能源利用的过程中,这些硫会转化为硫化氢、羰基硫、硫醇、硫醚、噻吩等有机与无机硫.如煤在气化后,其中的主要硫化物为硫化氢,而天然气中硫化物除H2S外,还有少量硫醇、硫醚、噻吩等.一方面,硫化物对环境和人体都会造成严重危害,如煤气经燃烧后,其硫会转化为二氧化硫.二氧化硫对人体呼吸器官和眼膜具有刺激作用,吸入高浓度的二氧化硫可发生喉头水肿和支气管炎,长期吸入则会发生慢性中毒,不仅使呼吸道疾病加重,而且对肝、肾、心脏都有危害.大气中的二氧化硫还会形成酸雨,对湖泊、地下水、建筑物等构成腐蚀,长期的酸雨作用还将对土壤和水质产生不可估量的损失.因此,各国环境保护法对硫的排放要求越来越严格.另一方面,硫化物对许多工业用材料都有腐蚀毒作用,也是许多金属催化剂的主要毒物,如合成氨催化剂、变换催化剂、重整催化剂等.因而,工业原料气中硫化物的脱除一直都很受重视[1-2].脱硫有湿法脱硫与干法脱硫之分.干法脱硫具有脱硫精度高、易操作、占地小等优势,至今仍占有重要地位.干法脱硫剂有氧化锌、分子筛、活性炭及氧化铁脱硫剂等[2-7].分子筛和氧化锌脱硫剂价格昂贵,活性炭在脱硫时需要氧存在,限制了其使用.氧化铁脱硫剂则有价格低廉、设备投资费用少、使用地区广、硫容高、易再生,在有氧或无氧条件下都能脱除硫化氢的诸多优点,是工业中常用的脱硫方法[1,7,8].由于工业原料气中大都含有二氧化碳与水汽,因此考察二氧化碳与水汽对脱硫反应的影响是非常必要的.本文研究了这两种气体对氧化铁脱硫剂脱硫性能的影响.
1 实验部分
1.1 脱硫剂的制备
以铁矾土、炼铝工业副产物赤泥与石灰为原料,采用机械混合法制备氧化铁脱硫剂.煅烧成型的脱硫剂中含有氧化铁43%,氧化铝25%,氧化硅14%,氧化钙18%.实验用氧化铁脱硫剂为圆柱状固体颗粒,其物性参数见表1.

表1 氧化铁脱硫剂的物化性质Tab.1 Physical and chemical properties of iron oxide sorbent
1.2 实验方法
本研究采用热重法,在天津大学自行研制的微量动态热天平上进行.实验时,将含有硫化氢的反应气体通入微量热天平的反应管中,在一定温度及气氛下测取氧化铁脱硫剂在反应过程中的增重值随反应时间变化的热重曲线.实验所用反应气来自钢瓶供给的高纯氮气、高纯二氧化碳气,以及事先由纯硫化氢和高纯氮气配制好的高浓度硫化氢气体.各路气体流量采用转子流量计控制,并经各自的管路进入混合器中充分混合,配成所要求的反应气体.反应气中的水汽是将混合气通过一定温度的加湿器所带入的饱和水蒸气.反应气带水后,在进入热重反应器前,管路采用保温带加热,以避免水汽在管路凝结.反应尾气经碱液吸收后排空.热重实验示意图见图1,实验条件见表2.

图1 热重实验示意图Fig.1 Schematic diagram of thermogravimetric experiment

表2 实验条件Tab.2 Experimental conditions
2 结果与讨论
2.1 二氧化碳对脱硫的影响
首先在80~120℃ 的温区内,考察了无二氧化碳气氛中氧化铁脱硫剂的脱硫情况.具体的实验条件为:硫化氢浓度 15 g/m3,水汽含量19.65%,氮为平衡气.图2为脱硫剂在不同温度下的增重率-时间曲线.从图2可以看出,在硫化氢与水汽、氮气组成的简单气氛中,随反应温度的升高,脱硫活性也逐渐提高.在60 min的反应时间内,120℃ 时脱硫剂增重率可以达到近5%,而在80℃ 时增重率可达到4%.
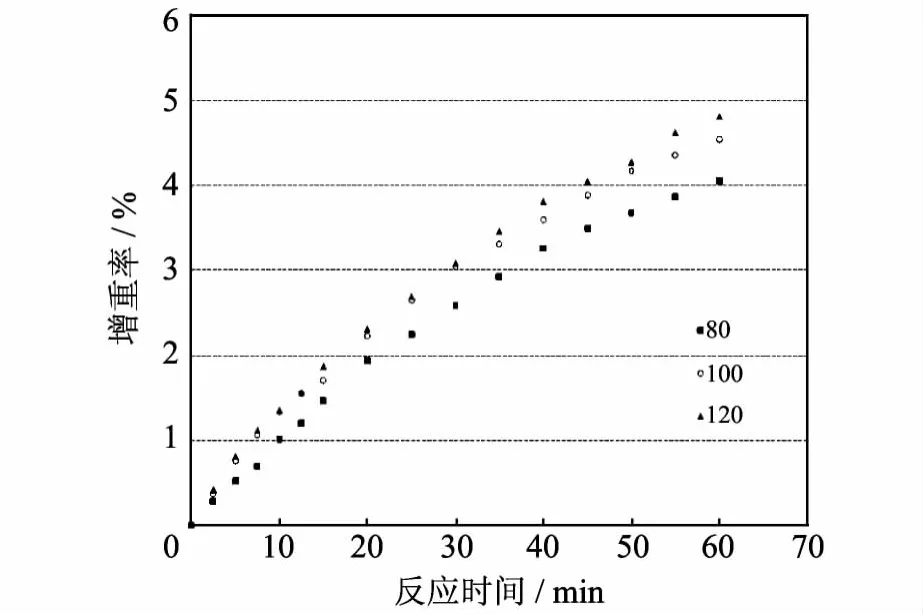
图2 不同温度下氧化铁脱硫剂在无二氧化碳气氛中的热重脱硫曲线Fig.2 TG curves of desulfurization of iron oxide sorbent at various temperatures in the absent of CO2
在相同实验条件下,考察了二氧化碳气氛对氧化铁脱硫剂脱硫速率的影响.即实验条件为:硫化氢浓度15 g/m3,水汽含量19.65%,二氧化碳浓度 25%,氮为平衡气;温度则同样选择在80~120℃ 的温区内.硫化实验结果如图3所示.可以看出,在二氧化碳参与的脱硫气氛中,脱硫剂的脱硫活性在80~120℃ 的温区内,也同样随着温度的升高而升高,表现出正效应.与图2相比,氧化铁脱硫剂在二氧化碳气氛下的脱硫活性显然低于无二氧化碳气氛下的活性.
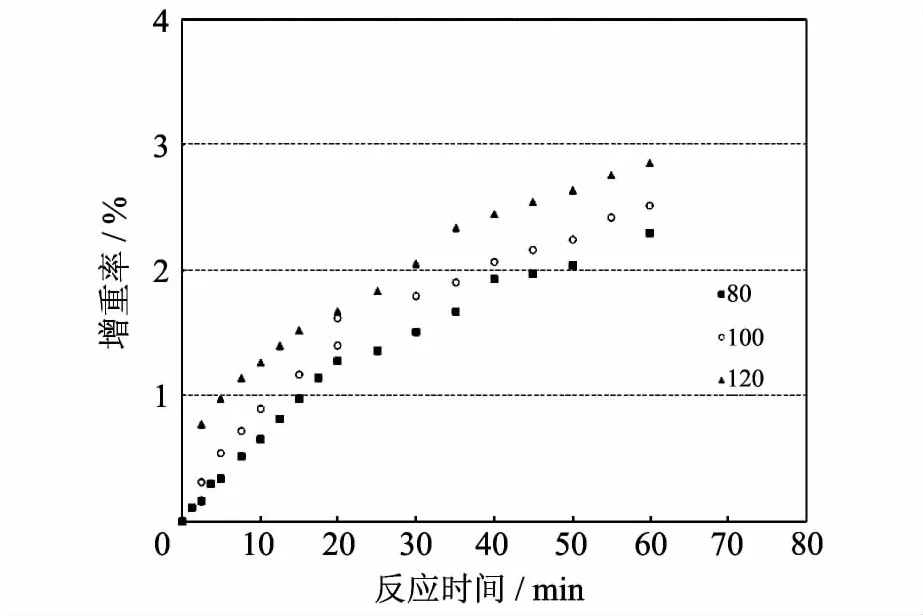
图3 不同温度下氧化铁脱硫剂在二氧化碳气氛中的热重脱硫曲线Fig.3 TG curves of desulfurization of iron oxide sorbent at various temperatures in the presence of CO2
为了更直观明确地说明二氧化碳的存在对氧化铁脱硫剂脱硫行为的影响,在同一温度下对两种气氛的实验结果进行了比较,结果如图4所示.
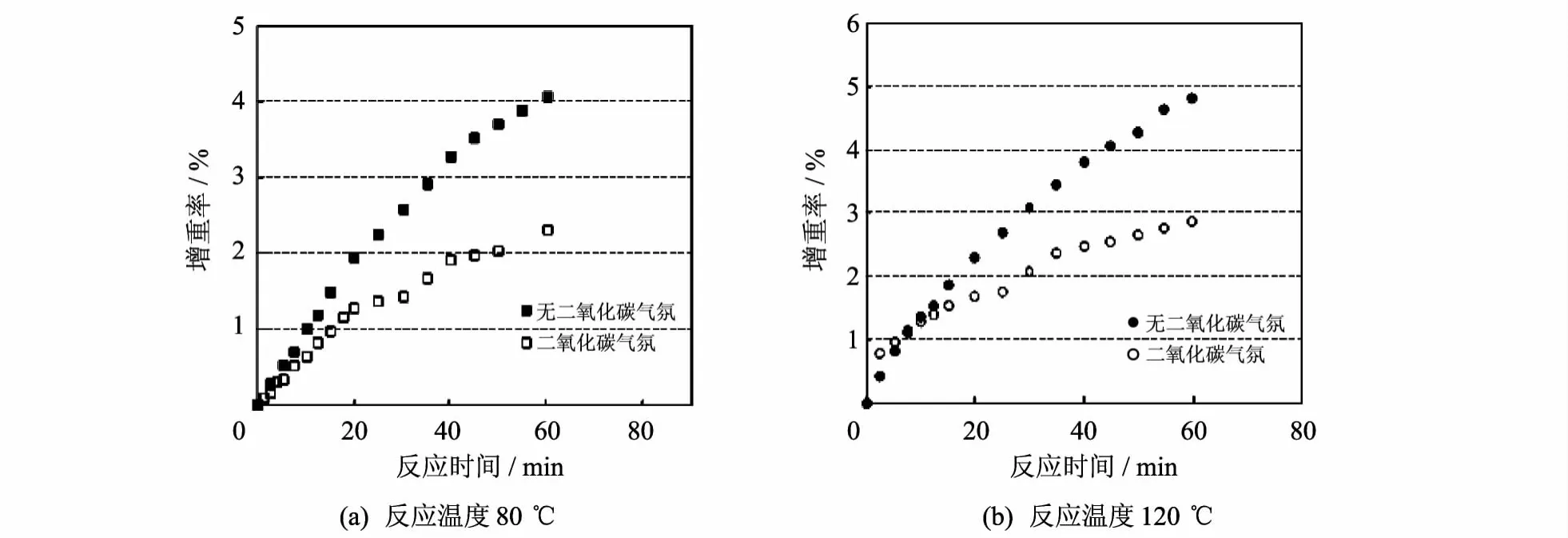
图4 氧化铁脱硫剂在不同气氛中的脱硫热重曲线Fig.4 TG curves of desulfurization of iron oxide sorbent in different atmospheres
由图4明显可见,在两个温度水平下,氧化铁脱硫剂在无二氧化碳气氛下的脱硫速率均高于二氧化碳气氛.在80℃ 时,经过60 min的反应时间,氧化铁的脱硫增重率可以达到4.03%,而在二氧化碳气氛中增重率则只有 2.30%;在120℃ 时,经相同的反应时间,无二氧化碳气氛下增重率达到4.81%,而在二氧化碳气氛中增重率却只有2.86%.可以看出,二氧化碳的存在不利于脱硫的进行,对脱硫有负效应.
氧化铁脱硫虽然是传统和较为古老的脱硫技术,但由于氧化铁中铁价态可变,其本身晶型又多样,且随温度、气氛等反应条件的不同,氧化铁脱硫具有不同的反应过程.因此,其涉及的脱硫反应机理实际上是很复杂的.如对于高温、有氢参与的气氛中,一般认为氧化铁的脱硫过程为:

但在无氢或无一氧化碳存在的非还原气氛下,氧化铁脱硫则非如此.刘生昕[9]等在280~320℃温度范围内,对氧化铁脱硫行为进行过研究.结合实验中观察到反应器出口有硫磺沉积,且在尾气中发现有H2生成的现象,认为在仅含硫化氢与氮气的简单气氛下,脱硫按如下方式进行:

如果是在室温条件下,有脱硫活性的氧化铁晶型为水合态的,反应历程又与上述两种不同.本研究采用的氧化铁为无水的无定形氧化铁,且实验过程中无论反应器壁还是反应管出口均未发现硫磺沉积.反应停止后,对样品进行了XRD检测,发现样品中既有FeS2也有FeS存在(如图5所示),因此认为反应是按如下方程进行:


图5 硫化后氧化铁脱硫剂的XRD图谱Fig.5 XRD patterns of iron oxide sorbent after desulfurization
解释二氧化碳对氧化铁对脱硫行为的影响,需要结合以上反应机理与整个反应过程来说明.一般认为,对于固体金属氧化物与气体硫化氢间的脱硫反应,整个过程需经历:①气相本体中的H2S经气膜扩散到固体脱硫剂的颗粒外表面;②H2S从颗粒外表面从孔道内扩散进入到脱硫剂内表面;③H2S在脱硫剂内表面吸附;④吸附在内表面的硫化氢与表面活性金属氧化物反应生成硫化铁;⑤金属氧化物表层新生的硫化物与内层的新鲜活性成分进行固体离子交换,更新表面并使其可继续脱硫反应;⑥生成的水汽经由脱硫剂的毛孔反向扩散到颗粒外表面;逸至脱硫剂颗粒外表面的水汽经气膜扩散进入气相本体中[10-11].由于硫化氢是一种酸性气体,与同为酸性气体的二氧化碳在脱硫过程中会产生竞争吸附,致使硫化氢在氧化铁固体表面吸附速率减弱,从而影响了整个脱硫进程,表现出负效应.这一现象在以氧化锌为活性组分的中温脱硫反应过程中也同样存在[12-13].
2.2 水气氛对氧化铁脱硫的影响
在温度为120℃,H2S浓度11.4 g/m3,无二氧化碳气氛下考察了水汽含量对氧化铁脱硫行为的影响,结果见图6.表3给出了不同水汽含量下,在经相同反应时间后,氧化铁脱硫剂的增重率值,以便于更为直观地比较.由图表可见,水的影响较为复杂,但对于脱硫反应存在一个最佳水汽含量值.热重研究结果显示,少量水的存在对脱硫是有利的,可以促进脱硫的进行,但促进作用在水含量为4.19% 时最大.当脱硫气氛中水含量超过此值时,虽然研究结果也显示有促进作用,但这一促进作用减弱.当气氛中有更大量的水存在时,热重结果显示的增重率就明显低于无水条件下的,表明此时水对脱硫有抑制作用,即出现了负效应.上文提到了固体氧化铁在脱硫过程中的各个过程,但未提及氧化铁表面的液膜形成.液膜作用在室温氧化铁脱硫反应中被常常提到[14].

图6 水汽含量对氧化铁脱硫的影响Fig.6 Influence of the content of water vapor on the desulfurization
虽然本研究所采用的温度高于室温,但作者认为,氧化铁脱硫剂在水汽包裹中也可形成水膜,而这一水膜呈碱性,因此对于硫化氢在其表面的吸附是有利的.K.Polychronopoulou等在研究锌钛锰及铁锌钛锰复合型脱硫剂在低温下的脱硫中也发现,水可使脱硫剂表面羟基化,进而利于硫化氢的吸附[15-16].不过,当系统中有大量的水存在时,可能会对脱硫反应的平衡造成左移影响.这样,水对反应平衡造成的负面影响就部分抵消了由于水膜的存在而形成的积极作用.而且,当脱硫剂处于大量的水汽包裹中时,对于硫化氢向脱硫剂表面的扩散也变得不利.因此,在工业中使用脱硫剂时,应避免水汽夹带过多的情况出现.
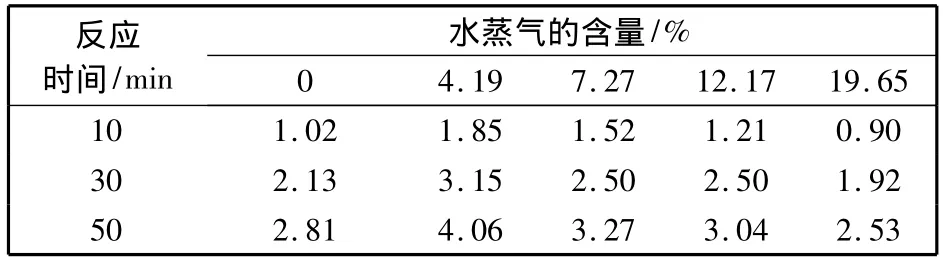
表3 不同水气氛下氧化铁脱硫剂在不同反应时间增重率对比结果Tab.3 Comparison of weight increasing rate of iron oxide sorbent in variousatmosphere with water vapor at different reaction time (%)
3 结论
1)二氧化碳对低温氧化铁脱硫具有抑制作用,这主要是由于竞争吸附所导致的.
2)水汽含量对低温氧化铁脱硫的影响较为复杂.少量水汽因可在脱硫剂表面形成水膜,利于硫化氢在脱硫剂表面溶解吸附,因而会促进脱硫.但大量的水汽存在,也会对平衡产生影响,使得脱硫速率减慢.
[1]李芬,张杰.低温脱硫剂的研究进展[J].化工进展,2007,26(7):519-525.Li Fen,Zhang Jie.Research progress of desulfurizer at a low temperature[J].Chemical Industry and Engineering Progress,2007,26(7):519-525.(in Chinese)
[2]Samokhvalov A,Tatarchuka B.Characterization of active sites,determination of mechanisms of H2S,COS and CS2sorption and regeneration of ZnO low-temperature sorbents:past,current and perspectives[J].Physical Chemistry Chemical Physics,2011,13:3197-3209.
[3] Balouriaa V,Kumar A,Samanta S.Nano-crystalline Fe2O3thin films for ppm level detection of H2S[J].Sensors and Actuators B:Chemical,2013,181:471-478.
[4] Dhage P.Copper-promoted ZnO/SiO2regenerable sorbents for the room temperature removal of H2S from reformate gas streams[J].Industrial and Engineering Chemistry Research,2010,49:8388-8396.
[5]Yasyerli S,Ar I,Dogu G,et al.Removal of hydrogen sulfide by clinoptilolite in a fixed bed adsorber[J].Chemical Engineering and Processing,2002,41:785-792.
[6]Yu Jianglong.Sulfur removal property of activated-charsupported Fe-Mo sorbents for integrated cleaning of hot coal gases[J].Fuel,2013,108:91-98.
[7] Fan Huiling.A comparative study of the effect of clay binders on iron oxide sorbent in the high-temperature removal of hydrogen sulfide[J].Process Safety and Environmental Protection,2013,91(3):235-243.
[8]郭汉贤.我国脱硫技术发展的回顾及展望[J].煤化工,2003,105(2):51-54.Guo Hanxian.The development of desulfurizing technique and its future progress in China[J].Coal Chemical Industry,2003,105(2):51-54.(in Chinese)
[9]刘生昕.氢对氧化铁脱硫剂脱硫行为的影响[J].煤炭学报,2013,38(1):156-160.Liu Shengxin.The effects of hydrogen on the desulfurization behavior of iron oxide sorbents[J].Journal of China Coal Society,2013,38(1):156-160.(in Chinese)
[10]郭汉贤.应用化工动力学[M].北京:化学工业出版社,2003.
[11]侯璐达,周立辉.脱除 H2S的固定床反应器研究[J].西安交通大学学报,2010,44(5):91-96.Hou Luda,Zhou Lihui.Study of fixed bed reactor for removing H2S by ferric oxide[J].Journal of Xi'an Jiaotong University,2010,44(5):91-96.(in Chinese)
[12]Sasaoka E,Hirano S,Kasaoka S,et al.Characterization of reaction between zinc oxide and hydrogen sulfide[J].Energy& Fuels,1994,8(5):1100-1105.
[13]Fan Huiling.Influence of gas composition on hydrogen sulfide removal at moderate temperature[C].Wuhan:The 5th International Conference on Bioinformatics and Biomedical Engineering,2011.
[14]郭汉贤,刘明清.干法氧化铁脱硫的动力学特征(1)过程描述及SLP型吸附性能[J].太原工学院学报,1983(3):105-112.Guo Hanxian,Liu Mingqing.Kinetic characteristics of dry desulfurization by iron oxide.1 description of process and properties of supported liquid-phase absorption[J].Journal of Taiyuan University of Technology,1983(3):105-112.(in Chinese)
[15]Polychronopoulou K,Fierro J,Efstathiou A.Novel Zn-Ti-based mixed metal oxides for low-temperature adsorption of H2S from industrial gas streams[J].Applied Catalysis.B:Environmental,2005,57:125-137.
[16]Polychronopoulou K.Novel Fe-Mn-Zn-Ti-O mixed-metal oxides for the low-temperature removal of H2S from gas streams in the presence of H2,CO2,and H2O[J].Journal of Catalysis,2005,236:205-220.

