一种真菌吸附剂对废水中Pb2+的吸附
曲娟娟,彭泓杨,顾海东,金 羽,李太君
(1.东北农业大学资源与环境学院,哈尔滨 150030;2.黑龙江贝因美乳业有限公司,黑龙江 安达 151400)
一种真菌吸附剂对废水中Pb2+的吸附
曲娟娟1,彭泓杨1,顾海东1,金 羽1,李太君2
(1.东北农业大学资源与环境学院,哈尔滨 150030;2.黑龙江贝因美乳业有限公司,黑龙江 安达 151400)
利用工业发酵产生的黑曲霉废弃菌丝体为吸附剂,研究其对重金属模拟废水中铅的吸附效果。运用单因素试验确定吸附条件为30℃,pH 5.0,初始铅离子浓度50 mg·L-1,吸附剂投加量2 g·L-1,转速160 r·min-1,吸附时间为30 min,吸附率为91.5%,吸附行为符合Freundlich方程。正交试验极差分析表明,影响吸附主要因素为吸附剂投加量、初始Pb2+浓度和pH。经正交试验优化,当吸附剂投加量为2 g·L-1,初始铅离子浓度40 mg·L-1,pH 4.5时,吸附率可提高2.7%。电镜结果显示,菌丝体表面疏松多孔,极易通过物理吸附方式吸附Pb2+,菌丝体表面氨基、羧基、磷酸基和羟基可有效配位络合Pb2+。结果表明,废弃菌丝体可用作吸附剂去除废水中Pb2+。
废弃菌丝体;Pb2+;生物吸附;单因素试验;正交试验
目前处理高浓度难降解重金属废水方法主要有化学沉淀法、离子交换法、活性炭吸附法、蒸发和反渗透法等[1-2],但处理效率低、成本高,尤其是废水中重金属浓度低于100 mg·L-1时[3-4]。生物吸附法设备简单、处理能力大、运行成本低,不易造成二次污染,尤其适用于低浓度重金属废水处理[5-7]。研究发现,死细胞、“半存活”或“半完整”状态细胞能高效吸附重金属,显著降低重金属离子对活生物体的毒性,具有广泛应用前景和实用价值[8]。
黑曲霉是发酵工业重要生产用菌,可用于多种有机酸和酶制剂生产,但废料处理困难[9]。菌丝细胞壁上胞外聚合物中含大量活性基团,如巯基、羟基和羧基等,可通过离子交换、络合、配位作用与金属离子发生定量化合反应将重金属离子从污水中去除[10]。利用废弃菌丝体为吸附剂处理重金属废水,具有原料来源充足、成本低、操作简单、去除效率高等优点[2,9-11]。本试验利用废弃黑曲霉菌丝体制备吸附剂,通过单因素和正交试验确定该吸附剂对铅离子的最佳吸附条件,研究吸附机理,为重金属废水的生物处理提供理论依据。
1 材料与方法
1.1 吸附剂的制备
取废弃的黑曲霉菌丝体,经无菌水反复清洗后,60℃烘干,研钵中研磨成粉。
1.2 生物吸附测定
采用模拟污水,对影响铅离子吸附的单因素条件进行研究。铅标准曲线配制:将铅标准溶液分别配制成浓度为1、2、3、4和5 mg·L-1的铅溶液,用原子吸收分光光度计(日本岛津)测定后绘制标准曲线,利用该标准曲线校正仪器误差(其中该仪器检测限为≤0.005 μg·mL-1,精密度为≤1%)。将Pb(NO3)2·3H2O配制成1 g·L-1的铅溶液作母液,使用时用去离子水稀释到所需浓度。测定前,重金属溶液要用ddH2O适当稀释,以确保样品中离子浓度与测定吸光度呈线性关系。吸附后离心,原子吸收分光光度计测定上清液中的铅离子浓度,吸附容量和铅离子去除率计算公式如下:

式中,Q-吸附容量(mg·g-1);R-对重金属离子的吸附效率(%);Co-溶液初始重金属离子浓度(mg·L-1);Ce-上清液中残余重金属离子浓度(mg·L-1);V-吸附体系的体积(L);M-菌体干重(g)。
1.3 吸附条件单因素试验设计
对可能影响生物吸附的条件,即初始Pb2+浓度、pH、菌粉投加量、转速和温度等进行单因素试验。初始Pb2+浓度为25、50、75、100、125 mg·L-1;pH 为3、4、5、6、7;菌粉投加量为0.5、1.0、1.5、2.0、2.5、3.0 g·L-1;转速为80、100、120、140、160、180 r·min-1;温度为15、20、25、30、35、40℃;吸附时间为10、20、30、40、50、60 min。每个处理设置3个重复。除非另作说明,基本培养条件一致为:初始Pb2+浓度75 mg·L-1,初始pH 6,转速120 r·min-1,温度30℃,培养时间30 min,吸附剂投加量2 g·L-1。
1.4 吸附等温模型
在菌体投加量为2 g·L-1,溶液pH 6,吸附时间30 min,温度30℃,摇床转速为120 r·min-1条件下,调节Pb2+初始浓度分别为25、50、75、100、125、150 mg·L-1,测定吸附平衡时滤液中的Pb2+浓度Ce。
1.5 吸附条件正交优化设计及验证
在多个单因素试验的基础上,设计培养条件的4因素3水平正交试验L9(34),以铅的生物吸附率为考查指标,对菌粉吸附剂的铅离子吸附条件进行优化。按照优化后的条件进行吸附试验,计算吸附率,验证吸附率是否提高。
1.6 扫描电镜分析
吸附前后的冻干菌粉粘到碳导电介质板上镀金,室温扫描,通过SEM进行形貌分析。
1.7 红外光谱分析
将吸附前后的菌丝体低温干燥,用红外光谱分析仪(ALPHA-T),KBr压片后进行红外光谱分析,扫描波长范围400~4 000 cm-1。
1.8 数据处理和分析
每次处理设3次重复,用SPSS 17.0软件进行正交试验的极差分析以及方差分析。
2 结果与分析
2.1 单因素试验结果
2.1.1 菌粉投加量对吸附的影响
由图1可知,随菌粉投加量由0.5 g·L-1增加到2 g·L-1,菌粉对铅离子吸附率随之增加,最高吸附率达92.7%。可能因为适当增加菌粉投加量,可增加吸附剂的表面积,给Pb2+提供更多吸附位点,振荡过程中菌粉表面的活性基团充分与Pb2+接触,吸附率提高。但当吸附剂用量继续增大时,吸附剂颗粒相互碰撞机会增加,使颗粒粘在一起,有效吸附基团被覆盖,吸附剂粒径逐渐增大,吸附表面积逐渐变小,吸附率下降。故菌粉最佳投加量为2 g·L-1。姜烛等研究生物量在给定的平衡浓度下,低生物浓度要比高生物浓度吸附更多的金属离子,可证明吸附剂过量对吸附不利[9]。
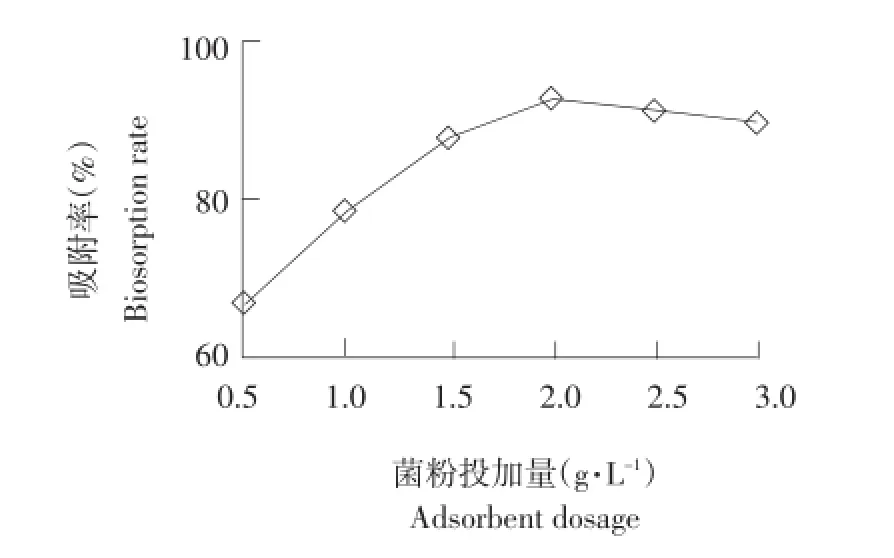
图1 菌粉投加量对Pb2+吸附效果的影响Fig.1 Effect of adsorbent dosage on Pb2+biosorption
2.1.2 初始铅离子浓度对吸附的影响
结果见图2。

图2 初始铅浓度对Pb2+吸附效果的影响Fig.2 Effect of initial Pb2+concentration on Pb2+biosorption
由图2可知,随Pb2+溶液浓度增加,菌粉吸附率逐渐增大,在Pb2+溶液浓度为50 mg·L-1时吸附率达最大值为91.3%。之后吸附率开始大幅度下降。重金属离子的吸附过程与重金属离子浓度和吸附剂投加量比值有关,在一定范围内,重金属离子浓度与吸附剂投加量比值越大,吸附率就越大,直到饱和,如继续增加重金属离子浓度,表面位点被充分占满的吸附剂已不能再吸附过多重金属离子。根据试验结果选择Pb2+浓度为50 mg·L-1。
2.1.3 吸附温度对吸附的影响
结果见图3。

图3 温度对Pb2+吸附效果的影响Fig.3 Effect of temperature on Pb2+biosorption
由图3可知,菌粉对Pb2+的吸附率随温度的升高而增大,在温度为30℃达到最大值91.8%。胡正等报道,在温度为37℃时,吸附最好[10]。在高温条件下,菌粉的一些吸附位点被活化,吸附剂表面活性基团内化学键断裂,吸附位点数量增加。此外生物吸附是吸热反应过程,温度升高也有利于吸附平衡向吸热方向移动[11]。但是本研究发现在温度为30℃时吸附率最大,生产实践中,温度越高,耗能越大,高温加剧溶液中铅离子热运动,使铅离子与吸附剂脱离,不利于吸附,选择30℃为最佳温度。
2.1.4 吸附时间对吸附的影响
结果见图4。

图4 吸附时间对Pb2+吸附效果的影响Fig.4 Effect of adsorption time on Pb2+biosorption
由图4可知,菌粉对Pb2+的吸附率随着吸附时间的增加而增大,30 min达到最大值89.5%。分析原因是开始时溶液中Pb2+浓度高于菌粉表面Pb2+的浓度,菌粉表面空白吸附位点较多,故Pb2+可与其表面的吸附位点快速结合;随着吸附进行,吸附位点逐渐饱和,固液两相中Pb2+浓度梯度也逐渐减小,故吸附率趋向平衡。在不影响吸附率的前提下,缩短吸附时间对污水处理具有重要意义[12]。选择30 min为最佳吸附条件。
2.1.5 转速对吸附的影响
结果见图5。
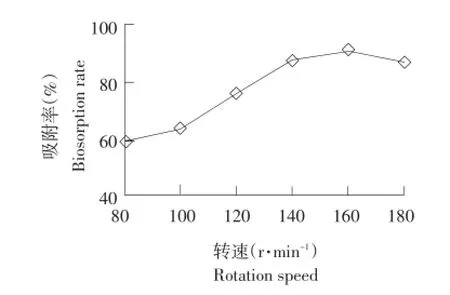
图5 摇床转速对Pb2+吸附效果的影响Fig.5 Effect of rotation speed on Pb2+biosorption
由图5可知,摇床转速80~160 r·min-1时,吸附率随摇床转速增加而缓慢增大,当摇床转速160 r·min-1时吸附率达最大值90.7%。超过160 r·min-1后,吸附率开始下降。可能是在一定范围内转速升高可增加吸附剂与Pb2+碰撞机会,从而增加吸附可能性,故吸附率增大;然而转速过高时,吸附剂与Pb2+的碰撞过于剧烈,影响Pb2+与吸附剂表面官能团反应,从而影响吸附剂有效吸附[13],故选用160 r·min-1为最佳转速。
2.1.6 pH对吸附的影响
结果见图6。
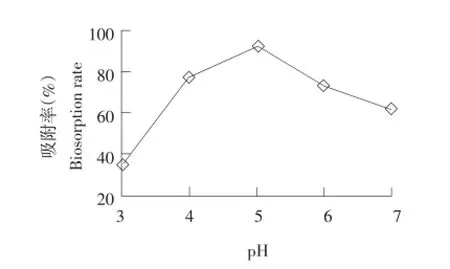
图6 pH对Pb2+吸附效果的影响Fig.6 Effect of pH on Pb2+biosorption
由图6可知,在pH 3时,菌粉吸附率很低,只有35.5%,可能由于在pH较低时,溶液中存在的大量H+会与同样为阳离子的Pb2+竞争吸附剂表面的吸附位点,从而降低吸附位点与Pb2+的结合能力和反应机会,因此吸附率很低。pH 5时,吸附率达最大值91.2%,因为随pH增大,H+逐渐减少,同时吸附剂易暴露出更多的吸附位点,使吸附率逐渐增大;但当pH继续增大时,部分Pb2+会以Pb (OH)2的沉淀形式存在,影响吸附效果[14],因此pH 5为最佳条件。
2.2 等温吸附方程的建立
由吸附容量和平衡浓度关系绘出的曲线即吸附等温线。试验用Langmuir等温吸附方程和Freundlich等温吸附方程拟合菌粉吸附剂对铅的吸附过程。

式中,Q-平衡时的重金属吸附容量,Ce-重金属的平衡浓度,Qmax-Langmuir方程常数,即表征理论饱和吸附量,b-Langmuir方程与吸附能量有关的常数,即表征吸附剂与吸附质的亲和力,k-Freun⁃dlich方程吸附平衡常数,即表征吸附剂的吸附能力,n-Freundlich方程吸附平衡常数。用Langmuir吸附等温式和Freundlich吸附等温式分别对吸附等温线进行线性拟合,结果见图7。
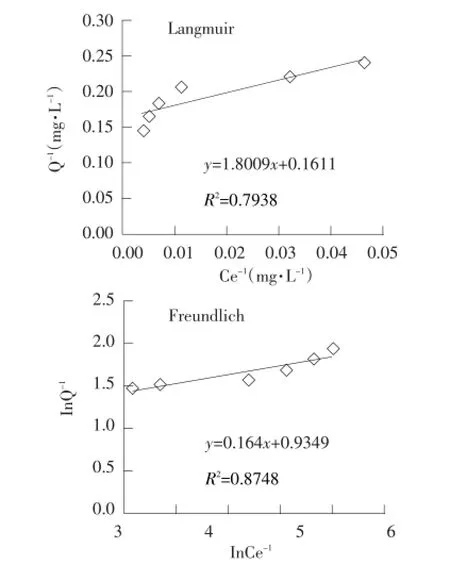
图7 Langmuir和Freundlich吸附等温线Fig.7 Langmuir and Freundlich absorption isotherm
由图7可知,Langmuir方程的相关系数为0.7938,而Freundlich方程的相关系数为0.8748,说明Freundlich方程拟合的相关系数比Langmuir方程的相关系数高,即Freundlich拟合效果较好,表明随吸附平衡时的Pb2+质量浓度增大,吸附容量也随之增加,但吸附平衡时Pb2+质量浓度增加到一定程度后,吸附容量不再变化。
2.3 正交因素水平的测定
在单因素试验基础上,选择对生物吸附影响较大的3个因素,即菌粉投加量(A)、初始Pb2+浓度(B)、初始pH(C),并设置随机因素(D)检验试验误差。每个因素各选取3个水平,进行L9(34)正交试验(见表1)。

表1 L9(34)正交试验因素水平Table 1 Factor and levels in L9(34)orthogonal experiment
2.4 正交结果的直观分析与方差分析
按L9(34)正交表,以Pb2+吸附率为指标,进一步优化Pb2+吸附条件。正交试验设计及结果直观分析见表2,方差分析见表3。
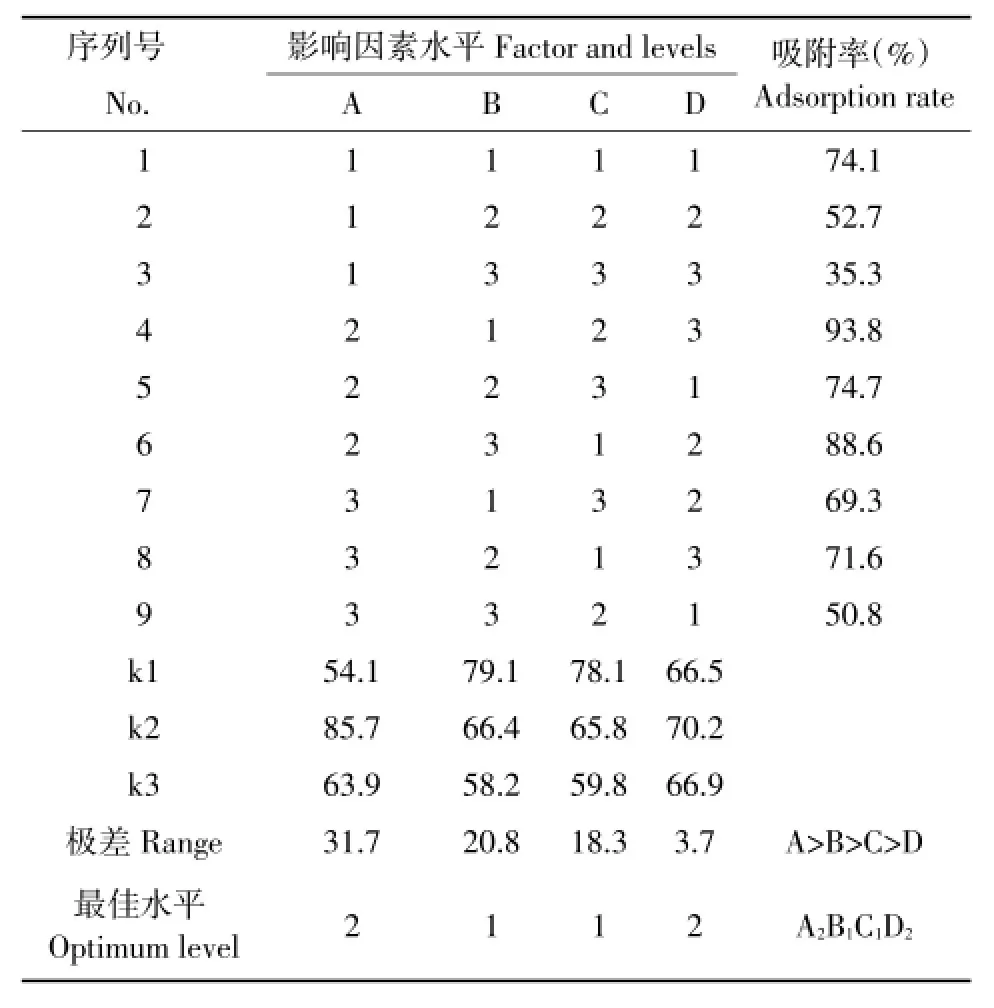
表2 Pb2+生物吸附条件的L9(34)正交表安排及直观分析结果Table 2 Orthogonal matrix method and results of visual analysis for biosorption conditions of Pb2+

表3 Pb2+生物吸附条件优化的正交试验方差分析Table 3 Variance analysis of orthogonal experiment for optimization of Pb2+biosorption conditions
正交试验可对各因素影响进行综合评价,由极差比较可知,A、B、C、D 4个因素影响真菌吸附剂对Pb2+吸附的主次顺序为:A>B>C>D,即菌粉投加量>初始Pb2+浓度>pH,最佳吸附条件为A2B1C1D2,即菌粉投加量为2 g·L-1,初始Pb2+浓度为40 mg·L-1,初始pH 4.5。
为从有限数据挖掘科学结论,正交表必须考虑留有不排入因素或互作空列用来估算试验误差。表3为正交试验方差分析结果。由结果知校正模型R2=0.993,AdjR2=0.973。A、B、C为显著因素,说明这3个因素对试验结果可造成很大影响。
2.5 正交最优吸附条件的验证
3个平行重复试验,对正交试验所得的最佳Pb2+吸附条件A2B1C1D2进行验证。按正交优化条件进行Pb2+生物吸附。在最优条件下,吸附率可达94.2%,比单因素试验的最高生物吸附率(91.5%)提高2.7%。说明通过正交试验对吸附条件进行优化,吸附率有一定幅度提高。
2.6 扫描电镜分析
利用扫描电镜对吸附前后黑曲霉菌丝的表观形貌进行观察。如图8a可见菌丝团聚在一起,菌丝间错综复杂,形成较大孔洞。吸附后(见图8b)菌丝较为松散,周围形成颗粒物。由吸附变化推测,存在物理吸附行为,而物理吸附主要通过比表面积实现[15]。菌丝体间形成很多微孔,比表面积很大,能够满足物理吸附,在微孔中,被吸附颗粒受到周围孔壁的共同作用,吸附势能高于一般的平面吸附。

图8 黑曲霉吸附Pb2+前后扫描电镜Fig.8 SEM of Aspergillus niger before and after Pb2+adsorption
2.7 红外光谱
黑曲霉吸附前后的红外光谱如图9所示。由图9a可知,3 500~3 200 cm-1范围内出现较宽的吸收带,为O-H/N-H的伸缩振动吸收峰,来自蛋白质、多糖及脂肪酸等组分。2 925.42 cm-1处是典型的脂碳链=CH、C-H键的伸缩振动吸收带,反映不饱和脂肪酸、膜结构及细胞壁组分的亲水脂分子信息。1 732.62 cm-1处为羧酸的C=O振动吸收峰。典型的酰胺Ⅰ带(C=O的伸展运动)、酰胺Ⅱ带(-NH的弯曲振动与-CN伸展振动的叠加)分别出现在1 652.21和1 540.75 cm-1处,1 456.12 cm-1附近的谱峰为蛋白质中受O、N原子影响的甲基的对称和反对称振动区。1 338.69 cm-1(C-O伸缩振动)与1 235.32 cm-1处的吸收峰说明存在-COOH基团。1 235.32 cm-1的峰主要来自P=O和C=S的伸缩振动以及-C(C=O)O-与-OH的叠加。1 029.10 cm-1处为碳水化合物中C-O-C和C-O的伸缩振动吸收峰。此外,胺基中C-N的伸缩振动、脂肪酸及酯类分子的C-O振动也在其附近。低于600 cm-1的586.65 cm-1处的谱峰是M-O和O-M-O(M为金属离子)振动吸收峰。由此可初步推断,黑曲霉主要含有羟基、羧基、胺基、酰胺基和磷酸基。
由图9b可知,-OH峰与-NH峰发生较明显变化,分别漂移至3 293.89和2 924.79 cm-1处;羧酸C= O振动吸收峰由1 732.62cm-1漂移至1 747.09 cm-1;酰胺基与C-H键基本无变化;P=O与C=S振动吸收峰漂移至1 238.87 cm-1处;位于1 000~1 100 cm-1糖类C-OH伸缩振动吸收峰从1 029.10 cm-1迁移至1 034.52 cm-1;M-O和O-M-O振动吸收峰漂移至574.12 cm-1。可见黑曲霉对Pb2+的吸附主要通过细胞成分中的氨基、羧基、磷酸基和羟基。
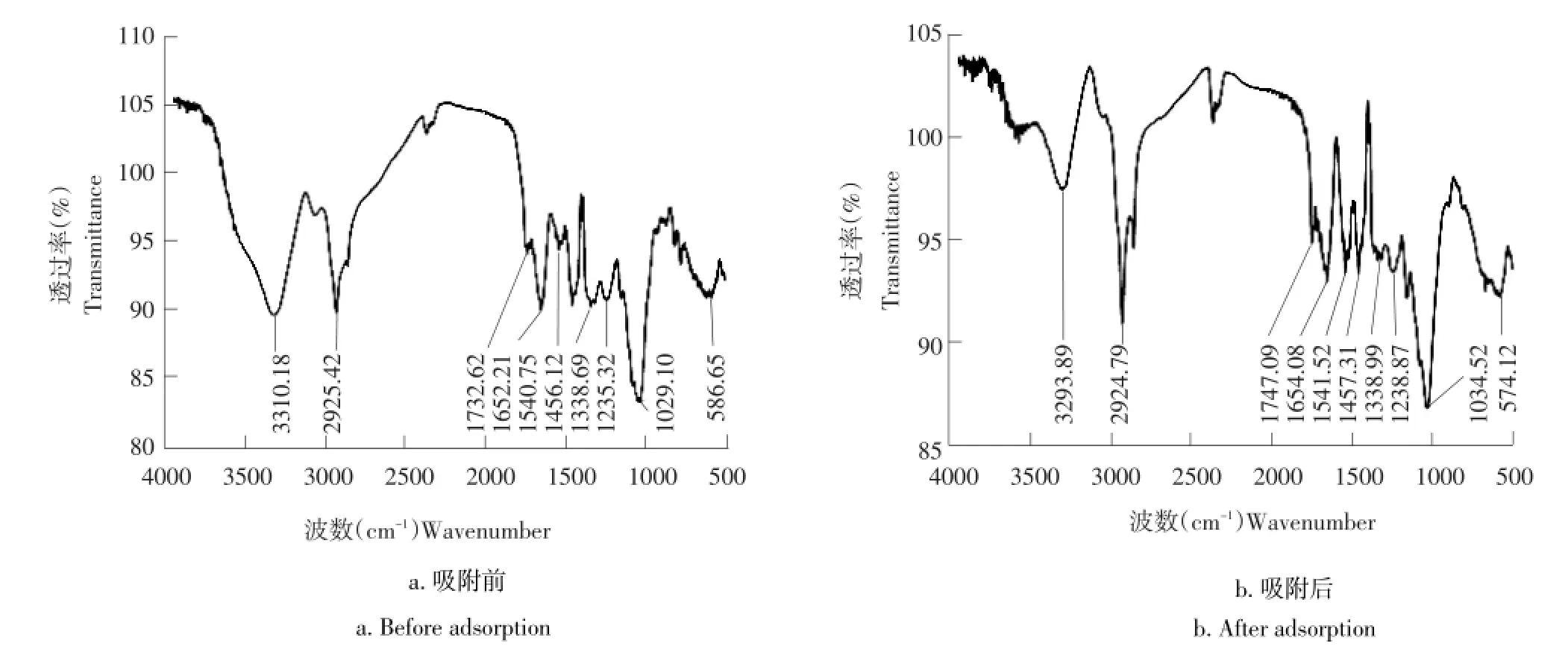
图9 黑曲霉吸附Pb2+前后红外光谱图Fig.9 FTIR spectrometer of Aspergillus niger before and after Pb2+adsorption
3 讨论与结论
生物吸附方法及材料在污水处理应用很多,包括所有微生物细胞、各种植物材料、食品工业的废弃物在内的各种原料均可用于生物吸附剂制备和吸附研究。发酵工业生产中废弃物近年来引起广泛关注,尤其是食品工业中废弃黑曲霉菌丝体,具有安全、价廉、吸附能力强等优点,在重金属废水的生物治理中有广阔应用前景。霉菌吸附剂利用其细胞壁自身结构和化学成分通过物理和化学作用将金属离子吸附在胞外聚合物及官能团上,减少水体中金属离子的含量。研究表明,黑曲霉吸附Pb2+通过与吸附剂表面Ca2+、Mg2+、K+等发生离子交换作用实现[16]。pH通过影响溶液中金属的化学特征、吸附剂表面官能团的活性及与被吸附金属离子竞争的H+数量,间接影响吸附效果,尤其是对活体生物吸附剂,吸附效率随pH变化而出现较大波动[17],本研究利用无生命活力菌粉吸附剂,pH对其影响较小。
本研究利用工业废气菌丝体粉末为吸附剂,去除模拟废水中铅离子,通过单因素,确定吸附Pb2+的最佳条件为:初始Pb2+浓度50 mg·L-1,初始pH 5,转速160 r·min-1,温度30℃,吸附时间30 min,菌粉投加量2 g·L-1,最高吸附率为91.5%。正交试验的极差分析与方差分析表明,主次顺序为菌粉投加量>初始Pb2+浓度>初始pH,最佳吸附条件为菌粉投加量为2 g·L-1,初始Pb2+浓度为40 mg·L-1,初始pH 4.5,正交试验最高生物吸附率达94.2%,提高2.7%。电镜结果显示菌丝体表面疏松多孔,极易通过物理吸附方式吸附Pb2+,菌丝体表面的氨基、羧基、磷酸基和羟基可有效配位络合Pb2+。结果表明,黑曲霉废弃菌丝体可有效去除模拟废水中Pb2+,是极具潜力的生物吸附剂。
[1]Areco M M,Hanela S,Duran J,et al.Biosorption of Cu(Ⅱ), Zn(Ⅱ),Cd(Ⅱ),and Pb(Ⅱ)by dead biomasses of green alga Ulva lactuca and the development of a sustainable matrix for adsorp⁃tion implementation[J].Journal of Hazardous Materials,2012, 213:123-132.
[2]金科,李小明,杨麒,等.白腐真菌吸附废水中重金属离子的研究进展[J].工业用水与废水,2005,36(2):15-18.
[3]Tsekova K,Todorova D,Dencheva V,et al.Biosorption of cop⁃per(Ⅱ)and cadmium(Ⅱ)from aqueous solutions by free and im⁃mobilized biomass of Aspergillus niger[J].Bioresource Technolo⁃gy,2010,101(6):1727-1731.
[4]Brinza L,Nygard C A,Dring M J,et al.Cadmium tolerance and adsorption by the marine brown alga Fucus vesiculosus from the Irish Sea and the Bothnian Sea[J].Bioresource Technology,2009, 100(5):1727-1733.
[5]Prigion V,Zerlottin M,Refosco D,et al.Chromium removal from a real tanning effluent by autochthomous and allochthonous fungi [J].Bioresource Technology,2009,100(11):2770-2776.
[6]李慧芬,林雁冰,王娜娜,等.一株Zn抗性菌株的筛选鉴定及吸附条件优化[J].环境科学学报,2010,30(11):2189-2196.
[7]刘云国,周娜,樊霆,等.铜锌离子抗性菌筛选及重金属作用下富集特性研究[J].湖南大学学报,2009,36(2):80-84.
[8]刘恒,王建龙,文湘华.啤酒酵母吸附重金属离子铅的研究[J].环境科学研究,2002,15(2):26-29.
[9]姜烛,张宝善,胡海霞.霉菌吸附重金属的研究进展[J].微生物学报,2008,35(7):1129-1135.
[10]胡正,张利,童明容,等.龟裂链霉菌对废水中Pb2+的吸附作用[J].南开大学学报,2000,33(2):28-31.
[11]陈翠雪,李清彪,邓旭,等.黄孢展齿革菌菌丝球同时吸附铅镉离子的动力学[J].离子交换与吸附,2003,19(2):133-138.
[12]张玉秀,宋小庆,黄琳,等.煤矿区耐镉细菌的筛选鉴定和重金属耐性研究[J].煤炭学报,2011,35(10):1735-1741.
[13]孟庆娟,刘建平,戚秀云,等.啤酒酵母生物吸附剂的应用研究进展[J].东北农业大学学报,2008,39(10):122-126.
[14]Sud D,Mahajan G,Kaur M P.Agricultural waste material as po⁃tential adsorbent for sequestering heavy metal ions from aqueous solutions-A review[J].Bioresource Technology,2008,99(11): 6017-6027.
[15]Tan L F,Zhu D W,Zhou W B,et al.Preferring cellulose of Eich⁃hornia crassipes to prepare xanthogenate to other plant materials and its adsorption properties on copper[J].Bioresource Technology, 2008,99(10):4460-4466.
[16]Akar T,Tunali S.Biosorption characteristics of Aspergillus flavus biomass for removal of Pb(II)and Cu(II)ions from an aqueous so⁃lution[J].Bioresource Technology,2006,97(15):1780-1787.
[17]Chergui A,Bakhti M Z,Chahboub A,et al.Simultaneous biosorp⁃tion of Cu2+,Zn2+and Cr6+from aqueous solution by Streptomyces rimosus biomass[J].Desalination,2007,206(1-3):179-184.
Adsoption of Pb2+in waste water by a fungal absorbent
QU Juanjuan1,PENG Hongyang1,GU Haidong1,JIN Yu1,LI Taijun2(1.School of Resources and Environmental Science, Northeast Agricultural University,Harbin 150030,China;2.Heilongjiang Beingmate Dairy Co.,Ltd., Anda Heilongjiang 151400,China)
This study is to investigate performance of mycelium waste absorbent from industrial fermentation on heavy metal ions adsorption in aqueous.The optimum condition of single factor experiments was determined at temperature of 30℃,pH 5.0,the initial Pb2+concentration of 50 mg·L-1,absorbent dosage of 2 g·L-1,rotation speed of 160 r·min-1,adsorption time of 30 min,and absorption rate was 91.5%. Analysis of variance revealed that absorbent dosage initial Pb2+concentration and pH significantly affected the adsorption.Under absorption condition optimized by orthogonal experiment of 2 g·L-1absorbent dosage pH 4.5,40 mg·L-1initial Pb2+concentration,adsorption rate increased 2.7%.Physical adsorption occurred easily on the loose and porous surface of mycelium,active groups,such as amino,carboxyl,phosphate and hydroxyl group participated absorption by complexation with Pb2+.This study identified that mycelium waste could be used as adsorbent to remove Pb2+from waste water.
mycelium waste;Pb2+;biosorption;single factor experiment;orthogonal experiment
TQ085.1
A
1005-9369(2014)07-0031-07
时间2014-7-4 17:29:29 [URL]http://www.cnki.net/kcms/detail/23.1391.S.20140707.0843.014.html
曲娟娟,彭泓杨,顾海东,等.一种真菌吸附剂对废水中Pb2+的吸附[J].东北农业大学学报,2014,45(7):31-37.
Qu Juanjuan,Peng Hongyang,Gu Haidong,et al.Adsoption of Pb2+in waste water by a fungal absorbent[J].Journal of Northeast Agricultural University,2014,45(7):31-37.(in Chinese with English abstract)
2013-10-16
黑龙江省科学基金资助项目(D201402);黑龙江省教育厅面上项目(12541043)
曲娟娟(1974-),女,教授,博士,研究方向为生物修复。E-mail:juanjuanqu@126.com

