交联QCS/PS阴离子交换膜的制备及表征
李晓楠, 封瑞江*, 王吉林, 封 辰, 邱 辉
(1.辽宁石油化工大学石油化工学院,辽宁抚顺113001;2.中国石油天然气股份有限公司河北秦皇岛销售分公司,河北秦皇岛066000;3.中国石油抚顺石化公司洗化厂,辽宁抚顺113001)
近几年,膜技术发展迅速,已应用于各种工业领域。因为离子交换膜具有独特的荷电性质,因此受到国内外的重视和研究[1]。离子交换膜的种类很多,其中阴离子交换膜的应用颇为广泛,例如:叶丽等[2]对阴离子交换膜的卤甲基化改性进行了研究,避免了有毒卤甲基化试剂的使用,同时消除了亚甲基的二次交联。而张守海等[3]则利用PES 为原材料进行氯甲基化、季铵化改性,制得不同离子交换容量的季铵化聚醚砜阴离子交换膜。目前这些改性后的阴离子交换膜的性能有很大程度的提高,但要使其达到商业化仍然还需要改进。因此,新型阴离子交换膜就成为目前刻不容缓的研制对象,同时也具有很大发展前景。
而在众多制膜原料中壳聚糖突显了很大的优势。壳聚糖具有成膜性好、来源丰富和原料廉价等特点,已应用在反渗透、离子交换及气体分离等领域[4]。姚冬梅等[5]就利用壳聚糖的特性来吸附水中的Cu2+和Ni2+。虽然其分离效果较好,但由于机械强度差、水溶性较差和脱膜难等问题,因此有必要对其进行改性[6]。目前关于壳聚糖的改性有很多报道,由于壳聚糖存在可反应的羟基和氨基,所以壳聚糖容易进行如酰基化、羧基化、醚化、N-烷基化、酯化、水解等改性[7]。改性后的壳聚糖衍生物种类繁多,其各有优势的应用在医药、生物、化工、环保等方面。其中季铵化壳聚糖(QCS)是壳聚糖衍生物的一种,季铵化壳聚糖既可在酸性条件下溶解,也可在碱性条件下溶解。它对羟自由基的抗氧化活性强于壳聚糖,抑菌性能也优于壳聚糖、席夫碱壳聚糖和N-取代壳聚糖[8]。同时季铵盐类抗菌剂价格低廉,杀菌速度快。改性后的季铵化壳聚糖具有良好的水溶性、稳定性、相比纯壳聚糖来说,提高了吸湿、保湿及抗菌性能[9]。
本文利用2,3-环氧丙基三甲基氯化铵对壳聚糖进行季铵化改性,在壳聚糖中引入位阻大、水合能力强的季铵盐基团,制备了季铵化壳聚糖(QCS)[10]。但许多报道研究显示QCS仍然具有溶胀性较大等缺点,因此本实验在季铵化改性后,加入了戊二醛为交联剂增强膜的韧性[11],同时加入了带有正电小球的聚苯乙烯微乳液,制备了一系列QCS/PS阴离子交换膜,研究了PS微球和交联剂的含量对膜的含水率、离子交换量等性能的影响。
1 实验部分
1.1 试剂与仪器
壳聚糖(CS),国药集团化学试剂有限公司;冰乙酸(CH3COOH)、异丙醇(C3H8O)、盐酸(HCl)、无水乙 醇(C2H6O)、酚 酞(C20H14O4)、氢氧化钠(NaOH),沈阳市东兴试剂厂;2,3-环氧丙基三甲基氯化铵(C6H14ClNO),山东东营国丰精细化学品有限公司;戊二醛(C5H8O2),沈阳新兴试剂厂;苯乙烯(C8H8),沈阳试剂一厂;十六烷基三甲基溴化铵(C16H33(CH3)3NBr),天津市科密欧化学试剂有限公司;过硫酸钾(K2S2O8),国药集团化学试剂有限公司。以上试剂均为分析纯。
Spectrum One(B)傅里叶变换红外光谱仪,美国Perkin-Elmer公司;FA(N)/JA(N)系列电子天平,上海民桥精密科学仪器有限公司;CMT6502微机控制电子拉力实验机,深圳新三思材料检测有限公司。
1.2 季铵化壳聚糖(QCS)的合成
季铵化壳聚糖的合成方法参照文献[12]。
1.3 聚苯乙烯微乳液的合成
将苯乙烯,无水乙醇和去离子水按照体积比1∶5∶10的配比依次加入容器中,再将占反应物总质量5%的十六烷基三甲基溴化铵加入到容器中,另外加入占反应物总质量0.25%的过硫酸钾(均分4次加入,每次间隔1.5h)。于80 ℃反应6h,待温度降低至室温,置于密闭的玻璃瓶中待用。
1.4 QCS/PS阴离子交换膜的制备
将一定质量的QCS 粉末溶于体积分数为2%的冰乙酸溶液中,室温下搅拌溶解后加入一定比例的PS乳液,室温下搅拌均匀,再加入一定量的交联剂戊二醛。将制得的膜溶液静置脱泡。采用流延法成膜,60 ℃下干燥48h后得到一系列交联度不同的QCS/PS阴离子交换膜,表示为QCS/PS(x),其中x 为PS加入的质量分数。
交联度的计算公式如下:
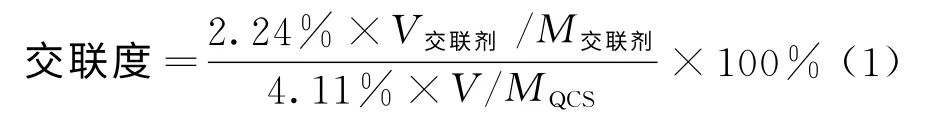
式中:V交联剂—交联剂水溶液的体积,mL;V—QCS醋酸水溶液的体积,mL;M交联剂—交联剂的相对分子质量;MQCS—QCS的平均相对分子质量。
1.5 红外光谱分析
本 实 验 采 用 美 国Perkin-Elmer 公 司 的Spectrum One(B)傅里叶变换红外光谱仪记录膜的红外光谱,样品采用KBr压片。
1.6 含水率的测定
膜的含水率是膜吸水达到饱和时吸水膜的质量与干膜质量的比值。
膜的含水率测定方法是将膜样品在室温条件下,浸泡在去离子水中48h,然后将膜取出,用滤纸将表面吸附的水擦干,迅速称重。将膜放入60℃烘箱干燥至质量不再变化,称其干重。
含水率的计算公式如下:
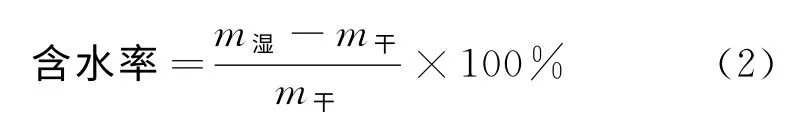
式中:m湿—湿膜质量,g;m干—干膜质量,g。
1.7 溶胀度的测定
取一定面积的干膜置于去离子水中使其溶胀,每隔一定的时间取出后,迅速用滤纸擦干表面的水珠后测量湿膜面积,待其面积不再变化时计算其溶胀度。实验平行测定3次,取平均值。
溶胀度计算公式如下:
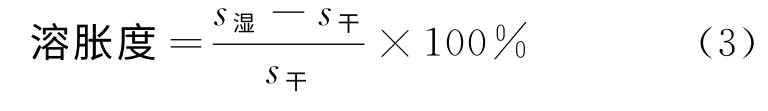
式中:s湿—湿膜的面积,cm2;s干—干膜的面积,cm2。
1.8 离子交换量的测定
离子交换容量是每克干膜或湿膜与外界溶液中相应离子进行等量交换的值。
将QCS/PS 阴离子交换膜放在烘箱中,在60℃下烘至质量恒定,称量干膜的质量。在室温条件下,将干膜浸泡在浓度为0.1mol/L的NaOH 溶液中48h将膜转化为OH 型。然后将膜取出用去离子水清洗干净。将OH 型膜浸泡在浓度为0.1 mol/L 的盐酸溶液中48h。以酚酞为指示剂,用NaOH 溶液对其进行返滴定,记下消耗NaOH 溶液的量,以等量去离子水作空白试验。
离子交换容量的计算公式如下:
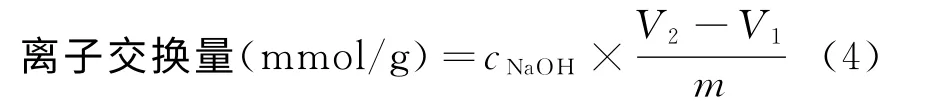
式中:cNaOH—滴定含膜溶液的NaOH 浓度,mol/L;V1—空白溶液消耗NaOH 溶液体积,mL;V2—滴定含膜的溶液时消耗NaOH 溶液体积,mL;m—干膜的质量,g。
1.9 机械强度的测定
实验采用CMT6502微机控制电子拉力实验机对制备的膜进行机械性能测定。在进行实验前,膜用模具切割成统一的形状,如图1所示。待测部分的长度是24mm,待测部分的宽度为4mm,膜的厚度用电子数显外径千分尺进行测量,膜断面面积为4mm2。实验条件:空气环境,拉伸速率为5 mm/min,测试膜在室温25 ℃条件下的断裂伸长率。膜的断裂伸长率由计算公式如下:


图1 测定膜机械性能的膜规格Fig.1 Measurement membrane and mechanical properties of membrane specifications
2 结果与讨论
2.1 CS、QCS和QCS/PS(x)红外光谱
图2是对比CS、QCS和QCS/PS(x)的红外光谱。
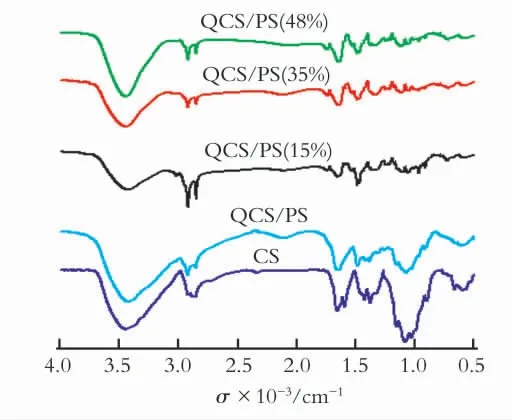
图2 CS、QCS、QCS/PS(x)的红外光谱Fig.2 FT-IR spectra of CS,QCS和QCS/PS(x)
由图2可知,在3 490cm-1处CS和QCS的特征峰基本相似,这是由O—H 和N—H 的伸缩振动产生的;CS曲线中在1 594cm-1处出现的吸收峰是由伯胺基中N—H 的弯曲振动产生的,在1 660 cm-1处出现的吸收峰是由酰胺基的C-O 伸缩振动产生的,而这两个吸收峰却在QCS曲线中消失,由此说明壳聚糖骨架上的氨基团被其他官能团取代[13]。QCS曲 线 中 出 现 在2 920、2 850、1 485 和728cm-1等处的吸收峰是由于季铵基团中C—H 键的弯曲振动产生的,这说明在该复合膜中存在季铵基团。综上分析可证明季铵基团已经被接枝在壳聚糖的骨架上。而不同PS微球含量的3条曲线中并没有看到明显的苯环特征峰,这可能是因为PS微球被十六烷基三甲基溴化铵包围在里面的关系。唯一能证明QCS/PS 膜结构中存在苯环的应该就是曲线在3 025、1 600、1 493cm-1处出现的由芳环骨架伸缩振动产生的吸收峰了,这属于聚苯乙烯的结构特征。而不同PS微球含量的曲线特征峰明显程度也有所不同,这可能是因为掺杂PS 微球的比例较小所致的。结果表明,聚苯乙烯微乳液小球已和季铵化壳聚糖融合一起成膜。
2.2 含水率和离子交换量与交联剂含量的关系
图3显示不同交联剂含量QCS膜的含水率和离子交换量的变化关系。
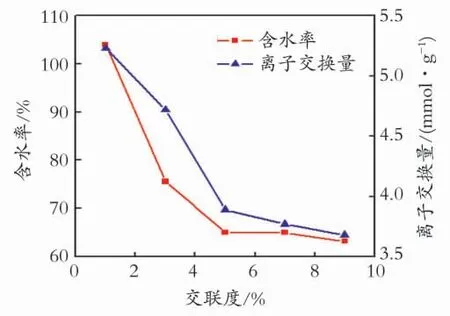
图3 不同交联剂含量QCS膜的含水率和离子交换量Fig.3 The water content and ion-exchange capacity of QCS membrances in different degree of crosslinking
如图3 所示,在QCS/PS 阴离子交换膜中PS微球的质量分数均为35%条件下,QCS/PS阴离子交换膜含水率随着交联度的增加而降低,主要原因是交联剂的加入,与壳聚糖发生了交联反应,在壳聚糖分子间形成了致密的网状结构,从而增强了分子间的作用力,降低了其含水率,当交联度为5%之后,含水率趋于平缓,综上所述,交联度为5%较适宜;QCS/PS阴离子交换膜的离子交换量随着交联度的增加而减小,这是因为交联反应在壳聚糖分子间形成的紧密结构抑制了离子的移动,因此在含水率降低的同时,离子交换量也随之降低,而在交联度为5%之后,离子交换量有平缓的趋势,可见在交联度为5%时较适宜。
2.3 含水率和离子交换量与PS微球含量的关系
图4显示不同PS微球含量QCS膜的含水率和离子交换量的变化关系。
如图4所示,所用QCS/PS阴离子交换膜的交联度均为5%,QCS/PS 阴离子交换膜的含水率随着PS微球含量的增加而降低,并在PS微球质量分数为35%之后趋于平稳,这是因为PS是疏水性的物质,所以在季胺化壳聚糖中加入聚苯乙烯微乳液后,膜的自由体积下降,使阴离子膜结构更致密,从而抑制了膜溶胀度和含水量的增加,因此PS 微球质量分数为35%时较适宜。
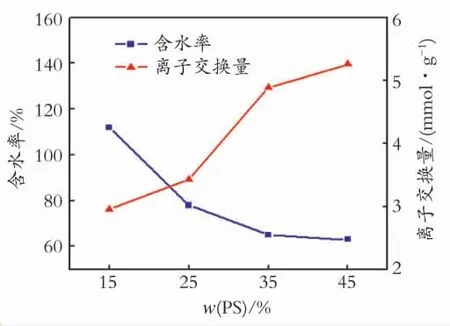
图4 不同PS微球含量QCS膜的含水率和离子交换量Fig.4 The water content and ion-exchange capacity of QCS membranes in different microspheres content of PS
如图4所示,所用QCS/PS阴离子交换膜的交联度均为5%,随着PS微球含量的增加,离子交换量由2.96mmol/g增加到5.26mmol/g。当PS微球质量分数为35%以后,离子交换量曲线出现平缓的趋势,这是因为在合成聚苯乙烯微乳液的过程中,以十六烷基三甲基溴化铵作为带有高正电荷的阳离子醚化剂,苯乙烯单体在引发剂过硫酸钾的引发下聚合形成PS聚合物微球,而十六烷基三甲基溴化铵分子被包夹在PS微球间,导致PS微球的表面是呈荷正电的,随着加入PS微乳液的量的增加,能够交换阴离子的正电荷微球也增加,正电荷的增加成为离子移动的前提,因此离子交换量的值也随之增加。
2.4 溶胀度
图5显示不同交联度和PS微球含量与QCS膜的溶胀度变化关系。
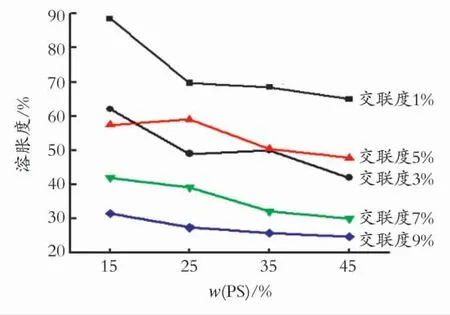
图5 不同交联度和PS微球含量QCS膜的溶胀度Fig.5 The swelling ratio of QCS membrances in different degree of crosslinking and in different microspheres content of PS
如图5所示,QCS/PS阴离子交换膜的溶胀度随着PS微球的含量的增加和交联度的增加而降低,这是因为加入聚苯乙烯微乳液后,膜的自由体积下降,使阴离子膜结构更致密,从而抑制了膜溶胀度的增加,同时交联剂的加入,与壳聚糖发生了交联反应,在壳聚糖分子间形成了致密的网状结构,从而增强了分子间的作用力。体系溶胀时需要克服交联网络内部的弹性自由能,因此降低了溶胀度,可有效抑制QCS膜的形变。而当交联度为5%,PS 微球质量分数为25%时,溶胀性并没有降低反而略有增高,这可能是因为QCS/PS阴离子交换膜在水溶液中长时间浸泡时,导致PS微粒从膜上脱落,降低了PS微球的作用,从而溶胀性略有升高。溶胀度的降低显示就是增长了膜本身的寿命,可见聚苯乙烯微乳液和交联剂对膜的性质有很大的影响。
2.5 QCS/PS阴离子交换膜的力学性能
图6 显示QCS/PS 阴离子交换膜伸长率与交联剂用量的变化关系。
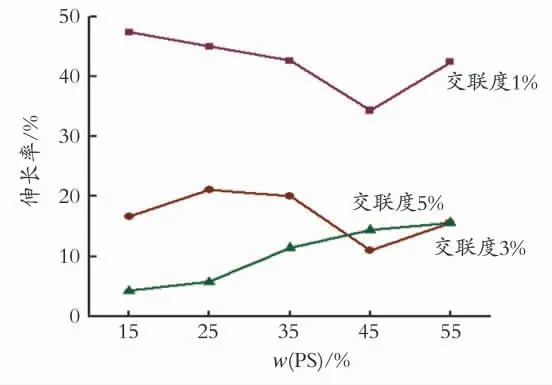
图6 QCS/PS阴离子交换膜伸长率与交联剂用量的关系Fig.6 The relationship of QCS/PS anion exchange membrane elongation at break and crosslinking agent
如图6所示,在交联度为1%时,断裂伸长率随着PS微球含量的增加而减小,又在PS微球质量分数为45%后升高,这可能是因为在交联度较小时,QCS/PS阴离子交换膜的内部结构很疏松,没有很好的包夹PS微球,导致硬单体聚苯乙烯流失,从而降低了其伸长率,但聚苯乙烯作为硬单体,必然会随着PS微球含量持续增加而增强伸长率[14]。在交联度为3%,PS微球质量分数小于35%时,伸长率是随着PS微球含量的增加而增大的,却在PS微球质量分数为45%处急剧降低后又升高,这同样是因为QCS/PS膜没有很好的包夹PS微球所致。而在交联度为5%时,断裂伸长率随着PS微球含量的增加而增加,由此聚苯乙烯微球作为硬单体的作用就体现的很明显了。因此需要根据实际的应用来选择PS微球的加入量。
如图6所示,随着交联度的增加会使膜变脆,伸长率呈下降趋势,力学性能降低[15]。这是因为加入交联剂后,壳聚糖膜与交联剂发生交联反应,交联剂将线形大分子连接成网状体形大分子,新增的交联点对增强膜的韧性起着重要的作用。同时交联点的产生也使伸长率降低[16]。而在交联度为5%,PS微球量分数为45%时,伸长率略有升高的趋势,这可能是因为交联剂的加入部分程度上破坏了季铵化壳聚糖分子的规整性,因此会有略微升高的现象。
[1] 徐铜文.离子交换膜的重大国家需求和创新研究[J].膜科学与技术,2008,28(5):1-10.
[2] 叶丽,管蓉,王妹姗,等.阴离子交换膜的卤甲基化改性研究进展[J].电池工业,2010,15(2):124-128.
[3] 张守海,王皤,邢东博,等.VRB用季铵化聚醚砜阴离子交换膜[J].电池,2010,40(3):137-139.
[4] 刘越,黄家兰.壳聚糖膜的制备及性能研究[J].武汉科技学院学报,2009,22(5):23-26.
[5] 姚冬梅,赵杉林,商丽燕,等.天然高分子吸附剂吸附水中的Cu2+和Ni2+[J].辽宁石油化工大学学报,2006,26(1):42-44.
[6] 何旭敏,丁马太,丁俊琪,等.壳聚糖的改性及改性壳聚糖膜的富氧性能[J].厦门大学学报:自然科学版,1995,34(1):56-70.
[7] 于娜娜,王笃政.壳聚糖改性最新研究进展[J].精细与专用化学品,2011,19(6):43-48.
[8] 张晓发,袁斌,高娟.壳聚糖季铵盐的研究进展[J].化学试剂,2009(3):1-3.
[9] 金海琴,董勤政,李小红,等.壳聚糖的季铵化改性及其应用[J].胶体与聚合物,2007,25(2):42-44.
[10] 张荣,龙柱.壳聚糖与环氧丙基三甲基氯化铵接枝物的制备及其应用[J].造纸化学品,2007,19(2):19-22.
[11] Bergera J,Reista M,Mayera J M,et al.Structure and interactions in covalently and ionically crosslinked chitosan hydrogels for biomedical applications[J].European Journal of Pharmaceutics and Biopharmaceutics,2004,57:19-34.
[12] 王蕊.有机-无机杂化阴离子交换膜的制备及应用[D].抚顺:辽宁石油化工大学,2011.
[13] 王蕊,封瑞江,王吉林,等.q—CS/TEOS复合膜的制备及吸附性能的研究[J].辽宁石油化工大学学报,2011,31(1):13-20.
[14] 强志斌,陈寅生,郭华文,等.壳聚糖膜的制备及膜性能[J].东华大学学报:自然科学版,2007,33(2):212-220.
[15] 凌敏,李茂政,廖有为.壳聚糖/壳聚糖季铵盐交联共混阴离子交换膜的制备与性能研究[J].应用化工,2010,39(1):60-79.
[16] 刘维锦,别亚琴.湿相分离法壳聚糖膜的结构与性能研究[J].应用化工,2008,37(5):530-532.

