脑干肿瘤三维适形放疗的疗效和预后因素分析
骆华春 李东石 程惠华 林贵山 傅志超
脑干肿瘤(brainstem gliomas,BSG)在儿童肿瘤中,以每年20%的速度增长,且成为致死率最高的脑部肿瘤[1];在成人脑干肿瘤中,因为生物学特性的不同,恶性程度较儿童脑干肿瘤低[2]。但进展仍非常迅速,中位生存时间只有8~11个月[1]。由于脑干的特殊解剖部位和生理功能,手术通常难以切除。在治疗方法上缺乏前瞻性随机临床试验研究,因此对其治疗方式选择及预后因素存在争议。本研究回顾性分析17例BSG患者的临床资料,对其临床表现、治疗结果和预后影响因素进行探讨。
1 资料与方法
1.1 入组标准
经影像学检查确诊且临床资料完整;至少有2个以上典型脑干占位症状(脑神经损伤或者运动失调)。
1.2 一般资料
收集2002年12月~2006年9月我院收治的初诊BSG患者,共17例入组。其中男性11例,女性6例,年龄7~51岁,中位年龄25岁,其中6例年龄<20岁。根据脑干分期系统[3]:局限型10例,外生型0例,弥漫浸润型3例,颈髓型4例。患者初诊最常见临床表现为头晕,11例(65%)以头晕伴头痛就诊,4例(24%)以走路不稳就诊,2例(11%)以头晕伴呕吐就诊。患者健康状态评分采用美国东部肿瘤协作组(eastern cooperative oncology group,ECOG)体力状况评分(performance status,PS)法:0~1 分12例,2~3 分5例。国际预后指数(international prognosis index,IPI)评分:0~1 分13例,2分4例。
1.3 治疗方法
采用美国瓦里安公司600C直线加速器6Mv 的X线照射。依据CT或MRI影像检查结果确诊,并通过CT模拟定位机定位,勾画靶区,设GTV外放1 cm为CTV,应用TPS治疗计划系统进行布野、给量、优化并计算,最后通过DVH图进行受量分析,照射野3~4个,放疗剂量DT1.8~2.0 Gy/次,1次/天,5天/周,CTV总剂量DT36~60 Gy(中位剂量50.4 Gy)。治疗同时给予甘露醇注射液脱水,每次125 ml,每天1~2次。
1.4 观察指标
按2009年美国临床肿瘤学会(ASCO)和北美放射学会(RSNA)新修订的RECIST1.1评价标准[4,5]:完全缓解(complete response,CR)定义为所有目标病灶消失;部分缓解(partial response,PR)指基线病灶最大径之和至少减少30%;疾病进展(progressive disease,PD)指基线病灶最大径之和至少增加20%或出现新病灶;稳定(stable disease,SD)指基线病灶最大径之和有减少但未达PR或有增加但未达PD。总生存时间(overall survival,OS)为确诊日至死亡日,无进展生存时间(progression-free survival,PFS)为确诊日至出现疾病进展、复发或死亡时间。
1.5 统计学方法
应用SPSS13.0软件,对患者性别、年龄、体力状况评分、国际预后指数评分、肿瘤分型、初治症状、肿瘤部位、照射剂量及首次治疗后反应进行单因素预后分析,生存率采用Kaplan-Meier法计算,单因素分析采用Logrank法。因本研究的样本量太小,未进行Cox回归检验。
2 结果
2.1 生存分析结果
随访至2011年6月31日,随访时间为6.0~82.5个月,中位时间30.2个月。随访率为100.0%,17例患者治疗后总缓解率为82.0%(CR 35%+PR 47%),SD 18.0%,PD 0。1、3、5年生存率分别为76.4%、52.9%和41.2%。随访中发现4例出现局部复发,1例出现脊髓远处转移。
2.2 单因素分析结果
单因素分析结果显示:体力状况评分、国际预后指数评分、肿瘤分型、初治时症状、肿瘤部位和照射剂量与患者预后相关,患者性别、年龄及首次治疗后反应与患者预后无关,见表1。
2.3 不良反应
17例接受放疗患者中,3例出现1级消化道反应,2级2例;3例出现骨髓抑制,Ⅰ度2例,Ⅱ度1例;未出现3级以上不良反应。
3 讨论
脑干肿瘤的中位进展时间和生存时间分别为6、9个月[6,7]。而在一项研究中,在出现症状后未进行放射治疗的中位生存时间仅为4.5个月[8]。因此,如何提高无病生存率成为脑干肿瘤放射治疗的难点。放疗增敏剂的使用并不能提高生存时间[9],同时大量Ⅰ/Ⅱ临床试验证实辅助化疗或者同步放化疗对总生存率并无明显改善,如托泊替康、顺铂、依他硝唑或者卡铂[10~13]。本研究所有患者均进行单纯三维适形放射治疗,临床症状改善率100%,影像学疗效评价有效率为82.3%,无1例出现进展,且1、3、5年生存率分别为76.4%、52.9%、41.2%,明显高于其他文献报道的,可能与研究的病例数少及年龄分布有关(年龄≤20岁6例,占35.3%;年龄>20岁11例,占65.7%)。
关于脑干肿瘤的放疗靶区,根据放射肿瘤治疗学指南,放疗靶区只需要包括原发肿瘤及周围一定的边界。目前对于外扩的距离仍未有统一的认识。本组研究的射野包括原发灶及在病变周围外扩1 cm。研究的患者中在观察1、2年后出现射野内复发的例数分别为3例和1例,而PFS超过3年的患者在随访期间未出现复发,1、2年局部病灶控制率分别为82.3%、76.4%。表明这种靶区限定方式是可行的,且初步证实三维适形放射治疗对脑干肿瘤的远期疗效是值得期待的。尽管过去有大量关于肿瘤复发治疗的临床研究,包括提高放疗次数、联合化疗药物和提高放疗敏感度,但如何有效的再次进行积极治疗仍然是一个难题[14],本研究对复发患者仍进行2次放疗,在临床上能减轻相应的临床症状,因不在本研究范围内,另行讨论。
在剂量学研究方面,标准的肿瘤放疗剂量为54 Gy/30次/5w。由于对脑干肿瘤进行放疗的经验欠缺及为确保脑干在正常耐受剂量的范围内等原因,本组研究放疗剂量波动范围较大,为36~60 Gy。研究对象中12例剂量≥50 Gy,而12例患者未出现局部复发,4例局部复发的肿瘤剂量均<50 Gy。由于目前针对脑干肿瘤多主张以单纯放射治疗为主,结合本组病例情况认为50 Gy是可以接受的,因为在放疗不良反应中以轻度的消化道反应和Ⅰ、Ⅱ度骨髓抑制为主,未出现Ⅲ级以上不良反应。
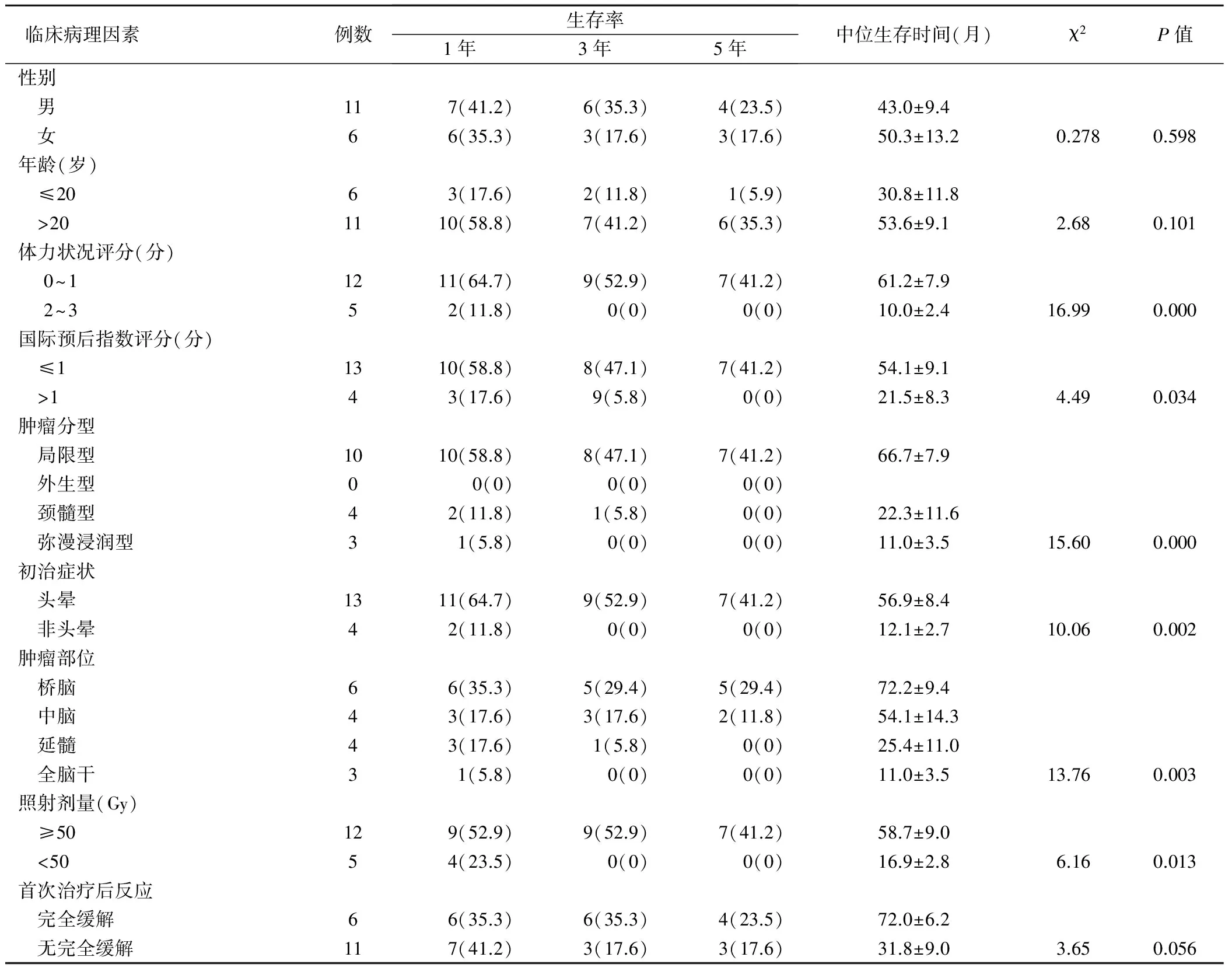
表1 脑干肿瘤各临床病理因素与患者预后的关系(例,%)
在关于影响预后因素方面,现有的研究多集中在儿童的脑干肿瘤方面[1],鲜有对脑干肿瘤的相关因素进行综合性的分析。本研究结果显示,在年龄、性别及首次治疗后反应进行单因素分析未发现对预后有影响。因为脑干肿瘤好发于未成年人,因此,将研究对象分为≤20岁和>20岁两组,虽然未得到阳性结果,这跟研究的病例数量少有关。体力状况评分、国际预后指数评分、肿瘤分型、初治症状、肿瘤部位和照射剂量认为是影响预后的密切因素。由于体力状况评分和国际预后指数评分直接取决于患者发病的直接症状及自身的相关因素。在肿瘤分型方面,本研究中有3例为弥漫浸润型患者,临床观察中这3例无1例生存到3年,提示弥漫浸润型预后不佳,表明预后与病理类型有相关性。初治症状和肿瘤部位与肿瘤侵犯的部位及程度有关,本研究的4例未出现头晕症状,而直接出现偏瘫的神经压迫症状,肿瘤侵犯范围广,而照射剂量是决定预后的直接因素。
综上所述,本研究显示,针对脑干肿瘤应用单纯三维适形放射治疗可以取得较好的临床疗效。放疗剂量≥50 Gy是可行的。肿瘤侵犯部位越小、体力状况较好、预后指数较高及初始未出现头晕症状的患者预后更好。
[1] Hargrave D,Bartels U,Bouffet E.Diffuse brainstem glioma inchildren:critical review of clinical trials〔J〕.Lancet Oncol,2006,7(3):241.
[2] Guillamo JS,Monjour A,Taillandier L,et al.Brainstem gliomas inadults:prognostic factors and classification〔J〕.Brain,2001,124:2528.
[3] 殷蔚伯,余子豪,徐国镇,等.肿瘤放射治疗学〔M〕.中国协和医科大学出版社,2008:1131~1132.
[4] Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumors:revised RECIST guideline(version 1.1)〔J〕.Eur J Cancer,2009,45(2):228.
[5] Schwartz LH,Bogaerts J,Ford R,et al.Evaluation of lymph nodes with RECIST 1.1〔J〕.Eur J Cancer,2009,45(2):261.
[6] Donaldson SS,Laningham F,Fisher PG.Advances toward an understanding of brainstem gliomas〔J〕.J Clin Oncol,2006,24:1266.
[7] Mandell LR,Kadota R,Freeman C,et al.There is no role for hyperfractionated radiotherapy in the management of children with newly diagnosed diffuse intrinsic brainstem tumors:Results of a Pediatric Oncology Group phase Ⅲ trial comparing conventional versus hyperfractionated radiotherapy〔J〕.Int J Radiat Oncol Biol Phys,1999,43:959.
[8] Langmoen IA,Lundar T,Storm-Mathisen I,et al.Management of pediatric pontine gliomas〔J〕.Childs Nerv Syst,1991,7:13.
[9] Hargrave D,Bartels U,Bouffet E.Diffuse brainstem glioma in children:critical review of clinical trials〔J〕.Lancet Oncol,2006,7(3):241.
[10] Bernier-Chastagner V,Grill J,Doz F,et al.Topotecan as a radiosensitizer in the treatment of children with malignant diffuse brainstem gliomas:results of a French Society of Paediatric Oncology Phase II Study〔J〕.Cancer,2005,104(12):2792.
[11] Marcus KJ,Dutton SC,Barnes P,et al.A phase I trial of etanidazole and hyperfractionated radiotherapy in children with diffuse brainstem glioma〔J〕.Int J Radiat Oncol Biol Phys,2003,55(5):1182.
[12] Freeman CR,Kepner J,Kun LE,et al.A detrimental effect of a combined chemotherapy-radiotherapy approach in children with diffuse intrinsic brain stem gliomas? 〔J〕.Int J Radiat Oncol Biol Phys,2000,47(3):561.
[13] Doz F,Neuenschwander S,Bouffet E,et al.Carboplatin before and during radiation therapy for the treatment of malignant brain stem tumours:a study by the Socie′te′ Franc?aise d'Oncologie Pe′diatrique〔J〕.Eur J Cancer,2002,38(6):815.
[14] Geert O R J Janssens,Corrie E M Gidding,Erik J Van lindert.The role of hypofracttionation radiotherapy for diffuse intrinsic〔J〕.Int J Radiation Oncology Biol Phys,2009,73(3):722.

