肾康注射液对单侧输尿管梗阻大鼠肾间质纤维化的影响
田晓 孟晓华 董科 冯晓明 徐潺 王玉浔 史国辉
(唐山河北联合大学附属医院肾内科,063000)
肾间质纤维化是各种肾脏疾病进入终末期的共同病理损害,采取各种措施阻止肾间质纤维化的发生是临床防治肾小管间质病变、保护肾功能的重要目标之一。以往对多种中药单味药或复方制剂的研究均显示中药可能在不同的慢性肾脏病治疗中具有改善肾功能、减轻肾间质纤维化的功效。本研究目的在于对于肾康注射液的抗肾脏纤维化作用的探讨。
1 材料与方法
1.1 药品 缬沙坦胶囊由诺华制药公司提供,肾康注射液由西安世纪盛康药业有限公司提供。本研究中选用的药物剂量均为以往相关研究已证实的有效剂量[1-2]。
1.2 主要试剂 第一抗体包括兔抗人转化生长因子-β1、小鼠抗人α-平滑肌肌动蛋白。第二抗体为生物素标记的山羊抗兔lgG(ZB 2010)及马抗小鼠lgG(ZB 2020),均购自北京中杉金桥生物技术有限公司。第三抗体为辣根过氧化物酶耦联琏卵白素(福州迈新生物有限公司)。显色底物为DAB(福州迈新生物有限公司)。
1.3 动物模型制备与标本收集 雄性SD大鼠36只(SPF级,河北联合大学实验动物中心提供),体质量(270±10)g,随机分为3组(每组12只),肾康组:术前1 d及术后给予肾康注射液,20 mL/支,每支内含原生药6 g,按10 g/(kg·d),腹腔注射每天一次(08:00—09:00);缬沙坦组:缬沙坦混悬液30 mg/(kg·d),每天一次(08:00—09:00)1 mL灌胃;模型组(UUO组):每天同体积的生理盐水灌胃。
UUO模型的制备参照文献[2]方法。各药物治疗组均于术前1 d开始用相应药物等量灌胃,UUO组以等量自来水灌胃。术后第14天处死各组大鼠12只,心脏取血制备血清,-80℃冰箱保存待测肾功能指标,梗阻侧经肾门正切的肾组织用10%中性甲醛溶液固定、常规方法制备切片。
1.4 病理学观察 病理学观察肾组织切片行HE染色、免疫组织化学染色,单盲法于光镜下观察HE染色切片皮质肾间质炎细胞浸润、肾小管扩张、萎缩和纤维化等病理改变。
1.5 肾功能测定 肾功能测定采用自动生化分析仪(BECKMANCOUL TERL×20)测定血清肌酐(Scr)和尿素氮(BUN)及电解质。
2 结果
2.1 大鼠生化指标的变化(表1) 由表1可知第14天时3组大鼠的肾功能及电解质均有升高,但模型组(UUO)升高更明显,两个用药组(肾康、缬沙坦)虽有升高,但更接近正常值,模型组与两个用药组(肾康、缬沙坦)肾功能和电解质之间有明显变化,差异有统计学意义(P<0.05),两个用药组(肾康、缬沙坦)肾功能和电解质之间没有明显变化,差异无统计学意义(P>0.05),所有指标中以BUN、Scr、P3+变化最为明显。
2.2 肾脏病理改变 光镜下可见(HE)。实验第14天,模型组肾间质炎细胞呈弥漫性浸润,局灶性加重,肾小管明显扩张,上皮肿胀,空泡变性,并出现间质纤维化;而肾康组及缬沙坦组的变化相仿,间质内炎细胞则呈小灶性浸润,少许上皮细胞肿胀,少部分肾小管轻度扩张,肾间质纤维化明显较模型组轻。
2.2.1 TGF-β1在肾间质的表达(表2) UUO组:TGF-β1在皮层间质细胞浆中表达增多,小管上皮细胞中也有表达,一直处于较高水平。两个治疗组:TGF-β1在皮层间质细胞中较UUO同期表达有所减少。半定量分析显示:两个治疗组肾小管间质中TGF-β1表达均低于同期UUO(P<0.05),肾康组与缬沙坦组在抑制UUO鼠肾小管TGF-β1表达的作用相似,两组差异无统计学意义(P>0.05)。
2.2.2 α-SMA在肾间质的表达 (表2) UUO组可见α-SMA在肾间质细胞中表达为主,部分肾小管上皮细胞中也有表达,维持较高水平。两个治疗组呈局灶性沉积,半定量分析显示:肾小管间质中α-SMA表达均低于同期UUO(P<0.05),肾康组与缬沙坦组在抑制UUO鼠肾小管α-SMA表达的作用相似,两组相比差异无统计学意义(P>0.05)。
表1 第14天3组大鼠肾功能、电解质指标比较(±s)
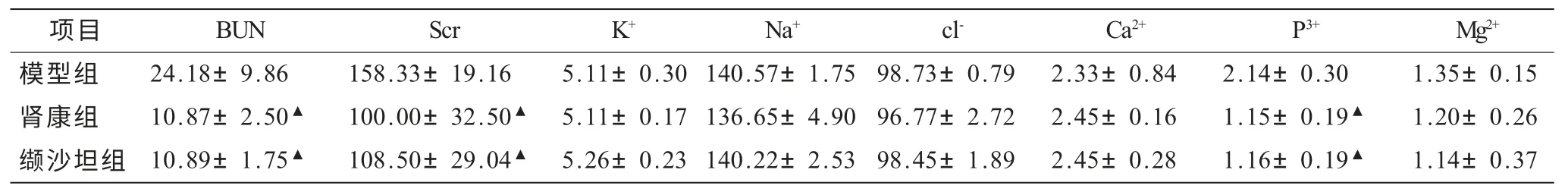
表1 第14天3组大鼠肾功能、电解质指标比较(±s)
注:与模型组比较,▲ P<0.05
项目 BUN Scr K+ Na+ cl- Ca2+ P3+ Mg2+ 模型组 24.18±9.86 158.33±19.16 5.11±0.30 140.57±1.75 98.73±0.79 2.33±0.84 2.14±0.30 1.35±0.15肾康组 10.87±2.50▲ 100.00±32.50▲ 5.11±0.17 136.65±4.90 96.77±2.72 2.45±0.16 1.15±0.19▲ 1.20±0.26缬沙坦组 10.89±1.75▲ 108.50±29.04▲ 5.26±0.23 140.22±2.53 98.45±1.89 2.45±0.28 1.16±0.19▲ 1.14±0.37
表2 第14天各组大鼠肾小管间质表达TGF-β1、α-SMA的比较(±s)
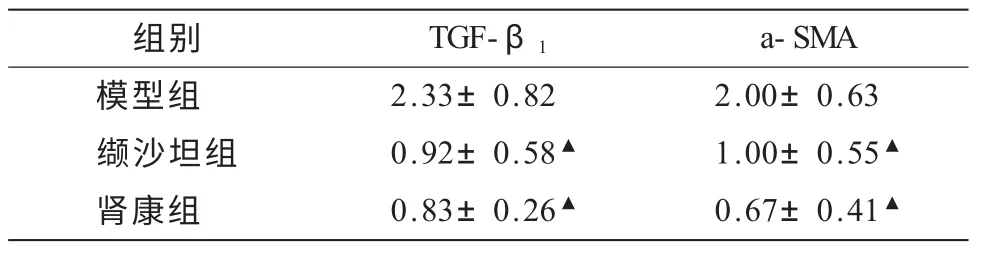
表2 第14天各组大鼠肾小管间质表达TGF-β1、α-SMA的比较(±s)
注:与模型组比较,▲ P<0.05
组别 TGF-β1 a-SMA模型组 2.33±0.82 2.00±0.63缬沙坦组 0.92±0.58▲ 1.00±0.55▲ 肾康组 0.83±0.26▲ 0.67±0.41▲
3 讨论
肾间质纤维化是所有慢性肾脏疾病进行性发展的共同通路,是导致慢性肾功能衰竭(CRF)的病理学基础,寻求其早期可逆因子或防治措施对肾脏疾病转归有重要意义[3]。在本研究中,我们分别观察了肾小管间质细胞转分化的标志物α-SMA表达、促纤维化因子TGF-β1表达在UUO所致肾间质纤维化中的变化,结果发现肾康注射液可以使肾小管和肾间质α-SMA表达减少,抑制肾小管上皮TGF-β1的表达。我们发现肾康注射液可以明显改善UUO模型鼠的肾功能,表现为用药后Scr和BUN水平较模型组明显降低。这些结果证实肾康注射液在肾脏疾病中确实具有抗纤维化作用。肾康注射液复方中药注射液,其主要成分为大黄、黄芪、丹参、红花。方中大黄为主药可通腑泄浊,具消除水肿,降低血肌、尿素氮,延缓肾小管间质纤维化的功效。大黄不仅能降低血液中尿素氮的水平,改善慢性肾衰竭病人的临床症状,还可使细胞外基质合成减少和降解增加,降低血压,增加毛细血管的通透性,以及减轻肾硬化,延缓慢性肾衰竭的发生发展[4-5]。黄芪主要含黄芪多糖、氨基酸、蛋白质和大量无机离子,具有扩张血管,降低血压,加强造血功能,增加肾血流量,调节机体免疫的功能。此外,黄芪可抑制TGF-β1的产生,延缓肾功能恶化,保护肾功能。大黄助胃降浊[6],黄芪助脾升清,脾胃升降有力,可使肾功能恶化延缓。张东亮等[7-9]在腺嘌呤致肾间质纤维化大鼠动物模型中发现,用复方丹参合剂,可下调TGF-β1的表达,抑制细胞外基质的生成,具有抗肾间质纤维化的作用。通过本实验可知肾康注射液能抑制单侧输尿管结扎大鼠肾间质中TGF-β1和α-SMA的过度表达,发挥肾脏保护作用[10-12]。综上所述,肾康注射液可作用于肾间质纤维化的早期,可以通过抑制TGF-β1的活性,减少α-SMA的表达,从而达到其对肾间质纤维化的抑制作用。由于肾康注射液具有疗效佳、副作用小等特点,因而对于延缓慢性肾脏疾病向终末期肾功能衰竭发展有一定的临床指导意义,是一种很有前景的药物,值得继续深入研究。
[1]王海燕,李惊子,潘辑圣,等.中药黄芪当归合剂对肾病综合征肾损伤的保护作用及对代谢紊乱的影响[J].北京大学学报:医学版,2002,34(5):542-552.
[2]Diamond JR,Levinson M,Kreisberg R,et al.Increased expreesion of TGF-β1mRNA in the obstructed kidney of rats with unilateral ureteral ligation[J].Kidney Int,1997,51(4):1133-1139.
[3]崔俊起,韩平杰.肾康注射液对早期糖尿病肾病的治疗观察[J].中国误诊学杂志,2008,8(9):2996-2097.
[4]张志英,董利平,杨海燕.丹红注射液对糖尿病患者血液流变学的影响[J].时珍国医国药,2007,18(9):2272-2273.
[5]吕莉,李欣燕,韩国柱,等.重组水蛭素体内抗凝活性的实验研究[J].中草药,2002,33(6):520-522.
[6]柯凌.大黄的药理及其在肾脏病中的运用[J].中国中西医结合肾病杂志,2001,2(6):347-348.
[7]张东亮,王质刚.复方丹参合剂对肾间质纤维化影响的实验研究[J].中华实用中西医杂志,2004,4(7):509-511.
[8]水华,徐联芳,陈德基.缬沙坦对单侧输尿管梗阻大鼠肾脏的保护作用[J].武汉大学学报:医学版,2004,25(6):708-710.
[9]孙世澜,周朝阳.肾脏病理论与实践[M].北京:人民军医出版社,2005:4.
[10]王玉,李晓政.α-肌动蛋白在肾系膜细胞重塑过程中的变化及其意义[J].国外医学:泌尿系统分册,1997(4):172-175.
[11]Lijnen HR.Pleiotropic functions of plasminogen activator inhibitor-1[J].J Thromb Haemost,2005,3(1):35-45.
[12]Muller GA,Zeisberg M,Strutz F,et al.The importance of tubulointerstitial damage in progressive renal disease[J].Nephrol Dial Transplant,2000,15(suppl 6):76-77.

