HPLC法测定穿白痢康丸中穿心莲内酯和脱水穿心莲内酯的含量
李毅竦,崔艳莉,杨武宁,孙舒放,覃雪斌,何 琼
(广西兽药监察所,南宁530001)
穿白痢康丸是《中华人民共和国兽药典》二○一○年版收载的新制剂,穿心莲是主药但质量标准无含量测定[1]。穿心莲药材中主要有效成分为穿心莲内酯、脱水穿心莲内酯,以叶子含量多,叶子中又以嫩叶多,中老叶有逐渐减少趋势[2];商品穿心莲药材在采收、晒干、包装、运输和贮存过程中叶片被大量丢失损耗,穿心莲内酯、脱水穿心莲内酯是欠稳定的化合物,药材久置后含量会降低,制剂生产受热的工艺中损失也较多[3]。为了能够测定穿心莲内酯、脱水穿心莲内酯的含量,保证制剂质量,实验采用高效液相色谱法对穿白痢康丸中穿心莲内酯、脱水穿心莲内酯含量测定方法进行了研究。
1 材料
1.1 仪器 岛津LC20型系列高效液相色谱仪(SPD-20A紫外检测器,LCSOLUTION色谱工作站,SIL-20A自动进样器、柱温箱);AG 245型电子天平;KQ-250 DB超声波仪。
1.2 供试药品与试剂 10批次穿白痢康丸(广西三家药厂提供),阴性对照样品(缺穿心莲的穿白痢康丸)按《中华人民共和国兽药典》2010年版收载的穿白痢康丸标准的处方(去穿心莲)和制法自制;供含量测定用穿心莲内酯对照品(批号110797-201108,含量98.7%)和脱水穿心莲内酯对照品(批号110854-201007,含量99.7%)由中国食品药品检定研究院提供;层析用中性氧化铝、流动相中甲醇为色谱纯、水为超纯水;其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:lnertsil®ODS-SP(250 mm ×4.6 mm ,5 μm)Column;流动相:甲醇 -水(52:48);检测波长为240 nm;流速1.0 mL/min;柱温30℃;进样量:10 μL。
2.2 供试品溶液的制备 取本品研细,取约1 g,精密称定,置具塞锥形瓶中,精密加入甲醇20 mL,密塞称定重量,冷浸30 min,超声处理(功率250 W频率40 KHZ)30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液10 mL,置中性氧化铝柱(200-300目,5 g,内径为1.5 cm)上,用甲醇15 mL洗脱,收集洗脱液,置25 mL量瓶中,加甲醇至刻度,摇匀,经微孔滤膜(0.45 μm)滤过,即得。
2.3 对照品与阴性溶液的制备 取穿心莲内酯对照品约15 mg,脱水穿心莲内酯对照品约10 mg,精密称定,置100 mL量瓶中,加甲醇溶解并稀释至刻度作为贮备液。精密吸取贮备液5 mL置25 mL量瓶中加甲醇稀释至刻度,摇匀,即得每1 mL含穿心莲内酯30 μg,脱水穿心莲内酯20 μg的对照品溶液。取自制阴性对照样品,按2.2“供试品溶液的制备”方法制成阴性对照溶液。
2.4 系统适用性试验 分别取上述对照品溶液、供试品溶液及阴性对照溶液各10 μL,注入液相色谱仪,记录色谱图(图1-图3),从供试品色谱图可以看出,在上述色谱条件下,理论塔板数按脱水穿心莲内酯峰计大于2000,在与对照品色谱相应的位置上,有相同保留时间(穿心莲内酯6.9 min;脱水穿心莲内酯16.9 min)的色谱峰,穿心莲内酯和脱水穿心莲内酯与相邻共存物之间的分离度分别为3.1和17.5(药典要求应大于1.5),阴性对照在穿心莲内酯和脱水穿心莲内酯相同保留时间处无干扰峰。

图1 穿心莲内酯、脱水穿心莲内酯对照品混合液HPLC色谱图
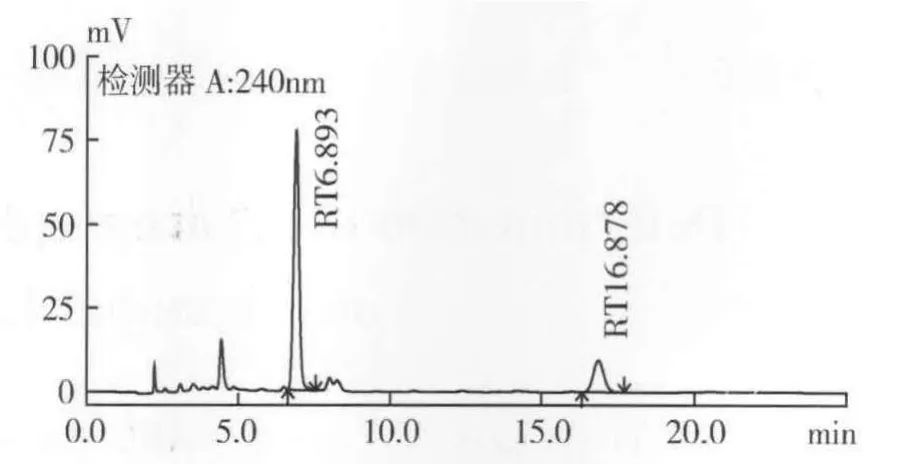
图2 穿白痢康丸样品HPLC色谱图

图3 穿白痢康丸阴性对照样品HPLC色谱图
2.5 线性范围考察 分别精密称取穿心莲内酯对照品15 mg,脱水穿心莲内酯对照品10 mg,置100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为对照品贮备液。分别精密吸取对照品贮备液1,5,10,15,20 mL,置 25 mL 量瓶中,用甲醇稀释至刻度,摇匀,吸取10 μL,注入高效液相色谱仪,以上述色谱条件测定峰面积。以对照品浓度作为横坐标(X),峰面积作为纵坐标(Y),得线性回归方程:穿心莲内酯 Y=37105X-19283,r=0.9996;脱水穿心莲内酯Y=31264X-16722,r=0.9999。结果表明,穿心莲内酯在0.06~1.2 μg、脱水穿心莲内酯在0.04~0.80 μg范围内具有良好的线性关系。
2.6 精密度试验 分别精密吸取同一份对照品溶液10 μL,重复进样6次,测定峰面积,穿心莲内酯、脱水穿心莲内酯RSD分别为0.46%和0.28%,表示仪器精密度良好,可以满足含量测定的要求。
2.7 稳定性与重复性试验 取同一批供试品(批号130101),按上述色谱条件分别在 0、1、2、4、8、24 h进样10μL,记录色谱图,测定峰面积,穿心莲内酯、脱水穿心莲内酯 RSD分别为0.83%和0.95%,表明供试品溶液在24 h内测定值基本稳定。另平行称取供试品6份,按照样品含量测定项下的方法测定,穿心莲内酯、脱水穿心莲内酯的含量RSD分别为0.88%和0.56%,表明重复性良好。
2.8 系统耐用性实验 对同一批供试品(批号:130101)分别用 Symmetry®C18(250 mm×4.6 mm,5 μm)、watersC18(250 mm × 4.6 mm,5 μm)、lnertsil®ODS-SP(250 mm × 4.6 mm,5 μm)的色谱柱,流动相甲醇-水(55∶45)、甲醇-水(52∶48),穿心莲内酯检测波长225 nm、脱水穿心莲内酯检测波长254 nm,240 nm波长同时测定穿心莲内酯和脱水穿心莲内酯等不同的因素试验,用相对平均偏差(计算公式:平均偏差除以平均值)比较上述条件的测定数值与标准规定方法测定数据,结果相对平均偏差为0.96%,表示受测定条件的小变动影响有限,能通过本系统适用性试验。
2.9 回收率试验 采用加样回收试验法,取同一批已知含量的穿白痢康丸(批号:130101)分别加一定量的穿心莲内酯、脱水穿心莲内酯对照品,按上述色谱条件测定,用公式:回收率%=C-A/B×100%(C:为加入对照品后的测得总量,A:样品中所含被测成分量,B:加入对照品量)计算回收率,结果见表1。

表1 回收率测定结果(n=9)
2.10 样品含量测定 取穿白痢康丸(10个批次)按2.2“供试品溶液的制备”的方法操作,分别精密吸取供试品溶液与上述的对照品溶液各10 μL,注入液相色谱仪,测定10批次样品穿心莲内酯、脱水穿心莲内酯中峰面积,按外标法计算其含量,结果见表2。
3 讨论与结论
蔡松涛等[4]认为在穿心莲内酯、脱水穿心莲内酯含量测定的前处理,超声提取优于热回流法,甲醇提取效率最高。通过对比实验认为,氧化铝5 g,柱子内径1.5 cm,净化10 mL的供试液,用15 mL甲醇洗脱,能达到既能吸附杂质,又能完全洗脱穿心莲内酯、脱水穿心莲内酯供检测。超声提取时间选用30 min能提取完全[5-7],因此,实验经过方法优选,采用妇科千金片甲醇超声提取法,以及穿心莲药材[8]的过柱净化方法。
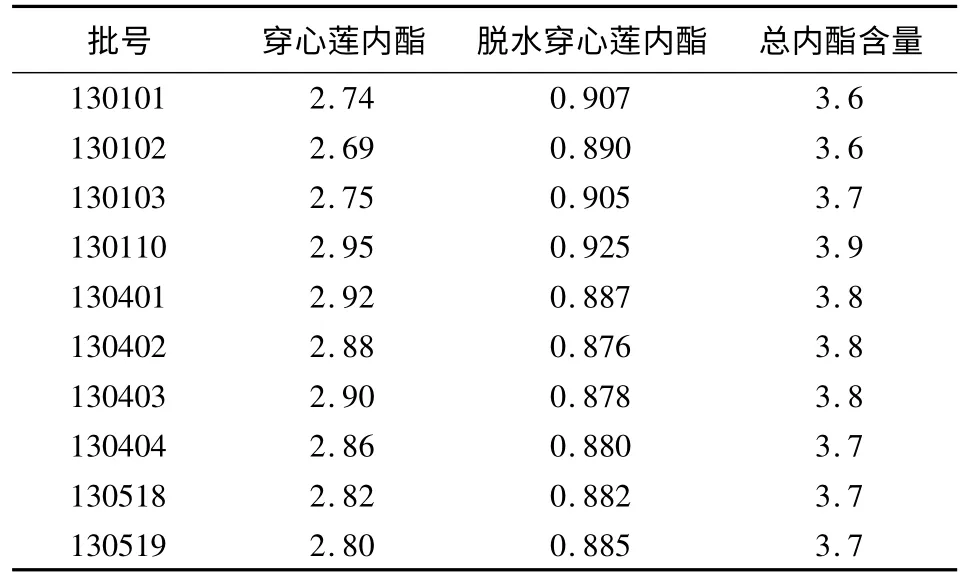
表2 10批次样品含量测定结果 (mg/g)
HPLC法测定复方制剂中的穿心莲内酯、脱水穿心莲内酯,文献多参照《中华人民共和国药典》二○一○年版的穿心莲药材测定穿心莲内酯、脱水穿心莲内酯含量的流动相(甲醇/水,52/48)和测定波长(穿心莲内酯 225 nm,脱水穿心莲内酯254 nm)[8],扫描有最大吸收[9-10],通过对比实验,本试验最终采用流动相为甲醇 -水(52/48),用240 nm波长同时测定穿心莲内酯、脱水穿心莲内酯的含量[8],取得了较好的效果。
本研究仿妇科千金片[8]以二者的总量作为质量标准的限量。供试品的穿心莲内酯含量为脱水穿心莲内酯3倍,与文献报道[11]相符。穿白痢康丸为水丸,在泛丸中不可避免的热处理,会导致穿心莲内酯损失和部分转化为脱水穿心莲内酯,二者含量变化是动态的,也是不可控的。因此,以穿心莲内酯与脱水穿心莲内酯的总量来控制产品质量较单控制其中一种成分更为科学、合理[11],10批样品的穿心莲内酯、脱水穿心莲内酯总量最高为3.9 mg/g,最低为 3.6 mg/g,平均为 3.7 mg/g。考虑到不同产地、不同采收季节的穿心莲药材中穿心莲内酯、脱水穿心莲内酯的含量差别较大[9],从穿心莲药材的采收到制剂成品生产链中穿心莲内酯、脱水穿心莲内酯的含量诸多不稳定的因素,参照中药口服复方制剂质量标准制订方法,拟定穿白痢康丸的穿心莲内酯、脱水穿心莲内酯总量限度为10批样品平均量的80%为标准的控制量,即每1 g含穿心莲以穿心莲内酯(C20H30O5)、脱水穿心莲内酯(C20H28O4)的总量计,不得少于3.0 mg。
[1]中国兽药典委员会.中华人民共和国兽药典二○一○年版二部[S].
[2]郑虎占.中药现代研究与应用[S].
[3]黄晓丹.穿心莲片生产过程中脱水穿心莲内酯的含量变化[J].中国中药杂志,2002,27(12):911-912.
[4]蔡松涛,陈向红,马 琳,等.影响穿心莲片中穿心莲内酯和脱水穿心莲内酯含量测定的因素[J].中成药,2005,27(3):361-362.
[5]李玮玲.HPLC测定穿王消炎片中脱水穿心莲内酯的含量[J].广东药学,2004,14(6):15-17.
[6]黄全勇,艾金钟,喻志林,等.穿黄消热胶囊质量标准研究[J].中国实验方剂学杂志,2011,17(9):110-112.
[7]赵宏荣,王立英.HPLC测定复方苦木消炎颗粒中脱水穿心莲内酯含量[J].中国执业药师,2010,7(11):36-38.
[8]国家药典委员会.中华人民共和国药典二○一○年版一部[S].
[9]苏 丹,祝 晨,刘中秋,等.RP-HPLC法测定不同产地穿心莲叶中穿心莲内酯、脱水穿心莲内酯含量的研究[J].Chinese Archives of Traditional Chinese Medicine,2002,20(7):36,56.
[10]狄永良.穿黄消炎胶囊的制备及质量标准研究[J].中国药业,2010,19(21):36-37.
[11]朱宁江,蒋云根,邵卫中,等.高效液相色谱法测定穿黄消炎片中穿心莲内酯和脱水穿心莲内酯的含量[J].中南药学,2007,5(4):337-339.

