吡罗昔康新制剂微乳的药效学研究
刘娜 杨保仲 王颖莉 葛曙光
吡罗昔康(piroxicam)为非甾体类抗炎药,具有镇痛、抗炎及解热作用,临床上主要用于缓解各种关节炎及软组织病变的疼痛和肿胀的对症治疗,通过抑制环氧合酶使组织局部前列腺素的合成减少,抑制白细胞的趋化性和溶酶体酶的释放而发挥药理作用,具有半衰期长(50 h)、剂量小、无蓄积作用等特点,但由于药物口服存在首过效应,易刺激胃肠道,长期服用易导致消化道出血、溃疡、肝功能异常、血小板减少等不良反应。经皮给药是其有效给药途径之一,它可以提高患部药物浓度,增强局部抗炎作用,避免对胃肠道的不良反应[1]。近年来对新型吡罗昔康透皮制剂的研究很多,如贴片、凝胶等。药物只有溶解后才能透过皮肤[2-4],但在普通外用制剂中,吡罗昔康溶解度较小,药物含量较低,透皮较差,影响药效发挥。
微乳是由水、油、表面活性剂和助表面活性剂按适当比例混合,自发形成的稳定制剂,且对难溶性药物的增溶作用明显,可明显提高药物含量,增大药物浓度梯度及膜的通透性,使其透皮扩散速率增加,药物吸收明显加快,减轻首过效应,提高生物利用度[5-6]。本研究制备吡罗昔康微乳并初步探讨其抗炎镇痛作用。
1 材料与方法
1.1 实验动物 昆明种小鼠(20±2)g,雄性Wistar大鼠(150±10)g,均由山西医科大学实验动物中心提供。
1.2 药品与试剂 丙二醇月桂酸酯Lauroglycol FCC、聚氧乙烯蓖麻油EL-35 Cremophor EL-35、辛酸葵酸聚乙二醇甘油酯Labrasol、二乙二醇单乙基醚Transcutol P(均购自南京都莱生物科技有限公司),吡罗昔康(金坛市前药制药原料厂,白色粉末,批号20120906),卡拉胶(天津市博迪化工有限公司),二甲苯、甲醛、无水乙醇(均为分析纯,天津市北辰方正试剂厂),醋酸(分析纯,天津市耀华化学试剂有限责任公司),双氯芬酸钠凝胶(武汉马应龙药业集团股份有限公司,H10950214,1%),吡罗昔康凝胶(湖北广济药业股份有限公司,国药准字H10960333,20 g:100 mg),脱毛膏(广州尚慧化妆品有限公司,SH/03/29,80 g)。
1.3 仪器 JA4003精密电子天平(上海良平仪器仪表有限公司),78-1型磁力加热搅拌器(江苏省金坛市荣华仪器制造有限公司),GZX-9076 MBE电热鼓风干燥箱(上海博迅实业有限公司医疗设备厂),微量移液器(上海求精生化试剂仪器有限公司),8 mm打孔器,千分尺(北京第二量具厂)。
1.4 方法
1.4.1 微乳的制备 采用油相Lauroglycol FCC,表面活性剂Labrasol、Cremophor EL,助表面活性剂Transcutol P,在室温下将上述处方成分按比例充分混合后,加吡罗昔康原料药,超声溶解,在搅拌条件下加入水,即得透明的吡罗昔康微乳。本实验制得的药物含量为0.4%[7]。
1.4.2 动物分组及给药 取昆明种小鼠72只,雌雄各半,随机平均分为六组,即空白对照组,阳性对照组,低、中、高剂量微乳组,吡罗昔康凝胶组。各组小鼠用推子和脱毛膏去毛,面积不小于1.5 cm×1.5 cm。在去毛处,吡罗昔康微乳低、中、高剂量组分别按1、2、4 mg/kg用移液器精确给药。吡罗昔康凝胶组涂抹0.5%的吡罗昔康凝胶0.008 g,阳性对照组涂抹1%的双氯芬酸钠凝胶0.02 g[8]。空白对照组则给予相当于中剂量组给药体积的生理盐水,2次/d,连续7 d。
热板法:控制热板温度为(55±0.5)℃,将小鼠逐只放在热板上,测定其正常痛反应(舔后足或抬后足并回头)时间,每只测两次,间隔5 min,以平均值在5~30 s内为合格。选出初试合格的雌性小鼠72只,随机平均分为以上六组,给药同上[6]。
取Wistar雄性大鼠60只,给药前用千分尺测量各大鼠右后肢的正常足上下径。微乳低、中、高剂量组分别按0.67、1.33、2.67 mg/kg给药。吡罗昔康凝胶组涂抹0.036 g,阳性对照组涂抹0.2 g[8]。分组及给药同上。
1.4.3 吡罗昔康微乳镇痛作用研究
1.4.3.1 小鼠痛阈值的测定(热板法) 给药7 d,末次给药后分别记录各组小鼠15、30、45、60、90 min时的痛反应时间,如小鼠在热板上60 s无反应计60 s。计算:痛阈提高百分率 =(b-a)/a×100%(b:用药后痛阈值;a:用药前痛阈值)[9]。
1.4.3.2 抑制醋酸致小鼠扭体反应实验 六组小鼠给药7 d,末次给药30 min后各只小鼠腹腔注射0.6%的醋酸0.2 ml。观察记录注射醋酸后15 min内小鼠扭体次数,计算:镇痛抑制率=(a-b)/a×100%(a:空白对照组扭体数;b:给药组扭体数)[10]。
1.4.4 吡罗昔康微乳抗炎作用研究
1.4.4.1 抑制二甲苯致小鼠耳廓肿胀实验 六组小鼠给药7 d,末次给药1 h后各只小鼠右耳涂20 μl二甲苯致炎,以左耳作对照。30 min后颈椎脱臼处死小鼠,沿耳廓基线剪下双耳,用直径8 mm的不锈钢圆冲沿耳缘相同部位冲下,电子天平称重,计算:肿胀度=右耳重-左耳重,肿胀抑制率=(a-b)/a×100%(a:空白对照组平均肿胀度;b:给药组平均肿胀度)[8]。
1.4.4.2 抑制卡拉胶致大鼠足跖肿胀实验 大鼠给药7 d,末次给药1 h后于各鼠右后足跖中部皮下注入1%的卡拉胶0.1 ml致炎,于致炎后30、60、90、120、240、360 min,分别用千分尺测定致炎侧足的上下径,计算:肿胀度=致炎后的足上下径 致炎前的足上下径。肿胀抑制率=(a-b)/a×100%(a:空白对照组平均肿胀度;b:给药组平均肿胀度)[8]。
1.5 统计学处理 使用SPSS 13.0统计软件进行分析,计量资料以(±s)表示,热板实验和卡拉胶致大鼠足跖肿胀实验的比较采用重复测量资料的方差分析,醋酸致小鼠扭体实验和二甲苯致小鼠耳肿胀实验进行单因素方差分析,各实验组间两两比较采用DUNNET法分析检验,P<0.05为差异有统计学意义。
2 结果
2.1 各组对小鼠痛阈的影响 与空白对照组相比,高、中、低剂量微乳组、凝胶组和阳性对照组于给药后均能提高小鼠痛阈值。中、低剂量微乳组与空白对照组比较,差异有统计学意义(P<0.01)。中剂量组与阳性对照组相比,差异无统计学意义(P>0.05);与吡罗昔康凝胶组相比,差异有统计学意义(P<0.05)。高剂量组对小鼠痛阈的提高在60 min时达最大,仅有41.97%。低剂量组在60 min内镇痛作用逐渐增强,且痛阈提高率在60 min时达到最大,可达136.06%以上。见表1。
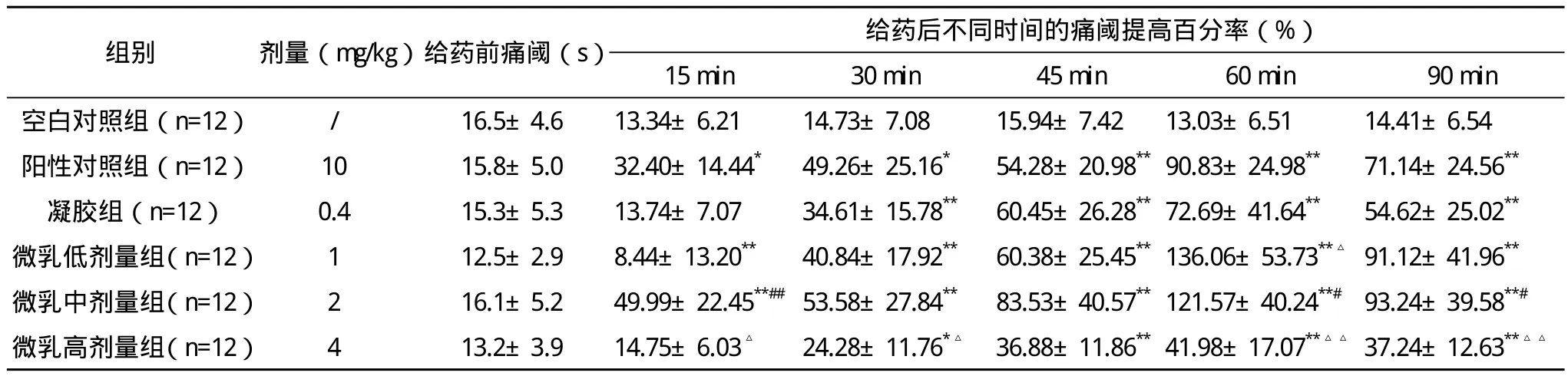
表1 对小鼠痛阈提高百分率的影响
2.2 各组对醋酸致小鼠扭体反应的影响 与空白对照组相比,局部外用不同剂量的吡罗昔康微乳、吡罗昔康凝胶及双氯芬酸钠凝胶均能抑制醋酸所致小鼠腹部疼痛,减少扭体次数,其中中、低剂量组更为明显,抑制率分别为75.7%、59.6%,比较差异有统计学意义(P<0.01)。与阳性对照组比较,中剂量组差异有统计学意义(P<0.05),高、低剂量组差异无统计学意义(P>0.05)。从剂型比较来看,微乳与凝胶相比,中剂量组差异有统计学意义(P<0.05)。见表2。
2.3 各组对二甲苯所致小鼠耳肿胀的影响 与空白对照组比较,微乳高剂量组抑制二甲苯所致小鼠耳肿胀作用不明显,比较差异无统计学意义(P>0.05);中、低剂量组有明显抑制作用,比较差异有统计学意义(P<0.05),抑制率分别为61.39%和60.25%。与阳性对照组比较,高剂量组差异有统计学意义(P<0.05),中、低剂量组差异无统计学意义(P>0.05),剂型比较差异亦无统计学意义(P>0.05)。见表3。
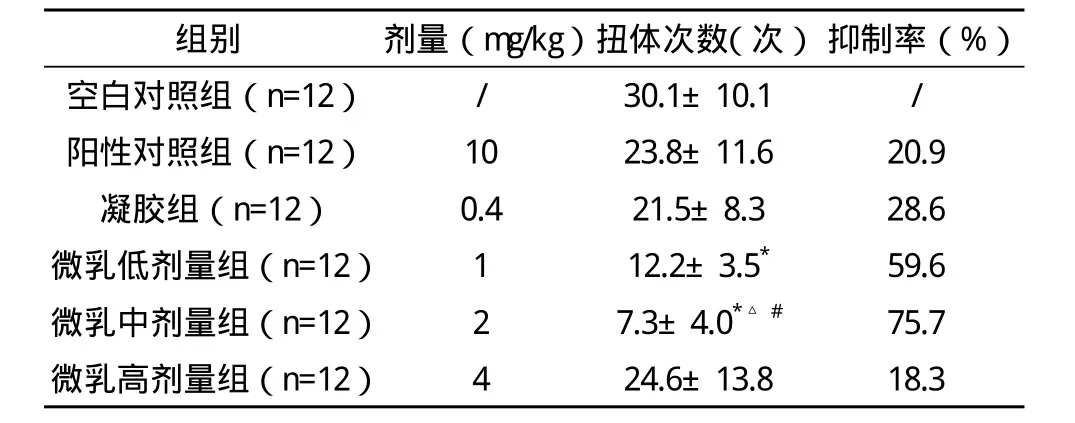
表2 各组小鼠扭体次数及抑制率比较
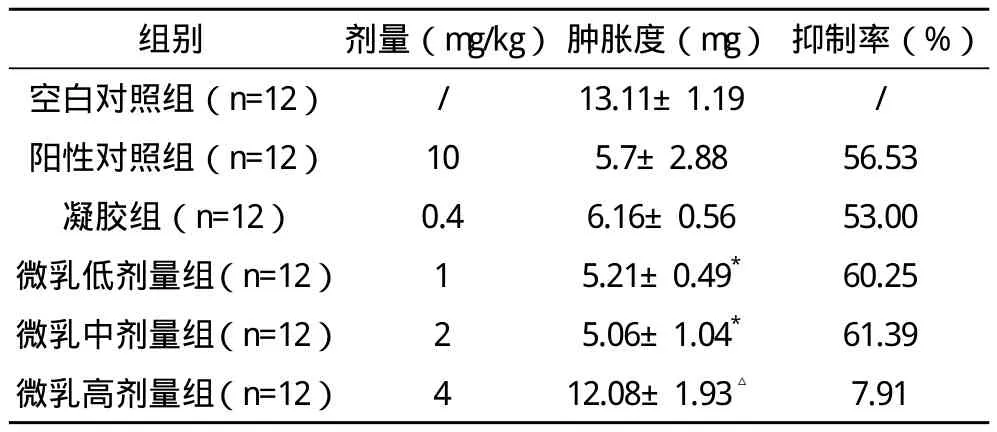
表3 各组小鼠耳廓肿胀度及抑制率比较
2.4 各组对卡拉胶致足跖肿胀的影响 与空白对照组相比,各微乳组均能显著抑制卡拉胶所致大鼠的足跖肿胀(P<0.01),与阳性对照组比较,高、中剂量组有显著差异(P<0.01),低剂量组无统计学差异(P>0.05),中剂量微乳组与凝胶组比较2 h后无统计学差异(P>0.05)。见表4。
2.5 给药后皮肤给药部位病理结果 实验结束后,取下空白组和中剂量微乳组皮肤制作切片。显微镜下观察:对照组皮肤结构完整(如图1中A图所示),被覆鳞状上皮完整无缺失,表皮层未见增厚,真皮内未见血管扩张充血、炎细胞浸润,毛囊、皮脂腺结构完整,无皮肤刺激性;微乳组皮肤经处理后(如B图所示),皮肤结构完整,角化层未见增厚,同A图对比,皮下视野所见基本相同,无皮肤刺激性。综上所示,在多次给药的皮肤刺激性实验中,微乳是安全的,对皮肤无刺激性。
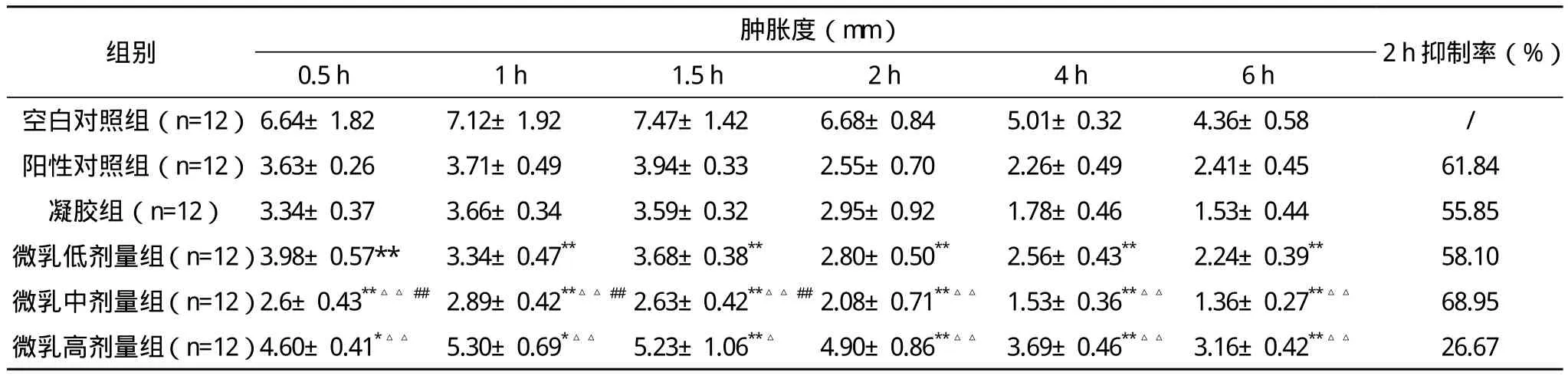
表4 各组对卡拉胶致足跖肿胀作用的影响
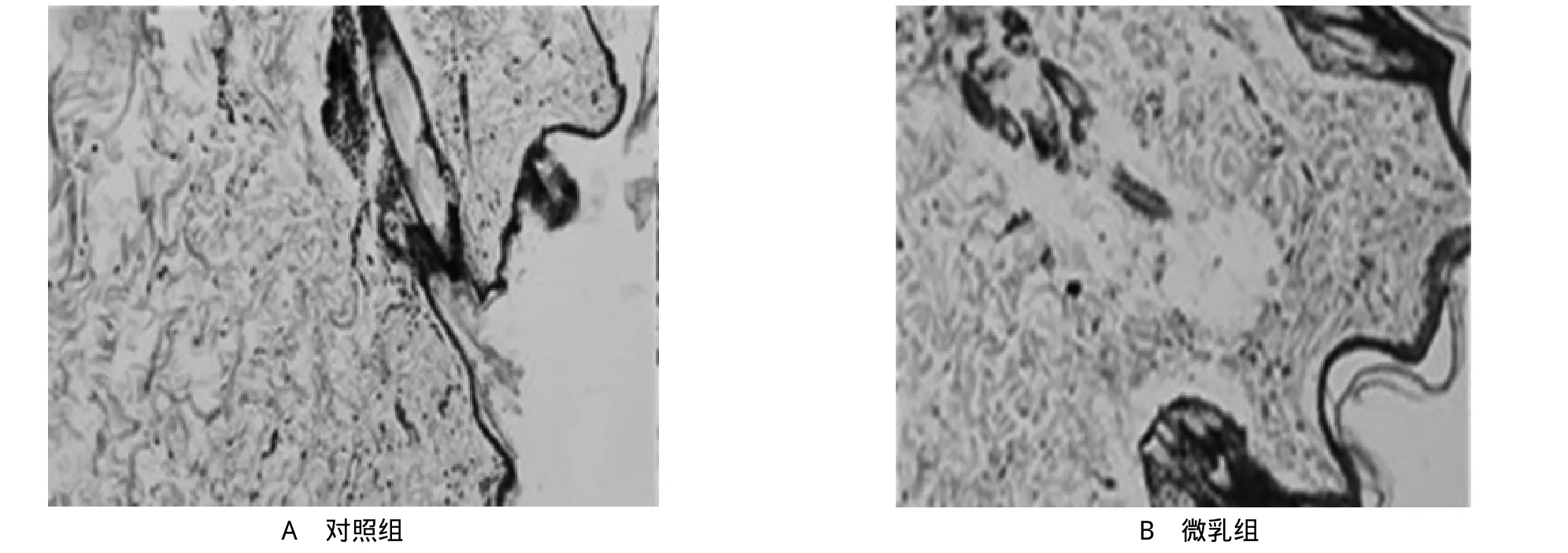
图1 多次给药皮肤刺激性实验病理切片图
3 讨论
动物脱毛后,要用棉签蘸取温生理盐水清洗皮肤并恢复1 d后再给药,防止脱毛膏对皮肤造成的损伤影响经皮渗透结果,给药后可见,微乳比凝胶经皮吸收迅速,为避免药物流失,要待其充分吸收后方能将动物放入侍养箱中,以免影响实验结果。
药效学实验结果表明:(1)抗炎实验结果表明,低、中、高剂量的吡罗昔康微乳都有不同程度的抗炎作用,以中、低剂量组的效果更为显著。(2)镇痛实验中,吡罗昔康各剂量组均能抑制醋酸所致小鼠腹部疼痛,减少扭体反应的发生。中、低剂量组可明显改善小鼠痛阈提高率,以中剂量组镇痛作用最为显著,且可延长小鼠的痛反应潜伏期,有效镇痛作用持久,可见其有与阳性对照药相近或更优的镇痛作用,并且优于市售的吡罗昔康凝胶。(3)吡罗昔康微乳具有促渗和缓释的双重作用,使药物能够快速、持续的发挥作用且连续使用对皮肤无刺激性。
由此可见,吡罗昔康新制剂微乳局部外用安全可靠,经皮吸收效果良好,有明显的抗炎镇痛作用,可提高生物利用度,减少不良反应的发生,作为一种新型制剂,为下一步开发及在临床方面的深入研究奠定了基础。
[1]杨其莲,卢静,张瑞雯,等.艾司氟比洛芬凝胶抗炎镇痛作用的药效学研究[J].中国新药与临床杂志,2006,25(4):266.
[2]Yuan Y, Li S M, Mo F K, et al. Investigation of microemulsion system for transdermal delivery of meloxicam[J]. Int J Pharm,2006,321(9):117.
[3]陈华兵,翁婷,常雪灵.布洛芬微乳的制备及其透皮吸收研究[J].中国药学杂志,2004,39(1):42.
[4]Rhee Y S, Choi J G, Chi S C, et al. Transdermal delivery of ketoprofen using microemulsions[J]. Int J Pharm,2001,228(1-2):161-170.
[5]Gupta S, Moulik S P. Biocompatible microemulsions and their prospective uses in drug delivery[J]. J Pharm Sci,2008,97(1):22-45.
[6]Kawakami K, Yoshikawa T, Moroto Y, et al. Microemulsion formulation for enhanced absorption of poorly soluble drugs.I.Prescription design[J].J controlled Release,2002,81(1-2):65-74.
[7]董平,吴娟,沙先谊,等.吡罗昔康外用微乳的制备及其透皮吸收的研究[J].药学实践杂志,2010,28(6):418-425.
[8]徐叔云,卞如濂,陈修.药理实验方法学[M].第3版.北京:人民卫生出版社,2002:882-891.
[9]杨其莲,卢静,张瑞雯,等.艾司氟比洛芬凝胶抗炎镇痛作用的药效学研究[J].中国新药与临床杂志,2006,25(4):266.
[10]Ribeirora, Valeml, Ferreirash, et al. Analgesic effect of thalidomideon inflammatory pain[J]. Eur J Pharma-col,2000,39l(1-2):97-103.

