参芎明胶微球含量测定方法的建立*
王曦 于书仪 刘旭红
中药丹参和川芎具有增强免疫作用[1],临床应用广泛。明胶微球是明胶的一种衍生物,作为药物载体[2],能够明显降低药物崩解速度,延长体内的存留时间,增加药物疗效[3]。制备微球的方法很多,有乳化-化学交联法,挥散有机溶剂法,照射聚合法,加热固化法等,本文采用明胶做基质,采取乳化-化学交联法制备参芎明胶微球[4]。
1 材料与仪器
1.1 材料 丹参素钠标准品(中国药品生物制品检定所);盐酸川芎嗪标准品(中国药品生物制品检定所,);
1.2 主要仪器 JUV757CRT型紫外可见分光光度计(上海精密科学仪器有限公司)
2 方法和结果
2.1 检测波长的选择 精密称取丹参素钠对照品、盐酸川芎嗪对照品各20.0 mg,用60%乙醇溶液溶解并稀释适当倍数,在200~500 nm波长范围内扫描,最大吸收波长分别为280 nm、290 nm。按照处方量制成的空白微球,用60%乙醇溶液稀释适当浓度,在200~500 nm扫描,实验表明在同等条件下空白辅料对丹参、川芎嗪的测定没有干扰,见图1、图2。
2.2 标准曲线的建立 精密称取丹参素钠对照品2.0 mg(相当于丹参素标准品1.4 mg),用蒸馏水定容至10 ml容量瓶中,浓度(以丹参素计)为1.4 mg/mL。然后分别稀释至浓度为0.70 mg/ml,0.0350 mg/mL,0.1750mg/ml,0.08750 mg/ml的标准溶液。以蒸馏水为空白,在280 nm处分别测定空白微球和参芎微球的吸光度。标准曲线为y=0.9965x+0.0195,r=0.9995,表明在8.750 μ g/ml~1.4 mg/mL线性关系良好。

图1 参芎明胶微球紫外扫描图谱
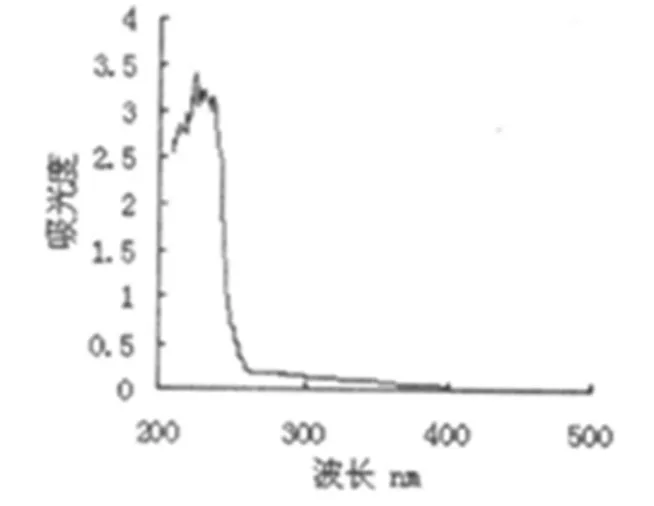
图2 空白明胶微球紫外扫描图谱
精密称取盐酸川芎嗪对照品20 mg,蒸馏水定容至20 ml容量瓶中,浓度为1 mg/ml,分别量取2 ml、4 ml、6 ml、8 ml、10 ml稀释定容至20 ml容量瓶中,制成不同浓度的标准溶液。以蒸馏水为空白,在290 nm处分别测定空白微球和参芎微球的吸光度。标准曲线为y=4.0732x-0.0436,r=0.9995,表明在0.1~0.5 mg/ml线性关系良好。按标准曲线方程计算微球的包封率。求得参芎明胶微球的包封率为51.20%。
2.3 重现性试验 精密称取丹参素钠对照品2.0 mg(相当于丹参素标准品1.4 mg),用纯化水定容至10 ml容量瓶中,浓度(以丹参素计)为1.4 mg/ml。然后分别稀释至浓度为 0.70 mg/ml,0.0350 mg/ml,0.1750mg/ml,0.08750 mg/ml的标准溶液。以蒸馏水为空白,在280 nm测定吸收度,重复测定5次,试验结果见表1。

表1 丹参总酚酸重现性测定结果
精密称取盐酸川芎嗪对照品20 mg,用纯化水定容至20 ml容量瓶中,浓度为1 mg/ml,分别量取2 ml、4 ml、6 ml、8 ml、10 ml稀释定容至20 ml容量瓶中,作为不同浓度的标准溶液。以蒸馏水为空白,在290 nm处测定盐酸川芎嗪的吸光度,重复测定5次,结果表明,该方法测定结果重现性良好。试验结果见表2。

表2 盐酸川芎嗪重现性测定结果
2.4 精密度试验 精确配制丹参素钠5种浓度的标准溶液,于1 d内分别测定5次,计算日内误差;同法每日测定1次连续测定5 d,计算日间误差,结果见表3、表4。丹参总酚酸日间精密度测定结果见表5。川芎嗪日间精密度测定结果见表6。
2.5 稳定性试验 取1.4 mg/ml的丹参素钠对照品溶液,分别于 0、2、4、6、8、12 h 测定吸收度,结果分别为 0.345、0.340、0.344、0.336、0.335、0.337,RSD为 1.33%。 取 1 mg/ml的盐酸川芎嗪对照品溶液,分别于0、2、4、6、8、12 h测定吸收度,结果分别为12.112、12.134、12.234、12.135、12.243、12.246,RSD为0.51%,结果表明,该方法测定结果稳定性良好。
2.6 回收率试验 分别准确称取126.6 mg的空白微球9份,和丹参素钠9份混合后置于烧杯中,加入40 ml蒸馏水,然后调节pH至3.5,分别加入0.2 g胃蛋白酶,将烧杯置于(37±1)℃的水溶液中先超声1 h,搅拌震荡3 h使微球完全水解。微孔滤膜过滤,,取续滤液定容至20 ml容量瓶中。
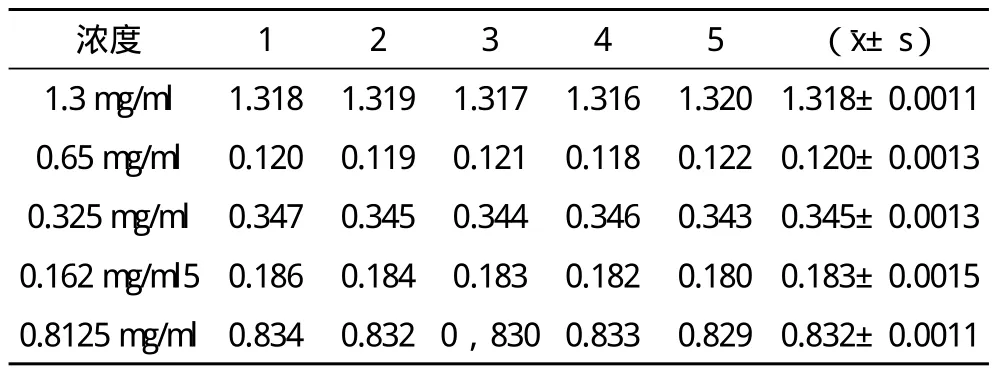
表3 丹参总酚酸日内精密度测定结果

表4 川芎嗪日内精密度测定结果
结果表明,该方法测定结果日内精密度良好。

表5 丹参总酚酸日间精密度测定结果
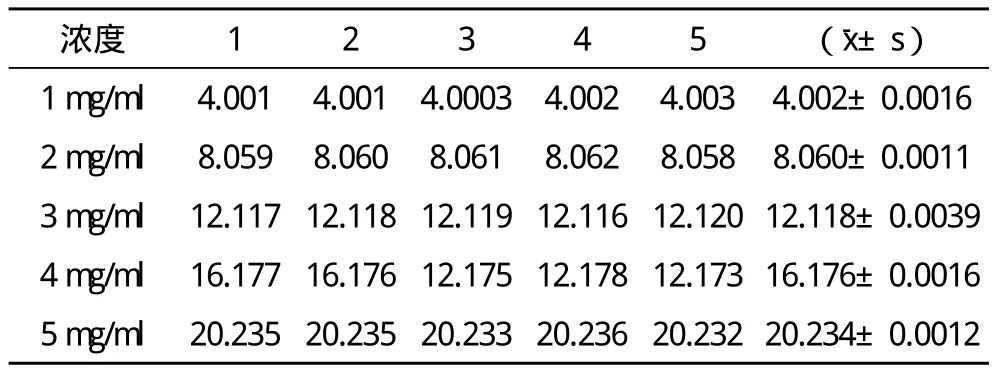
表6 川芎嗪日间精密度测定结果
结果表明,该方法测定结果日间精密度良好。在280 nm处测定吸收度,根据标准曲线方程计算,结果见表7。
分别准确称取126.6 mg的空白微球9份,和盐酸川芎嗪9份混合后置于烧杯中,加入40 ml蒸馏水,然后调节pH至3.5,再分别加入0.2 g胃蛋白酶,将烧杯置于(37±1)℃的水溶液中先超声1 h,搅拌震荡3 h使微球完全水解。微孔滤膜过滤,取续滤液定容至20 ml容量瓶中。在290 nm处测定吸收度,根据标准曲线方程计算,结果见表8。
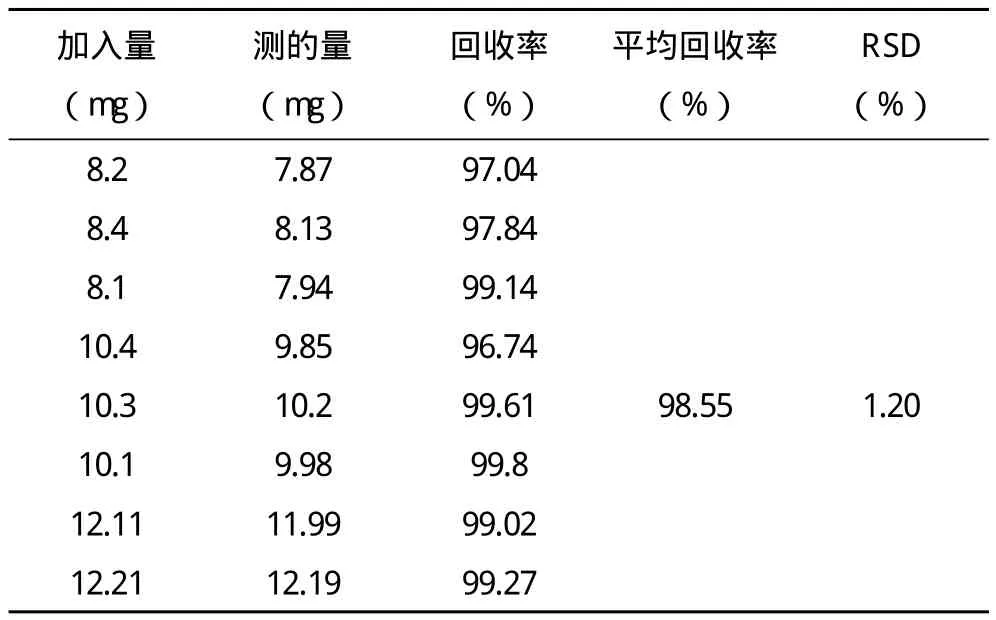
表7 丹参素钠回收率测定结果
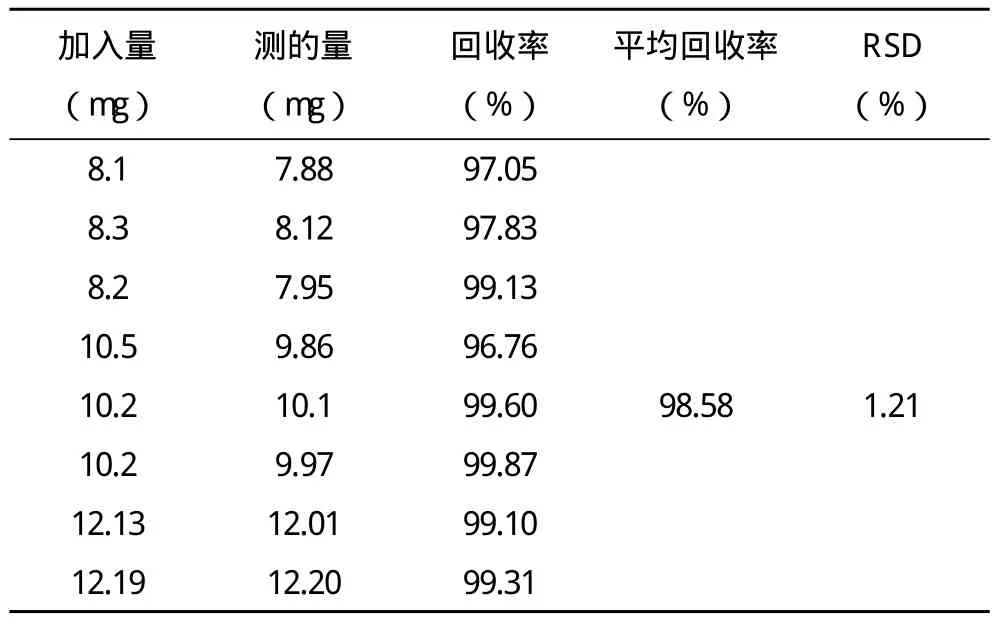
表8 盐酸川芎嗪回收率测定结果
丹参的平均回收率为98.55%,川芎平均回收率为98.58%,表明该方法回收率良好,辅料对丹参、川芎的含量测定不产生干扰。
2.7 含量测定方法 称参芎明胶微球126.6 mg,加入40 ml蒸馏水,再调节pH至3.5,各加入0.2 g胃蛋白酶,将烧杯置于(37±1)℃的水溶液中先超声1 h,再搅拌3 h使微球完全水解。微孔滤膜过滤,取续滤液定容至20 ml容量瓶中。以蒸馏水作为空白溶剂,分别在200~500 nm扫描参芎明胶微球的图谱测定吸收度,代入标准曲线,并计算微球的载药量和包封率。
3 结论
3.1 近年来,川芎临床应用研究广泛[5-6],本研究建立了紫外分光光度法,该方法精密度良好,重现性良好,样品在12h内性质稳定。
3.2 标准曲线为y=0.9965x+0.0195,r=0.9995,表明在8.750 μ g/ml~1.4mg/ml线性关系良好。盐酸川芎嗪检测波长为290 nm,标准曲线为y=4.0732x-0.0436,r=0.9995,表明在0.1~0.5 mg/ml线性关系良好,辅料对检测无干扰。
[1]于莲,张传美,李爱臣,董宇,张喆,等.参芎明胶微球的制备工艺研究[J]. 时珍国医国药,2010,21(3):667-668.
[2]Maria Angela Vandelli,Marcello Romagnoli,Aless-andra Monti,Manuela Gozzi, Paolo Guerra,Francesco Rivasi,Flavio Forni.Journal of Controlled Release 2004,96(1):67-84.
[3]余丽丽,范涛,杨黎燕,邓文婷,等.明胶微球载药及其体外释放性能研究[J]化工科技,2012,20(6):11-14.
[4]陆彬.药剂学[M].北京:中国医药科技出版社,2003:437.
[5]胡江平,罗方.参芎葡萄糖注射液治疗慢性肾小球肾炎的临床观察[J].中国医学创新,2012,9(16):14-15.
[6]王华杰,刘新铭,王瑾晔,等.天然高分子药物微球载体材料的研究进展[J].高分子通报,2006,19(8):1-9.

