重组人类促红细胞生成素防治早产儿贫血观察
李淑敏 谢子昂 杨英伟
早产儿贫血是儿科常见疾病,可引起频繁呼吸暂停,体重增加缓慢,代谢性酸中毒及反复感染等相关并发症,影响早产儿生存质量,因此早产儿贫血作为早产儿营养管理的常见问题,应引起重视。红细胞生成素水平及其对贫血反应低下是导致早产儿贫血的主要原因之一[1]。我们使用重组人类红细胞生成素(Rhu-EPO)防治早产儿贫血,取得较好疗效,报告如下。
1 资料与方法
1.1 一般资料 选取2009年3月至2011年3月在石家庄市第一医院儿科住院的早产儿贫血患儿46例,随机分为治疗组和对照组,每组23例。治疗组:胎龄28~36周,出生体重1 100~2 150 g,对照组:胎龄 28~36+4周,出生体重 1 120~2 200 g。2组早产儿在胎龄、出生体重、性别比、血红蛋白、红细胞、网织红细胞计数(Ret)等方面差异无统计学意义(P>0.05)。所有早产儿均排除G-6-PD缺乏症、溶血、出血及其他血液疾病、先天畸形。
1.2 方法 2组患儿自出生第1周起口服维生素E 25 mg/d,维生素 C 0.2 g/d,元素铁 6 mg·kg-1·d-1。治疗组在常规治疗基础上于生后第7天给予Rhu-EPO 750 U·kg-1·周-1,每周分3次皮下注射,共4周。
1.3 检测指标 2组早产儿均于治疗前、治疗后1、2、3、4周检查Ret、血红蛋白(Hb)、红细胞压积(Hct)等。
1.4 输血指征 早产儿输血指征[2]:Hct≤0.25、Hb≤80 g/L,婴儿需要供氧,但不需要机械通气,有以下表现:心动过速(>180次/min),气急(180次/min)超过24 h;需氧量较前48 h增加;鼻导管流量从1/4到1 L/min;鼻塞CPAP从10 cm H2O到12 cm H2O;乳酸浓度升高(≥2.5 mmol/L);体重增加 <10 g·kg-1·d-1,能量≥100 kal·kg-1·d-1;呼吸暂停及心动过缓增加(24 h≥2次,需要面罩呼吸);Hct≤0.20、Hb≤70 g/L,婴儿无症状,网织红细胞绝对值<0.1×1012/L,输同型新鲜浓缩红细胞,每次10~15 ml/kg,并记录输血次数。
1.5统计学分析应用SPSS 11.0统计软件,计量资料以±s表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 2组患儿Ret、Hb、Hct变化比较 治疗后3、4周治疗组患儿 Ret、Hb、Hct均显著高于对照组(P <0.05)。见表1 ~3。
2.2 2组输血发生率比较 对照组输血9例(39.1%),而治疗组输血3例(13.0%),2组输血发生率比较,治疗组明显低于对照组,差异有统计学意义(P<0.05)。
表12组患儿Ret比较n=23,%,±s

表12组患儿Ret比较n=23,%,±s
组别 1周 2周 3周 4周3.0 ±0.5 3.4 ±0.4 4.2 ±0.7 4.5 ±0.3对照组 3.1 ±0.5 3.2 ±0.6 3.5 ±0.3 3.2 ±0.5 P值治疗组>0.05 >0.05 <0.05 <0.05
表23组患儿Hb比较n=23,g/L,±s

表23组患儿Hb比较n=23,g/L,±s
组别 1周 2周 3周 4周166±17 159±12 150±15 144±15对照组 167±17 157±13 143±12 127±11 P值治疗组>0.05 >0.05 <0.05 <0.05
表32组患儿Hct比较n=23,%,±s
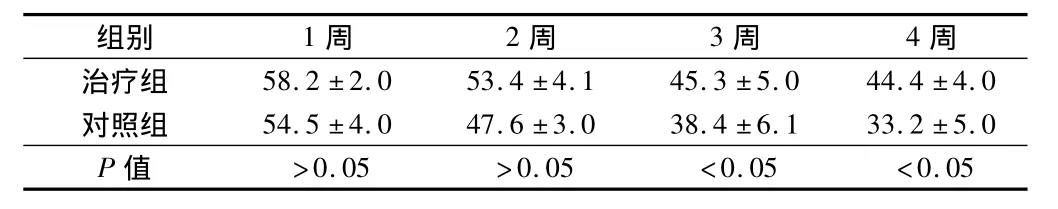
表32组患儿Hct比较n=23,%,±s
组别 1周 2周 3周 4周>0.05 >0.05 <0.05 <0.05 58.2 ±2.0 53.4 ±4.1 45.3 ±5.0 44.4 ±4.0对照组 54.5 ±4.0 47.6 ±3.0 38.4 ±6.1 33.2 ±5.0 P值治疗组
3 讨论
早产儿贫血是临床常见疾病,极低出生体重儿尤为严重。早产儿生后短期内Hb迅速下降,在生后4~8周达最低值,胎龄愈小,出生体重愈低,贫血出现愈早,程度愈严重,严重影响早产儿的生长发育[3]。临床上严重贫血常采用输血治疗,输血可造成包括病毒感染、移植物抗宿主反应、电解质及酸碱平衡紊乱、溶血及免疫抑制等危害。故常立文等[4]开始应用Rhu-EPO来防治早产儿贫血。本文应用Rhu-EPO治疗早产儿贫血,治疗组 Ret、Hb、Hct明显高于对照组(P <0.05),且治疗组仅3例输血,对照组有9例输血治疗,差异有统计学意义(P<0.05),Rhu-EPO治疗早产儿贫血能减少输血量和输血次数。
促红细胞生成素水平低下是早产儿贫血的主要原因,Rhu-EPO是人体包括胎儿在内骨髓红系造血功能重要调控因子,其水平高低可直接反应体内红细胞生成情况。红细胞生成素(EPO)产生减少,其机制[5]可能是:对缺氧感知能力异常,缺氧信号转运至EPO产生的细胞核有缺陷,转录因子与基因的启动因子或强化因子地区的联系减少或存在缺陷,转录激活剂的产生减少或稳定性降低,EPOmRNA产生减少或稳定性降低,EPO蛋白产生减少或不稳定,一些对抗调节蛋白IL-1,肿瘤细胞坏死因子等产生增加。研究表明,如给予Rhu-EPO,早产儿骨髓及血液循环中可有红细胞系的前体细胞出现,且显示正常增值和分化;提供了Rhu-EPO作为替代或减少早产儿贫血时输血治疗的依据,这为应用外源性Rhu-EPO治疗早产儿贫血提供了理论依据[1],采用EpO治疗早产儿贫血缩短了贫血持续时间,减轻了贫血程度,减少了输血次数和输血量,Rhu-EPO能及时、安全、有效地纠正贫血[6]。应用Rhu-EPO治疗期间铁消耗增加可引起功能性缺铁而影响Rhu-EPO治疗效果,蛋白质也是红细胞生成的必需营养素之一,蛋白质供给不足也能影响Rhu-EPO的疗效,为确保Rhu-EPO治疗效果,治疗期间所有早产儿均供给足够的蛋白质及适量铁剂。治疗过程中未发现明显不良反应,说明Rhu-EPO防治早产儿贫血是安全的。
1 金汉珍,黄德珉,官希吉主编.第1版.实用新生儿学.北京:人民卫生出版社,2003.195,270.
2 邵肖梅,叶鸿瑁,丘小汕主编.第1版.实用新生儿学.北京:人民卫生出版社,2010.597.
3 陈晓文,吕回,王卫,等.影响早产儿贫血的因素.实用儿科临床杂志,2001,16:209-210.
4 常立文,刘皖君,廖财绪.不同剂量重组促红细胞生成素防治早产儿贫血的疗效观察.中国实用儿科杂志,2000,15:740-742.
5 张巍,童笑梅,王丹华主编.早产儿医学.第1版.北京:人民卫生出版社,2008.210.
6 林泌,姜洪,杨秀玉.红细胞生成素的临床研究进展.基础医学与临床,2002,20:9-11.

