三聚氰胺-甲醛-硫脲树脂/SBA-15复合材料的合成及其对水溶液中Au(Ⅲ)吸附性能的研究
黄 毅,廖九英,袁丽嫔,曾爱风,谢祥林,苏胜培,喻宁亚
(湖南师范大学湖南省资源精细化与先进材料重点实验室,中国长沙 410081)
金作为一种贵重金属,在地壳中的含量极少.近些年随着科技的日益发展,金在用作珠宝首饰的同时已经被广泛运用于催化[1-2],电子[3],医疗器械[4]等领域,相对于日益增长的需求而显得极其稀缺.因此,金的富集分离在很长一段时间内备受国内外学者关注和研究.
自Mobil公司的科学家发现了MCM系列[5]介孔氧化硅材料以来,由于其具有均一有序的孔道,可调节的孔径,较大的比表面积等优点,掀起了国内外学者的研究热潮.1998年赵东元等人合成出水热稳定的SBA-15[6]更是受到了极大的关注.作为一种新型的材料,介孔氧化硅在催化领域的应用[7-8]取得了显著的成果,而其在吸附分离[9-12]中的应用也展现出良好的发展前景.1997年刘俊等人[9]首次将巯基功能化的介孔材料用于水溶液中Hg2+的吸附,最高吸附量达到了2.56 mmol/g,由此引起了杂化介孔材料对金属的吸附的重视.杨经纶等[11]运用不同的氨基官能化的MCM-41吸附Au(Ⅲ),吸附量可达1.1 mmol/g.廖学品等人[12]将单宁酸接枝到介孔氧化硅上,考察了其对水溶液中Au(Ⅲ)的吸附性能,发现在pH=2,温度为50℃时对Au(Ⅲ)的吸附量达到了3.26 mmol/g.不难发现,介孔材料由于具有均一的孔径分布和较大的比表面积,对水溶液中金属离子具有很好的吸附效果,但是上述吸附剂的合成都需要用到有机硅氧烷进行改性,引入与金属离子具有配位能力的功能基团,而相关有机硅氧烷是一类昂贵的化学原料,这将限制有机官能化介孔材料在金属吸附分离中的实际应用前景.
1967年,Koster等[13]首先采用螯合树脂富集分离贵金属.经过多年的发展,研究者已经合成出了种类繁多,性能各异的螯合树脂[14-18],并对树脂吸附贵重金属的性能进行了广泛探究.与活性碳[19]和离子交换树脂[20]吸附剂相比,螯合树脂具有更大的吸附容量,更快的吸附速率以及更好的吸附选择性.金属螯合吸附剂的设计主要依照软硬酸碱理论[21],文献中提出Au,Pt,Pd等贵金属属于软碱,易与软酸类原子S和中性原子N进行配位,因此含S,N的螯合树脂对贵重金属具有较好的吸附效果.Gülfen等[22]运用三聚氰胺,硫脲,甲醛直接在水溶液中合成出了三聚氰胺-甲醛-硫脲树脂,研究发现该树脂能够从Cu和Zn中很好的分离出Au(Ⅲ),然而在运用MFT树脂单独静态吸附Au(Ⅲ)时,吸附量仅有0.246 mmol/g.不难发现,虽然上述螯合树脂对贵重金属的吸附具有良好的选择性,但是其对贵重金属的吸附容量并不高,原因可能是树脂低的比表面积使得其内部部分配位原子被包裹而难以与重金属离子接触[22],从而使得该螯合树脂对Au(Ⅲ)的吸附容量偏低.
为结合螯合树脂与介孔材料在贵金属富集分离的优势,并克服各自存在的不足,本文设计合成了一系列新型新型的三聚氰胺-甲醛-硫脲树脂(MFT)/SBA-15复合材料.该材料以廉价MFT代替有机硅氧烷,对贵金属有吸附配位能力,同时又具有介孔硅材料较大的比表面积和均一孔径分布的特点,有助于树脂内部配位原子的暴露.实验结果表明,在30℃下,该复合材料对Au(Ⅲ)的饱和吸附量达到3.04 mmol/g.
1 实验部分
1.1 实验试剂
试验中所使用的试剂有三聚氰胺(分析纯,天津市博迪化工有限公司),甲醛(分析纯,湖北奥生新材料科技有限公司),硫脲(分析纯,天津市恒兴化学试剂制造有限公司),正硅酸乙酯(分析纯,天津市大茂化学试剂公司),P123(EO20PO70EO20,Aldrich),四水合氯金酸(分析纯,上海化学试剂研究所),盐酸(分析纯,湖南株洲化学工业研究所),氢氧化钠(分析纯,天津市化学试剂三厂).
1.2 样品的制备
复合材料的典型合成如下:在100 mL烧杯中加入10.2 mL质量分数37%的甲醛水溶液和30 mL去离子水,用氢氧化钠(0.1 mol/L)溶液调整上述溶液pH值至8.5~9.0,之后加入3.20 g三聚氰胺和1.92 g硫脲,于60℃下搅拌2 h形成溶液A.取1 g P123加入250 mL烧杯中,再加入3.2 mL(4 mol/L)HCl溶液和15 mL去离子水,在40℃下搅拌使P123完全溶解,然后加入2.12 g正硅酸乙酯,搅拌1 h,形成溶液B.将溶液A倒入溶液B中,在40℃继续搅拌20 h后,再于90℃下陈化48 h.将得到的白色沉淀过滤,洗涤,然后干燥,用乙醇索氏抽提48 h,即得复合材料.为了考察有机物与无机物物质的量比及有机物中三聚氰胺与硫脲物质的量比对Au(Ⅲ)吸附的影响,合成了一系列样品MFT/S15-x-y,其中x为有机物与无机物的物质的量比,y为有机物中三聚氰胺与硫脲的物质的量比.
1.3 样品的表征
用Avatar 370 FT-IR型红外光谱仪测定样品的红外光谱图,选择波数范围在4 000~400 cm-1内,分辨率为4 cm-1.将样品放在陶瓷马弗炉中550℃焙烧1 h,通过焙烧前后质量的变化确定样品的有机物含量.以Micromeritics Tristar 3000型物理吸附仪测试样品的比表面积及孔径分布,吸附温度为液氮温度-196℃,通过BET方法计算样品比表面积,由等温线吸附支通过BJH模型计算样品孔径分布.
1.4 吸附实验
取50 mg复合材料加入100 mL带塞锥形瓶中,准确移取50 mL预先配置的已知浓度的氯金酸溶液放入锥形瓶,用盐酸(1 mol/L)或氢氧化钠(1 mol/L)调节溶液的pH,在一定温度下磁力搅拌.在预定的吸附时间后,取清液,稀释后使用WFX-110A原子吸收分光光度计测定溶液中Au(Ⅲ)的质量浓度.复合材料的吸附容量按式(1)计算,其吸附率按式(2)计算.

其中Q为复合材料的吸附量,mmol/g;C0为Au(Ⅲ)的初始质量浓度,g/L;Ce为吸附后Au(Ⅲ)的平衡质量浓度,g/L;V为溶液体积,mL;M为Au(Ⅲ)的摩尔质量,g/mol;m为实验中复合材料的质量,mg;E为吸附百分率,%.
2 结果及讨论
2.1 样品的表征
图1为MFT/S15-5-1的红外谱图.样品在2 940 cm-1和2 873 cm-1的吸收峰为—CH2的伸缩振动和剪切弯曲振动;3 300~3 500 cm-1处是N—H的伸缩振动吸收峰,其变形振动吸收出现在1 543 cm-1;在1 120 cm-1处有 ==C S的特征吸收峰[23-24];在 1 074 cm-1和 808 cm-1处有 Si—O—Si的特征吸收峰[25].上述结果说明合成的样品符合预期结构.
由图2可知,MFT/S15-5-1的N2等温吸附-脱附曲线是介孔材料特有IV型吸附-脱附等温线,并且还具备SBA-15型介孔材料的H1型回滞环[8],在N2相对压力p/p0=0.4~0.7处有一个明显的毛细凝聚突跃.从孔径分布图可以得出样品具有较窄的孔径分布.表1给出了所有复合材料的比表面积、孔径以及孔容的结果.材料合成中有机物加入量逐步增加时,样品的比表面积和孔容逐步降低.焙烧实验结果表明,当有机物与无机物物质的量比大于1时,有机物的复合效率高于95%.考虑到纯MFT树脂的比表面积低于0.1 m2/g,因此,复合材料比表面积和孔容的降低正是材料中所有MFT树脂量的增加造成的.事实上,当有机物与二氧化硅的物质的量比达到8∶1时,样品的比表面积和孔容几乎为零.值得指出的是,当有机物与无机物物质的量比为5∶1时,改变有机物中硫脲跟三聚氰胺的比例对所得复合材料的织构性质影响不大.
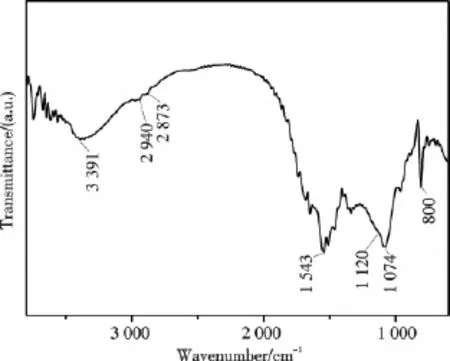
图1 MFT/S15-5-1的红外谱图Fig.1 FT-IR spectrum of MFT/S15-5-1
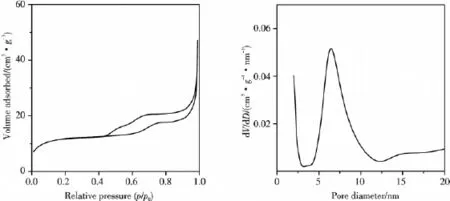
图2 MFT/S15-5-1的N2吸附-脱附等温曲线(左)与孔径分布图(右)Fig.2 Nitrogen adsorption-desorption isotherm(left)and pore size distribution(right)of MFT/S15-5-1
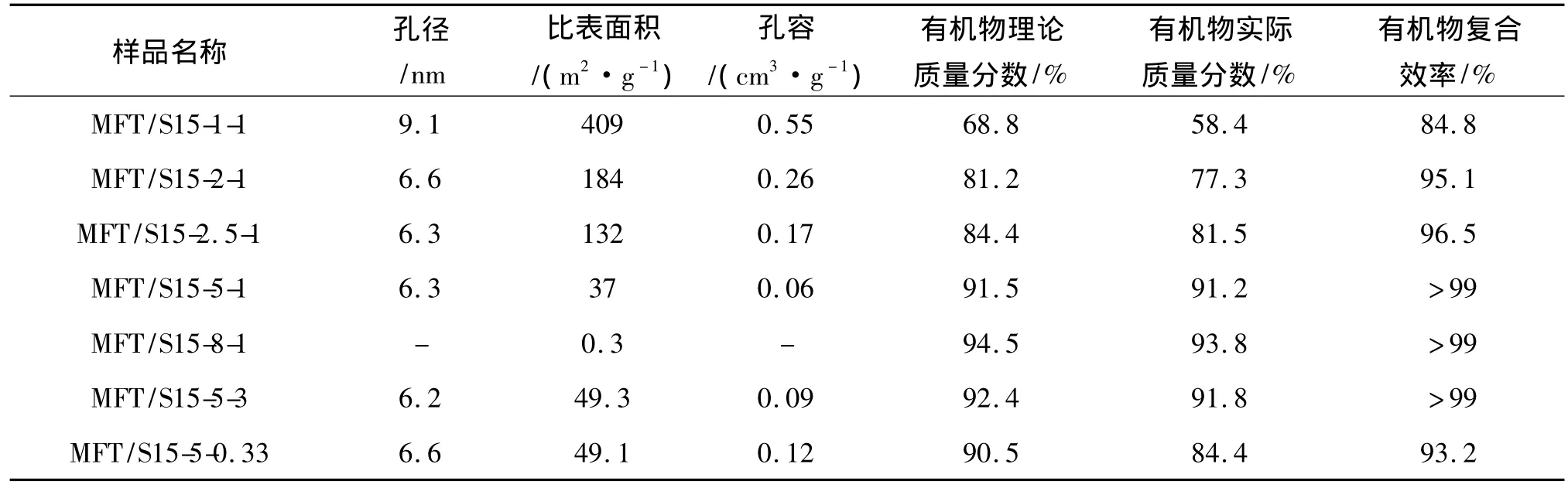
表1 样品的织构性质Tab.1 Textural parameters of the samples
2.2 对Au(Ⅲ)的吸附结果
2.2.1 初始pH与时间的影响 为了得到较为优化的吸附条件,以MFT/S15-5-1为吸附剂,考察了Au(Ⅲ)溶液初始pH与吸附时间对Au(Ⅲ)吸附的影响.在氯金酸溶液中,根据pH值的不同,Au(Ⅲ)能够以氢氧化物,氯化物和氯化氢氧化物的形式存在,而且溶液中氯离子的浓度对溶液中Au(Ⅲ)的存在形式同样有很重要的影响[22].当溶液中氯离子浓度大于0.01 mol/L,Au(Ⅲ)在酸性溶液(pH≤4)中主要以AuCl-4的形式存在,在碱性溶液(pH>8)中主要以Au(OH)-4,Au(OH)3和Au(OH)3Cl-三种形式存在;在中性溶液中出现Au(OH)Cl-3(pH=3.5~6.5)和Au(OH)2Cl-2(pH=4.5~8).因而在不同pH值,溶液中可能会出现多种形式的Au(Ⅲ)物种共存现象.由图3可知当溶液pH=2时,MFT/S15-5-1对溶液中Au(Ⅲ)的吸附效果最好,当溶液pH高于4时,其对Au(Ⅲ)的吸附效率明显下降,由此可以推断AuCl-4更容易被MFT/S15-5-1吸附.当溶液pH值下降到1时,MFT/S15-5-1对Au(Ⅲ)的吸附性能降低,这是因为此时溶液中存在高浓度的Cl-,其与AuCl-4发生竞争吸附.上述结果与文献中纯MFT树脂对Au(Ⅲ)的吸附结果基本一致[22],这说明复合材料中氧化硅的存在没有改变MFT树脂对Au(Ⅲ)的吸附特性.由于Au(Ⅲ)溶液在pH=2时复合材料有最好的吸附性能,因而在接下来的吸附实验中都将Au(Ⅲ)溶液的初始pH值调节至2.图4是MFT/S15-5-1在不同时间下对Au(Ⅲ)的吸附结果.从图中可以看出,在吸附时间小于15 min时,复合材料对Au(Ⅲ)的吸附量随着时间的延长而快速增加,之后吸附速率逐渐降低.这是因为在吸附初始阶段,复合材料中有大量的吸附活性位点,浓度差造成的传质推动力大,从而表现出了较快的吸附速率.随着吸附时间的推移,复合材料吸附的Au(Ⅲ)物种浓度越来越高,其可提供的吸附活性位点减少,吸附速率降低,吸附越接近平衡状态.由图4结果,吸附时间为30 min是较优的参数.
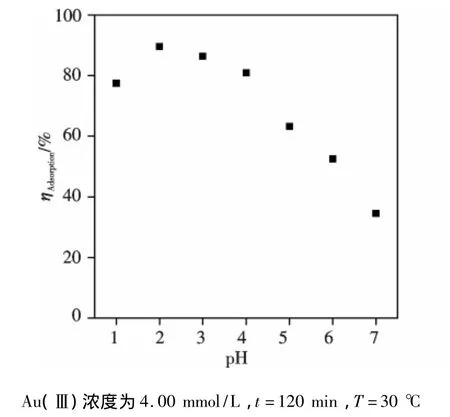
图3 初始pH的影响Fig.3 Effect of initial pH on Au(Ⅲ)adsorption
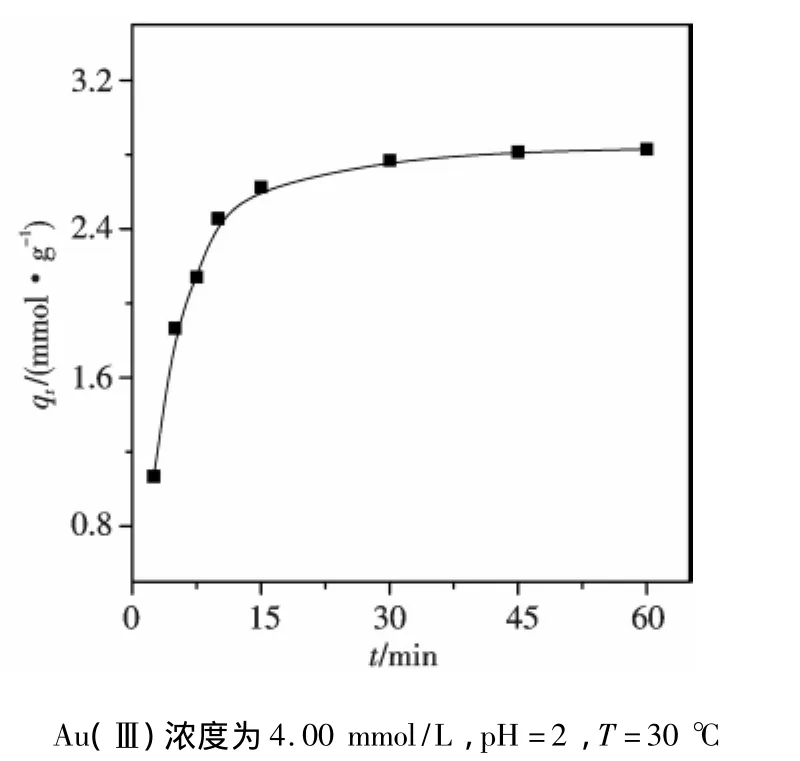
图4 时间的影响Fig.4 Effect of contact time on Au(Ⅲ)adsorption
2.2.2 复合材料合成中原料配比的影响 在得到较优的吸附pH值及时间之后,考察了复合材料合成中有机物与无机物物质的量比及有机物中三聚氰胺与硫脲物质的量比对Au(Ⅲ)吸附的影响,实验结果如表2所示.当合成中有机物与无机物物质的量比增加时,在对不同的起始浓度Au(Ⅲ)溶液的吸附中,复合材料的吸附量都是先增加后下降,有机物与无机物物质的量比为5时合成的样品MFT/S15-5-1表现了最高的吸附量.复合材料中有机组分具有对Au(Ⅲ)物种的吸附位,而纯硅SBA-15材料对Au(Ⅲ)基本没有吸附,但合成中有机物与无机物物质的量比增加到8后,样品MFT/S15-8-1反而下降.通过对比样品MFT/S15-5-1和MFT/S15-8-1,两者有机物复合效率都高于99%,MFT/S15-8-1由于有机物量太高基本没有孔道结构,而MFT/S15-5-1则保留了一定的孔道结构(见表1).上述分析说明复合材料的孔道结构对Au(Ⅲ)的吸附有较大的影响,孔道结构的存在可以使更多的有机物内部吸附位得以暴露.
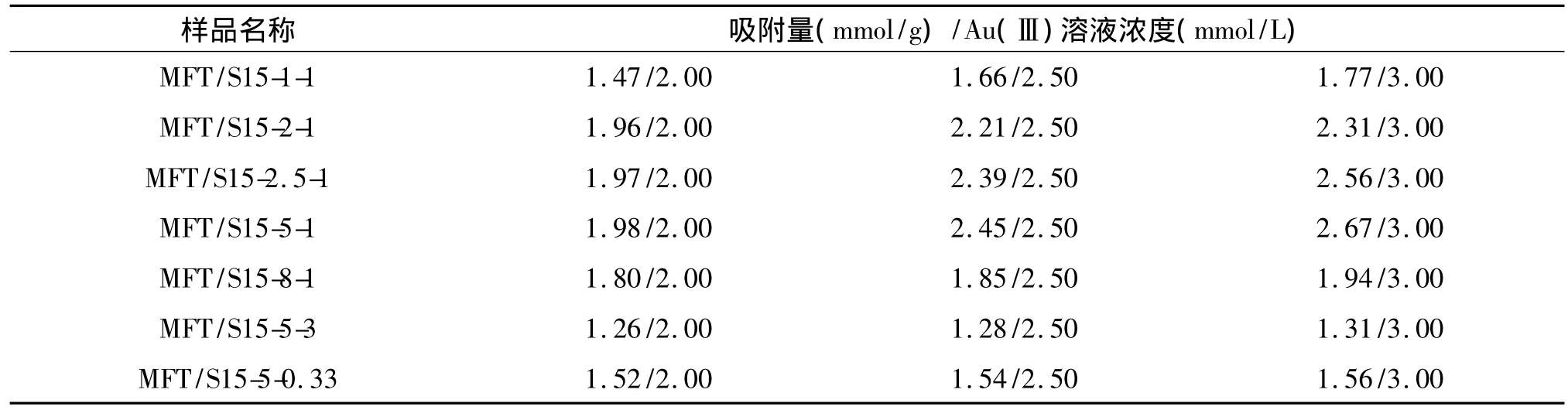
表2 不同原料配比合成出的样品对Au(Ⅲ)的吸附性能Tab.2 Performance of the samples prepared by using various proportions of raw materials in Au(Ⅲ)adsorption
在确定了优化的有机物与无机物物质的量比后,继续对复合材料合成中三聚氰胺与硫脲的物质的量比对Au(Ⅲ)吸附的影响进行了考察.由表2可知当三聚氰胺与硫脲的物质的量比从0.33增加到3时,复合材料对不同的起始浓度Au(Ⅲ)溶液吸附时的吸附量都是先上升后下降,在三聚氰胺与硫脲的物质的量比为1时,复合材料对Au(Ⅲ)物种有最高的吸附量.值得指出的是,当三聚氰胺与硫脲的物质的量比变化时,复合材料的织构性质基本没有变化(见表1),这说明复合材料对Au(Ⅲ)物种吸附量的变化并非由织构性质所造成.
为了验证所合成的复合材料是否真正提高了MFT树脂对Au(Ⅲ)的吸附性能,按照文献[22~24]的方法合成出了纯的MFT树脂,根据表2中MTF/S15-5-1的有机物质量分数为91.2%,以相同的有机-无机配比得到了MFT树脂与纯硅SBA-15(由MFT/S15-5-1在550℃下焙烧1 h得到)的机械混合物.分别取50 mg MFT/S15-5-1、纯MFT树脂、MFT与SBA-15的机械混合物和纯硅SBA-15样品加入100 mL带塞锥形瓶中,准确移取50 mL 4.00 mmol/L的氯金酸溶液放入锥形瓶,用盐酸(1 mol/L)调节溶液的pH为2,在30℃下磁力搅拌30 min,所得吸附量分别为2.84、0.65、0.59、0.11 mmol/g.实验结果表明复合材料相对于纯 MFT树脂,其对Au(Ⅲ)的吸附性能有了极大的提高.
2.3 吸附动力学和吸附热力学
为了更进一步研究复合材料对Au(Ⅲ)吸附的动力学行为,同时运用准一级(3)和准二级(4)动力学模型线性方程[26-27]对图4数据进行拟合.

其中t为吸附时间,min;Qe为平衡时吸附量,mmol/g;Qt是时间为t时的吸附量,mmol/g;K1为准一级动力学吸附常数,min-1;K2为准二级动力学吸附常数,g/(mmol·min).
图5为准一级和准二级动力学模型线性拟合曲线,表3为线性拟合后所计算出来的动力学参数.通过对比表3中准二级动力学与准一级动力学模型线性拟合的结果,准二级动力学拟合计算得到的平衡吸附量2.99 mmol/g更接近实验值2.84 mmol/g,而且准二级动力学模型线性拟合相关系数为0.998 3更接近于1,说明复合材料对溶液中Au(Ⅲ)的吸附更符合准二级动力学模型.因此作者认为复合材料MTF/S15-5-1对Au(Ⅲ)的吸附过程符合准二级动力学模型,化学吸附为该吸附过程的限速步骤,与理论预期一致.
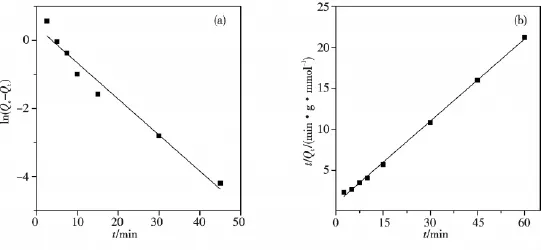
图5 准一级动力学拟合(a)和准二级动力学拟合(b)Fig.5 Kinetic plots fitted by pseudo first-order(a)and pseudo second-order(b)methods

表3 动力学拟合结果Tab.3 The results of kinetic fitting
图6反映了Au(Ⅲ)溶液初始浓度和吸附温度对MFT/S15-5-1吸附性能的影响,从图中可以看出,在相同的温度下,MFT/S15-5-1对Au(Ⅲ)的吸附量随着初始浓度的升高而增加,当浓度达到一定程度时,MFT/S15-5-1对Au(Ⅲ)吸附量的增加逐渐缓慢,并达逐渐到该温度下的饱和吸附.同时在相同的初始浓度及其他吸附条件下,MFT/S15-5-1对Au(Ⅲ)吸附量随着温度的升高而增加,该结果说明复合材料对Au(Ⅲ)的吸附过程为吸热过程.
采用Langmuir等温吸附模型(5)和Freundlich(6)等温吸附模型线性方程[26-27]对图6进行数据拟合得图7,表4给出了所得到的拟合参数.
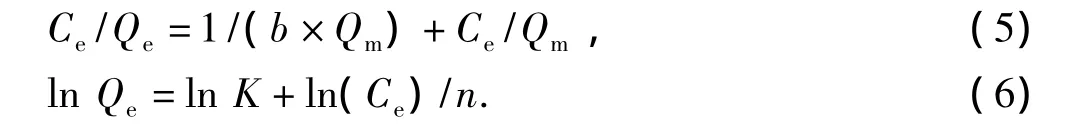
其中Qe为平衡时吸附量,mmol/g;Qm为饱和吸附量,mmol/g;Ce是平衡时溶液中Au(Ⅲ)浓度,mmol/L;b为Langmuir吸附常数,L/mmol;K为表征吸附能力的常数,mmol/g;n为Freundlich常数.
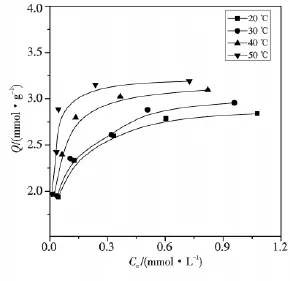
图6 吸附等温线(t=30 mim,pH=2)Fig.6 Adsorption isotherms at different temperature
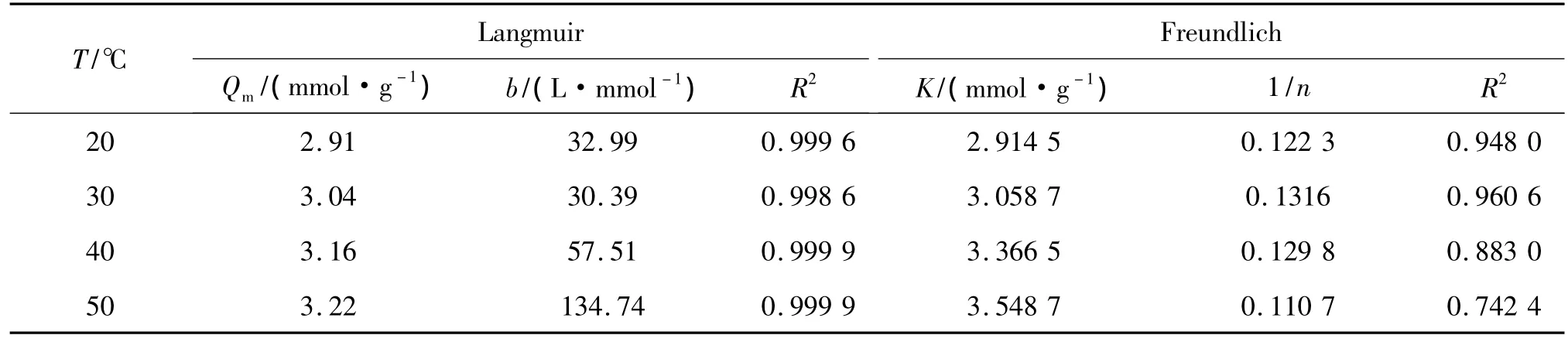
表4 Langmuir与Freundlich线性拟合结果Tab.4 The results deduced from fitting the adsorption data to Langmuir and Freundlich equations
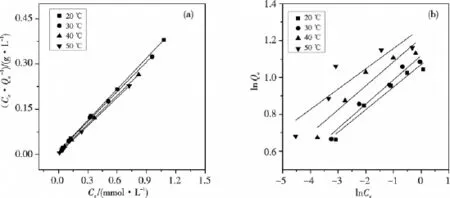
图7 Langmuir等温吸附线性拟合(a)和Freundlich等温吸附线性拟合(b)Fig.7 Fitting the adsorption data to Langmuir(a)and Freundlich equation(b)
由表4中拟合的参数结果可知Langmuir等温吸附模型拟合的相关系数均大于0.99,其与Freundlich等温吸附模型拟合相关系数0.74~0.94相比更接近1,由此可以得出复合材料对Au(Ⅲ)的吸附过程更符合Langmuir等温吸附模型,吸附原理为单分子层吸附.通过计算,吸附温度为20、30、40、50℃时MFT/S15-5-1对 Au(Ⅲ)的饱和吸附量分别为2.91、3.04、3.16、3.22 mmol/g,可以看出 MFT/S15-5-1 对 Au(Ⅲ)具有很好的吸附性能.
3 结论
研究结果表明:制备的复合材料对Au(Ⅲ)的吸附在30 min可达到吸附平衡;pH为2时吸附效果最佳;SBA-15与MFT树脂的复合极大的提高了MFT树脂对Au(Ⅲ)的吸附性能;通过比较发现MFT/S15-5-1对Au(Ⅲ)的吸附性能最好;随着温度的升高MFT/S15-5-1对Au(Ⅲ)的饱和吸附量增加,30℃时的饱和吸附量达到了3.04 mmol/g;吸附过程符合准二级动力学方程和Langmuir等温吸附模型,为化学吸附中的单分子层吸附.
[1]JIN Y,WANG P J,YIN D H,et al.Gold nanoparticles prepared by sonochemical method in thiol-functionalized ionic liquid[J].Colloid Surf A-Physicochem Eng Asp,2007,302(1-3):366-370.
[2]JIN Y,ZHUANG D Y,YU N Y,et al.Epoxidation of styrene over gold nanoparticles supported on organic-inorganic hybrid mesoporous silicas with aqueous hydrogen peroxide[J].Microporous Mesoporous Mater,2009,126(1-2):159-165.
[3]TIMOTHY W,ELLIS PH D.The future of gold in electronics[J].Gold Bull,2004,37(1-2):66-71.
[4]NAVARRO M.Gold complexes as potential anti-parasitic agents[J].Coordin Chem Rev,2009,253(11-12):1619-1626.
[5]BECK J S,VARTUI J C,ROTH W J,et al.A new family of mesoporous molecular sieves prepared with liquid crystal templates[J].J Am Chem Soc,1992,114(27):10834-10843.
[6]ZHAO D Y,HUO Q S,STUCKY G D.Nonionic triblock and star diblock copolymer and oligomeric surfactant syntheses of highly ordered,hydrothermally stable,mesoporous silica structures[J].J Am Chem Soc,1998,120(24):6024-6036.
[7]JIN Y,WANG P G,YU N Y,et al.Gold nanoparticles stabilized in a novel periodic mesoporous organosilica of SBA-15 for styrene epoxidation[J].Microporous Mesoporous Mater,2008,111(1-3):569-576.
[8]YU N Y,GONG Y J,SUN Y H,et al.One-pot synthesis of mesoporous organosilicas using sodium silicate as a substitute for tetraalkoxysilane[J].Microporous Mesoporous Mater,2004,72(1-3):25-32.
[9]FENG X,FRYXELL G E,LIU J,et al.Functionalized monolayers on ordered mesoporous supports[J].Science,1997,276:923-926.
[10]张三山,张德喜,肖建国,等.氨基酸在微波辅助钙改性SBA-15上的吸附性能[J].湖南师范大学自然科学学报,2012,35(2):52-57.
[11]LAM K F,YEUNG K L,MCKAY G,et al.An investigation of gold adsorption from a binary mixture with selective mesoporous silica adsorbents[J].J Phys Chem B,2006,110(5):2187-2194.
[12]HUANG X,WANG Y P,SHI B,et al.Adsorptive recovery of Au3+from aqueous solutions using bayberry tannin-immobilized mesoporous silica[J].J Hazard Mater,2010,183(1-3):793-798.
[13]KOSTER G,SCHMUCKLER G.Separation of noble metals from base metals by means of a new chelating resin[J]Analytica Chimica Acta,1967,38(1):179-184.
[14]ZELIYHA C,MUSTAFA G,ALI O A,et al.Synthesis of a novel dithiooxamide-formaldehyde resin and its application to the adsorption and separation of silver ions[J].J Hazard Mater,2010,174(1-3):556-562.
[15]DURGA P,HIDETAKA K,KATSUTOSHI I,et al.Recovery of gold(Ⅲ),palladium(Ⅱ),and platinum(Ⅳ)by aminated lignin derivatives[J].Ind Eng Chem Res,2006,45(19):6405-6412.
[16]DING S M,ZHANG X Y,FENG X H,et al.Synthesis of N,N'-diallyl dibenzo 18-crown-6 crown ether crosslinked chitosan and their adsorption properties for metal ions react[J].Funct Polym,2006,66(3):357-363.
[17]张超灿,庞金兴,李 曦,等.核-壳型巯基胺螯合树脂的制备及其吸附性能[J].武汉大学学报:理学版,2001,47(2):189-191.
[18]王 帅,钟 宏,王爱萍,等.聚酯基硫脲树脂对金离子的吸附性能研究[J].黄金,2007,28(7):34-37.
[19]伍喜庆,黄志华.改性活性炭吸附金的性能[J].中国有色金属学报,2005,15(1):129-132.
[20]IGLESIAS M,ANTICÓ E,SALVADÓ V.Recovery of palladium(Ⅱ)and gold(Ⅲ)from diluted liquors using the resin duolite GT-73[J].Analytica Chimica Acta,1999,381(1):61-67.
[21]PEARSON G.Hard and soft acids and bases[J].J Am Chem Soc,1963,85(22):3533-3539.
[22]AYDIN A L,IMAMOLU M,GÜLFEN M,et al.Separation and recovery of gold(Ⅲ)from base metal ions using melamineformaldehyde-thiourea chelating resin[J].J Hazard Mater,2008,107(2):1201-1206.
[23]BIRINCI E,GÜLFEN M,AYDIN A O,et al.Separation and recovery of palladium(Ⅱ)from base metal ions by melamineformaldehyde-thiourea(MFT)chelating resin[J].Hydrometallurgy,2009,95(1-2):15-21.
[24]YIRIKOGLU H,GÜLFEN M.Separation and recovery of silver(Ⅰ)ions from base metal ions by melamine-formaldehyde-thiourea(MFT)chelating resin[J].Sep Sci Technol,2008,43(2):376-388.
[25]WANG X,LIN K S K,CHENG S,et al.Direct synthesis and catalytic applications of ordered large pore aminopropyl-functionalized SBA-15 mesoporous materials[J].J Phys Chem B,2005,109(5):1763-1769.
[26]YIN P,WANG C H,YANG Y X,et al.Thermodynamics and kinetics of Au(Ⅲ)adsorption on silica gel chemically modified by diethylene triamine bis(methylene phosphonic acid)[J].J Chem Eng Data,2011,56(3):450-457.
[27]DEBNATH S,GHOSH U C.Kinetics,isotherm and thermodynamics for Cr(Ⅲ)and Cr(Ⅵ)adsorption from aqueous solutions by crystalline hydrous titanium oxide[J].J Chem Thermodyn,2008,40(1):67-77.

