呋喃丹在玻碳电极上的阳极伏安行为
张美娜, 李明超
(1.吉林工业职业技术学院,吉林 吉林 132013;2.中国石油吉林石化公司电石厂,吉林 吉林 132022)
0 引 言
呋喃丹(Carbofuran)又名克百威,在碱性介质中不稳定,为高毒广谱性杀虫剂。具有触杀和胃毒作用,稻田水面撒药,残效期短,施于土壤中残效期长。可适用于棉花、水稻、甘蔗、花生等作物,对人、畜有很强的毒性。目前,呋喃丹的分析方法有高效液相色谱法(HPLC)[1-2]、气相色谱法(GC)[3-5]、液相色谱法(LC)[6]等。用上述方法测定样品处理过程繁琐,有关呋喃丹在玻碳电极(GCE)的伏安法研究和测定目前尚未见报道。文中用GCE研究了呋喃丹在酸性介质中产生一个与呋喃丹浓度呈良好线性和再现性的氧化峰。同时,对pH值、干扰物质等的影响进行了研究,并取得满意的结果。
1 实验部分
1.1 仪器和试剂
BAS-100A电化学系统(美国BAS仪器公司),玻碳电极(GCE,A=0.125 6cm2)为工作电极,Ag/AgCl为参比电极,Pt丝为对电极。
1×10-3mol/L呋喃丹溶液:称取2g呋喃(安徽省无为县花卉肥料厂),用水稀释至50mL容量瓶内,室温保存。
其它试剂均为分析纯试剂,水为二次蒸馏水。
1.2 实验方法
取一定量的呋喃丹溶液和0.1mol/L HCl(pH=1.0)的缓冲溶液共10.00mL于电解池内,在0.3~1.2V之间进行阳极伏安扫描,记录其氧化峰(富集时间为45s,静止时间为10s,扫描速度为60mV/s)。
2 结果与讨论
2.1 呋喃丹在GCE上的伏安行为
在含有1.0×10-4mol/L呋喃丹 HCl(pH=1.0)的底液中,从0.3~1.2V (vs.Ag/AgCl)以玻碳电极为工作电极进行循环伏安扫描所得循环伏安图如图1所示。
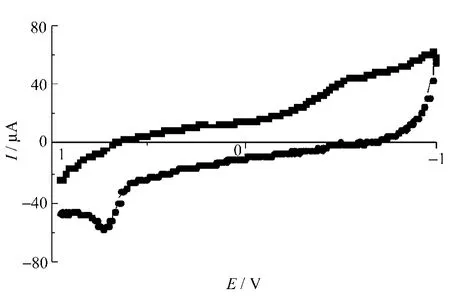
图1 呋喃丹的循环伏安图
微分脉冲溶出伏安曲线如图2所示。
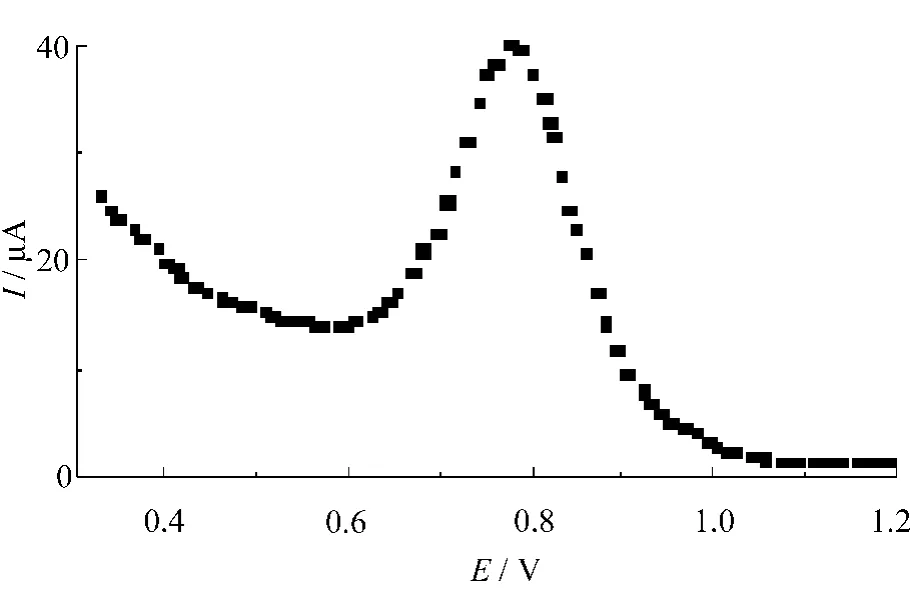
图2 呋喃丹的微分脉冲溶出伏安曲线
2.2 支持电解质的比较及pH值影响
实验了呋喃丹溶液在0.1mol/L HCl,0.01mol/L HCl pH值从3.0到5.7的NaAc-HAc缓冲溶液,以及0.1mol/L NaCl,NH4Ac等缓冲溶液的循环伏安行为。发现以0.1mol/L HCl缓冲溶液(pH=1.0)为底液,线性扫描伏安法测定时还原电流(ip)高且峰形好。故选择0.1mol/L HCl缓冲溶液作为支持电解质。
底液pH值对峰电流、峰电位的影响如图3所示。
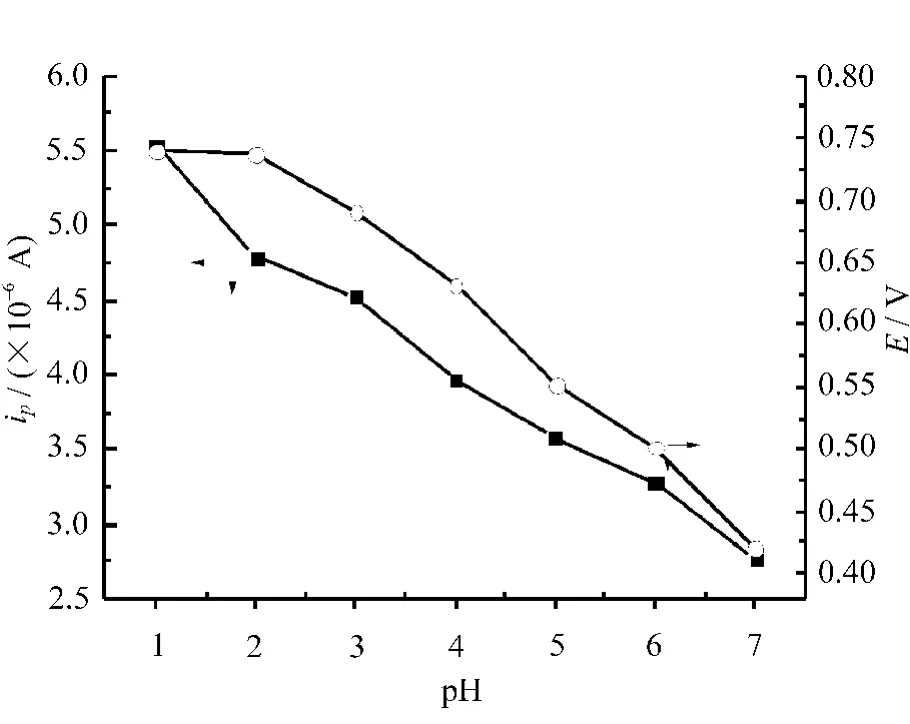
图3 底液pH值对峰电流、峰电位的影响
v=60mV/s,t=45s,1×10-4mol/L呋喃丹溶液,0.1mol/L HCl。
2.3 扫描速度的影响
对1.0×10-4mol/L的呋喃丹溶液测定了扫描速度对峰电流的影响,当扫描速度在20~100mV/s之间变化时,ip与v1/2呈线性关系,其线性方程为ip=3.452 6+0.068 4 v1/2,r=0.993 2,表明了呋喃丹在电极界面上的传质属于线性扩散,其还原过程主要受扩散速率控制。
扫描速度对峰电流的影响如图4所示。
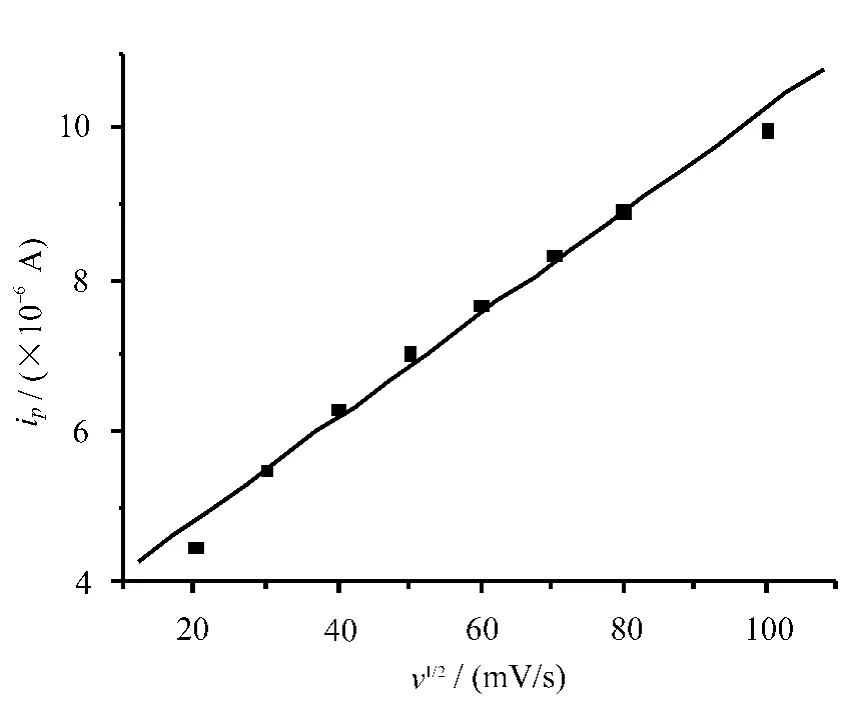
图4 扫描速度对峰电流的影响
v=60mV/s,t=45s,1.0×10-4mol/L呋喃丹溶液,0.1mol/L HCl。
2.4 富集时间的影响
考察了富集时间对峰电流的影响。实验表明,当富集时间在0~120s之间逐渐变化时,随着富集时间的增加,峰电流逐渐增大,到达45s之后,峰电流有下降趋势。
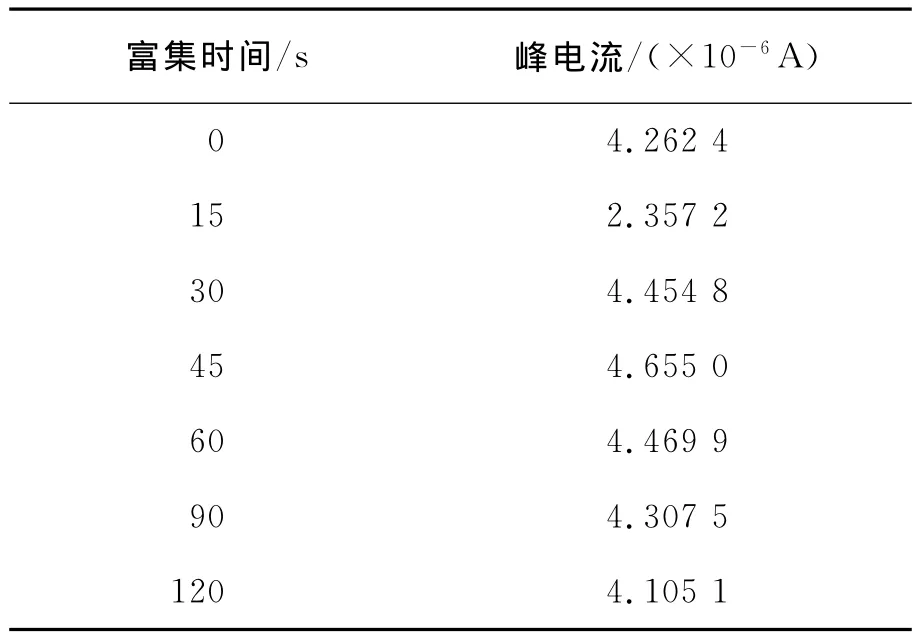
表1 富集时间对峰电流的影响
2.5 共存物质的影响
在强酸溶液中,大多数阳离子不干扰测定:呋喃丹浓度为1.0×10-4mol/L 时,K+,NH4+,Mn2+,Sb2+,Na+,Se2+,Cu2+,Al3+,Fe3+,Cd2+,Pb2+,Bi3+等均不干扰测定,Cr3+对其测定产生严重干扰,峰形消失。
2.6 重现性的影响
在一定实验条件下,浓度为1.0×10-4mol/L的呋喃丹溶液连续测定峰电流7次,其相对平均标准偏差(RSD)为1.8%,重现性好。
2.7 线性范围与检测限
在pH=1.0的HCl缓冲溶液中,呋喃丹溶液浓度在1.8×10-5~8×10-4mol/L范围内成线性关系,如图5所示。
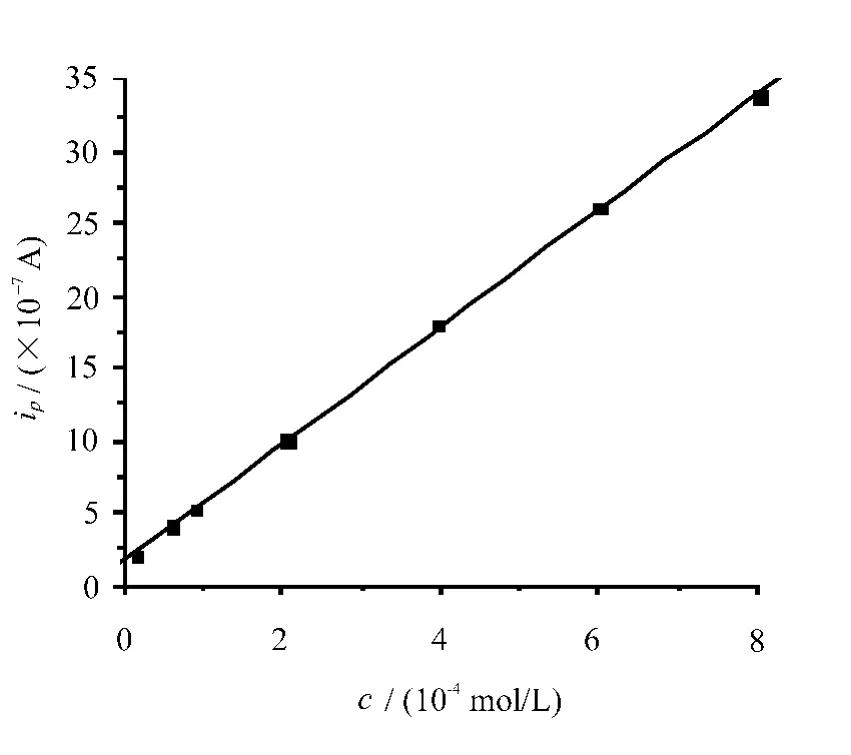
图5 工作曲线
对pH=1.0的HCl底液进行扫描,该方法检测限为1.0×10-7mol/L。
2.8 电极反应机理探讨
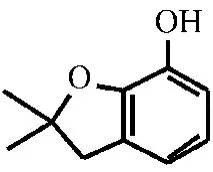
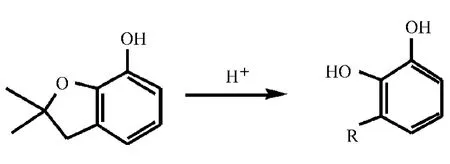
3 样品测定
采用本法对模拟土壤进行了样品测定,结果见表2。
表2 模拟土壤样品测定结果
模拟土壤样品分析程序[8-10]:称取样品20g,研磨,加入100mL蒸馏水,充分搅拌均匀,抽滤。加入80mL乙醚萃取2次。合并萃取液于烧瓶,蒸馏至近干,取下烧瓶,自然干燥。在烧瓶中加入10mL的0.1mol/L HCl(pH=1.0)缓冲溶液,按原药测定程序进行测定。
极谱法可以对土壤样品中呋喃丹残留进行测定,同时有助于土壤中呋喃丹降解过程的研究。
[1]张洪兰.用固相提取和高效液相色谱法分离检测生物体液中7种氨基甲酸酯类农药[J].色谱,1997,15(5):442-444.
[2]杨容,博承光.基质固相分散-高效液相色谱法测定玉米中痕量呋喃丹[J].分析测试学报,1994,13(5):72-74.
[3]粱祈,颜庆嫦.中药材黄芪中氨基甲酸酯农药残留量的毛细管气相色谱法测定[J].分析测试学报,1999,18(2):66-68.
[4]方洪矩.高分辨气相色谱法及其在药物分析中的应用[J].药学学报,1990,25(11):869-871.
[5]Blaicher G,Pfannhauser W,Woidich H.Problems encountered with the routine application of HPLC to the analysis of carbamate pesticides[J].Chromatographia,1980,13(7):438-446.
[6]Kikt E J,许满英.液相色谱法测定克百威(呋喃丹)原药及制剂的协作研究[J].农药译丛,1989,11(3):40-43.
[7]荆新堂,李勤凡.呋喃丹降解菌的研究进展[J].动物毒物学,2009,24(1-2):9-14.
[8]嵇正平,汪世新,陆自强,等.光度法快速测定土壤中呋喃丹[J].理化检验:化学分册,2005,41(4):279-280.
[9]石守良,郭永泽.蔬菜和土壤中呋喃丹残留量的分析方法研究[J].天津农林科技,2001(2):19-21.
[10]沈丽艳,马春龙.基于数据融合的土壤电导率测量方法[J].长春工业大学学报:自然科学版,2012,33(2):151-154.

