两种方式姑息治疗肝门胆管癌对比分析
丁国乾,秦鸣放,邹富胜,赵宏志
(天津市南开医院微创外科中心 300070)
肝门胆管癌是指位于胆囊管开口以上的胆管包括肝总管,左、右肝管汇合部和左右肝管的黏膜上皮癌,占肝外胆管癌的58%~75%[1]。尽管影像技术与外科技术在当今得到快速发展,但肝门胆管癌由于解剖部位特殊,难以早期诊断,因而预后很差[2]。本院2000年1月至2009年12月对肝门胆管癌195例行姑息治疗,取得了较为满意的效果,现将两种姑息治疗方法对比分析如下。
1 资料与方法
1.1 一般资料 本院2000年1月至2009年12月姑息治疗肝门胆管癌195例,其中男101例,女94例,年龄49~87岁,平均年龄(60.74±9.2)岁。按采取的治疗方法不同分为内镜组及经皮组,其中内镜组113例,经皮组82例。所有病例均经B超、CT、磁共振胰胆管造影(megnetic resonance cholangiopancreatography,MRCP)明确梗阻部位及程度,证实手术无法切除,或不愿接受手术,临床分型采用Bismuth-Corlette分型标准。所有患者均有不同程度的黄疸,血清总胆红素(total bilirubin,TBIL)、直接胆红素(direct bilirubin,DBIL)、谷丙转氨酶(alanine aminobansferase)、碱性磷酸酶(alkaline phospha-tase,ALP)、及 γ-谷氨酰转肽酶(γ-glutamyltranspeptidase,γ-GGT)均有增高。两组一般资料比较见表1。
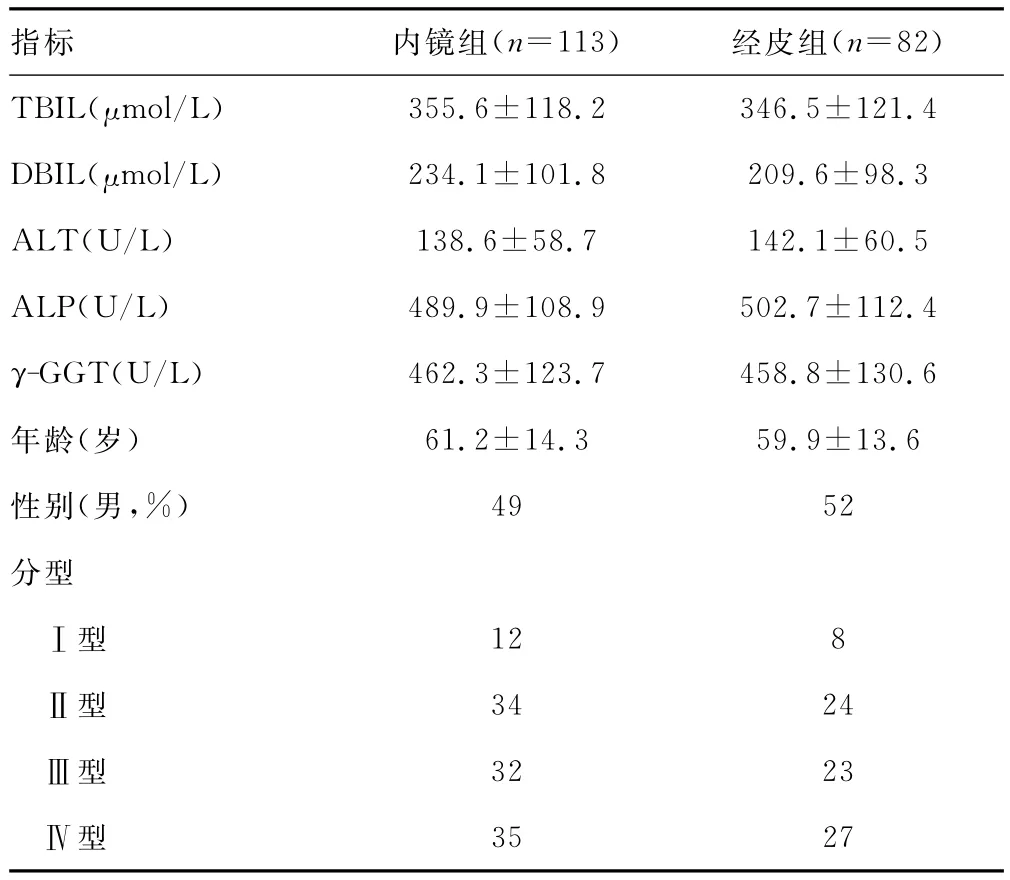
表1 两组一般资料
1.2 治疗方法 内镜组:基础麻醉,按常规经内镜逆行性胆胰管造影(endoscopic retrograde cholangiopancreatography,ERCP)准备。左侧俯卧位,用十二指肠镜行ERCP术,造影明确梗阻部位、程度及范围后,将导丝插入胆道并超过梗阻部位,经胆道扩张探条扩张狭窄后,放置长6~8cm金属支架或8.5~10Fr塑料支架,其两端均超过梗阻段至少1cm。经皮组:按常规经皮经肝穿刺(PTC)术前准备,患者仰卧位,穿刺前先行CT检查,了解病变及胆道情况。在X线监视下,选择走向较平直,管径相对较粗的胆管为目标胆管,根据目标胆管的位置确定进针点和进针角度。无菌条件下用18~21G塑料套管针穿刺进入皮肤,快速经肝进入胆道,回抽见胆汁后,将塑料导管外鞘推入胆管,金属导丝沿套管针外鞘插入胆管达梗阻远端,调整方向,使其通过梗阻段达十二指肠内,然后将预选好的金属支架套管沿导丝送至梗阻段远端1cm释放支架,再造影见胆道通畅,留置胆道外引流管以防支架闭塞,3d后经外引流管行泛影葡胺造影,支架扩张状态良好即拔除外引流管。
2 结 果
两组成功置入胆道支架患者,术后第2天开始全身瘙痒、皮肤巩膜黄染症状均有不同程度的明显好转,放置胆道支架1周后,两组血清TBIL、DBIL、ALT、ALP、γ-GGT较术前均明显下降(P<0.05),而两组相比较差异无统计学意义(P>0.05),见表2。
内镜组113例患者中,成功放置胆道支架80例,成功率70.8%,其中放置金属胆道支架72例,塑料支架8例。33例未成功患者择日改为经皮经肝胆道支架置入术或胆管穿刺引流术。术后发热20例,其中大于39.5℃7例,38.5~39.5℃13例,除1例患者死亡外,均经保守治疗或行经皮经肝胆道穿刺引流后好转。其他并发症如术后胰腺炎、胆道出血、十二指肠穿孔等均经治疗后好转。死亡1例,放置金属支架术后10h开始发热,最高41.5℃,对症治疗无明显好转,于术后第3天死亡。
经皮组82例患者,成功放置胆道支架71例,成功率86.6%,均放置金属支架。11例未成功患者仅行经皮经肝胆管穿刺引流术者9例,2例保守治疗。胆道出血患者9例,行保守治疗好转7例,1例行数字减影血管造影术明确出血部位后行栓塞术,死亡1例,因腹腔出血严重,抢救无效死亡。
两组Ⅰ、Ⅱ、Ⅲ成功率差异无统计学意义(P>0.05),而Ⅳ型差异显著(P<0.05)。两组术后并发症及各类型成功率见表3。
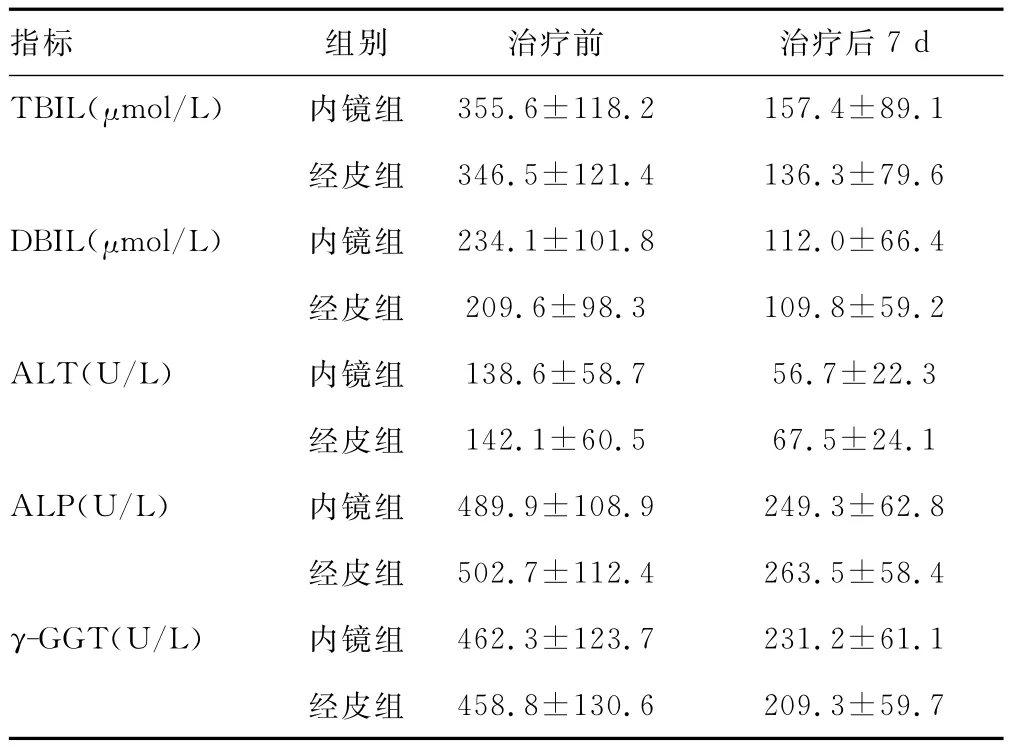
表2 两组术前、术后生化指标比较
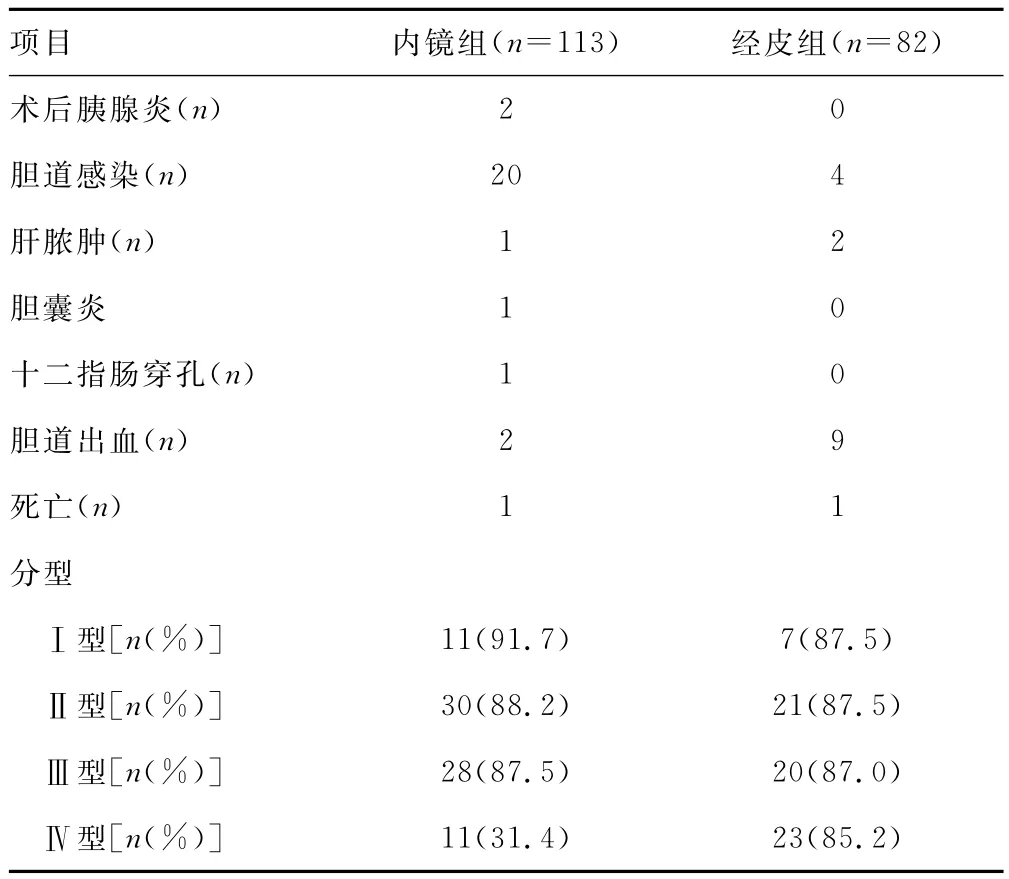
表3 两组术后并发症及各类型成功率
3 讨 论
肝门胆管癌是胆道外科的一种疑难病症,由于特殊的解剖部位和肿瘤细胞的生物学特性,根治性切除是治愈的惟一选择,但遗憾的是在大多数医院内,半数以上的住院患者是属于不能切除的病例,即使是勉强切除,术后3~5年生存率也仅为较低的水平[3],真正的根治性切除治疗的前景仍是很严峻的[4]。此种疾病难以早期诊断,一旦发生黄疸就医,说明肿瘤已经完全阻塞胆管,甚至有的已有远位转移失去根治机会,故本病预后极差。
从20世纪90年代以来,外科对确诊为肝门部胆管癌患者的治疗,抱着积极态度。然而,手术中常因发现肿瘤侵犯肝十二指肠韧带、淋巴结和门静脉而放弃根治性切除术[5],原因在于该病早期症状无典型,多数患者皆因黄疸后就医,而癌肿本身具有浸润性生长,向邻近肝组织肝动脉及门静脉侵犯并沿胆管内膜扩展的特点,在梗阻性黄疸时已往往是本病的晚期而失去根治的机会[6]。
胆管癌的直接致死原因主要为梗阻性黄疸,胆道感染和脓毒血症,因此如何控制黄疸,保护肝细胞功能和预防感染,以及由梗黄所致的全身各脏器功能的变化是提高肝门胆管癌外科治疗效果的重要基础[7],所以,以减黄为目的姑息治疗在晚期肝门胆管癌的治疗中至关重要。减黄术的目的在于解除梗阻性黄疸所致肝脏损害以及黄疸对全身的影响,尽管其疗效远不如切除手术,但它可以缓解症状,改善患者生活质量,延长生存时间[8],而且可以为部分患者创造化疗、放疗的机会[9-10]。
内镜及经皮经肝胆道支架置入术是临床减黄最常见方式,两种方式都能很好地改善肝功能、减轻黄疸。然而对于两种方式的利弊,临床争论还很大。本文通过对比研究发现,内镜组术后胆道感染显著高于经皮组,内镜组20例,高达56.3%,Cheng等[11]报道用7~10Fr内支撑管早期胆管炎并发率高达30%,与本文结果相似。造成这种情况的原因可能是内镜术后行造影的同时加重了胆道压力,尽管ERCP后可以进行较为充分的引流,但是其管腔狭小,引流管够不到或者侧孔堵塞的情况是很常见的,三级胆管和分支小胆管引流不畅,加重了胆系感染。如放置金属支架则有可能压迫对侧胆管,加重胆系感染,有可能造成肝胆管化脓,甚至出现严重后果,因此,在左、右肝管相通的情况下,由于对侧肝管的胆汁可以通过支架的网孔,通过左或右肝管置入一个支架就能达到胆汁完全引流。如果左、右肝管不相通,多数的情况下需要左右肝管分别外引流或置入多枚支架治疗。本文内镜组有1例患者,术后10h开始发热38.6℃,最高体温41.5℃,予解热镇痛药及激素对症治疗无明显好转,于术后第3天死亡。
经皮组主要并发症为胆道出血,本组有7例患者出现胆道出血。胆道出血是经皮肝穿刺胆道引流操作较为严重和常见的并发症,其主要原因,包括PTC时误伤肝内血管分支,形成胆血瘘[12];导丝或支架对胆管壁及肿瘤组织的机械性损伤;恶性胆道梗阻造成肝功能损伤,引起凝血物质的合成障碍,导致一些凝血因子减少,表现为出血倾向。如出血量大时,应给予补充血容量和输入红细胞治疗,必要时行数字减影血管造影术,以明确出血部位及原因,本组有1例患者行数字减影血管造影术,明确出血部位后行介入栓塞术后出血停止。本组死亡1例,因腹腔出血严重,抢救无效死亡。
两种治疗方法各有利弊,由于内镜途径相对无创、损伤较少,故对于Ⅰ、Ⅱ、Ⅲ型肝门胆管癌患者应首选内镜途径,不成功者可考虑经皮途径。内镜治疗虽有优势,但也存在较多的并发症[13],而经皮途径可作为内镜治疗失败时的一种弥补性治疗方法。由于Ⅳ型经皮途径成功较内镜组高,因此,对于Ⅳ型建议选择经皮经肝穿刺胆道支架置入术[14]。
总之,肝门胆管癌的姑息治疗方法的合理应用,对改善肝功能、延长患者的生存时间、提高生活质量具有重要意义。由于本研究病例相对较少,今后还需扩大样本进一步研究验证,以期更好地指导临床。
[1]吴瑜,秦鸣放.肝门部胆管癌的诊断和内镜治疗进展[J].中国中西医结合外科杂志,2011,17(4):441-443.
[2]朱宏毅,季福,李可为,等.肝门胆管癌预后的影响因素分析[J].肝胆胰外科杂志,2012,24(2):92-95.
[3]汪谦.不能切除的肝门部胆管癌的外科治疗[J].临床外科杂志,2004,3(12):135-136.
[4]牟洪超,董立军,姜小清.肝门胆管癌26例手术治疗[J].中华肝胆外科杂志,2010,16(1):63-64.
[5]黄志强.肝门部胆管癌外科治疗效果有待提高[J].临床外科杂志,2006,14(2):65-66.
[6]陈曹臻,陈春雷,林晖.双侧内引流治疗晚期肝门胆管癌的临床应用[J].实用医学杂志,2005,21(14):1570-1571.
[7]周宁新,黄志强.肝门胆管癌外科治疗方式的选择和预后[J].腹部外科,1993,6(1):43-45.
[8]黄越海.64例肝门部胆管癌患者的诊治分析[J].重庆医学,2010,39(21):2936-2937.
[9]Shitara K,Ishinguro A,Munakata M,et al.A case of advanced gastric cancer with obstructive jaundice that responded TS-1/CPT-11combinati on therapy after percutaneous transhepatic cho1angio drainage[J].Gan To Kagaku Rynho,2005,32(10):1465-1468.
[10]Matsui T,Kojima H,Kato J,et al.A case report of unresectable gastric cancer that responded to 5-FU plus paclitaxel(FT)therapy[J].Gan To Kagaku Rynho,2004,31(6):939-942.
[11]Cheng JL,Bruno MJ,Bergman JJ,et al.Endoscopic palliation of patients with biliary obstruction caused by nonresectable hilar cholangiocarcinoma:efficacy of self-expandable metallic wall-stents[J].Gastroinstent Endosc,2002,56(1):33-39.
[12]虞希祥,朱国庆,施昌盛,等.高位胆道梗阻介入治疗[J].中华肝胆外科杂志,2010,16(1):30-33.
[13]Jaap J,Kloek S,Niels A,et al.Endoscopic and percutaneous preoperative biliary drainage in patients with suspected hilar cholangiocarcinoma[J].J Gastrointest Surg,2010,14(1):119-125.
[14]彭承宏,程坤.肝门部胆管癌手术方式的正确选择[J].中华消化外科杂志,2012,11(1):11-14.

