气相色谱法分析生物润滑油三羟甲基丙烷脂肪酸三酯的研究
王尔佩 汪 勇 蔡子哲 孙浩洋 唐书泽 Martin J.T.Reaney
(暨南大学食品科学与工程系1,广州 510632)
(加拿大Saskatchewan大学农业与生物资源学院2,Saskatoon S7N5A8)
润滑油在使用、储存和运输等过程中会因泄露、飞溅、蒸发、包装用品中的残留、抛弃不当等原因进入环境。据不完全统计,全世界每年约有500~1 000万吨石油基化学品进入生物圈,即使在润滑剂回收利用率较高(大于60%)的国家,仍有4%~10%的润滑油进入环境[1],仅欧盟每年约有60万吨润滑油进入环境[2]。进入环境的非环境友好型润滑油造成的环境污染已不容忽视,特别是对水生植物和动物造成严重影响,甚至破坏生态平衡。矿物油对地下水的污染长达100年之久,0.1 μg/g的矿物油能降低海中小虾的寿命达20%[3]。
三羟甲基丙烷(trimethylolpropane,TMP)脂肪酸酯不仅具有良好的热稳定性能和低温性能[4],而且具有良好的生物降解性和低毒性等特点[5],是一类环境友好的生物润滑油,可应用于润滑油基础油,通过动植物油来源的脂肪酸甲酯和TMP酯交换反应得到[6-7]。在三羟甲基丙烷脂肪酸酯中,三羟甲基丙烷脂肪酸一酯(trimethylolpropane fatty acid monoester,TFAME)和三羟甲基丙烷脂肪酸二酯(trimethylolpropane fatty acid diester,TFADE)的游离羟基导致产品的热稳定性下降[9],三羟甲基丙烷脂肪酸三酯(trimethylolpropane fatty acid tiester TFATE)质量分数高的基础油品质较高,为有效的监测产品质量,建立快速准确分析TFATE的方法尤为重要。
TFATE的分析可以用薄层色谱法(TLC)、高效液相色谱法(HPLC)和气相色谱法(GC)等。TLC操作设备简单,但是精度不高[8];使用 HPLC分析TFATE操作比较复杂,分析成本较高,溶剂选择非常困难,且出峰重叠[9];GC具有灵敏度高、时间短、进样量小、高效等优点。本研究选择非极性二甲基聚硅氧烷固定相毛细管柱(DB-1ht),采用高温气相色谱程序升温法,不需要对样品进行衍生化,通过自制TFATE标准样品,建立TFATE的标准曲线,达到快速准确分析和检测反应混合物及最终纯化产品中TFATE的目的,为进一步研究合成反应,奠定分析检测基础。
1 材料与方法
1.1 材料与仪器
GC-7820A气相色谱仪(配7693A自动进样器)、GC-5975C气相色谱质谱联用仪、毛细管柱(DB -1ht型,15 m × 250 μm × 0.1 μm)、毛细管柱(DB -Wax型,10 m ×100 μm ×0.2 μm):美国安捷伦公司;MD-80型分子蒸馏设备:广州汉维有限公司;SIL GF254硅胶板:青岛海洋化工有限公司;棕榈油(熔点42℃):广州市至润油脂食品工业有限公司;三羟甲基丙烷:分析纯。正己烷:色谱纯;其他试剂均为分析纯。
1.2 试验方法
1.2.1 三羟甲基丙烷脂肪酸酯混合物的合成
以碳酸钾为催化剂,催化剂与TMP物质的量比0.075∶1,FAME 与 TMP 物质的量比 4∶1,减压至真空度0.095 MPa,128℃反应1 h,反应结束后使用过量磷酸中和碳酸钾,用热水(80℃)水洗2~3次,旋转蒸发除去剩余水分得到酯交换产物。
1.2.2 TFATE 标准样品的制备
TFATE标准样品通过分子蒸馏和柱层析制备,方法如下:将酯交换产物进分子蒸馏进料罐,脱水脱气后在蒸馏柱温165℃、压力0.3 Pa、刮膜转速250 r/min下分子蒸馏除去脂肪酸甲酯和TFAME,收集重相(主要成分为TFATE和TFADE)。取重相1.00 g溶解在20 mL的正庚烷/乙酸乙酯(95∶5,体积比)中,然后溶液上硅胶柱(<1.5 cm ×30 cm),用200 mL的正庚烷/乙酸乙酯(95∶5,体积比)洗脱收集TFATE,TFATE标准样品用旋转蒸发真空下脱溶剂,得到TFATE标准样品。标准样品的纯度通过薄层色谱(TLC)和GC-MS鉴定纯度。TLC展开剂为正庚烷/乙酸乙酯(95∶5,体积比),通过紫外显色。
1.2.3 棕榈油脂肪酸甲酯的分析
棕榈油脂肪酸甲酯通过GC-MS分析,分析条件为[10]:毛细 管柱(DB - Wax 型,10 m × 100 μm ×0.2 μm),进样器温度240℃,FID检测器温度240℃,燃烧气H2流量30 mL/min,空气流量300 mL/min,进样量为1.0 μL,载气为氦气。初始温度100℃,以100℃/min的速率升温至220℃,保持2 min;60℃/min升到 240 ℃,保持 4 min。进样量 1.0 μL,分流比30∶1,恒速模式,总流量 139 mL/min,分流流量 132 mL/min,隔垫吹扫流量132.23 mL/min。质谱方法:四极杆质谱,离子源温度:230℃。溶剂延迟时间:2 min;扫描方式:全扫描;扫描范围:40~500 amu。
1.2.4 TFATE标准样品的GC-MS分析
将 TFATE 标准样品配成10.0 μg/μL 的样品,使用GC-MS进行分析,GC-MS条件为:毛细管柱(DB -1ht型,15 m ×0.25 mm ×0.1 μm),进样器温度380℃,FID检测器温度400℃,燃烧气H2流量30 mL/min,空气流量300 mL/min,载气为氦气。初始温度50℃保持0 min,以50℃/min升至220℃保持0 min,以30℃/min升至290℃保持0 min,以40℃/min升至330℃保留2 min,以30℃/min升至370 ℃保留3 min;进样量1.0 μL,分流比30∶1,恒速模式,总流量139 mL/min,分流流量132 mL/min,隔垫吹扫流量132.23 mL/min。质谱方法:四极杆质谱,离子源温度:230℃。溶剂延迟时间:2 min;扫描方式:全扫描;扫描范围:40~1 050 amu。
1.3 TFATE 分析
1.3.1 标准曲线绘制
将各标准品配成 20.0、10.0、5.0、2.5、1.0、0.5 μg/μL的标准溶液,用气相色谱分析不同质量浓度的标准溶液,色谱条件为:色谱柱:DB-1ht(15 m×0.25 mm ×0.1 μm);进样量 1 μL,进样口:380 ℃,分流比20∶1;FID检测器:400℃;柱温:起始50℃以50℃/min升至220℃,以30℃/min升至290℃,以40℃/min升至330℃保留2 min,以30℃/min升至370℃保留3 min;载气:高纯氮气,4.41 mL/min;空气:300 mL/min;氢气:30 mL/min。以标准溶液质量浓度为横坐标,各物质特征峰面积为纵坐标做标准曲线。
1.3.2 样品组成的分析测定
分别将酯交换产物、分子蒸馏重相配成10.0 μg/μL的样品溶液,分析各样品组成,通过标准曲线得到样品中TFATE的质量分数,每个样品测定3次求得平均值。
1.3.3 加样回收
将酯化产物配成10.0 μg/μL的样品溶液(A),与其他一定质量浓度的标准溶液(B1、B2、B3、B4)分别按一定比例配成待测定样品,测定各样品中目标物质的质量浓度,分别计算加样回收率和RSD。
2 结果与讨论
2.1 标准曲线及加样回收
通过GC-MS分析对棕榈油脂肪酸甲酯组成进行定性,其主要成分有豆蔻酸甲酯,棕榈酸甲酯,硬脂酸甲酯,油酸甲酯,以及亚油酸甲酯(见表1)。
TFATE标准样品的GC图谱见图1。可以看出,标准样品中都只有TFATE的峰。通过TLC展开分析,再经过紫外显色也只能观测到TFATE的斑点。再经过GC-MS检测在标准样品中没有发现FAME、TFAME和TFADE的分子离子流,从而证明了制备的标准样品的高纯度。

表1 棕榈油脂肪酸甲酯GC-MS分析的成分及质量分数

图1 棕榈油TFATE标准样品的GC图谱
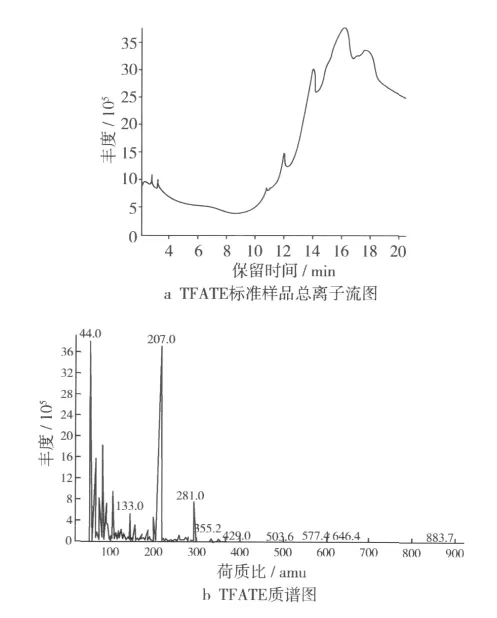
图2 棕榈油TFATE标准样品组分的总离子流图和质谱图
通过GC-MS按照出峰时间以及分子离子峰的质荷比数值可以准确有效地分析酯交换反应产物及其分子蒸馏产物中TFATE的成分。四极杆质谱灵敏度高,通过选择适当的离子可使干扰组分不被采集,实现检测的特异性。由图1可以看出,标样TFATE保留时间在9~11 min,GC根据三羟甲基丙烷脂肪酸三酯中脂肪酸基团的碳原子数量分离不同脂肪酸组成的TFATE,碳原子总数相同的TFATE分子同时出峰,例如,TMP与三分子棕榈酸甲酯(C16)反应产生TFATE 48,TMP与两分子棕榈酸甲酯(C16)和一分子油酸甲酯(18∶1)反应为TFATE 50,如TFATE的离子流图如图2a所示,大部分集中在9 min以后,这与GC的出峰一致。与文献[9]对比,保留时间在9~11min的成分是碳数在46~54的 TFATE,其中TFATE50和TFATE52为主要成分,选取的各组分的质谱图如图2b所示,由于TFATE分子量较大,未发现分子离子峰,但是可以观测到m/z为281的油酸的碎片峰。
建立了TFATE标准物的标准曲线,利用外标法对各标准物进行定量分析,在进样量为1 μL时,质量浓度0.5~20.0 mg/μL范围内均具有很好的线性关系(线性方程 y=6 773 975.895x-72 570 283.654,线性系数 R2=0.997 5)。酯交换产物溶液(A)与一定质量浓度的标准溶液(B)按一定比例配成不同质量浓度的溶液,通过分析测定得到不同质量浓度TFATE标准品平均加样回收率分别在96.64%~98.06% 之间,RSD(相对标准偏差)在0.20%~0.45%之间,具体分析测定结果见表2。RSD和加样回收率数据表明,本方法对TFATE分析有良好的精密度和重复性。
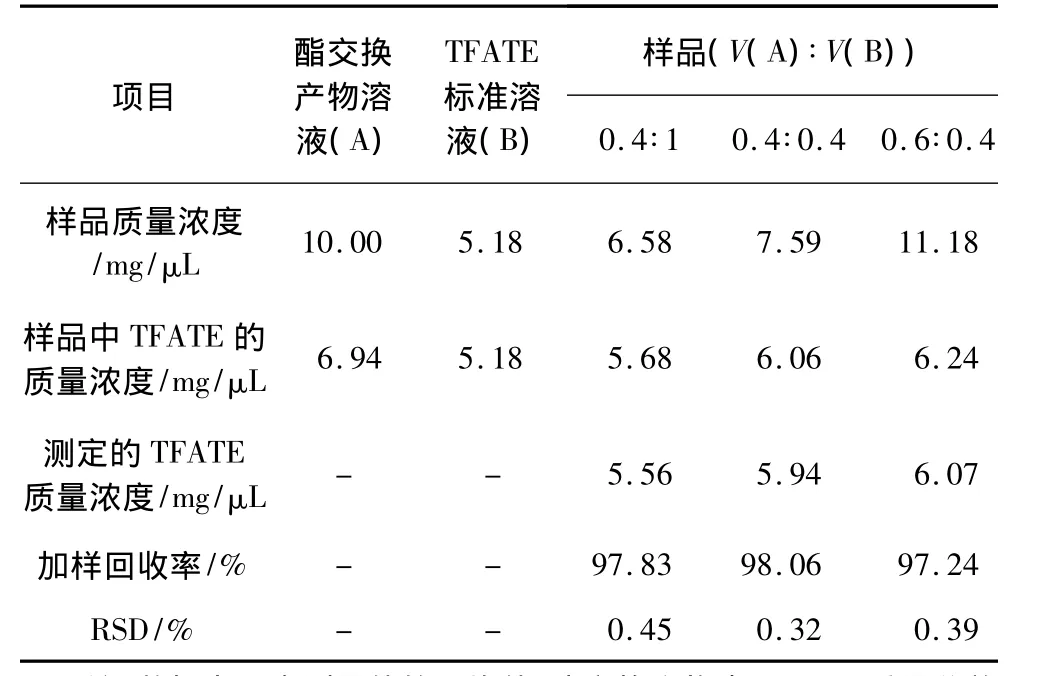
表2 TFATE标准品加样回收率
2.2 酯交换产物中TFATE质量分数的测定
通过以上建立的方法分别测定酯交换产物、分子蒸馏分离酯交换产物的重相中的TFATE的质量分数,结果见表3,GC色谱图见图3~图4。
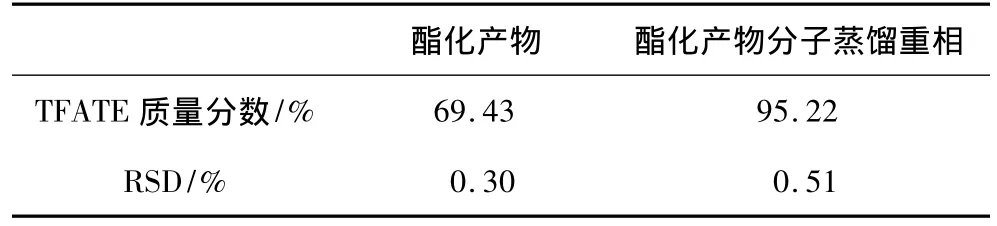
表3 本方法测定的不同样品TFATE质量分数
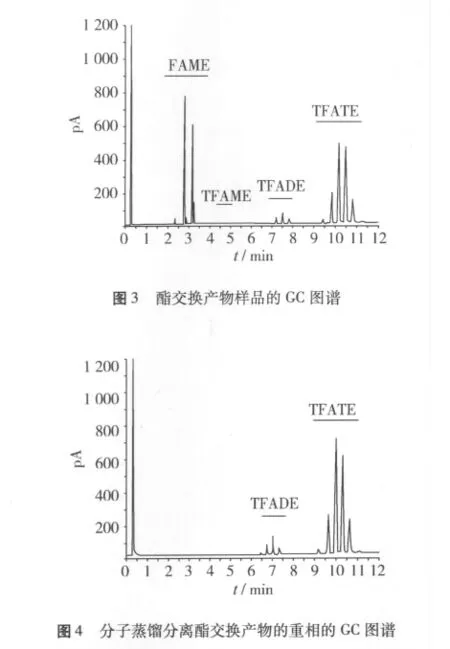
研究结果表明,FAME和TMP的酯交换反应主要生成了TFADE和TFATE,在蒸馏柱温165℃、压力0.3 Pa、刮膜转速250 r/min的条件下分子蒸馏后,TFATE和TFADE主要存在于重相中,其中TE质量分数为95.22%,ME和酯交换反应体系中过量的FAME主要存在于轻相。可见,分子蒸馏能够除去TMP脂肪酸酯混合物中的FAME和TFAME,得到纯度较高TFATE,本研究建立的方法能够准确测定酯交换反应合成目标产物TFATE,可望应用于监控新型生物润滑油中的酯交换反应。
3 结论
3.1 采用分子蒸馏和柱层析的方法制备了棕榈油TFATE的标准样品,通过GC-MS和TLC分析该标准样品中无FAME、TFAME和 TFADE组分,TFATE纯度高。
3.2 TFATE的标准曲线和加样回收试验表明,在质量范围0.5~20.0 μg内峰面积与被测物质量浓度线性关系良好,平均加样回收率在96.64%~98.06%之间,RSD在0.20%~0.45%之间,该方法对TFATE分析有较好的精密度和重复性。
3.3 建立的气相色谱分析方法可以准确测定酯交换反应合成的TMP脂肪酸酯混合物中TFATE质量分数的变化,可测定酯交换反应产物及其分子蒸馏产物的组成从而达到监测产品质量的目的。
[1]Martin V.Biodegradability of lubrication base stucks and fully formalated products[J].Synthetic Lubricants,1995,12(3):215-230
[2]冯克权.可生物降解的润滑油[J].合成润滑材料,1996(2):21-26
[3]陈波水,方建华,李芬芳.环境友好润滑剂[M].北京:中国石化出版社,2006:2-3
[4]颜志光.润滑材料与润滑技术[M].北京:中国石化出版社,2000:160-168
[5]Wanger H,Lutheer R,Mang T.Lubricant base fluids based on renewable raw materials,Their catalytic manufacture and modificatuion[J].Synthetic Lubricants,2001,221(1 - 2):429-442
[6]Salimon J,Salih N,Yousif E.Biolubricants:Raw materials,chemical modifications and environmental benefits[J].European Journal of Lipid Science and Technology,2010,112:519-530
[7]郭晓昕,周永红,张猛,等.三羟甲基丙烷类酯的合成及应用进展[J].广州化工,2010,38(1):19 -22
[8]Basu H.N.,Robley E.M.Norris M.E.Preparation of glycol derivatives of partially hydrogenated soybean oil fatty acids and their potential as lubricants[J].Ibid,1994,71:1227 -1230
[9]Yunus R,Lye O T,Fakhru’l- Razi A,et al.A simple capillary column GC method for analysis of palm oil-based polyol esters[J].Journal of the American Oil Chemists Sociery,2002,79(11):1075 -1080
[10]蔡子哲,汪勇,王丽丽,等.鱼油脂肪酸组成气相色谱法快速分析条件优化研究[J].农业机械,2011,29:75-79.

