广东凉茶颗粒苷类化学成分研究*
王志芳,符 崖,向 俊,黄兆胜,张中强,宋化灿,钟 莹,张翠仙
(1.广州中医药大学中药学院,广东广州 510006;2.广州中医药大学第二附属医院,广东广州 510120;3.中国广州分析测试中心广东省分析测试技术公共实验室,广东广州 510070)
广东凉茶颗粒 (王老吉)是由10味中药按照不同比例组成 (岗梅、山芝麻、五指柑、淡竹叶、木蝴蝶、布渣叶、火炭母、金沙藤、广金钱草、金樱根)。其味甜、苦,具有清热解暑,去湿生津的功效,用于四时感冒,发热喉痛,热积滞,口干尿黄。自2006年广东凉茶成功申请国家非物质文化遗产,使其在国内外盛销。然而目前国内外关于凉茶物质基础及质量标准研究相关报道甚少[1]。为充分开发凉茶国际市场、药效物质基础及谱效结合指纹图谱,本课题组采用正反相硅胶、凝胶等多种现代色谱分离技术对广东凉茶颗粒 (王老吉)甲醇提取物乙酸乙酯相进行了系统研究,从中分离得到5个化合物,采用物理常数对照和现代波谱分析方法确定其结构分别为:4-p-香豆酸-D-吡喃葡萄糖苷 (1)、2α,3α,19α-三羟基乌苏-12-烯-28-酸 28-O-β-D-吡喃葡萄糖苷 (2)、2α,3β,19α-三羟基乌苏-12-烯-28-酸 28-O-β-D-吡 喃 葡萄 糖 (3)、2α,3β,19α,23-四羟基乌苏-12-烯-28-酸 28-O-β-D-吡喃葡萄糖苷 (4)、木犀草素-6-C-葡萄糖苷 (5)。化合物1为首次从自然界中分离得到的天然产物,且首次报道其NMR数据。文献查阅表明,化合物1为苯乙醇苷类化合物的生源前体[2-3]。苯乙醇苷类化合物具有保肝、抗氧化、免疫调节、增强记忆、抗衰老等广泛的生物学活性[4],但此化合物的药理活性还有待于进一步验证。1,2,3,4,5均首次从广东凉茶颗粒中分离得到,为进一步研究其药效及药理活性打下基础。

图1 广东凉茶中分离得到的苷类成分Fig.1 Glycosides from Guangdong Liangcha
1 结果与讨论
化合物1,淡黄色针晶 (MeOH),FeCl3反应阳性,提示1可能为芳香酚酸类化合物;Molish反应阳性暗示其为苷类。ESI-MSm/z:325[MH]-结合 NMR数据 (1×CH2,11×CH,3×C)确定化合物1分子式为C15H18O8,不饱和度为7。NMR显示1有1个酯羰基 [δC169.2/169.1(s)],1个对位取代的芳香环 [(δH7.44(2H,dd,J=2.0,8.0 Hz),6.82(2H,dd,J=2.0,8.0 Hz)]和 [δC161.2(s),146.7/146.7(d),131.1(d),127.1(s),116.8(d)],1个反式共轭双键 [δH7.62(1H,d,J=16.0 Hz),6.33(1H,d,J=16.0 Hz)和 δC146.7/146.7(d),115.0/114.9(d)],说明1存在典型苯丙素结构单元。同时NMR还显示1明显存在糖的端基信息:δH5.80(1H,d,J=4.0 Hz)和δC98.2(d)和94.0(d)。
将化合物1进行酸水解,糖的GLC分析结果表明该化合物所含的糖为D-葡萄糖。将化合物1中糖的NMR数据与肉苁蓉苷Cistanoside F相对应糖的NMR数据 (见图2,结构特征:由E-Δ7,8-3,4-二羟基-苯丙酰基 (即咖啡酰基)、葡萄糖和鼠李糖组成,鼠李糖与葡萄糖的3位连接)对照[5],基本一致,故确定1为4-p-香豆酸-D-吡喃葡萄糖苷[6-7]。
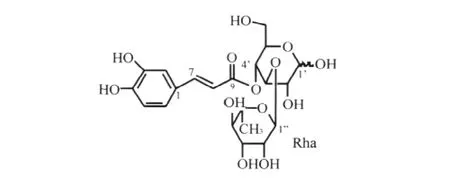
图2 肉苁蓉苷cistanoside F结构示意图Fig.2 Structure of cistanoside F

表1 化合物1和cistanoside F糖部分13C NMR数据 (CD3OD)Table 1 13C NMR analysis of glucose 1 and cistanoside F(CD3OD)
化合物2,白色针状结晶 (CHCl3-MeOH),θmp230~232℃;φ=5%硫酸乙醇溶液显蓝色斑点,Libermann-Burchard和Molish反应均为阳性。ESI-MSm/z673[M+Na]+,结合1H NMR、13C NMR和DEPT谱 (7×CH3,9×CH2,12×CH和8×C)确定化合物2分子式为C36H58O10,不饱和度为8。1H NMR共显示7个-CH3信号峰,分别为δH0.92、1.05、1.22、1.26、1.38、1.61(each 3H,s)和 1.08(3H,d,J=6.4 Hz)。另外 δH5.40(1H,br.s)及δC139.4(s)和128.6(d)说明化合物2存在1个双键。δC177.2(s)提示含有羰基碳,除此外无任何不饱和度信息,提示该化合物可能为熊果烷型三萜。δH6.30(1H,d,J=8.0 Hz)和δC96.0(d)为一典型糖的端基信息,说明2为含有1个糖的皂苷类化合物。同时C-28化学位移值为δC177.2,说明其为酯苷键。将2进行酸水解,糖的GLC分析结果表明该化合物所含的糖为β-D-葡萄糖。将2的NMR数据与文献[8]对照基本一致,确定2为2α,3α,19α-三羟基乌苏-12-烯-28-酸28-O-β-D-吡喃葡萄糖苷。经文献检索发现2首次从广东凉茶颗粒中分离得到。采用HPLC-MS方法与单味药化学成分对比研究发现,其可能来源于金樱根。
化合物3,白色针状结晶 (MeOH),θmp219~221℃;φ=5%硫酸乙醇溶液显蓝色斑点,Libermann-Burchard和Molish反应均为阳性。ESI-MSm/z673[M+Na]+结合13C NMR和DEPT谱 (7×CH3,9×CH2,12×CH和8×C)确定3分子式为C36H58O10,不饱和度为 8。1H NMR共显示 7个-CH3信号峰,分别为 δH1.67,1.40,1.26 1.21,1.08,1.06(each 3H,s)和1.09(3H,d,J=5.6 Hz)。另外 δH5.02(1H,br.s)及 δC139.4(s)和128.5(d)说明化合物3存在1个双键。δC177.1(s)提示含有羰基碳,除此外无任何不饱和度信息,提示该化合物可能为熊果烷型三萜。δH6.30(1H,d,J=8.0 Hz)和δC96.0(d)为糖的端基信息,说明3也为含有1个糖的皂苷。将3的NMR数据与2对照,发现除了C-3的化学位移值明显想低场移动4.5外[3:δC84.0(d,C-3);2:δC79.5(d,C-3)],其他基本一致,将3的NMR数据与文献[9]对照基本一致,故确定3为2α,3β,19α-三羟基乌苏-12-烯-28-酸 28-O-β-D-吡喃葡萄糖苷。经文献检索发现3首次从广东凉茶颗粒中分离得到。采用HPLC-MS方法与单味药化学成分对比研究发现,其可能来源于金樱根。
化合物4,白色粉末 (CHCl3-MeOH),θmp271~272℃,φ=5%硫酸乙醇溶液显蓝色斑点,Libermann-Burchard和Molish反应均为阳性,ESI-MSm/z:689[M+Na]+;结合1H NMR、13C NMR和DEPT谱 (6×CH3,10×CH2,12×CH和8×C)确定4分子式为C36H58O11,不饱和度为8。1H NMR共显示6个-CH3信号峰,分别为δH0.71,0.78,1.21,1.30,1.34(each 3H,s)和 1.04(3H,d,J=4.0 Hz),另外 δH5.50(1H,br.s)及δC139.7(s)和129.5(d)说明4存在1个双键。δC178.6(s)提示含有羰基碳,除此外无任何不饱和度信息,提示该化合物可能为熊果烷型三萜。δH5.33(1H,d,J=6.8 Hz)和 δC95.8(d)为一典型的糖的端基信息,说明4也为含有1个糖的三萜皂苷。将4的NMR数据与3对照,发现少了一个甲基信息 [δC29.5(q,C-23)]而增加了一个羟甲基信息 [δC66.6(t,C-23)],其他基本一致。将4的NMR数据与文献[8]对照基本一致,故确定4为2α,3β,19α,23-四羟基乌苏-12-烯-28-酸 28-O-β-D-吡喃葡萄糖苷。经文献检索发现4首次从广东凉茶颗粒中分离得到。采用HPLC-MS方法与单味药化学成分对比研究发现,其亦可能来源于金樱根。
化合物5,淡黄色粉末 (MeOH),AlCl3、盐酸-镁粉反应阳性,暗示5为黄酮类化合物。NMR端基碳信息δC73.1(d),说明5可能是碳苷类化合物,同时MS中m/z299[M-149]-进一步提示5为碳苷类化合物[10]。ESI-MSm/z:447[M-H]-结合NMR谱 (1×CH2,10×CH和10×C)确定化合物5分子式为C21H20O11,不饱和度为12。NMR中δH6.87(1H,s),6.67(1H,s)为黄酮类化合物H-3和H-8的典型特征信息。δC183.0(s)为黄酮类化合物4位羰基典型特征。而δH7.86(1H,d,J=2.0 Hz),7.49(1H,dd,J=8.0,1.6 Hz),7.27(1H,d,J=8.4 Hz)显色 B环为3',4'-二氧取代的黄酮类化合物。δH5.83(1H,d,J=9.6 Hz,Glc-1″)和 δC110.2(s)为典型的C-6取代的黄酮碳苷类化合物特征。将其NMR数据与文献报道木犀草素-6-C-葡萄糖苷对照[11],基本一致。故鉴定5为木犀草素-6-C-葡萄糖苷。经文献检索发现此化合物首次从广东凉茶颗粒中分离得到。采用HPLC-MS方法与单味药化学成分对比研究发现,其可能来源于广金钱草。
2 实验部分
2.1 材料与仪器
北京泰克光学仪器厂X-6型熔点仪 (熔点未矫正);旋光由德国POLARTRONIC H H W5 polarimeter(SCHMIDT+HAENSCH,Germany)测定;NMR数据由瑞士Bruker公司 AVANCE AV 400超导核磁共振仪测试;质谱由美国 Finnigan公司LCQDECAXP高效液相色谱-质谱联用仪测试完成;旋转蒸发仪 (RE2010,巩义市予华仪器有限责任公司);电子分析天平 (AUY120,广州湘仪机电设备有限公司);凝胶为Sephadex LH-20(日本YMC);柱层析硅胶 (200~300目)为青岛海洋化工有限公司生产;所有溶剂、试剂均为广州化学试剂厂产品 (分析纯)。
广东凉茶颗粒 (广州王老吉药业股份有限公司批号:1002037)。
2.2 提取与分离
广东凉茶颗粒 (10 kg),经甲醇渗漉提取,减压回收甲醇,得深黄褐色浸膏 (1.18 kg)。浸膏用蒸馏水捏溶,依次用石油醚 (PE)、乙酸乙酯(EtOAc)、正丁醇 (n-BuOH)萃取,萃取液减压浓缩得 PE相 (5 g),EtOAc相 (51.5 g),n-BuOH相 (188.0 g)和H2O相 (500 mL)。
乙酸乙酯部位 (51.5 g)进行硅胶 (200~300目)柱层析。以极性逐渐增加的氯仿-甲醇溶剂体系 (V(EtOAc)∶V(MeOH)=19∶1,17∶3,7∶3,6∶4,1∶1,4∶6,2∶8,0∶100)洗脱。TLC 跟踪,得到14个流分 (Fr1至Fr14)。流分Fr-6经硅胶 (200~300目)柱层析 (V(CHCl3)∶V(Acetone)=3∶2)和凝胶柱层析 (洗脱剂V(CHCl3)∶V(MeOH)=1∶1)的化合物 2(30 mg)、3(20 mg);流分Fr-7经硅胶 (200~300目)柱层析 (V(EtOAc)∶V(MeOH)=15∶1)和凝胶柱层析 (洗脱剂V(CHCl3)∶V(MeOH)=1∶1)的化合物1(15 mg);流分Fr-8经硅胶(200~300目)柱层析 (V(CHCl3)∶V(MeOH)=6∶1)和凝胶柱层析 (洗脱剂V(CHCl3)∶V(MeOH)=1∶1)的化合物4(25 mg);流分Fr-9经硅胶 (200~300目)柱层析 (V(PE)∶V(EtOAc)∶V(MeOH)=2∶2∶1)和凝胶柱层析(洗脱剂V(MeOH)∶V(H2O)=7∶3)的化合物5(15 mg)。
2.3 化合物酸水解
化合物 (1和2各5 mg)用φ=9%HCl水溶液在90℃条件下水解5 h,反应结束后冷却。反应液冷冻干燥,用吡啶溶解,添加氯化L-半胱氨酸甲基酯60℃条件下硅醚化,反应液离心后取上清液用GLC检测。
2.4 化合物的物理常数及波谱数据
化合物1:淡黄色针晶 (MeOH),ESI-MSm/z:325[M -H]-;1H NMR(400 MHz,CD3OD)δH:7.62(1H,d,J=16.0 Hz),7.44(2H,dd,J=2.0,8.0 Hz),6.82(2H,dd,J=2.0,8.0 Hz),6.33(1H,d,J=16.0 Hz),5.80(1H,d,J=4.0 Hz,Glc-1',4.23~4.54(4H,m);3.98~4.07(1H,m),3.72(1H,dd,J=9.6,9.2 Hz),3.48 ~ 3.58(1H,m);13C NMR(100 MHz,CD3OD)δC:127.1(C -1,s),131.1(C -2,6,d),116.8(C -3,5,d),161.2(C -4,s),146.7/146.7(C -7,d),115.0/114.9(C -8,d),169.2/169.1(C -9,s),98.2/94.0(C -1',d),73.7/72.0(C - 2',d),77.9/76.2(C - 3',d),71.7/70.8(C - 4',d),75.4/74.8(C - 5',d),64.9/64.8(C -6',t)。
化合物2:白色针状结晶 (CHCl3-MeOH),θmp230~232 ℃,[α]+7.8°(c,0.84,MeOH);ESI-MSm/z673[M+Na]+;1H NMR(400 MHz,Pyr-d5)δH:6.30(1H,d,J=8.0 Hz,Glc -1',5.40(1H,br.s),4.20~4.50(6H,m),2.92(1H,s),2.43 ~ 2.51(1H,m),1.61,1.38,1.26,1.22,1.05,0.92(each 3H,s),1.08(3H,d,J=6.4 Hz);13C NMR(100 MHz,Pyr-d5)δC:43.1(C-1,t),66.3(C -2,d),79.5(C -3,d),38.8(C-4,s),48.9(C-5,d),18.8(C -6,t),33.7(C-7,t),41.0(C-8,s),47.8(C-9,d),38.9(C -10,s),24.3(C -11,t),128.6(C-12,d),139.4(C-13,s),42.3(C-14,s),29.6(C-15,t),26.9(C -16,t),48.8(C-17,s),54.6(C-18,d),72.8(C -19,s),42.3(C -20,d),27.2(C -21,t),37.9(C -22,t),29.4(C-23,q),22.5(C-24,q),16.9(C-25,q),17.7(C -26,q),24.7(C -27,q),177.2(C-28,s),26.3(C-29,q),16.9(C-30,q),96.0(C -1',d),74.2(C -2',d),79.1(C -3',d),71.5(C -4',d),79.4(C -5',d),62.6(C -6',t)。
化合物3:白色针状结晶 (MeOH),θmp219~221℃;ESI-MSm/z:673[M+Na]+;[α]+4.1°(c,0.84,MeOH);1H NMR(400 MHz,Pyrd5)δH:6.30(1H,d,J=8.0 Hz,Glc -1',5.55(1H,t,J=3.2 Hz),5.02(1H,br.s),4.20 ~4.51(6H,m),4.04~4.14(2H,m),3.38(1H,d,J=9.6 Hz),2.93(1H,s),2.44~2.52(1H,m),1.67,1.40,1.26 1.21,1.08,1.06(each 3H,s),1.09(3H,d,J=5.6 Hz);13C NMR(100 MHz,Pyr-d5)δC:48.0(C -1,t),68.8(C -2,d),84.0(C-3,d),38.7(C-4,s),56.1(C -5,d),19.2(C-6,t),33.7(C-7,t),40.8(C-8,s),48.2(C-9,d),40.0(C -10,s),24.3(C-11,t),128.5(C -12,d),139.4(C -13,s),42.3(C-14,s),29.3(C-15,t),26.3(C-16,t),48.8(C -17,s),54.6(C -18,d),72.8(C-19,s),42.3(C-20,d),27.2(C-21,t),37.9(C -22,t),29.5(C -23,q),16.8(C -24,q),17.1(C -25,q),17.8(C -26,q),24.7(C-27,q),177.1(C-28,s),26.8(C-29,q),17.6(C -30,q),96.0(C -1',d),74.2(C -2',d),79.1(C -3',d),71.4(C -4',d),79.4(C -5',d),62.5(C -6',t)。
化合物4:白色粉末 (CHCl3-MeOH),θmp271~272℃,[α]+10.2°(c,1.01,MeOH);ESI-MSm/z:689[M+Na]+;1H NMR(400 MHz,CD3OD)δH:5.50(1H,br.s),5.33(1H,d,J=6.8 Hz,Glc-1'),3.79~3.85(1H,m),3.67~3.73(2H,m),3.51(1H,d,J=8.8 Hz),3.26~3.43(9H,m),1.34,1.30,1.21,0.78,0.71(each 3H,s),1.04(3H,d,J=4.0 Hz);13C NMR(100 MHz,CD3OD)δC:48.0(C - 1,t),69.7(C-2,d),78.4(C -3,d),42.9(C -4,s),47.1(C-5,d),19.3(C -6,t),33.5(C -7,t),41.3(C-8,s),47.8(C-9,d),39.0(C-10,s),24.8(C -11,t),129.5(C -12,d),139.7(C-13,s),42.8(C-14,s),29.6(C -15,t),26.5(C -16,t),48.3(C -17,s),55.0(C-18,d),73.7(C-19,s),48.0(C -20,d),25.2(C-21,t),38.3(C -22,t),66.6(C-23,t),13.8(C-24,q),17.7(C-25,q),16.6(C-26,q),24.9(C -27,q),178.6(C -28,s),27.1(C-29,q),17.6(C-30,q),95.8(C-1',d),73.9(C -2',d),78.3(C -3',d),71.2(C -4',d),78.5(C -5',d),62.5(C -6',t)。
化合物5:淡黄色粉末 (MeOH),ESI-MSm/z:447[M -H]-,299[M -149]-。1H NMR(400 MHz,Pyr-d5)δH:14.35(1H,s),7.86(1H,d,J=2.0 Hz),7.49(1H,dd,J=8.0,1.6 Hz),7.27(1H,d,J=8.4 Hz),6.87(1H,s),6.67(1H,s),5.83(1H,d,J=9.6 Hz,Glc - 1″),5.15(1H,t,J=9.6 Hz),4.43~4.56(4H,m),4.18(1H,m);13C NMR(100 MHz,Pyr-d5)δC:164.8(C-2,s),104.1(C-3,d),183.0(C-4,s),157.8(C-5,s),110.2(C-6,s),157.6(C-7,s),94.8(C -8,d),164.8(C -9,s),105.0(C -10,s),119.7(C -1',s),114.8(C -2',d),147.9(C - 3',s),151.8(C - 4',s),117.0(C -5',d),123.0(C -6',d),73.1(C -1',d),75.1(C -2',d),80.7(C -3',d),72.1(C -4',d),83.1(C -5',d),62.9(C -6',t)。致谢:感谢中山大学分析测试中心姚俊华、关山越老师对化合物结构测试工作的支持。
[1]何蓉蓉,姚新生,栗原博.广东凉茶的“泻火”作用与物质基础研究[J].世界科学技术—中医药现代化,2009,11(6):834-839.
[2]吴立军.天然药物药物化学[M].5版.北京:人民卫生出版社,2008:12-13.
[3]PAUL M D.Medicinal Natural Products:A Biosynthetic Approach[M].3rd ed.A John Wiley and Sons Ltd Publication,2009:137 -165.
[4]郑晓坷,刘媛媛,冯卫生,等.天然苯乙醇苷类化合物研究进展[J].中国新药杂志,2009,18(18):2211-2213.
[5]李友宾,李军,李萍,等.臭牡丹苯乙醇苷类化合物的分离鉴定[J].药学学报,2005,40(8):722-727.
[6]VONLEONHARDBIRKOFER, CHRISTELARMGOT KAISER,HORST KOSMOL,et al.D-Glucose- undL-rhamnoseester derp-cumar- und ferulas?ure,liebigs ann[J].Chem,1966,699:223 -231.
[7]VONLEONHARDBIRKOFER, CHRISTELARMGOT KAISER,BARBARA HILLGES,et.al.NMR - spektroskopische untersuchungen von acyl-glykosen,liebigs ann[J].Chem,1969,725:196-202.
[8]SETO T,TANAKA T,TANAKA O,et.al.β - Glucosyl esters of 19α -hydroxyursolic acid derivatives in leaves ofRubusspecies[J].Phytochemistry,1984,23(12):2829-2834.
[9]ZHOU X H,KASAI R,OHTANI K,et al.Oleanane and ursane glucosides fromRubusspecies[J].Phytochemistry,1992,31(10):3642-3644.
[10]WU W,YAN C Y,LI L,et al.Studies on the flavones using liquid chromatography- electospray ionization tandem mass spectrometry[J].Chromatography A,2004,1047:213 -220.
[11]刘卓伟,阙兆麟,叶志文,等.毛鸡骨草地上部分的化学成分[J].中国天然药物,2008,6(6):415-417.

