氧化铝基复合陶瓷人工髋关节初期临床观察
刘庆 田伟 周一新
(北京大学第四临床医学院北京积水潭医院矫形骨科,北京100035)
人工全髋关节置换术是治疗严重髋关节病变的有效方法。陶瓷对陶瓷人工髋关节作为一种假体选择已经取得广泛的认可和可靠的长期疗效[1-5]。近年来,以Biolox®delta为代表的新一代氧化铝基复合陶瓷(alumina-matrix composite ceramic,AMC)人工髋关节假体开始应用于临床。本研究随访观察AMC人工髋关节假体的初期临床疗效,并与同期采用纯氧化铝陶瓷假体的病例进行对比。
1 资料与方法
1.1 临床资料
2010年1月至2012年9月我科共收治人工全髋关节置换患者1160例1186髋。AMC组639例657髋采用氧化铝基复合陶瓷人工LOOIK TYU YHRTY H TI8髋关节假体,即Biolox®delta陶瓷髋,男217例,女422例;年龄15~79岁,平均47.2岁;股骨头缺血坏死376例,髋发育不良继发髋骨关节炎223例,创伤性关节炎10例,强制性脊柱炎20例,髋关节陈旧感染10例;术前髋关节Harris评分20~71分,平均58.9分。对照组521例529髋采用纯氧化铝陶瓷人工髋关节假体,即Biolox®forte陶瓷髋,男241例,女280例;年龄20~83岁,平均53.1岁,术前髋关节Harris评分22~70分,平均58.9分;股骨头缺血坏死288例,髋发育不良继发髋骨关节炎203例,强制性脊柱炎16例,髋关节陈旧感染14例。手术方式和手术假体均经患者知情同意。
1.2 手术方法
手术均采用髋关节后外侧入路。AMC组选用Exceed®假体(Biomet,美国)262例,Pinnacle®假体(Depuy,美国)377例;髋臼假体直径为44~62 mm,平均51.58 mm,股骨头假体直径28~36 mm,平均34.35 mm。对照组选用 Secrufit®假体(Stryker,美国)231 例,Option®假体(Depuy,美国)290例,髋臼假体直径44~58 mm,平均50.98mm,股骨头假体直径28~32mm,平均30.67mm。
1.3 疗效评估
术后3、6、12个月及之后每年1次随访,随访内容为临床资料评估、影像学评估和髋关节Harris评分。
1.4 统计学处理
采用SPSS10.0统计软件,两组病例的术前术后Harris评分、股骨球头直径比较采用t检验,术后并发症发生例数比较采用χ2检验。
2 结果
1160例1186髋全部获得随访,随访时间为3~21个月,平均13.3个月。AMC组末次随访的Harris评分为75~100分,平均96.3分;2例陶瓷内衬碎裂需行翻修手术,无关节异响、假体脱位、假体周围骨溶解、假体松动、感染和异位骨化发生。对照组末次随访的Harris评分为75~100分,平均95.3分;1例陶瓷部件碎裂行翻修手术,1例术后7个月脱位后闭合复位成功,1例术后出现髋关节周围异位骨化Brooker 2级,但关节功能良好,4例关节异响,无假体松动、感染和假体周围骨溶解发生(表1)。
两组术后Harris评分比较无统计学差异;股骨球头直径比较有统计学差异(P<0.001);关节异响发生率比较有统计学差异(P=0.025);其他不良事件的发生率比较无统计学差异。
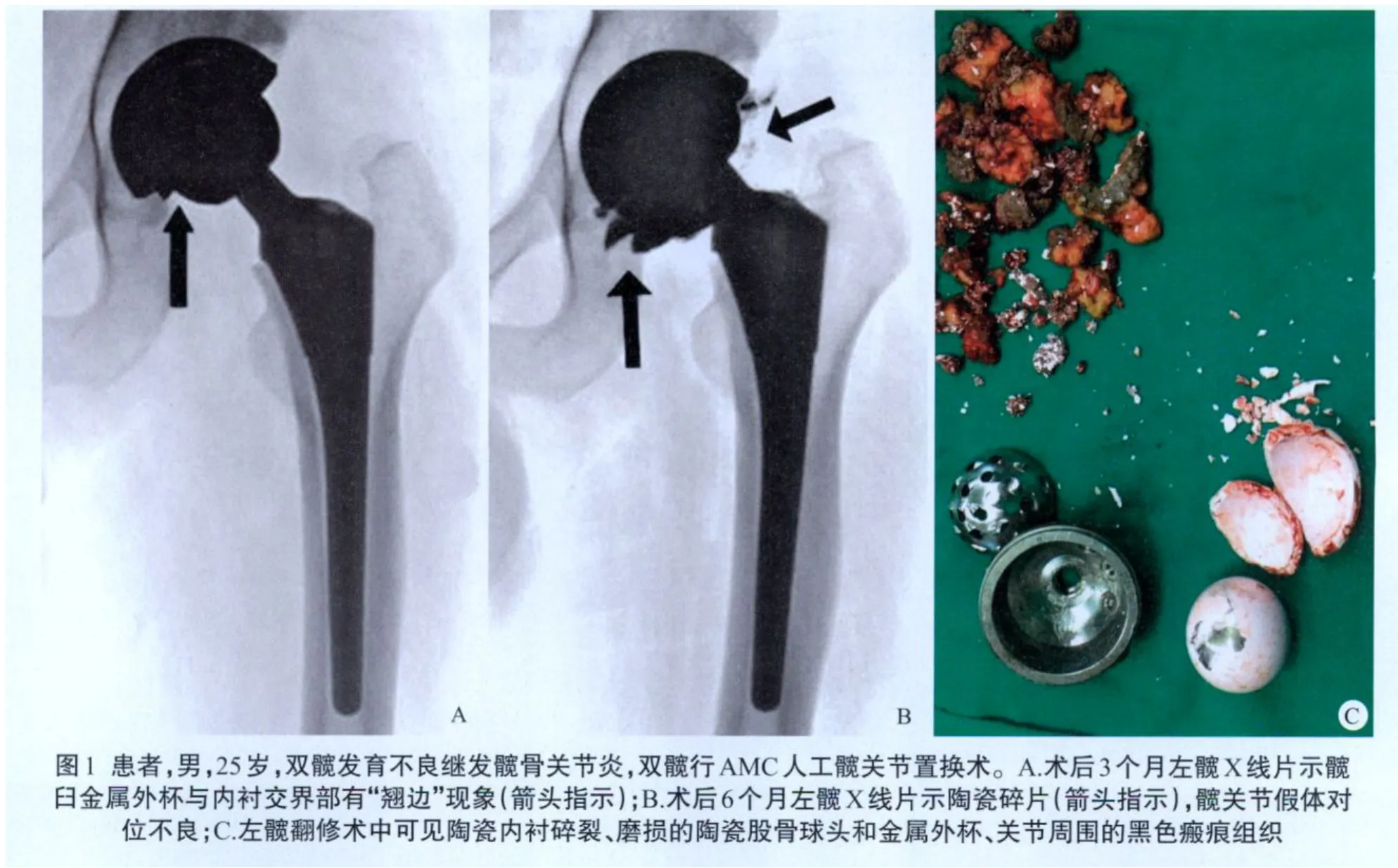
AMC组中2例发生陶瓷内衬碎裂,碎裂前随访X线片均示髋臼金属外杯与内衬交界部有“翘边”现象(图1A);碎裂后均可在X线片上观察到陶瓷碎片及髋关节假体对位不良(图1B),随即进行翻修。发生陶瓷内衬碎裂的2例患者均未受较大外力冲击或扭转作用,碎裂亦无明显疼痛,但即刻出现自觉摩擦感,患肢运动尚可。翻修术中可见陶瓷髋臼内衬严重碎裂散开,关节内大量陶瓷碎屑,髋臼金属外杯内面划伤明显;假体周围可见较多黑色软组织瘢痕,考虑与金属被陶瓷划伤产生的碎屑和陶瓷磨损产生的碎屑有关;陶瓷头刮擦明显,但完整无碎裂(图1C)。
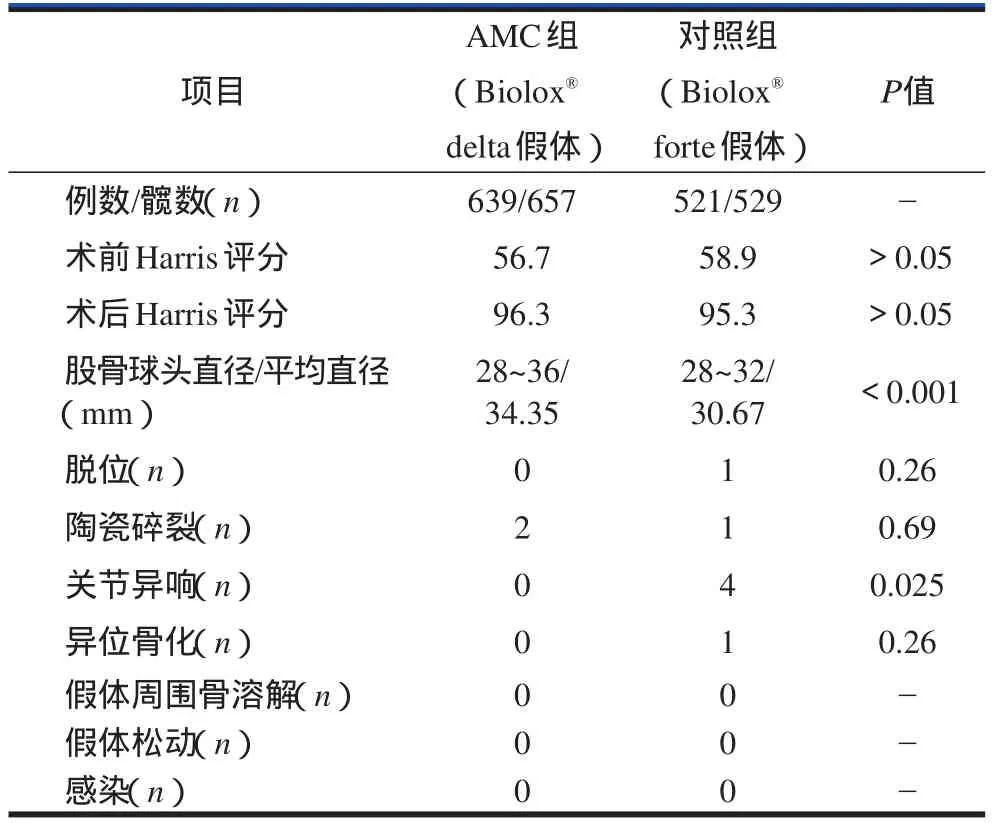
表1 两组的临床资料
3 讨论
陶瓷对陶瓷人工髋关节假体已经取得广泛的认可和可靠的长期疗效,但陶瓷部件的碎裂和关节异响等问题仍在一定程度上限制其在临床上的广泛应用。为改进陶瓷部件的性能,以Biolox®delta为代表的新一代AMC人工髋关节假体开始应用于临床。我国是继欧洲之后较早使用这种陶瓷假体的国家。
氧化铝陶瓷的晶格排列结构与金刚石一样,是一种十分坚硬和稳定的生物学材料。此前用的氧化铝陶瓷假体为黄色陶瓷,即纯度极高的氧化铝陶瓷。Nevelos等[6]测量发现氧化铝陶瓷髋的容积磨损率为40.7 μm3/年,线性磨损率为165.5 μm/年,其特点是硬度高、亲水性好,但同时脆性高,存在一定的碎裂风险。本研究中对照组(Biolox®forte假体)使用的即氧化铝陶瓷假体。Habermann等[7]报告50万例氧化铝陶瓷股骨头假体的碎裂率为0.4‱。因此,这种陶瓷对假体厚度有严格的要求,限制了假体的形状和大小。另外,术后出现关节异响的问题也引起业界的广泛重视[8,9]。
为改进陶瓷部件性能,AMC应运而生。该陶瓷在氧化铝中加入氧化锆、氧化钇等成分作为添加剂,制成氧化锆强韧氧化铝陶瓷(zirconia toughned alumina,ZTA)和氧化钇-氧化锆强韧氧化铝陶瓷(yttria-zirconia toughened alumina,Y-ZTP)[10]。氧化锆陶瓷晶体散布于氧化铝晶格之间,利用其可以在外力作用下改变相态的特性,起到缓冲作用而吸收应力。加入锶和铬等氧化物的氧化铝陶瓷不但具有上述优点,还可以在氧化铝晶体间形成小板样的晶体结构,更好地结合高强度、高韧度与热稳定性,比如Biolox®delta系列复合陶瓷。随着物理性能的优化,陶瓷部件可以被加工成更多形状和更薄,以适应临床上的各种需要,即在达到同样强度要求的前提下,髋臼陶瓷内衬可以更薄,陶瓷球头可以更大,这样的结果令人鼓舞,因为大直径球头人工髋关节受到关节外科医师的偏爱,它可以带来更好的关节活动度和稳定性,改善关节润滑[11]。金属对金属假体曾在一段时间内解决了这一问题,但近年来多项研究报告该假体存在金属离子释放、假体机械学失败和生物力学环境不良等问题[12]。目前已有研究显示,新型AMC假体临床效果优良[13,14]。
AMC假体改进了传统陶瓷易碎裂的问题,其陶瓷部件碎裂和关节异响的国内外报道鲜见,但该假体进入临床时间较短。本研究中AMC组2例陶瓷内衬碎裂,发生率为0.3%,这2例在发生陶瓷部件碎裂之前均可见影像学特征性改变,考虑与内衬在金属外杯发生移位有关,而这种移位又可能与金属外杯植入骨床后发生的形变或金属外杯与陶瓷内衬扣锁部分的形状设计以及这种设计的抗疲劳强度有关。2例陶瓷部件碎裂均为内衬一侧,且均与高能量损伤无关,这与此前认为陶瓷部件需较高冲击力才会碎裂的认识相悖[15],应对陶瓷假体的抗疲劳性能而不是抗冲击强度作进一步研究观察。
本研究结果示,新一代AMC假体的表现令人满意,临床和影像学评估及术后Harris评分均不逊于对照组的高纯度氧化铝陶瓷假体,以下方面还表现出一定的优势:①AMC组的股骨头直径平均为34.35 mm,大于对照组的30.67 mm,有统计学差异(P<0.001),理论上可为患者带来更大的活动度及更稳定的人工髋关节,随访中AMC组无一例发生术后假体脱位,较之小球头髋关节表现出更好的稳定性;②AMC组无一例主诉关节异响,有研究认为陶瓷髋关节术后的关节异响与陶瓷部件的条带磨损有关,而后者又因假体边缘负重所致[16-18]。AMC假体的出现使大直径陶瓷球头的假体配伍得以实现,理论上减少边缘负重的机会和产生条带磨损的条件,以降低关节异响的发生率。
本研究仅报告AMC假体的初期临床效果,并记录研究中发现的问题,希望引起假体使用者的关注。而对于一款假体或一种假体材料的疗效判定尚需长时间的随访观察。
[1]Hamilton WG,McAuley JP,Dennis DA,et al.THA with Delta ceramic on ceramic:results of a multicenter investigational device exemption trial.Clin Orthop Relat Res,2010,(468):358-366.
[2]Oonishi H,Wakitani S,Murata N,et al.Clinical experience with ceramics in total hip replascemet.Clin Orthop Relat Res,2000,(379):77-84.
[3]Heisel C,Silva M,Schmalzried TP.Bearing surface ptions for total hip replacement in young patients.Instr Course Lect,2004,53:49-65.
[4]Prudhommeaux F,Hamadouche M,Nevelos J,et al.Wear of alumina-on-alumina total hip arthroplasties at a mean 11-year follow up.Clin Orhop Relat Res,2000,(379):113-122.
[5]Winter M,Griss P,Scheller G,et al.Ten-to 14-year results of a ceramic hip prosthesis.Clin Orthop Relat Res,1992,(282):73-80.
[6]Nevelos JE,Prudhommeaux F,Hamadouche M,et al.Comparative analysis of two different types of alumina-alumina hip prosthesis retrieved for aseptic loosening.J Bone Joint Surg Br,2001,83(4):598-603.
[7]Habermann B,Ewald W,Rauschmann M,et al.Fracture of ceramic heads in total hip replacement.Archives of Orthopaedic and Trauma Surgery,2006,126(7):464-470.
[8]Walter WL,O'toole GC,Walter WK,et al.Squeaking in ceramic-on-ceramic hips:the importance of acetabular component orientation.JArthroplasty,2007,22(4):496-503.
[9]Keurentjes JC,Kuipers RM,Wever DJ,et al.High incidence ofsqueakinginTHAswithaluminaceramic-on-ceramicbearings.ClinOrthopRelatRes,2008,466(6):1438-1443.
[10]Kuntz M.Validation of a new high performance alumina matrix composite for use in total joint replacement.Seminars inArthroplasty,2006,17:141-145.
[11]Kluess D,Martin H,Mittelmeier W,et al.Influence of femoral head size on impingement,dislocation and stress distribution in total hip replacement.Med Eng Phys,2007,29(4):465-471.
[12]刘庆,张洪,周乙雄,等.髋关节表面置换术后生物力学参数的改变.中国组织工程研究与临床康复,2007,11(27):5281-5284.
[13]Hamilton WG,McAuley JP,Dennis DA,et al.THA with delta ceramic on ceramic:results of a multicenter investigational device exemption trial.Clin Orthop Relat Res,2010,468(2):358-366.
[14]Masson.B.Emergence of the alumina matrix composite in total hip arthroplasty.Int Orthop,2009,33(2):359-363.
[15]Park YS,Hwang SK,Choy WS,et al.Ceramic failure after total hip arthroplasty with an alumina-on-alumina bearing.J Bone Joint SurgAm,2006,88(4):780-787.
[16]Taylor S,Manley MT,Sutton K.The role of stripe wear in causing acoustic emissions from alumina ceramic-on-ceramic bearings.JArthroplasty,2007,22(7 Suppl 3):47-51.
[17]Barrack RL,Burak C,HB.Skinner HB.Concerns about ceramics in THA.Clin Orthop Relat Res,2004,(429):73-79.
[18]Willmann G.Ceramic femoral head retrieval data.Clin Orthop Relat Res,2003,(379):22-28.

