甘遂中激活NF-κB信号通路的化学成分
陈晓珍,张婷婷,2,李国友,方冬梅,张国林,罗应刚*
1中国科学院成都生物研究所,成都 610041;2中国科学院研究生院,北京 100049
常用中药甘遂为大戟科植物甘遂(Euphorbia kansui T.N.Liouex T.P.Wang)的干燥块茎,又名苦泽、干泽,因采掘时易肿手,山西俗称“肿手花根”[1]。该药材主要产于陕西、山西、河南、甘肃、河北、宁夏、内蒙古等地。甘遂苦寒有毒,归肺、肾、大肠经,《神农本草经》记载其具有泻水逐饮的功效,现代药理研究表明其在抗肿瘤、治疗重症胰腺炎等方面具良好疗效[2],临床常用来治疗晚期食道癌、乳腺癌等恶性肿瘤以及哮喘、慢性支气管炎等症。甘遂植物全株有毒,尤其根毒性较大;对皮肤和粘膜有刺激作用,食用过量出现腹痛、下泻、呕吐、脱水、严重时呼吸困难、循环衰竭而死亡,近年来对其化学成分和药理作用的研究不乏报道[3-5]。
NF-κB(Nuclear Factor-kappa B)是涉及机体防御反应、组织损伤和应激、细胞分化和凋亡以及肿瘤生长抑制过程中信息传递的一类重要核因子,它在炎症反应以及肿瘤生长等过程中起着重要作用[6]。临床广泛应用的甘遂具有明显的毒副作用,主要表现在对皮肤、眼睛的刺激作用,促使炎症发生。我们以NF-κB信号通路为炎症测试模型,对甘遂95%乙醇提取物以及各溶剂萃取物进行NF-κB信号通路激活测试。在此基础上,我们发现激活NF-κB信号通路作用最强的部位为非极性部位,因此我们采用GC-MS技术分离、分析并鉴定了该非极性部位中的化学成分并运用峰面积归一化法确定了各成分的相对含量。
1 材料与仪器
甘遂(产地:山西,生产批号:1005114)购于四川新荷花中药饮片公司,由中国科学院成都生物研究所高信芬研究员鉴定为大戟科植物甘遂(Euphorbia kansui T.N.Liou ex T.P.Wang)的块茎。
Hela细胞菌株购于上海工硕生物技术有限公司;pNF-κB-luc(报告基因质粒)、pTNF-α-promoterluc(报告基因质粒)、荧光素酶报告基因检测试剂盒均购于碧云天生物技术研究所;DMEM(高糖)培养液为Invitrogen公司生产的试剂盒。
GC(Focus)-MS(Polaris Q)联用仪(Thermo Scientific);色谱柱为ThermoTR-5ms SQC毛细管柱(30 m ×0.25 mm i.d.,0.25 μmd.f.)。
2 试验方法
2.1 甘遂粗提物、萃取物及非极性部位的制备
将20 kg干燥的甘遂粉碎后,用95%乙醇冷浸3次,每次用乙醇60 L浸泡7 d,将三次冷浸液回收浓缩后得粗提物(915 g)。将粗提物用5 L热水分散后,依次用石油醚、氯仿、乙酸乙酯、正丁醇萃取,每次用溶剂5 L,分别萃取三次。将上述制备的粗提物、各溶剂萃取物用于NF-κB信号通路活性测试。
选取激活作用最强的氯仿萃取物(40 g)进行硅胶柱层析,石油醚:丙酮溶剂系统(10∶1、5∶1、2∶1、0∶1)为洗脱液,TLC检测合并,得C1~C10共10个部位;将得到的各部位进行进一步的激活NF-κB信号通路测试,其中活性最强的为非极性部位C1(15 g)。
2.2 NF-κB 信号通路活性测试
本实验以NF-κB为研究对象,将NF-κB质粒转染到Hela细胞中,再加待测样品到细胞培养液中诱导NF-κB的表达,通过测定荧光素酶报告基因的表达情况来检测NF-κB的表达情况。如果NF-κB的表达增强,则所测得的荧光值相对于阴性对照值大。
2.2.1 Hela 细胞的体外培养
细胞的体外培养参照ATCC公司提供的培养方法操作[7]。
2.2.2 质粒的转染
2.2.2.1 用10%无雌激素血清-无双抗-有酚红的DMEM(高糖)培养基将Hela细胞按2.5×105个/mL密度接种于24孔板,置恒温培养箱中培养24小时,待细胞融合率到70% ~90%时,进行瞬时转染;
2.2.2.2 向 50 μL OPTI-MEM 培养基中加入 0.6 μgpNF-κB-luc+0.2 μg pSV-gal,混匀;将 2μL lipofectamine2000加入50 μL OPTI-MEM 培养基中,静置5 min;按 DNA(μg):Lipofectamine(μL)=0.8∶2的比例,将上述质粒溶液逐滴加入到 lipofectamine2000溶液中,再静置20 min,形成复合物;按2.2.2.1 中每孔 100 μL 的量加入得到的复合物到上述24孔板中进行转染共6 h即得。
2.2.3 样品的活性检测
2.2.3.1 Hela细胞共转染质粒6 h后换成10%无雌激素血清-无双抗-有酚红的DMEM(高糖)培养液,加入各浓度组(1、10、100 μg/mL)样品,每个浓度设3个复孔,并设对照组。
2.2.3.2 培养24小时后弃去细胞培养液,用PBS清洗三次后每孔加入细胞裂解液150 μL。充分裂解细胞后,转入1.5 mL EP管,于10000 rpm离心1 min,并将上清液转入干净EP管,混匀后取50 μL加入荧光素酶底物检测荧光素酶的活性[7]。
2.2.3.3 另取 70 μL 裂解液加入 133 μL ONPG、6 μL Mg2+及400 μL PBS的混合液,混匀后37℃水浴至黄色出现时测OD420。所有实验至少重复3次,每组设置3个复孔,所得结果以表示。
2.3 甘遂激活NF-κB信号通路的非极性部位化学成分的GC-MS分析
气相色谱条件:载气:He,1.0 mL/min;进样口温度:200℃;传输线温度:230℃;程序升温条件:初始温度80℃,保持5 min后以15℃/min的速率升温至150℃;然后以2℃/min的速率升温至260℃;再以20℃/min的速率升温至300℃并保持5 min;进样量:2 μL。
质谱条件:离子源(EI),温度280℃;电子能量为70 eV,扫描质量范围:50~500 amu。
将GC-MS联用分析所得各组分质谱数据,输入计算机谱库(NIST02)进行检索,对拟合指标和质谱数据进一步确认,同时运用峰面积归一化法对各化合物进行定量分析,计算各化学成分的相对含量。
3 结果与讨论
甘遂具有明显的皮肤刺激等毒副作用,我们推测甘遂中可能含有激活NF-κB信号通路的活性成分。首先对甘遂95%乙醇粗提物和各溶剂萃取物进行活性检测,结果表明氯仿萃取物的活性最强(表1);将氯仿萃取物按极性大小分成10段,进一步进行活性测试,结果发现非极性的第一段(C1)活性最强,其它各段也有不同程度激活NF-κB信号通路的活性(表2)。

表1 甘遂95%乙醇粗提物和各溶剂萃取物对NF-κB信号通路的激活情况Table 1 NF-κB signaling pathway activation results of 95%ethanol crude and different solvent-soluble extracts of Kansui
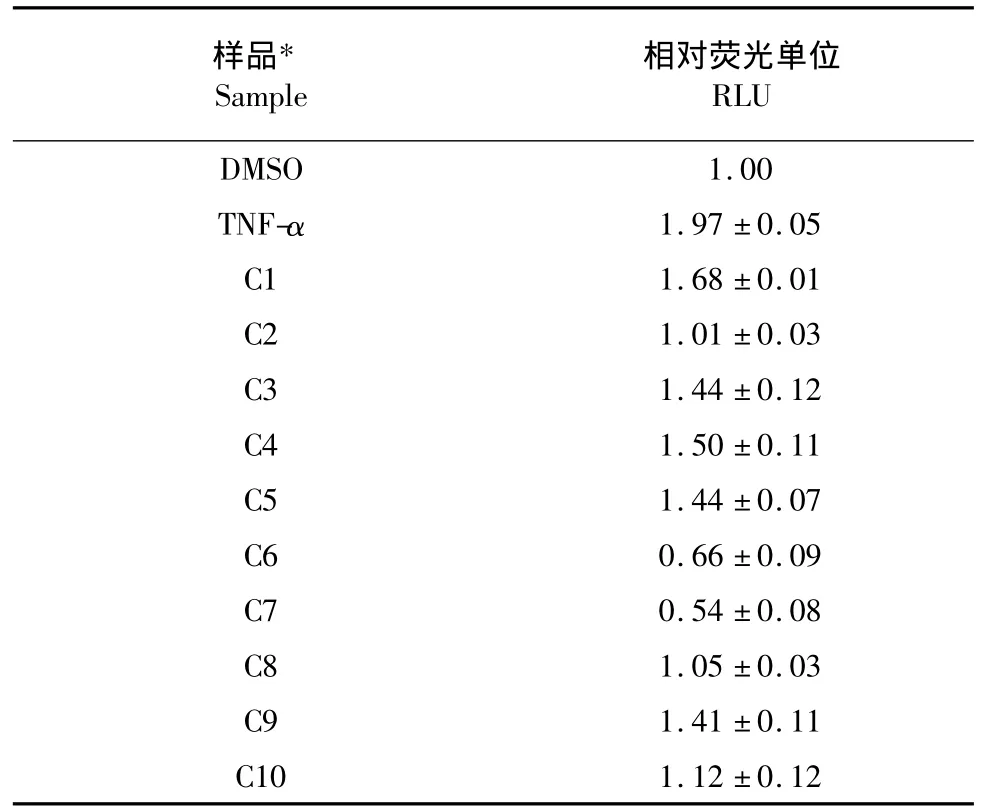
表2 甘遂氯仿萃取物各小段对NF-κB信号通路的激活情况Table 2 NF-κB signaling pathway activation results of sub-fractions of CHCl3-extract of Kansui
对甘遂的非极性部位C1段进行GC-MS分析,从中共分离、鉴定了56个化合物,占总量的99.72%,主要成分为脂肪酸及其衍生物(71.23%)、长链烷烃及其衍生物(13.73%),还有单萜、倍半萜类(7.1%)、芳香族类(3.57%)和脂肪醛(1.12%)等(图1,表3)。
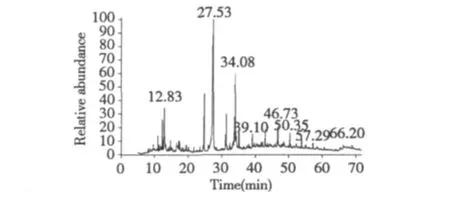
图1 激活NF-κB信号通路的甘遂非极性部位(C1)的GCMS总离子流图Fig.1 GC-MS totalion chromatogramofC1 sub-fraction of CHCl3-extract of Kansui

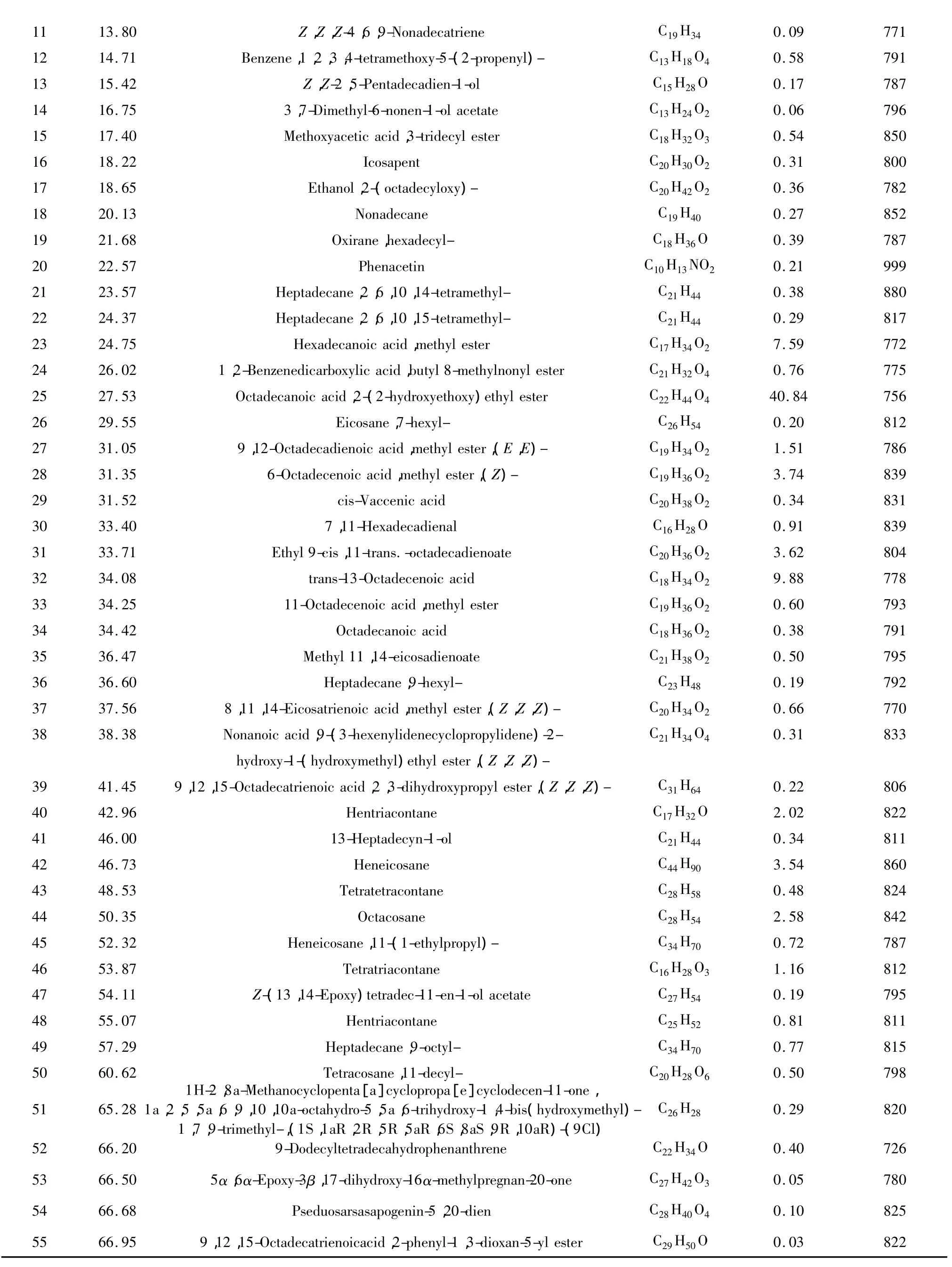
表3 激活NF-κB信号通路的甘遂非极性部位(C1)的化学成分Table 3 Chemical constituents of C1 sub-fraction ofCHCl3extract of Kansui
11 13.80 Z,Z,Z-4,6,9-Nonadecatriene C19H34 0.09 771 12 14.71 Benzene,1,2,3,4-tetramethoxy-5-(2-propenyl)- C13H18O4 0.58 791 13 15.42 Z,Z-2,5-Pentadecadien-1-ol C15H28O 0.17 787 14 16.75 3,7-Dimethyl-6-nonen-1-ol acetate C13H24O2 0.06 796 15 17.40 Methoxyacetic acid,3-tridecyl ester C18H32O3 0.54 850 16 18.22 Icosapent C20H30O2 0.31 800 17 18.65 Ethanol,2-(octadecyloxy)- C20H42O2 0.36 782 18 20.13 Nonadecane C19H40 0.27 852 19 21.68 Oxirane,hexadecyl- C18H36O 0.39 787 20 22.57 Phenacetin C10H13NO2 0.21 999 21 23.57 Heptadecane,2,6,10,14-tetramethyl- C21H44 0.38 880 22 24.37 Heptadecane,2,6,10,15-tetramethyl- C21H44 0.29 817 23 24.75 Hexadecanoic acid,methyl ester C17H34O2 7.59 772 24 26.02 1,2-Benzenedicarboxylic acid,butyl 8-methylnonyl ester C21H32O4 0.76 775 25 27.53 Octadecanoic acid,2-(2-hydroxyethoxy)ethyl ester C22H44O4 40.84 756 26 29.55 Eicosane,7-hexyl- C26H54 0.20 812 27 31.05 9,12-Octadecadienoic acid,methyl ester,(E,E)- C19H34O2 1.51 786 28 31.35 6-Octadecenoic acid,methyl ester,(Z)- C19H36O2 3.74 839 29 31.52 cis-Vaccenic acid C20H38O2 0.34 831 30 33.40 7,11-Hexadecadienal C16H28O 0.91 839 31 33.71 Ethyl 9-cis,11-trans.-octadecadienoate C20H36O2 3.62 804 32 34.08 trans-13-Octadecenoic acid C18H34O2 9.88 778 33 34.25 11-Octadecenoic acid,methyl ester C19H36O2 0.60 793 34 34.42 Octadecanoic acid C18H36O2 0.38 791 35 36.47 Methyl 11,14-eicosadienoate C21H38O2 0.50 795 36 36.60 Heptadecane,9-hexyl- C23H48 0.19 792 37 37.56 8,11,14-Eicosatrienoic acid,methyl ester,(Z,Z,Z)- C20H34O2 0.66 770 38 38.38 Nonanoic acid,9-(3-hexenylidenecyclopropylidene)-2- C21H34O4 0.31 833 hydroxy-1-(hydroxymethyl)ethyl ester,(Z,Z,Z)-39 41.45 9,12,15-Octadecatrienoic acid,2,3-dihydroxypropyl ester,(Z,Z,Z)- C31H64 0.22 806 40 42.96 Hentriacontane C17H32O 2.02 822 41 46.00 13-Heptadecyn-1-ol C21H44 0.34 811 42 46.73 Heneicosane C44H90 3.54 860 43 48.53 Tetratetracontane C28H58 0.48 824 44 50.35 Octacosane C28H54 2.58 842 45 52.32 Heneicosane,11-(1-ethylpropyl)- C34H70 0.72 787 46 53.87 Tetratriacontane C16H28O3 1.16 812 47 54.11 Z-(13,14-Epoxy)tetradec-11-en-1-ol acetate C27H54 0.19 795 48 55.07 Hentriacontane C25H52 0.81 811 49 57.29 Heptadecane,9-octyl- C34H70 0.77 815 50 60.62 Tetracosane,11-decyl- C20H28O6 0.50 798 51 65.28C26H28 0.29 820 52 66.20 9-Dodecyltetradecahydrophenanthrene C22H34O 0.40 726 53 66.50 5α,6α-Epoxy-3β,17-dihydroxy-16α-methylpregnan-20-one C27H42O3 0.05 780 54 66.68 Pseduosarsasapogenin-5,20-dien C28H40O4 0.10 825 55 66.95 9,12,15-Octadecatrienoicacid,2-phenyl-1,3-dioxan-5-yl ester C29H50O 1H-2,8a-Methanocyclopenta[a]cyclopropa[e]cyclodecen-11-one,1a,2,5,5a,6,9,10,10a-octahydro-5,5a,6-trihydroxy-1,4-bis(hydroxymethyl)-1,7,9-trimethyl-,(1S,1aR,2R,5R,5aR,6S,8aS,9R,10aR)-(9Cl)0.03 822
在上述鉴定的化合物中,已有研究表明不饱和 脂肪醛(Z)-7-Hexadecenal和7,11-Hexadecadienal可引起炎症反应,诱发神经退行性疾病和成人呼吸道窘迫症的产生等[8],这两种醛在甘遂非极性部位的含量分别为0.21%和0.91%。该部位中还有少量致癌物质如苯醌类衍生物和邻苯二甲酸酯类化合物[9,10]。在甘遂非极性部位中含量最大的是脂肪酸及酯类衍生物,且以十八碳烯酸和二十碳烯酸为主。这类脂肪酸属于多不饱和脂肪酸,是花生四烯酸的前体物质,在体内炎症反应和免疫调节方面起着重要的作用[11]。一般认为这类成分能够抑制炎症因子的释放,在抗炎方面起着积极作用。按化合物中最后一个双键离甲基端的距离将不饱和脂肪酸分为n-3和n-6两类,研究表明n-3类比n-6类抗炎作用好[12]。但也有研究表明,由于不同细胞中基因和酶的差异,导致花生四烯酸前体物质代谢途径的改变,这类化合物也可能加重炎症反应或者诱发炎症产生[11]。我们还从甘遂非极性部位中鉴定了增加癌症发生几率的化合物Vaccenic acid[12],该化合物的含量约0.34%。
4 结语
我们以NF-κB信号通路为炎症测试模型,对甘遂95%乙醇提取物及其各溶剂萃取物进行了NF-κB信号通路激活测试。在此基础上,我们发现激活NF-κB信号通路作用最强的部位为非极性部位。采用GC-MS技术,我们从中分离、分析并鉴定了该非极性部位中的化学成分。
甘遂非极性部位含有大量促炎成分,这些成分可能激活NF-κB信号通路的表达,从而引起炎症因子的释放,导致炎症。上述研究结果为阐明甘遂的毒效物质基础提供了参考,为有效利用甘遂中的有效成分、祛除其毒副作用成分奠定了基础。
1 Chinese Pharmacopoeia Commission(国家药典委员会).Pharmacopoeia of the People's Republic of China(中华人民共和国药典).Beijing:China Medical Science Press,2010.81-82.
2 Chen L(陈亮),Yu ZM(于志敏).The study of the inhibitory effect of Euphorbia kansui on Hep and S180.Modern Med JChina(中国现代医药杂志),2008,10(7):6-8.
3 Chen L(陈亮).In vitro experimental study of the effect of Euphorbia kansui extract on human BEL-7402.Acta Bot Boreal-Occident Sin(西北植物学报),2008,28:1889-1892.
4 Fan XS(范欣生),Zhu Q(朱荃),Fang TH(方泰惠),et al.Experimental observation on phlegm-removing,anti-asthmatic and anti-inflammatory actions of pill for phlegm retention.J Nanjing Univ Tradit Chin Med(南京中医学院学报),1992,3:152-154.
5 Ge W(葛玮),Ma B(马彬),Yang KH(杨克虎),et al.Kansui root for treating severe acute pancreatitis:asystematic review.Chin J Evid-based Med(中国循证医学杂志),2009,9:964-968.
6 Smith C,Andreakos E,Crawley JB,et al.NF-kappa B-inducing kinase is dispensable for activation of NF-kappa B in inflammatory settings but essential for lymphotoxin beta receptor activation of NF-kappa B in primary human fibroblasts.J Immunol,2001,167:5895-5903.
7 Yang LJ,Chen QF,Wang F,et al.Antiosteoporotic compounds from seeds of Cuscuta chinensis.J Ethnopharmacol,2011,135:553-560.
8 Guillen MD,Goicoechea E.Toxic oxygenated alpha,beta-unsaturated aldehydes and their study in foods:areview.CritRev Food Sci,2008,48:119-136.
9 Matsumoto M,Hirata-Koizumi M,Ema M.Potential adverse effects of phthalic acid esters on human health:areview of recent studies on reproduction.Regul Toxicol Pharm,2008,50:37-49.
10 Lis LB,Bakula T,Baranowski M,et al.The carcinogenic effects of benzoquinones produced by the flour beetle.Pol J Vet Sci,2011,14:159-164.
11 Stulnig TM.Immunomodulation by polyunsaturated fatty acids:mechanisms and effects.Int Arch Allergy Imm,2003,132:310-321.
12 King VR,Huang WL,Dyall SC,et al.Omega-3 fatty acids improve recovery,whereas omega-6 fatty acids worsen outcome,after spinal cord injury in the adult rat.J Neurosci,2006,26:4672-4680.

