pH值对餐厨垃圾厌氧发酵产挥发性脂肪酸的影响
张玉静,蒋建国,2*,王佳明 (.清华大学环境学院,北京 00084;2.固体废物处理与环境安全教育部重点实验室,北京 00084)
餐厨垃圾在我国城市生活垃圾中占有较大的比重,达到 40%~60%[1],且随着社会的发展,餐厨垃圾的产量也逐年增加[2].餐厨垃圾具有含水率高、有机物含量高、容易腐败等特点,如处理不当,必然造成资源的浪费和环境的污染.因此,如何对餐厨垃圾进行减量化、无害化、资源化处理已成为普遍关注的问题[3-5].
采用厌氧消化技术处理餐厨垃圾,既可以实现餐厨垃圾的减量化,也能够实现资源的回收,逐渐受到国内外研究者的青睐.厌氧消化一般包括水解发酵、产氢产乙酸、产甲烷 3个阶段.在水解发酵阶段,不溶性的大分子有机物首先被转化为能被细菌所利用的小分子有机物,之后在发酵细菌的作用下,转化为长链脂肪酸、糖类、氨基酸等物质,最终形成以短链挥发性有机酸(乙酸、丙酸、丁酸、戊酸、己酸等)、乙醇为主的末端发酵产物[6].餐厨垃圾发酵过程产生的VFA可以用作污水处理工艺中脱氮除磷的碳源[7-8].同时,在发酵产酸阶段也可能产生大量氢气[9-10],实现了资源的回收.
水解酸化产物及其组成受各种因素影响.pH值作为一个重要的环境因素,不仅能够影响微生物酶的活性,也能够决定挥发酸的存在形态,研究表明[11-13],pH值是影响发酵产物组成的重要因素,但所采用的并非餐厨垃圾.有学者[14-16]通过对餐厨垃圾进行厌氧发酵发现,pH值对VFA浓度及组分有影响,但所采用的实验装置均为锥形瓶,且通常是间隔12h或24h进行pH值的人工调节.何品晶等[17]发现,餐厨垃圾酸化极易实现,在 pH值不控制条件下,发酵液的pH 值迅速下降到4.0以下.这必然会造成对产酸菌的抑制,从而抑制VFA的产生.可见,有必要对反应器内的pH值实时连续调控,以保证反应器内 pH值的稳定,从而促进VFA的高效产出.
因此,本研究采用自动化程度较高的实验装置,通过实时连续控制反应器内pH值,研究pH值对餐厨垃圾厌氧发酵过程中VFA浓度及组成的影响,从而寻求餐厨垃圾发酵产酸的最适pH值.
1 材料与方法
1.1 实验材料
实验所用餐厨垃圾为自行配制,主要成分为米饭、白菜、猪肉与豆腐,质量分数分别为35%、45%、16%和4%.4种组分经混合后,放入食物搅拌机搅碎,之后储存于 4℃冰箱中待用.试验时,用自来水将餐厨垃圾稀释至总固体浓度(TS)为 16.1%.稀释后餐厨垃圾的 VS为15.8%,C/N 为 13.4,溶解性化学需氧量(SCOD)为 64.20g/L,挥发性脂肪酸(VFA)浓度为718mg/L,pH值为4.42.
接种污泥取自北京高碑店污水处理厂厌氧消化污泥,经自然存放 3d后倒出上清液使用.污泥TS为4.5%,VS为2.2%,C/N为8.5,SCOD为1775mg/L,pH值为6.34.
1.2 实验装置与实验方法
实验装置为高硼硅玻璃制成,有效容积为4.5L,高径比为 2.2:1,见图 1.将 3L 餐厨垃圾与800mL接种污泥混合倒入反应器中进行批式发酵.温度通过传感器控制在(35.0±1.0)℃,搅拌由可编程逻辑控制器(PLC)控制在200r/min,实时监测反应器内氧化还原电位(ORP).通过传感器实时加入 HCl(5mol/L)和 NaOH(5mol/L),将 3个反应器的pH值分别控制在5.0、6.0、7.0,另外一个反应器不控制 pH值.将物料加入反应器中,用高纯氮气吹脱1min以驱除反应器内的空气.实验过程中,每隔24h用蠕动泵取样,直到水解酸化过程达到稳定状态,即水解酸化液中VFA浓度变化幅度在5%以内.

图1 实验装置示意Fig.1 Schematic diagram of anaerobic fermentation
1.3 分析方法
TS、VS采用重量法[18]测定,ORP采用梅特勒pt4805-DPAS-Sc-K8S/225测定,C/N采用EAI公司 CE-440型快速元素分析仪测定,SCOD、VFA、乙醇等经过预处理后测定.预处理方法为将样品以 15000r/min离心 15min,上清液采用0.45μm 过滤.其中 SCOD 以重铬酸钾法[14]测定,VFA(乙酸、丁酸、异丁酸、丁酸、异戊酸、戊酸)和乙醇采用气相色谱法测定.所用仪器为岛津GC-2010plus,测试条件为进样口温度220℃,检测器温度 250℃,不分流进样,柱子为毛细管柱stabliwax-DA,柱温由 60℃以 7℃/min的速率升到150℃,保持5min,之后以20℃/min速率升高到230℃,保持 10min.
2 结果与讨论
2.1 VFA浓度随pH值的变化
由图 2可以看出,随着发酵时间的延长,各处理VFA浓度均为先迅速增加后逐步趋于平稳.从总量上看(表1),pH值为6.0时VFA浓度及单位VS(反应器初始VS)产酸量最多,在第68h达到最大值,分别为 40.89g VFA/L和 0.328g VFA/gVS,明显高于其他报道中的 VFA浓度[14,19-20],这可能是由于本实验所采用的自配垃圾,在成分上与实际餐厨垃圾有所区别,更易发酵产生 VFA,也可能是由于接种污泥的活性更高,接种比例更为合适.pH值为5.0、6.0、7.0时,发酵液中VFA浓度均比不控制pH值时大,说明控制pH值能够显著提高发酵液的VFA浓度.尤其在pH值为6.0时,其最高VFA浓度是不控制pH值的8倍.
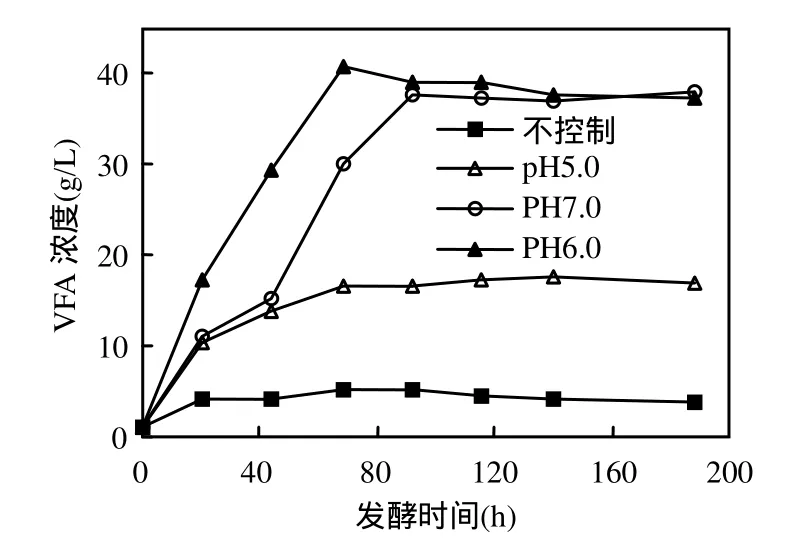
图2 不同pH值下VFA浓度随时间的变化Fig.2 Variation of VFA concentrations at different pH value
在发酵后期,pH值为6.0与7.0两种条件下水解液VFA浓度比较接近,均为37g/L左右.但在发酵前期,即第68h以前,pH值为6.0的产酸速率明显高于pH7.0时,这是因为pH值为7.0时,更易于产甲烷菌的生长,不利于 VFA 的积累.从工程角度分析,控制 pH值为 7.0需要消耗更多的NaOH,从而增加运行成本.因此,从VFA产量及经济效益等角度考虑,控制pH值为6.0更适合实际应用.不控制pH值、控制pH值为5.0、6.0、7.0情况下,乙醇浓度分别为7.60,2.38,1.61,5.27g/L.
VFA是由厌氧产酸细菌在代谢过程中所产生的,而 pH值则通过影响产酸细菌的代谢过程间接的影响VFA浓度.在较低pH值下,非离子态的有机酸会抑制产酸菌的活性,从而抑制VFA的产生[21].
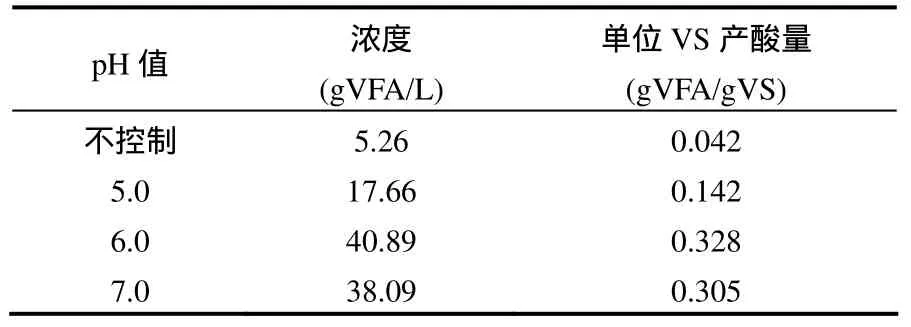
表1 不同pH值下最大VFA浓度及产酸量Table 1 Maximum VFA concentration and yield at different pH value
2.2 VFA组成随pH值的变化
根据末端代谢产物的组成可将厌氧产酸过程分为不同的发酵类型,主要包括乙醇型发酵、丁酸型发酵、丙酸型发酵和混合酸发酵.不同发酵类型主要是由厌氧发酵系统中优势菌群决定.厌氧发酵系统中存在多种微生物,由于每种微生物对外界环境(pH值、温度、ORP)的耐受性不同,因而在特定环境条件下,某些微生物会成为优势菌群,造成特定产物的大量产生.如乙醇型发酵菌群在 pH值<5.0时生长良好,因而发酵液中存在较多的乙醇.
表2显示了稳定运行时不同pH值下发酵产物的组成.在不添加NaOH时,发酵液中pH值能够下降到 3.3,此时,乙醇比例最高,达 59.8%,其次是乙酸,为26.7%,为典型的乙醇型发酵.这与其他文献的报道一致[22],即在 pH值<4.5,更易产生乙醇.当pH值为5.0时,乙酸为主要成分,占53.3%,其次是丁酸,占26.9%.pH值为6.0时,丁酸比例为50.9%,是最主要的产物,乙酸次之为26.5%.pH值为 7.0时,乙酸占 38.5%,其次是丁酸占 29.4%,在pH值为5.0、6.0、7.0时,主要产物均是乙酸与丁酸,两者之和均在 70.0%以上,可以认为都是丁酸型发酵.以上结果表明,pH值能够很大程度上影响发酵液中各有机酸组分的含量,是影响餐厨垃圾发酵类型的一个重要因素.
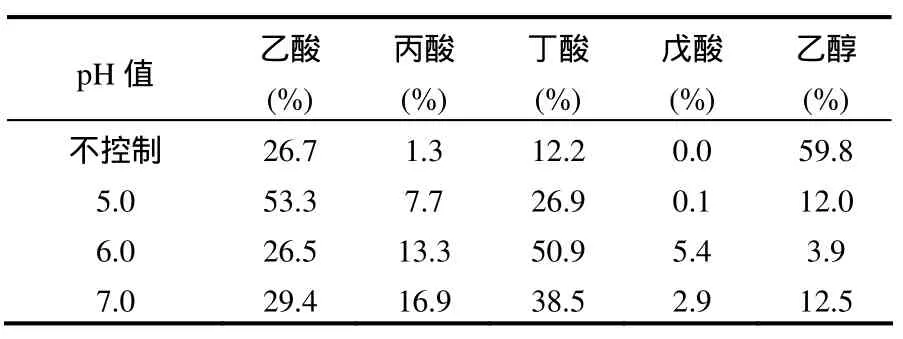
表2 不同pH值下VFA的组成Table 2 VFA composition at different pH value
发酵产物的组成直接影响其后续利用的效果.厌氧产酸末端产物富含短链的有机酸和乙醇,可以用作废水处理过程中脱氮除磷的碳源.在脱氮除磷过程中,酸的利用顺序为乙酸>丁酸>戊酸>丙酸[23].在pH值为6.0时,VFA总量最高,达到40.89g/L,且为典型的丁酸型发酵,脱氮除磷效率较高的乙酸与丁酸比例很大,有利于脱氮除磷过程的实现.因此,从发酵产物方面来说,pH值为6.0是餐厨垃圾厌氧发酵产酸的最佳pH值.

图3 pH值为6.0时有机酸组成Fig.3 VFA composition at pH 6.0
pH值为6.0时,水解液中有机酸组成及各种有机酸随发酵时间的变化见图 3.随着发酵时间的延长,乙酸比例逐渐减少,最后趋于平稳,在第20,44,116h,乙酸所占比例分别为 42.0%、38.9%和 24.6%.丙酸在第 2d迅速增长,之后变化不大,至稳定时占总VFA的比例为12.6%~13.8%.丁酸比例一直比较稳定,维持在 54.0%左右.戊酸出现最晚,在第66h才被检测出来,随后比例逐渐增大,最后达到9.5%.在pH值为6.0的条件下,乙酸、丁酸出现最早,其次是丙酸,最后是戊酸.乙酸与丁酸比例最多,为典型的丁酸型发酵.
3 结论
3.1 pH值对厌氧发酵液中VFA浓度影响显著.在pH值为6.0时,发酵液中VFA浓度及单位VS产酸量最大,达到40.89g/L和0.328gVFA/gVS,是不控制pH值时的8倍. pH值为7.0时,反应平稳阶段VFA浓度与pH值为6.0时接近,为37.00g/L左右,但在反应前期产酸速率明显更低.
3.2 pH值对厌氧产酸末端产物的组成影响显著.不控制pH值时,主要成分为乙醇,占所有发酵产物的 59.8%,为典型的乙醇型发酵.随着 pH值的升高,乙醇比例降低,乙酸与丁酸的比例升高.pH值为 5.0,6.0,7.0时,乙酸与丁酸之和均占70.0%以上,为丁酸型发酵.
3.3 控制反应器内pH值为 6.0时,餐厨垃圾发酵液中VFA浓度最大,且脱氮除磷效率较高的乙酸与丁酸较多,为批式实验下餐厨垃圾厌氧水解产酸的最佳pH值.
[1]王向会,李广魏,孟 虹,等.国内外餐厨垃圾处理状况概述 [J].环境卫生工程, 2005,13(2):41-44.
[2]崔亚伟,陈金发.厨余垃圾的资源化现状及前景展望 [J]. 中国资源综合利用, 2006,24(10):31-32.
[3]Komemoto K, Lim Y G, Nagao N, et al .Effect of temperature on VFA’s and biogas production in anaerobic solubilization of food waste [J]. Waste Management, 2009,29(12):2950-2955.
[4]Han S K, Shin H S. Enhanced acidogenic fermentation of food waste in a continuous-flow reactor [J]. Waste Management and Research, 2002, 20:110-118.
[5]Hafid H S, Rahman N A A, Omar F N, et al .A comparative study of organic acids production from kitchen wastes and simulated kitchen waste [J]. Australian Journal of Basic and Applied Sciences, 2010,4(4):639-645.
[6]Kim M, Gomec C Y, Ahn Y, et al. Hydrolysis and acidogenesis of particulate organic material in mesophilic and thermophilic anaerobic digestion [J]. Environmental Technology, 2003,24(9):1183-1190.
[7]Lim S J, Choi D W, Lee W G, et al. Volatile fatty acids production from food wastes and its application to biological nutrient removal [J]. Bioprocess Engineering, 2000,22:543-545.
[8]Lim S J, Ahn Y H, Kim E Y, et al. Nitrate removal in a packed bed reactor using volatile fatty acids from anaerobic acidogenesis of food wastes [J]. Biotechnol. Bioprocess Eng., 2006,11(6):538-543.
[9]Shin H S, Youn J H, Kim S H. Hydrogen production from food waste in anaerobic mesophilic and thermophilic acidogenesis [J].International Journal of Hydrogen Energy, 2004,29(13):1355-1363.
[10]Carlos Ramos, Germán Buitrón, Iván Moreno-Andrade, et al.Effect of the initial total solids concentration and initial pH on the bio-hydrogen production from cafeteria food waste [J].International Journal of Hydrogen Energy, 2012,37(18):13288-13295.
[11]Horiuchi J I, Shimizu T, Tada K, et al. Selective production of organic acids in anaerobic acid reactor by pH control [J].Bioresource Technology, 2002,82(3):209-213.
[12]Zhang P, Chen Y G, Zhou Q. Waste activated sludge hydrolysis and short-chain fatty acids accumulation under mesophilic and thermophilic conditions:Effect of pH [J]. Water Research,2009,43(15):3735-3742.
[13]Chen Y G, Jiang S, Yuan H Y, et. al. Hydrolysis and acidification of waste activated sludge at different pHs [J]. Water Research,2007,41(3):683-689.
[14]张 波,史红钻,张丽丽,等.pH对厨余废物两相厌氧消化中水解和酸化过程的影响 [J]. 环境科学学报, 2005,25(5):665-669.
[15]李定龙,戴肖云,赵宋敏,等.pH对厨余垃圾厌氧发酵产酸的影响[J]. 环境科学与技术, 2011,34(4):25-128.
[16]刘振玲,堵国成,刘 和,等.食品废弃物厌氧消化产乙酸的研究[J]. 环境污染与防治, 2007,29(1):49-52.
[17]何品晶,戴修疆,吕 凡,等.PH值对有机垃圾厌氧水解和酸化速率的影响 [J]. 中国环境科学, 2006,26(1):57-61.
[18]国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法 [M]. 4版.北京:中国环境科学出版社,2002:216-219.
[19]Lim S J, Kim B J, Jeong C M, et al. Anaerobic organic acid production of food waste in once-a-day feeding and drawing-off bioreactor [J]. Bioresource Technology, 2008,99(16):7866-7874.
[20]赵宋敏,李定龙,戴肖云,等,温度对厨余垃圾厌氧发酵产酸的影响 [J]. 环境污染与防治, 2011,33(3):44-47.
[21]Babel S, Fukushi K, Sitanrassamee B. Effect of acid speciation on solid waste liquefaction in anaerobic acid digester [J]. Water Research, 2004,38(9):2417-2423.
[22]任南琪,秦 智,李建政.不同产酸发酵菌群产氢能力的对比与分析 [J]. 环境科学, 2003,24(2):70-74.
[23]Elefsiniotis P, Wareham D G. Utilization patterns of volatile fatty acids in the denitrification reaction [J]. Enzyme and Microbial Technology, 2007,41(1,2):92–97.

