羧甲基葡甘聚糖铁凝胶球对磷的吸附性能
刘 凯 ,王 强 ,王 碧*,谢水仙
(1.内江师范学院 化学化工学院,四川 内江 641112;2.达州质量技术监督局,四川 达州 635000)
富营养化问题是当今世界面临的严峻的水污染问题之一,过量的磷会引起水体富营养化,刺激藻类和细菌大量繁殖,导致水质恶化.当湖海中磷的浓度超过0.03mg/L时,将会发生赤潮.因此磷是水体富营养化的限制因子,磷的去除对于消除污染、修复水体的富营养化以及保护环境具有重要的意义[1].同时,世界上的天然磷资源会在几十年内用光,因此无论从环境治理还是从资源有效利用的角度看,从废水中去除和回收磷酸盐都很有必要.常规的生化处理以及强化生物除磷装置难以保证磷的达标排放,往往需要三级物化除磷.吸附法被认为是一种能够较好地适用于宽浓度范围废水除磷的方法.吸附水体中磷酸盐的材料很多,包括无机吸附材料如:蛭石、沸石、粘土、各种矿渣粉煤灰、金属氧化物等;有机吸附材料如:活性炭,玉米秆等[2-12].近几年来,国内外许多研究者致力于探索廉价、制备简单、吸附容量大、可生物降解、容易再生的吸附材料,一些易获得的生物质改性吸附剂降低和消除水体中磷酸盐已有报道[12-14].
葡甘聚糖(konjac glucomannan,简称KGM)是魔芋块茎中所含的储备性多糖,它是由β-D-葡萄糖和β-D-甘露糖主要通过β-1,4糖甙键连接起来的高分子多糖.KGM 物理化学性质特别,已被广泛应用于食品,包装,涂料,生物医药等领域[15].近年来,葡甘聚糖基吸附材料也引起了研究者们的关注[16-21].然而天然魔芋葡甘聚糖固有的一些缺陷限制了其直接应用,为改善KGM 的理化性能,常常通过一定方法对KGM 改性.利用脱乙酰基葡甘聚糖吸附水溶液中的单宁[16];利用羧酸处理过的脱乙酰基葡甘聚糖除去水溶液中的铜和铅[17];已有将魔芋葡甘聚糖羧甲基化改性后制成交联羧甲基葡甘聚糖微球,吸附水体中的铅、镉等重金属离子的报道[18-20];还有研究者发现以魔芋葡甘聚糖微球为基质,偶联DEAE 基团形成的阴离子交换介质是一种价格低廉、性能优良、性价比较高的新型层析介质[21];也有将葡甘聚糖活化偶联制成Cu2+金属鳌合亲和胶用于纯化猪血SOD 的报道,但迄今未见有研究者利用葡甘聚糖金属离子凝胶做吸附材料的报道.
Fe3+可与水体中的磷酸根离子产生沉淀,但若直接使用铁盐会产生二次污染.因此开发新型吸附材料的难题是如何将Fe3+固定在非水溶性基础材料上并制备出较高吸附容量的新型吸附材料.本文基于Fe3+能使羧甲基葡甘聚糖凝胶化,同时Fe3+又能与水体中磷酸根离子结合这一特点,首先将葡甘聚糖羧甲基化制得羧甲基葡甘聚糖,再用Fe3+交联羧甲基葡甘聚糖制得性能优良的羧甲基葡甘聚糖铁凝胶球(CMKGM-Fe),并用数码显微镜和扫描电镜表征了微球结构.在此基础上,研究凝胶球CMKGM-Fe对水体中磷酸根离子的吸附性能,考察吸附时间、FeCl3浓度、CMKGM 浓度、温度、苯甲酸浓度以及微球直径等因素对吸附的影响,用红外光谱分析吸附前后微球的结构变化.拓宽魔芋葡甘聚糖的应用领域,为磷酸根离子等分离富集提供基础数据.
1 实验部分
1.1 仪器和试剂
仪器:日立4600紫外可见分光光度计(日本国日立公司),Thermo Fisher Nioolet 6700傅立叶变换红外光谱仪(美国Nicolet公司),数码显微镜(中国Digital公司),JSM-5900LV 扫描电镜(日本JEOL公司)和pHS-3C精密pH 计(上海精密仪器厂),DZF-6090真空干燥箱(上海精宏实验设备有限公司),HZS-HA 型水浴震荡器(哈尔滨东联六厂).
药品和试剂:魔芋葡甘聚糖(成都协力公司),含量>98%,粘均分子量为220kD;氯乙酸,无水乙醇,氢氧化钠,磷酸二氢钾,三氯化铁,硝酸,偏钒酸铵,钼酸铵等均为分析纯.
将磷酸二氢钾预先经105℃干燥1h,在干燥器中冷却后称取0.439 3g,用适量水溶解,定量转入1 000 mL容量瓶中,加硝酸3 mL,用蒸馏水稀释至刻度,混匀,即得磷标准溶液:0.10mg/mL[22].
1.2 实验方法
1.2.1 羧甲基葡甘聚糖及羧甲基葡甘聚糖铁凝胶球的制备 参考文献[23]等制得醚化度0.74的羧甲基葡甘聚糖.配置一定浓度的羧甲基葡甘聚糖溶液待用,将一定量的CMKGM 滴入到FeCl3溶液中(控制FeCl3溶液的质量分数),固化12h后过滤,于二蒸水中脱水3h,制得CMKGM 铁凝胶球吸附材料,过滤后干燥备用.
1.2.2 铁凝胶球机械强度的测定 将凝胶球放置在两块载玻片之间,在凝胶球上面的载玻片上加砝码,直至小球被压碎,以砝码的质量表征凝胶球的强度,用粒径相近的凝胶球平行测定3次[24].1.2.3 羧甲基葡甘聚糖铁凝胶球对磷酸根离子的吸附性能研究 将羧甲基葡甘聚糖铁凝胶球(干重0.2g)置于100mL 锥形瓶中,向其中加入一定浓度的溶液50mL.每组做平行实验5份,并用二蒸水做试剂空白.在设定温度下,以转速为150r/min在水浴振荡器中振荡吸附一定时间.取吸附残液,用钒磷钼黄显色法测定磷酸根的含量[23].以硫酸、磷酸和显色剂的混合溶液为空白参比.由吸附前后溶液中磷酸根离子浓度差计算吸附量,以mg/g吸附剂表示,以下各项实验中吸附量均按该法计算.吸附量的计算式:Q=(C0-C)*V/W.式中:V为溶液的体积,单位mL;W为吸附剂的干重,单位g,C0和C分别为吸附前、后溶液的浓度,单位mg/L;Q为吸附量,单位,mg/g.
1.2.4 微球的表征 分别用数码显微镜和扫描电镜观察羧甲基葡甘聚糖铁凝胶球微球全貌、表面和截面形貌并拍照.分别将羧甲基葡甘聚糖、羧甲基葡甘聚糖铁凝胶球及凝胶球复合物,经KBr压片后用傅立叶变换红外光谱仪做红外光谱分析.
2 结果与讨论
2.1 微球形貌及机械强度
分别用1.0%,1.5%,2.0%,2.5%的CMKGM溶液与1%的FeCl3溶液反应制备系列铁凝胶球,测定凝胶球的机械强度,每个凝胶球承担砝码质量依次分别为3.9g,13.5g,24.6g 和49g.表明凝胶球的强度随CMKGM 溶液的质量分数的增大而增加.微球的数码显微照片如图1所示.图1表明羧甲基葡甘聚糖铁凝胶球为深紫红色的空心球,数码显微下观察粒状微球球形不很规则.

图1 微球的数码显微照片Fig.1 Digital microscope photograph of CMKGM-Fe appearance
2.2 吸附磷酸根离子前后微球的红外光谱
CMKGM-Fe3+和 CMKGM-Fe3+-的FTIR 光谱如图2 所示,羧甲基葡甘聚糖(CMKGM)在3 500cm-1处的吸收峰为羧甲基中羟基的吸收峰,1 650cm-1和1 458cm-1处有2个反映羧基中羟基的特征吸收峰[23].
图2 表 明CMKGM 与Fe3+反 应 后,在1 750cm-1附近的吸收峰位移至1 704cm-1了,在1 650cm-1附近的峰位移至1 645cm-1了,这些事实表明-COO-与Fe3+发生了配位.CMKGM-Fe吸附后,在1 704cm-1附近的吸收峰加强了,在1 101cm-1附近出现了较窄的P-O 吸收峰,950cm-1附近也出现了基团的吸收峰,说明CMKGM-Fe吸附了磷酸根离子.

图2 羧甲基葡甘聚糖及其铁凝胶球吸附P(V)前后的红外光谱Fig.2 FTIR spectra of CMKGM-Fe3+andCMKGM-Fe3+-
2.3 影响吸附的因素
2.3.2 pH值对吸附的影响 图4表明,在稀HCl介质中,pH值≤2.0时,CMKGM-Fe微球对磷酸根离子几乎不发生吸附,之后微球对磷酸根离子的平衡吸附量随介质pH值升高而升高,pH值为4.0 时,升至最高,当水体中磷的初始浓度为50mg/L时,吸附量达12.27mg/g,吸附率达93.58%.pH值在4.0~5.0 之间,吸附量和吸附率基本不变.pH值在5.0~9.0范围内,磷酸根离子的平衡吸附量和吸附率随pH值的增加而逐渐降低,pH 为9时,吸附量降低至9.44mg/g,吸附率降低至75.51%.本文其它实验均在未加稀HCl或稀NaOH 介质的磷酸根离子溶液中进行,pH值约2.40.
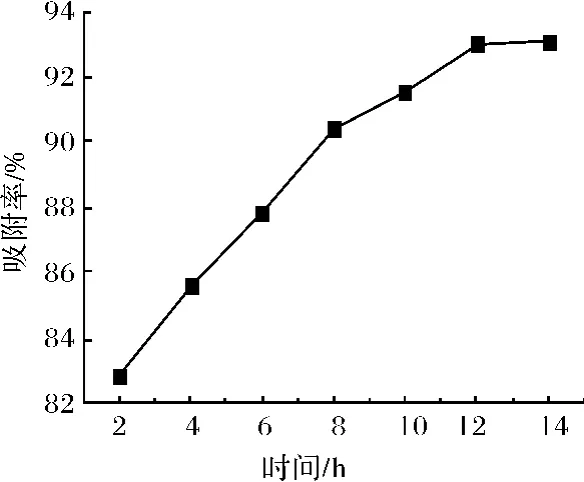
图3 时间对吸附的影响Fig.3 Effect of time on the adsorption capacity of phosphate by CMKGM-Fe.

图4 pH 对吸附的影响Fig.4 Effect of pH on the adsorption capacity of phosphate on CMKGM-Fe.
2.3.3 FeCl3质量分数对吸附的影响 预实验表明,质量浓度为1%和1.5%的羧甲基葡甘聚糖溶液形成的微球形状不规则且较软,2.5%和3%的羧甲基葡甘聚糖溶液均较粘稠,不方便操作,2%的羧甲基葡甘聚糖溶液形成的微球形状规则、均匀.故用2%的羧甲基葡甘聚糖溶液与不同浓度的FeCl3溶液制备微球,考察FeCl3溶液质量浓度对吸附的影响.结果表明:FeCl3的浓度1%、1.5%和2%时,微球对初始浓度为100 mg/L 的磷酸根离子的吸附率分别为:84.04%、88.61%和92.38%.显然FeCl3溶液的浓度对吸附有明显的影响,2%FeCl3的溶液制备的凝胶球吸附率最高.因此本文其它实验均用2%的羧甲基葡甘聚糖和2%的FeCl3溶液制备微球.
2.3.4 浓度对吸附的影响 控制温度为27℃,震荡吸附,考察磷浓度对吸附的影响.图5表明:同一温度下,吸附率先随磷初始浓度的增加而增加,当磷浓度由1mg/L增加到50mg/L时,吸附率由88.80%增至最高,此时吸附率达93.58%.之后再增加磷的浓度,吸附率不增反降,当磷浓度增至200mg/L时,吸附率下降至87.91%.当磷的初始浓度依次分别为1mg/L,10mg/L,50mg/L,80mg/L,100mg/L和200mg/L 时,凝胶球对磷的吸附量依次分别为0.22mg/g、2.32 mg/g、12.27mg/g、18.64 mg/g、23.26mg/g和43.96mg/g.
国家规定Ⅲ类水标准为总磷含量小于或等于0.005mg/L,Ⅴ类水体标准对总磷要求是小于0.4mg/L.现实生活中,较重的水质污染是1 mg磷/L(《钱江上游水质磷污染下降达Ⅱ类地表水质标准》),大大超过国家标准,段面水质处于污染较重的Ⅴ类水或劣Ⅴ类水.这些浓度均远远小于100mg/mL,属于CMKGM-Fe 微球的可使用范围,按88.8%的吸附率,1 mg/L 的重污染水经一次处理后即可达到Ⅴ类水的标准.
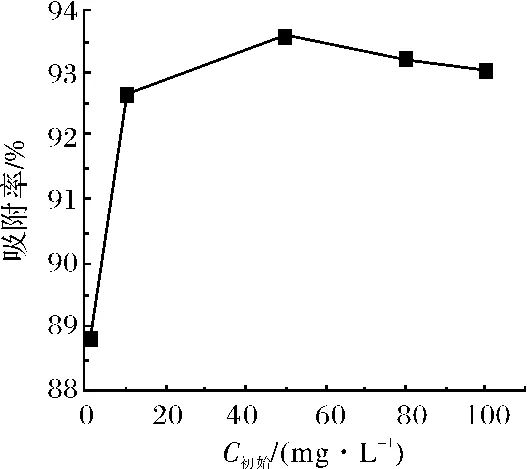
图5 浓度对吸附的影响Fig.5 Effect of concentration on the adsorption capacity of phosphate by CMKGM-Fe

图6 温度对吸附的影响Fig.6 Effect of temperature on the adsorption capacity of phosphate by CMKGM-Fe
2.3.5 温度对吸附的影响 控制磷浓度为50mg/L,震荡吸附,考察温度对吸附的影响.图6显示:一定温度范围内,吸附率和吸附量随着温度的升高总体变化较小.当温度由20℃升高到60℃时,吸附率和吸附量不断下降;温度低于50℃时,吸附率随温度的升高仅轻度下降,微球的吸附率稳定在92%以上.可能因为温度越高,Fe3+越易水解的缘故,当温度升高至50℃~60℃内,吸附率和吸附量下降程度明显增加,60℃时,吸附率下降至87.9%.吸附率随温度升高而不断下降这一事实还表明:CMKGM-Fe微球对磷酸根离子的吸附反应是放热反应,因此可以推测CMKGM-Fe与对磷酸根离子的吸附主要是物理吸附.本文其它实验均在27℃下进行.
3 结论
CMKGM-Fe球对磷酸根离子的吸附性能与时间、羧甲基葡甘聚糖的浓度、Fe3+浓度、温度、磷浓度均有关.在20℃下,用2.0%的FeCl3溶液与醚化度为0.78的2.0%的CMKGM 溶液反应,制得的羧甲基葡甘聚糖铁凝胶球振荡吸附初始浓度为100 mg/L 的磷溶液,对磷的吸附量达22.36mg/g,吸附反应以物理吸附为主.CMKGMFe凝胶球作为一种新型吸附材料可望用于磷酸根离子的分离富集.
[1]Jin X C,Wang S R,Pang Y,et al.The adsorption of phosphate on different trophic lake sediments[J].Colloids and Surfaces A:Physicochem Eng Aspects,2005,254:241-248.
[2]孟 洪,彭昌盛,肖举强.活化沸石去除水中磷化物的研究[J].矿产综合利用,2001(4):10-14.
[3]Seida Y,Nakano Y.Removal of phosphate by layered double hydroxides containing iron[J].Water Res,2002,36:1306-1312.
[4]邓雁希,许 虹,黄 玲.蛭石去除废水中磷酸盐的研究[J].中国非金属矿工业导刊,2003(6):42-44.
[5]Karageorgiou K,Paschalis M,Anastassakis G N.Removal of phosphate species from solution by adsorption onto calcite used as natural adsorbent[J].Journal of Hazardous Materials,2007,139(3):447-452.
[6]董庆洁,周学永,邵仕香,等.锆、铁水合氧化物对磷酸根的吸附[J].离子交换与吸附,2006,22(4):363-368.
[7]Biswas B K,Inoue K,Ghimire K N.Removal and recovery of phosphorus from water by means of adsorption onto orange waste gel loaded with zirconium[J].Bioresource Technology,2008,99(18):8685-8690.
[8]刘 焱,吴玲琳,王世和.工业废渣基除磷材料的静态吸附研究[J].环境工程学报,2009,3(2):275-278.
[9]项学敏,卫志强,周集体,等.污水中磷酸根的吸附研究进展[J].广州环境科学,2009,24(2):5-9.
[10]程 翔,黄新瑞,王兴祖,等.ZnAlLa类水滑石对污泥脱水液中磷酸根的吸附[J].化工学报,2010,61(4):955-962.
[11]朱润良,朱利中,朱建喜.Al-CTMAB 复合膨润土同时吸附处理水中菲和磷酸根[J].环境科学,2006,27(1):91-94.
[12]王 宇,高宝玉,岳文文,等.改性玉米秸秆对水中磷酸根的吸附动力学研究[J].环境科学,2008,29(3):703-708.
[13]丁 云,廖学品,石 碧.胶原纤维固载Fe(Ⅲ)对磷酸根的吸附特性[J].化工学报,2007,58(5):1225-1231.
[14]王文懿,岳钦艳,李 倩,等.改性芦竹对磷酸根动态吸附及脱附再生的研究[J].山东大学学报:工学版,2010,40(2):105-109.
[15]庞 杰,林 琼,张甫生,等.魔芋葡甘聚糖功能材料研究与应用进展[J].结构化学,2003,22(6):633-642.
[16]Liu F,Luo X G,Lin X Y.Adsorption of tannin from aqueous solution by deacetylated konjac glucomannan[J].Journal of Hazardous Materials,2010,178(1-3):844-850.
[17]Liu F,Luo X G,Lin X Y.Removal of copper and lead from aqueous solution by carboxylic acid functionalized deacetylated konjac glucomannan[J].Journal of Hazardous Materials,2009,171(1-3):802-808.
[18]Niu C M,Wu W H,Wang Z,et al.Adsorption of heavy met-al ions from aqueous solution by crosslinked carboxymethyl konjac glucomannan[J].Journal of Hazardous Materials,2007,141(1):209-214.
[19]Long X Y,Luo X G,Wang Y,et al.Adsorption of Pb(II)from aqueous solution by konjac glucomannan beads[J].Science in China Series E:Techbologechnological Sciences,2009,52(1):223-226.
[20]牛春梅,吴文辉,王 著,等.交联羧甲基魔芋葡甘聚糖吸附重金属离子的研究[J].离子交换与吸附,2006,22(5):402-408.
[21]葛佳丽,王佳兴,马光辉,等.魔芋葡甘聚糖DEAE 阴离子交换介质的制备及表征[J].离子交换与吸附,2007,23(4):289-296.
[22]李兴利.钒磷钼黄分光光度法快速测定磷酸二氢钾的纯度[J].化学分析计量,2007,16(1):46-47.
[23]汪 超,李 斌,谢笔钧,等.魔芋葡甘聚糖羧甲基化方法改性研究[J].农业工程学报,2005,21(5):140-143.
[24]陈维璞,张恩浩,林永波.海藻酸钠-钙-铁凝胶球对Cr2O2-7吸附的研究[J].环境保护科学,2010,36(6):14-16.

