羟丙基-β-环糊精包合当归油的工艺研究
苏秀霞, 杨玉娜, 李凯斌, 李仲谨, 耿肖莎
(教育部轻化工助剂化学与技术重点实验室,陕西科技大学,陕西西安 710021)
当归Angelica sinensis(Oliv.Diels)为伞形科植物当归的干燥根,含有黄酮、香豆素、挥发油、有机酸、多糖、氨基酸、微量元素及维生素等多种成分[1],其味甘、辛,性温、具有补血、活血、调经镇痛、润肠通便等功效[2],具有很高的药用和保健价值。目前,国家药品标准的成方制剂中以当归挥发油入药的品种多达40余种[3],因而当归油已在临床上得到广泛应用。
一般采用水蒸气蒸馏法提取当归挥发油,由于挥发油具有较强的挥发性,在制剂及储存过程中容易散失[4-5],影响了当归制剂的稳定性,而包合技术可增加药物溶解度、掩盖药物异味、提高生物利用度和患者顺应性[6-8],因此为了提高其利用率,将挥发油制备成环糊精包合物是常用方法之一。
环糊精有多种同系物,而在药物制剂方面应用较多的是β-环糊精 (β-CD),但其本身的水溶解度低限制了它在药学领域中更广泛的应用[9]。羟丙基-β-环糊精 (HP-β-CD)是一种环状低聚糖,外部具有亲水性而内部是亲脂性的内腔,能与脂溶性药物形成水溶性包合物[10],不仅水溶度高 (75 g/100 mL),对热稳定,且对肾、肌肉和黏膜几乎无刺激,被人们认为是一种低毒、安全、有效的具有广阔前景的水溶性包合材料[11],因此将易挥发的物质通过HP-β-CD包合后,可以提高制剂中挥发油成分的稳定、药物疗效,掩盖其异味[12],为当归油制成中成药提供了一定的理论基础。本实验采用HP-β-CD对当归油进行了包合,并通过正交实验设计对制备工艺进行了优化。
1 仪器与试剂
1.1 仪器与设备 磁力搅拌器 (上海浦东光学仪器厂);挥发油检测器 (4M/BB89X-8-016,上海玻璃仪器厂);真空干燥箱 (101A-I,上海亚明热处理设备有限公司);傅立叶红外光谱仪 (UV-265FW,日本岛津公司);DR5000型紫外可见光谱仪 (UV-Vis,美国Hach公司)。
1.2 材料与试剂 羟丙基-β-环糊精 (天津市红岩化学试剂厂);当归油 (陕西瑞正生物有限公司);无水乙醇 (天津市红岩化学试剂厂)等均为分析纯试剂,实验用水为蒸馏水。
2 方法与结果
2.1 当归油羟丙基-β-环糊精包合物的制备 称取一定量的HP-β-CD,用蒸馏水溶解后,加入1 mL当归油混合均匀,置于磁力搅拌器上恒温水浴搅拌一定时间,冷却至室温,于冰箱中冷藏 (24 h),用石油醚洗去未包合的当归油,即得当归油包合物的溶液。
2.2 当归油空白回收率的测定 按《中国药典》2010年版一部附录XD项下“挥发油测定法”依法进行测定[13]。将1 mL当归油加入到约300 mL的蒸馏水中,连接挥发油测定器,加热沸腾5 h,至油量不再增加,停止加热,冷却1 h,准确读取蒸出的油量,计算当归油的空白回收率为80%。
2.3 当归油包合率及包合物产率的测定 将制备的当归油包合物溶液用石油醚洗去未包合的当归油,与300 mL蒸馏水均匀混合置于圆底烧瓶中,加入几粒沸石,连接挥发油测定器,加热使其沸腾5 h,至油量不再增加,停止加热,冷却1 h,准确读取包合物的含油量 (mL),计算当归油包合率;冷冻干燥所得的包合物,计算包合物的产率。
2.4 包合工艺的正交优化
2.4.1 因素与水平 经初步试验,选定包合温度 (A)、包合时间 (B)、当归油和HP-β-CD投料比 (C)、当归油和水投料比 (D)为影响因素,每因素3水平,见表1。

表1 因素水平


表2 正交试验

表3 方差分析
由表2正交试验结果分析可得羟丙基-β-环糊精包合当归油的最佳条件为A1B2C2D1,即包合温度40℃,包合时间4 h,(HP-β-CD)∶(当归油)=6 ∶1,(水/mL)∶(当归油/mL)=15∶1。由方差分析可知,各因素对反应影响的大小顺序为包合温度>包合时间>当归油和HP-β-CD的投料比>当归油和水的投料比。在其他条件不变的情况下对温度作了进一步的单因素考察,结果表明:温度低于40℃时,不利于挥发油分子的扩散,使其不能充分地扩散到HP-β-CD分子之间,使一些挥发油分子能够被包合的几率下降,而温度过高时,加剧了分子的热运动,促使分子向外扩散,导致了能够被固化的有效当归油分子减少。经分析表2、表3,以方差值最小的因素C作为空白对照,从表3可知A、B、D都不存在显著性差异。
2.5 验证性实验 按最佳工艺取包合6批当归油,平均总经验得分10.02,与理论推导能够较好吻合。
2.6 包合物稳定性试验 按最佳条件A1B2C2D1制备当归油-HP-β-环糊精包合物7份置于烧杯中,另外取1 mL的当归油于相同的水量中7份置于烧杯中,使其于50℃通风恒温箱中,于1、2、3、4、5、6、7 d后取样,测定溶液中剩余当归油的量。
图1中曲线a和b说明包合物中当归油释放速率明显低于混合物中的释放速率;7 d之后包合物中的含油量大于混合物中的含油量,由此可得当归油的稳定性、缓释效果都得到了提高。
2.7 包合物的表征
2.7.1 包合物的紫外分光光度法分析 见图2。图2中,从a曲线可知当归油的特征吸收峰在338.2 nm和277.3 nm波长处;且物理混合物b曲线和当归油的相同,包合物在277.3 nm处没有出现特征峰,HP-β-CD的特征吸收峰出现在205.2 nm波长处,曲线c与a、b、d比较谱图发生了变化,说明包合物已构成了一种新物相,挥发油已被HP-β-CD包合。
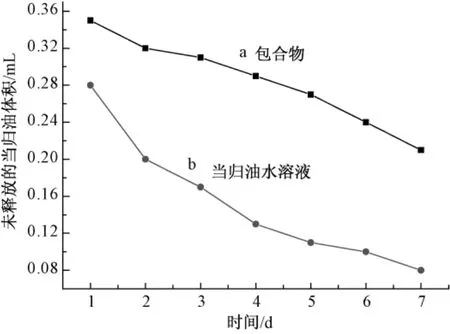
图1 当归油HP-β-CD包合前后的稳定性

图2 当归油、HP-β-CD、当归油和 HP-β-CD混合物、当归油-HP-β-CD包合物的紫外吸收光谱
2.7.2 包合物的IR分析 见图3。
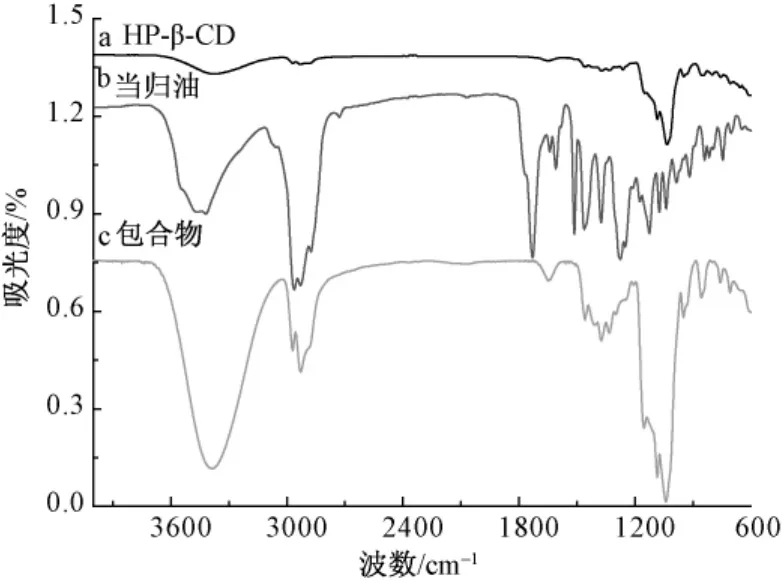
图3 当归油、HP-β-CD和当归油-HP-β-CD包合物的红外谱图
图3中b谱图3 900~2 500 cm-1是O-H,N-H,C-H等的伸缩振动;3 050~3 100 cm-1不饱和C-H键的特征峰;1 780~1 650 cm-1羰基的振动峰;1 500~1 480 cm-1和1 600~1 590 cm-1单核芳香的两个特征峰;1 300~1 050 cm-1醇、酚、醚、羧酸、酯等的C-O特征峰,而在c谱图中一些特征峰却没有被表征出来,这是由于嵌入HP-β-CD的空腔中,使其对当归油产生了屏蔽作用。
如果客体分子含有—COOH,—COOR和C-O等基团,在1 700 cm-1附近有拉伸振动吸收,从峰形、峰位和强度的变化还是能够提供关于客体分子是否进入空腔以及相互作用力性质的证据[14]。从 b谱图可以得出当归油在1 748.12 cm-1处存在强拉伸振动吸,而a和c谱图相比较,峰形和强度都有所变化,因此可判断当归油进入了H-P-β-环糊精的空腔。
2.7.3 包合物的薄层层析法分析 见图4。
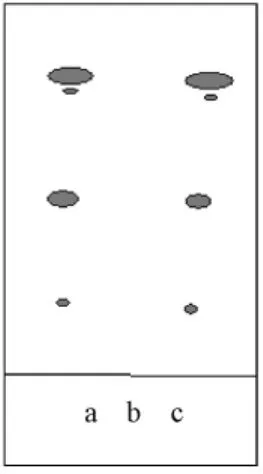
图4 当归油-HP-β-CD包合前后的TLC图
取适量的当归油、包合物、包合物中提取的当归油,分别点于同一硅胶薄层板上做TLC检测,以甲苯-乙酸乙酯(10∶1)为展开剂,展开,取出,晾干,喷以5% 香草醛酸溶液显色,并置紫外光灯 (365 nm)下检视[15],结果见图4,a和c出现了相同颜色的斑点,可以说明包合物中当归油与纯当归油挥发油一致,而b无相应展开斑点,表明HP-β-CD中已不存在游离的当归油,进而说明当归油与HP-β-CD形成了包合物而非混合物,且包合后当归油的化学成分未发生变化。
3 讨论
3.1 采用水浴恒温磁力搅拌使HP-β-CD对当归油进行了包合,并通过正交试验分析得出最佳包合工艺:包合温度40℃,包合时间4 h, (HP-β-CD)∶(当归油)=6∶1,(水/mL)∶(当归油/mL)=15∶1。
3.2 通过当归油的稳定性试验,表明当归油的缓释效果得到了提高;红外光谱分析了主要官能团吸收峰的变化,表明形成了当归油-HP-β-CD包合物;薄层层析法分析也进一步说明包合物的形成,且当归油的化学成分没有改变。
3.3 利用易溶性的HP-β-CD包合当归油的工艺简单、方便,因此在中成药生产中该工艺具有良好的应用前景。
[1]丁 毅.炮制对当归挥发油及多糖的影响[J].时珍国医国药,2004,15(8):496-497.
[2]马瑞君,王 钦,陈学林,等.当归的研究进展[J].中草药,2002,33(3):280-282.
[3]李桂生,李八方.GC法测定当归油中Z-藁本内酯[J].中草药,2005,36(12):1816-1818.
[4]Cho S K,Abd El-Aty A M,Choi J H,et al.Optimized conditions for the extraction of secondary volatile emetabolites inAngelicaroots by accelerated solvent extraction[J].J Pharm Biomed Anal,2007,44(5):1154-1158.
[5]Chan SS,Cheng TY,Lin G.Relaxation effects of ligustilide and senkyunolide A,two main constitants ofLigusticum chuanxiong,in rat isolated aorta [J].J Ethnopharmacol,2007,111:677-680.
[6]姚永萍,盛蓉武.β-环糊精及其衍生物在中药领域中的研究进展[J].现代医药卫生,2008,24(13):1930.
[7]Yotaro A,Shigeru K,Fumiyoshi Y,et al.Effect of low-molecular-weight β-cyclodextrin polymer on release of drugs from mucoadhesive buccal film dosage forms[J].Biol Pharm Bull,2005,28(9):1679-1683.
[8]李元波,殷辉安,周 琳,等,当归挥发油的提取与包合工艺研究[J].天然产物研究与开发,2006(8):838-839.
[9]杨彩琴,王 静,纪桂霞.羟丙基-β-环糊精对双苯氟嗪包合作用的热力学研究[J].化学研究与应用,2010,22(4):23-27.
[10]丁平田,吴雪梅.药物制剂的新型辅2-羟丙基-β-环糊精[J].国外医药·合成药、生化药、制剂分册,1996,17(2):107-111.
[11]TaoT. Characteristics and pharmaceuticalapplications of hydroxypropyl-betacyclodextrin[J].中国医药工业杂志,2002,33(6):304-309.
[12]汪付田,靳子明,郭 敏.薏苡仁油-羟丙基-β-环糊精包合物制备工艺研究[J].中国中医药信息杂志,2010,17(10):56-57.
[13]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[14]冯美卿,康怀萍,刘红梅,等.DL-苏氨酸的化学合成[J].河北科技大学学报,2001,22(2):22-24.
[15]钱 平,刘志辉,钱 芳.当归、甘松挥发油 β-环糊精包合工艺研究[J],中成药,2010,32(4):667-669.

