磷酸二氢钙和氯化钾对尿素处理的黄泥土水溶性铵态氮和硝态氮的影响
李寿田, 周健民, 王火焰, 杜昌文, 陈小琴, 钱剑林
(1.苏州农业职业技术学院,江苏 苏州 215008;2.中国科学院南京土壤研究所,江苏 南京 210008)
多种养分间的交互作用可发生于土壤、根际和植物体内,对养分的迁移转化、吸收和代谢有着深远的影响[1-5]。水溶性养分是植物可直接利用的养分形态,水溶性养分的多少决定着土壤对植物养分的供应强度。氮磷钾是农业生产中大量施用并且经常共同施用的肥料,三者在土壤中的相互作用影响着土壤对植物养分的供应强度和养分向环境的迁移[6-9]。因此,研究多养分同时存在时氮磷钾相互作用对土壤水溶性养分的影响,对养分的植物有效性、肥料的合理使用和生态环境保护具有重要意义。本试验通过研究磷酸二氢钙和氯化钾对尿素处理的黄泥土中水溶性铵态氮和硝态氮变化的影响,为研究自然条件下氮磷钾肥料共施对氮肥有效性和环境影响提供理论依据。
1 材料与方法
1.1 材料
所用土壤为江苏常熟黄泥土,属水稻土类。土壤采自耕层(0~15 cm),土壤采后放在实验室内自然风干,过2 mm筛。其基本理化性状均用常规方法测定[10],结果见表1。
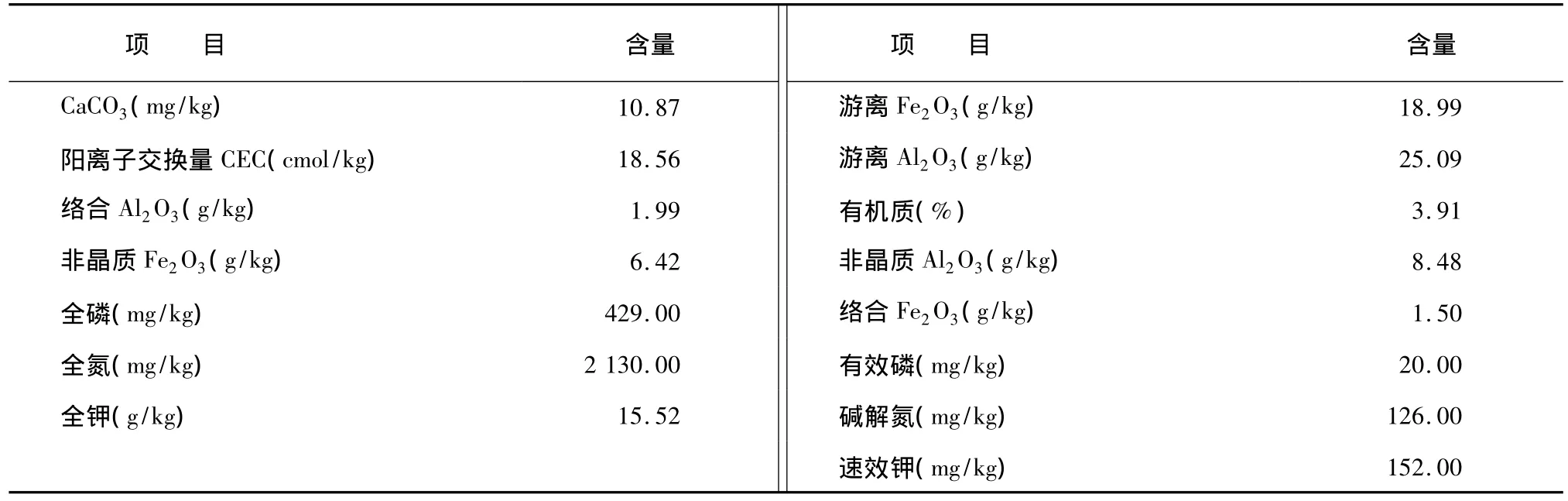
表1 供试土壤基本理化性状Table 1 Basic physico-chemical properties o f tested soil
1.2 试验处理
试验共设8个处理。处理1(1U):氮(尿素,下同)施入量为110 mg/kg;处理2(2U):氮施入量为220 mg/kg;处理3(1UP):氮、磷(磷酸二氢钙,下同)施入量分别为110 mg/kg和200 mg/kg;处理4(2UP):氮、磷施入量分别为220 mg/kg和200 mg/kg;处理5(1U1K):氮、钾(氯化钾,下同)施入量分别为110 mg/kg和310 mg/kg;处理6(2U2K):氮、钾施入量分别为220 mg/kg和620 mg/kg;处理7(1U1KP):氮、钾、磷施入量分别为110 mg/kg、310 mg/kg和200 mg/kg;处理8(2U2KP):氮、钾、磷施入量分别为220 mg/kg、620 mg/kg和 200 mg/kg;对照(Ctrl):只加蒸馏水。每个处理4次重复。按不同处理称取相应肥料溶解在蒸馏水中,然后用称重法将不同肥料溶液加入土壤中,放在(25±1)℃条件下进行培养。
1.3 方法
称取2.500 g土壤于小药瓶中,用称重法加入不同肥料配比的溶液,并使土壤含水量达到27.5%,然后用橡皮塞塞紧。在(25±1)℃条件下分别培养 2 d、15 d、36 d、66 d 和 107 d,其中,培养15 d、36 d、66 d和107 d的土壤,每隔7 d用称重法加入一定量的去离子水,使其保持在田间持水量的状态下。测定时,将小药瓶放入塑料瓶中,按水土比20∶1加入50 ml蒸馏水,在(25±1)℃条件下振荡30 min,然后用定量滤纸过滤,上清液用来测定水溶性铵态氮和硝态氮的含量,铵态氮含量用靛酚蓝比色法测定,硝态氮用紫外分光光度法测定[10]。
2 结果与分析
2.1 磷酸二氢钙对尿素处理土壤水溶性铵态氮和硝态氮的影响
磷酸二氢钙对尿素处理土壤水溶性铵态氮和硝态氮的影响见图1。从图1可看出,随着培养时间的延长,对照土壤铵态氮含量逐渐升高,但在整个培养期间,土壤水溶性铵态氮含量只是由培养2 d时的4.73 mg/kg增加到培养107 d时的8.58 mg/kg。向土壤中加入尿素后,培养前期土壤溶液中铵态氮含量均显著增加,加入的尿素量越大,土壤溶液中铵态氮含量也越大。培养2 d后,1U和2U处理铵态氮含量分别达到39.12 mg/kg和60.94 mg/kg,除去对照土壤中水溶性铵态氮的含量,1U和2U处理土壤水溶性铵态氮含量分别占施入尿素态氮量的35.56%和27.70%。随着培养时间的增加,尿素处理土壤溶液中的铵态氮含量出现急剧下降,并在培养后期与对照无显著差异。磷酸二氢钙可显著降低尿素处理土壤培养2 d后溶液中铵态氮的含量,1UP和2UP处理水溶性铵态氮分别为25.01 mg/kg和60.94 mg/kg,与1U和2U相比,分别下降了36.06%和24.94%。而在培养15 d后,1UP与1U、2UP和2U处理间土壤水溶性铵态氮含量无显著差异。

图1 磷酸二氢钙对尿素处理土壤水溶性铵态氮(a)和硝态氮(b)的影响Fig.1 Effects of monocalcium phosphate on water-soluble ammonium nitrogen(a)and nitrate-nitrogen(b)of soil treated with urea
从图1还可看出,随着培养时间的延长,不同处理硝态氮含量均显著升高,对照硝态氮含量增加幅度相对较小,由培养2 d的20.3 mg/kg增加到培养107 d的81.91 mg/kg。尿素处理土壤后,在处理前3个时期,硝态氮含量快速上升。其中,1U处理培养2 d后,硝态氮含量与对照处理无显著差异,但随着处理时间的延长,1U处理土壤硝态氮含量显著上升,培养 107 d后,其硝态氮含量达到 204.65 mg/kg,占总施入氮的111.58%。2U处理土壤在整个处理期间,其硝态氮含量均显著高于对照和1U处理,培养107 d后,土壤硝态氮含量为274.91 mg/kg,占施入氮的87.73%。磷酸二氢钙可显著提高尿素处理初期土壤硝态氮含量,使施磷处理土壤硝态氮含量显著高于不施磷处理,但在处理后期,磷酸二氢钙对土壤硝态氮的影响并不显著。
2.2 氯化钾对尿素处理土壤水溶性铵态氮和硝态氮的影响
氯化钾对尿素处理土壤水溶性铵态氮和硝态氮的影响见图2。从图2可看出,氯化钾显著提高了尿素处理2 d的土壤中水溶性铵态氮含量,1U1K和2U2K处理水溶性铵态氮含量分别为42.36 mg/kg和86.72 mg/kg,与1U和2U处理相比,水溶性铵态氮含量分别增加了8.27%和42.31%。而随着处理时间的延长,1U和1U1K处理水溶性铵态氮差异不显著,2U2K处理在前3个处理时期,土壤水溶性铵态氮含量显著高于2U处理,但处理36 d后,与2U处理的差异不显著。1U1K处理除了在第1次处理时显著高于1UP处理外,其他处理时期,两者均无显著差异,而2U2K处理在前3个处理时期,土壤水溶性铵态氮均显著高于2UP处理,在后2个处理时期,两者也无显著差异。
从图2还可看出,在处理第2 d,1U1K处理土壤硝态氮含量为10.01 mg/kg,显著低于1U处理,而在处理中后期,相对于1U处理,氯化钾抑制了土壤硝态氮含量增加;培养107 d后,1U1K处理土壤硝态氮含量为142.96 mg/kg,与1U处理相比,硝态氮含量下降了30.14%。在培养第2 d,2U2K处理土壤硝态氮含量与2U处理无显著差异,但在培养后期,2U2K处理土壤硝态含量显著低于2U处理;培养107 d后,2U2K处理硝态氮含量为240.64 mg/kg,与 2U处理相比,硝态氮含量下降了12.47%。另外,在第1个、第3个处理时期,1U1K处理土壤硝态氮含量显著低于1UP处理;其他处理时期,硝态氮含量虽低于1UP处理,但均未达到显著水平。2U2K处理除在第3个处理时期与2UP处理土壤硝态氮含量无显著差异外,其他处理时期,土壤硝态氮含量均显著低于2UP处理。

图2 氯化钾对尿素处理土壤水溶性铵态氮(a)和硝态氮(b)的影响Fig.2 Effects of potassium chloride on water-soluble ammonium nitrogen(a)and nitrate nitrogen(b)of soil treated with urea
2.3 磷酸二氢钙和氯化钾共处理对尿素处理土壤水溶性铵态氮和硝态氮的影响
磷酸二氢钙和氯化钾对尿素处理土壤水溶性铵态氮和硝态氮的影响见图3。从图3可看出,在培养2 d后,1U1KP处理土壤水溶性铵态氮含量为30.36 mg/kg,与1U处理相比,铵态氮含量显著下降了22.40%,但在其他培养时期,1U1KP处理土壤水溶性铵态氮含量与1U处理差异不大。在培养第1和第3个时期,1U1KP处理土壤水溶性铵态氮含量显著低于1U1K处理。在培养前2个时期,1U1KP处理土壤水溶性铵态氮含量显著高于1UP处理,但在随后的处理过程中,不同处理间差异不显著。在培养前3个时期,2U2KP处理土壤水溶性铵态氮含量均显著高于2U和2UP处理土壤,但在培养前2个时期,土壤水溶性铵态氮含量要显著低于2U2K处理,而在随后的培养过程中,不同处理间差异不显著。
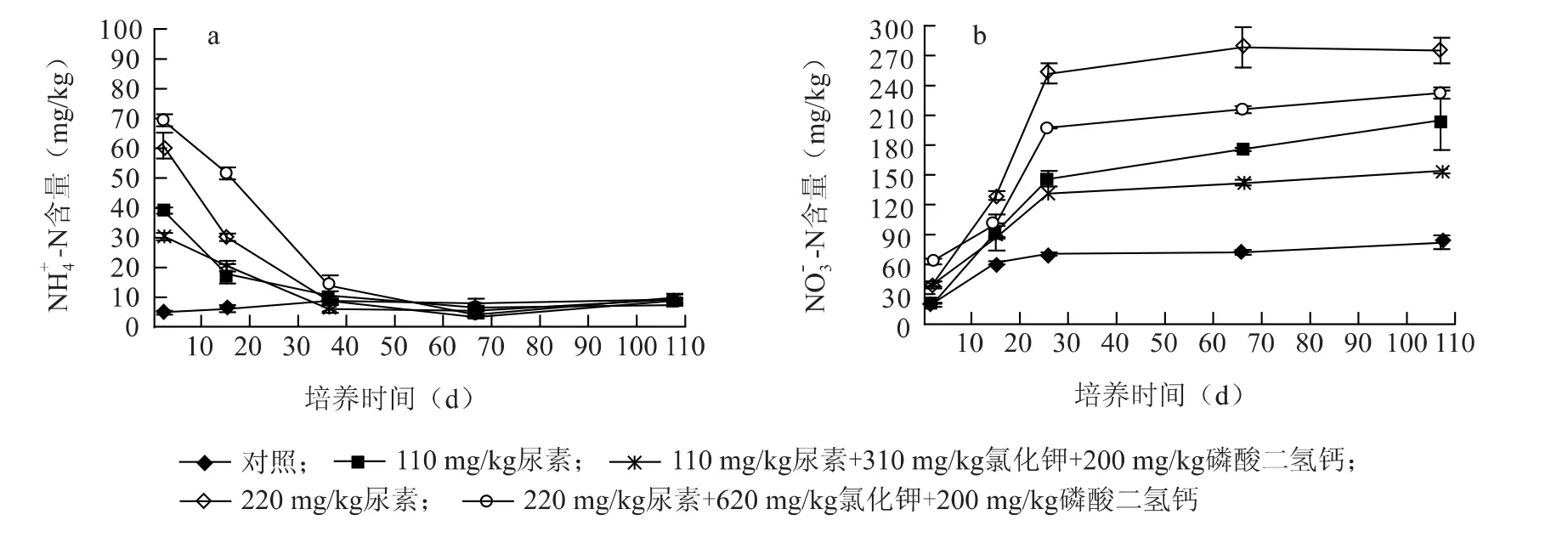
图3 氯化钾和磷酸二氢钙对尿素处理土壤水溶性铵态氮(a)和硝态氮(b)的影响Fig.3 Effects of potassium chloride and monocalcium phosphate on water-soluble ammonium nitrogen(a)and nitrate-nitrogen(b)of soil treated with CO(NH2)2
从图3还可看出,当磷酸二氢钙、氯化钾和尿素 共施时,在培养初期,1U1KP和2U2KP处理土壤硝态氮含量分别为39.97 mg/kg和62.73 mg/kg,均显著高于相应的1U和2U处理,但在培养中后期,1U1KP和2U2KP处理土壤硝态氮含量均显著低于相应的1U和2U处理;培养107 d后,1U1KP和2U2KP处理硝态氮含量分别为153.88 mg/kg和232.03 mg/kg,与1U和2U处理相比,土壤中硝态氮含量分别下降了24.81%和15.60%。在处理前期1U1KP硝态氮含量显著高于1UP和1U1K处理,但在其他处理时期,其硝态氮含量均显著低于1UP,而在后3个处理期间,硝态氮含量与1U1K处理无显著差异。2U2KP处理硝态氮含量除培养初期与2UP处理无差异外,其他培养时期均显著低于2UP处理。另外,2U2KP处理除第1次取样时硝态氮含量显著高于2U2K处理和第4次取样时显著低于2U2K处理外,在其他取样时间与2U2K处理无差异。
2.4 不同处理土壤水溶性铵态氮和硝态氮变化的相关性分析
将不同处理水溶性铵态氮的变化与相应处理硝态氮的变化进行相关性分析,结果见表2。由表2可看出,对照土壤水溶性铵态氮含量与硝态氮含量的相关系数为0.443(P>0.05),两者之间并无显著的相关性。而其他处理水溶性铵态氮含量与硝态氮含量之间存在着显著的负相关(相关系数在-0.997至 -0.930之间,均值为 -0.968(P<0.01)。这说明,除对照外,不同处理土壤水溶性铵态氮含量的下降与硝态氮含量的上升具有很好的相关性。
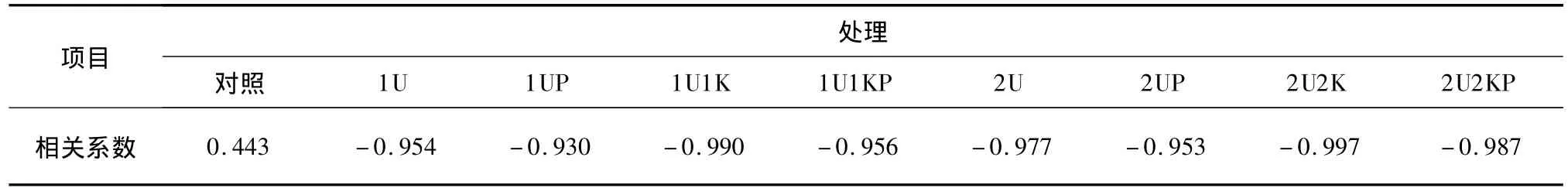
表2 不同处理土壤水溶性铵态氮与硝态氮相关性分析Table 2 Correlation analysis of water-soluble ammonium nitrogen and nitrate nitrogen in different treatments
3 讨论
尿素施入土壤后,酰胺态氮水解后形成铵态氮,造成土壤水溶性铵态氮含量增加,但与施入的氮量相比,铵态氮含量只占较小比例(110 mg/kg尿素和220 mg/kg尿素处理铵态氮含量分别占施入氮的35.56%和27.70%),这是由于尿素在水解过程中,有一部分尿素态氮并没有转变成铵态氮,而水解生成的铵态氮又被吸附在交换位点和非交换性位点上,从而使土壤中水溶性铵态氮含量显著下降。而当同时加入氯化钾时,由于土壤中的交换位点对K+的亲和性大于对NH+4的亲和性,而非交换性位点对NH+4的亲和性大于对K+的亲和性[11-12],加入的K+能够与NH+4竞争交换性位点和非交换性位点,使被吸附的NH+4减少,从而提高尿素处理土壤前期水溶性NH+4含量,这与氯化钾能够提高氯化铵处理土壤水溶性铵态氮含量的结果是一致的[13]。另外,氯化钾抑制了尿素处理土壤后期的硝化作用,使处理后期土壤硝态含量下降。这与钾促进铵的固定[14]和抑制固定态铵的释放[15]有关。另外,施入钾时所带入的伴随离子如氯离子对硝化细菌的活性有一定的影响,也能使硝化作用下降[16-17]。
磷酸二氢钙的加入显著降低了培养前期尿素处理土壤溶液中铵态氮的含量,但在培养中后期,磷酸二氢钙处理土壤水溶性铵态氮的含量与尿素处理土壤无显著差异。前人研究结果表明,尿素施入土壤后,存在着一个水解过程,其水解的最适pH在6.5左右[18],而磷酸二氢钙的加入会降低土壤的 pH值,使水解尿素的脲酶活性受到了一定的抑制[19],使尿素水解速率降低。因此,在培养前期,一部分的酰胺态氮并没有立即转变成铵成氮,从而造成土壤溶液中铵态氮含量较低。但随着培养时间的增加,土壤中酰胺态氮逐渐被脲酶水解完全转变成铵态氮,使不同处理间水溶性铵态氮含量差异不显著。磷酸二氢钙对尿素处理土壤硝态氮的影响主要表现在处理前期,使土壤硝态氮含量显著高于尿素处理土壤,这可能与土壤pH值降低抑制了氨挥发有关[20]。但磷酸二氢钙对处理中期土壤的硝化有轻微的抑制作用,使土壤硝态氮含量低于尿素处理土壤,但均未达到显著水平,这也与土壤pH的下降有正相关关系[21],而磷酸二氢钙对硝化作用的抑制,对提高肥料利用率、减少硝态氮的淋失是有益的。
[1]苏同庆,王火焰,周健民,等.水稻土肥际微域铵对钾形态转化与迁移的影响[J].土壤,2011,43(3):367-373.
[2]陈小琴,周健民,王火焰,等.铵钾施用次序和比例对油菜生长和氮钾养分吸收的影响[J].土壤,2008,40(4):571-574.
[3]TENG Y,TIMMER V R.Nitrogen and phosphorus interactions in intensively managed nursery soil-plant system[J].Soil Sci Soc Am J,1994,58(1):232-238.
[4]于 飞,周健民,王火焰,等.不同氮肥对潮土中磷肥转化的动态影响[J].中国土壤与肥料,2006(5):39-42.
[5]杜振宇,周健民,王火焰,等.氮钾肥对磷在红壤肥际微域中迁移转化的影响[J].土壤学报,2010,47(3):497-502.
[6]马茂桐.钾氮配施对土壤氮钾渗漏损失的影响[J].土壤,1999,31(3):136-139.
[7]周文利,吕静霞,苗艳芳.不同水分处理对丹参生长前期氮磷钾吸收的影响[J].江苏农业科学,2012,40(4):241-243.
[8]王祥菊,杜庆平,徐月明,等.氮磷钾肥配比对弱筋小麦扬麦15产量形成的影响[J].江苏农业科学,2011,39(6):132-135.
[9]李熙英,刘继生,黄世臣.氮磷钾施用量对一年生杨树扦插苗生长的影响[J].江苏农业科学,201l,39(5):254-256.
[10]鲁如坤.土壤农业化学分析方法[M].北京:中国农业科技出版社,1999.
[11]SHEN S,TU S I,KEMPER W D.Equilibrium and kinetic study of ammonium adsorption and fixation in sodium-treated vermiculite[J].Soil Sci Soc Am J,1997,61(6):1611-1618.
[12]CHAPPELL M A,EVANGELOU V P.Influence of added K+on inducing ammonium fixation and inhibiting nitrification[J].J Soil Sci,2000,165(5):420-426.
[13]李寿田,周健民,王火焰,等.磷酸二氢钙和氯化钾对氯化铵处理黄泥土水溶性铵态氮和硝态氮的影响[J].土壤,2012,44(6):941-946.
[14]王火焰,周健民,陈小琴,等.氮磷钾肥料在土壤中转化过程的交互作用Ⅱ.硫酸铵在水稻土中的转化[J].土壤学报,2005,42(1):70-77.
[15]钱晓晴,汤 炎,封 克,等.作物吸氮过程中NH+4、K+颉颃现象的土壤因素研究[J].土壤通报,1994,25(6):256-258.
[16]周丕东,石孝均,毛知耘.氯化铵中氯的硝化抑制效应研究[J].植物营养与肥料学报,2001,7(4):397-403.
[17]MCCLUNG G,FRANKENBERGER W T J.Soil nitrogen transformation as affected by salinity[J].Soil Sci,1985,139(5):405-411.
[18]CABRERA M L,KISSEL D E,BOCK B R.Urea hydrolysis in soil:effects of urea concentration and soil pH[J].Soil Biol Biochem,1991,23(12):1121-1124.
[19]FENN L B,HOSSNER L R.Ammonium volatilization from ammonium or ammonium-forming nitrogen fertilizers[J].Adv Soil Sci,1985,1:123-169.
[20]FENN L B,TATUM G,HORST G.Ammonia loss from surfaceplaced mixtures of urea-calcium-potassium salts in the presence of phosphorus[J].Fert Res,1990,21:125-131.
[21]王小治,孙 伟,尹微琴,等.pH升高对红壤硝化过程产生N2O的影响[J].土壤,2009,41(6):962-967.

