低C/N比污水反硝化过程中亚硝态氮累积特性研究
李玲玲 刘晓萍 杨兆雪
(青岛科技大学环境与安全工程学院,山东 青岛 266042)
低C/N比污水反硝化过程中亚硝态氮累积特性研究
李玲玲 刘晓萍#杨兆雪
(青岛科技大学环境与安全工程学院,山东 青岛 266042)
以乙酸钠为碳源,采用序批实验研究低C/N比污水在不同温度反硝化过程中的亚硝态氮累积规律。研究结果表明,不同温度下低C/N比污水均能在反硝化过程中累积亚硝态氮。在同一温度下,随着初始C/N比增加,亚硝态氮最大累积率随之增加,温度为15 ℃时亚硝态氮最大累积率增幅最大,C/N比为1.03时,亚硝态氮最大累积率仅为18.8%,而C/N比为4.16时,亚硝态氮最大累积率高达83.9%;在同一水平的C/N比下,随着温度升高,亚硝态氮最大累积率也随之呈增加的趋势;当C/N比为1左右,温度从15 ℃上升到25 ℃时,亚硝态氮最大累积率从18.8%上升到51.7%;在较高温度、较高C/N比下,反应初期由于乙酸钠具有一定弱碱性导致系统pH迅速上升,随着硝态氮逐渐还原成亚硝态氮,乙酸钠被分解成CO2,pH逐渐下降,待硝酸盐完全去除,进一步发生亚硝态氮还原,系统pH再次上升。
温度 低C/N比 亚硝态氮累积 pH
许多行业会产生低C/N比污水,如焦化废水、垃圾渗滤液、污泥厌氧消化液等,此类污水通常采用传统的生物硝化反硝化技术进行脱氮处理,由于硝化过程需要曝气,反硝化过程需要外加碳源,导致污水处理成本较高。近年来兴起的厌氧氨氧化工艺可利用亚硝态氮作为电子受体将氨氮直接氧化成氮气[1],此工艺脱氮途径短,不需投加碳源,在处理低C/N比污水上具有明显的优势[2-3]。
然而在实际应用过程中,污水中亚硝态氮含量低,目前主要通过短程硝化为厌氧氨氧化提供亚硝态氮。但不少研究发现,维持短程硝化的稳定运行比较困难[4-5],短程硝化易转变为全程硝化。实际上,亚硝态氮是反硝化的中间产物,也可通过反硝化过程获得亚硝态氮,为厌氧氨氧化反应提供电子受体。最近有学者提出短程反硝化—厌氧氨氧化脱氮工艺[6-7],即先将污水中的部分氨氮通过硝化反应氧化为硝态氮,再利用反硝化菌将硝态氮转化为亚硝态氮,进一步利用厌氧氨氧化菌将亚硝态氮和污水中剩余的氨氮转化为氮气,从而实现高效经济脱氮,此工艺的关键在于反硝化过程中要能实现亚硝态氮的大量累积。
现有研究中,有关低C/N比污水在不同温度反硝过程中的亚硝态氮累积特性研究较少。为此,本研究以乙酸钠为碳源,探索低C/N比污水在不同温度下亚硝态氮的累积规律,为短程反硝化—厌氧氨氧化工艺的工程应用提供一定参考。
1 材料与方法
1.1 实验用污泥及污水
实验所用污泥取自青岛某污水处理厂,污泥取回后在实验室序批式活性污泥反应器(SBR)中培养一段时间以富集反硝化菌。人工配制实验污水,污水中各试剂添加量为:硝酸钠516 mg/L、磷酸二氢钾5 mg/L、硫酸镁98 mg/L、氯化钙103 mg/L、氯化铁0.25 mg/L,乙酸钠按需添加。
1.2 实验方法
采用500 mL玻璃瓶作为反应器,反应器密封,利用磁力搅拌器进行搅拌,水浴控温,pH实时监控。由于实验操作原因, C/N比不能精准控制,本研究污水C/N比拟定在1、2、3、4左右。控制反应器内混合液挥发性悬浮固体(MLVSS)在1 500 mg/L左右,初始硝态氮质量浓度在85 mg/L左右,进水pH在8.0~8.3,反硝化时间为4 h,定时取样测定硝态氮、亚硝态氮和COD浓度。为考察温度对反硝化过程中亚硝态氮累积的影响,分别在15、25、35 ℃下开展反硝化实验,每组实验均进行3次平行实验。
1.3 分析项目与方法
亚硝态氮采用N-(1-萘基)-乙二胺光度法测定;硝态氮采用紫外分光光度法测定;COD采用重铬酸钾法测定,因亚硝态氮的存在会影响COD测定结果,根据式(1)对COD测定结果进行校正;pH采用玻璃电极法测定;MLVSS采用重量法进行测定[8]。
cCOD’=cCOD-2.339 5×c硝态氮+8.000 3
(1)
式中:cCOD’为校正后COD质量浓度,mg/L;cCOD为实测COD质量浓度,mg/L;c硝态氮为硝态氮质量浓度,mg/L。
2 实验结果
2.1 15 ℃时不同C/N比污水的反硝化过程
图1为15 ℃时不同C/N比污水在反硝化过程中硝态氮、亚硝态氮、COD及pH的变化曲线。

图1 15 ℃时不同C/N比污水在反硝化过程中硝态氮、亚硝态氮、COD及pH变化曲线Fig.1 Profile of sewage nitrate-N,nitrite-N,COD and pH during denitrification process under different C/N ratios at 15 ℃
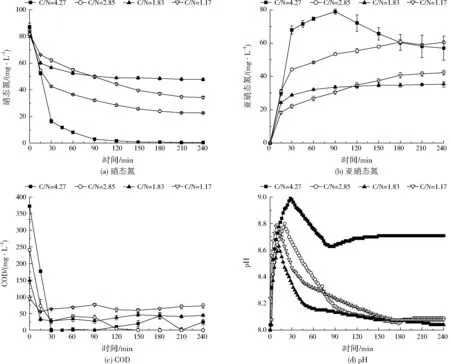
图2 25 ℃时不同C/N比下反硝化过程中硝态氮、亚硝态氮、COD及pH变化曲线Fig.2 Profile of sewage nitrate-N,nitrite-N,COD and pH during denitrification process under different C/N ratios at 25 ℃
由图1(a)可见,温度为15 ℃时,反硝化前30 min不同C/N比污水硝态氮浓度均快速下降,且随着C/N比的增加,硝态氮去除量相应增加;C/N比为4.16时,30 min内硝态氮质量浓度下降50.83 mg/L;而C/N比为1.03时,30 min内硝态氮质量浓度仅下降7.00 mg/L。由图1(b)可见,不同C/N比污水均存在亚硝态氮的累积;C/N比为4.16时,亚硝态氮质量浓度最大值为68.19 mg/L;C/N比为1.03时,亚硝态氮质量浓度最大值仅为15.46 mg/L。由图1(c)可见,C/N比为1.03、1.90、2.73时,COD在反应前15 min快速下降,此后COD变化较小;而C/N比为4.16时,COD在反应前60 min快速下降,60 min后COD缓慢下降,至90 min时,COD几乎完全去除,此后可能由于微生物发生溶胞现象导致COD又缓慢上升。由图1(d)可见,在不同C/N比下,反硝化过程中pH变化趋势一致,均呈现出先快速上升,达到峰值后再缓慢下降的趋势;但不同C/N比下pH达到峰值的时间及峰值大小不同;C/N比为4.16时,pH在40 min达到峰值(8.98);而C/N比为1.03时,pH在6 min即达到峰值(8.50)。
2.2 25 ℃时不同C/N比污水的反硝化过程
图2为25 ℃时不同C/N比污水在反硝化过程中硝态氮、亚硝态氮、COD及pH变化曲线。
由图2(a)可见,C/N比为4.27时,硝态氮在反应前30 min快速下降,至90 min时降到2.85 mg/L;C/N比为1.17~2.85时,硝态氮在反应前15 min下降较快,此后下降速度逐渐放缓。由图2(b)可知,C/N比为4.27时,反应90 min后亚硝态氮质量浓度达到最大值78.97 mg/L,此后亚硝态氮浓度开始下降;C/N比为1.17~2.85时,反应240 min内亚硝态氮浓度不断增加。由图2(c)可以看出,C/N比越高,COD去除效果越好,当C/N比为4.27时,COD在反应30 min内完全去除,随后可能由于微生物发生溶胞作用,COD波动上升;C/N比为2.85时,COD在反应150 min内完全去除;而C/N比为1.17时,至反应结束COD仅去除32.40 mg/L。由图2(d)可知,C/N比为1.17~2.85时,pH变化趋势相同,即先快速上升,达到峰值后再下降;而C/N比为4.27时,pH先升高后下降,在82 min时又开始缓慢上升。

图3 35 ℃时不同C/N比下反硝化过程中硝态氮、亚硝态氮、COD及pH变化曲线Fig.3 Profile of sewage nitrate-N,nitrite-N,COD and pH during denitrification process under different C/N ratios at 35 ℃
2.3 35 ℃时不同C/N比污水的反硝化过程
图3为35 ℃时不同C/N比污水在反硝化过程中硝态氮、亚硝态氮、COD及pH变化曲线。
由图3(a)可知,C/N比越高,硝态氮下降越快,当C/N比为4.32时,硝态氮在反应60 min时降至4.47 mg/L;C/N比为2.67时,硝态氮在105 min时下降到8.03 mg/L;C/N比为1.85、1.13时,反应过程中硝态氮浓度下降相对缓慢。从图3(b)可见,当C/N比为4.32时,亚硝态氮在反应60 min时质量浓度达到最大值76.04 mg/L,此后亚硝态氮浓度逐渐下降;当C/N比为2.67时,亚硝态氮在反应90 min时质量浓度达到最大值78.32 mg/L,此后亚硝态氮浓度也开始下降;当C/N比为1.85、1.13时,亚硝态氮在240 min的反硝化过程中浓度逐渐增加。由图3(c)可知,不同C/N比下,COD均在反应前30 min快速下降,尤其是C/N比为4.32、2.67时,COD分别由352.70、220.40 mg/L降到20 mg/L以下。由图3(d)可知,C/N比为4.32、2.67时,反硝化过程中pH均呈现先增加后降低,一段时间后再次上升的变化趋势;而C/N比为1.13、1.85时,pH先增加至峰值后逐渐降低。
3 讨 论
3.1 反硝化过程中亚硝态氮累积特性分析
现有研究中,有关反硝化过程中亚硝态氮累积的原因主要有3种解说:(1)部分反硝化细菌只含有硝态氮还原酶,系统中微生物以这类菌群为主时将导致亚硝态氮累积[9];(2)硝态氮还原速率大于亚硝态氮还原速率时,会产生亚硝态氮累积[10];(3)硝态氮的存在抑制亚硝态氮的还原,在硝态氮去除前会发生亚硝态氮的积累[11]。
OH等[12]、殷芳芳等[13]在以乙酸钠为反硝化碳源时均发现了亚硝态氮累积现象,且在反硝化过程中硝态氮去除量明显大于亚硝态氮累积量。而本研究反硝化过程中硝态氮去除量和亚硝态氮累积量几乎相等。存在差异的主要原因是前两位学者的反硝化研究中,硝态氮还原的同时发生亚硝态氮还原,硝态氮还原酶争夺电子的能力强于亚硝态氮还原酶,导致二步反应存在速率差,形成亚硝态氮累积。本研究中硝态氮先还原成亚硝态氮,硝态氮完全去除后再进一步发生亚硝态氮的还原,反硝化过程中硝态氮的存在抑制了亚硝态氮还原酶的活性,导致亚硝态氮大量累积;当硝态氮基本去除,亚硝态氮还原酶活性增强,亚硝态氮开始还原。KORNAROS等[14]在研究中也发现,系统中的硝态氮会抑制亚硝态氮还原酶的活性,导致亚硝态氮累积。
根据反硝化过程中亚硝态氮最大浓度与初始硝态氮浓度的比值,得到不同温度和不同C/N比下反硝化过程中亚硝态氮最大累积率(见图4)。
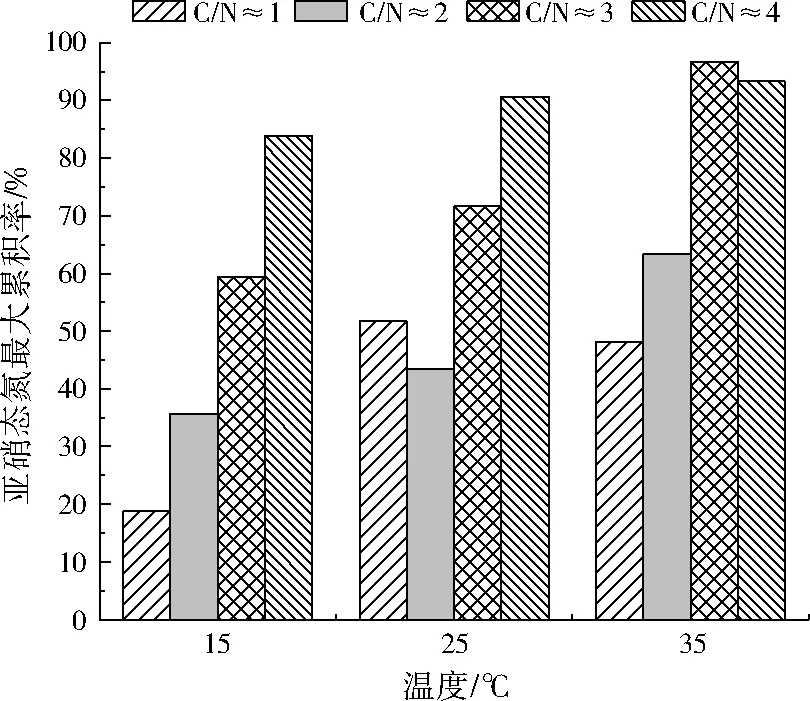
图4 不同温度和C/N比下亚硝态氮最大累积率Fig.4 Maximum nitrite accumulation ratio under different C/N ratios and temperatures during denitrification process
由图4可见,总体看来,同一温度下随着C/N比的增加,反应系统中碳源含量升高,碳源作为反硝化的电子供体使更多硝态氮还原成亚硝态氮,导致亚硝态氮最大累积率随之增加,这种趋势在温度较低时尤为明显,温度为15 ℃时不同C/N比下亚硝态氮最大累积率相差最大,C/N比在1.03时,亚硝态氮最大累积率仅为18.8%;而C/N比在4.16时,亚硝态氮最大累积率达到83.9%。在较高温度(25、35 ℃)、较高C/N比(约为3、4)下,亚硝态氮最大累积率均在70%以上。
总体看来,在同一水平的C/N比下,随着温度增加,反硝化菌体内酶的活性增大,亚硝态氮最大累积率也呈增加趋势。C/N比较低时,温度对亚硝态氮最大累积率的影响较大;C/N比在1左右时,15 ℃时亚硝态氮最大累积率仅为18.8%,而25 ℃时亚硝态氮最大累积率达到51.7%。C/N比在4以上时,不同温度下亚硝态氮最大累积率均能达到80%以上。
总而言之,低温下要实现亚硝态氮的充分累积,需给系统提供充足的碳源,初始C/N比要控制在4左右。在较高温度下(25~35 ℃),反硝化系统可适当降低C/N比,初始C/N比宜控制在3左右。
3.2 反硝化过程COD的变化
反硝化过程中通常先将硝态氮还原成亚硝态氮,再将亚硝态氮还原成氮气排除,反应方程式如下:
(2)
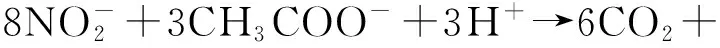
(3)
根据方程式计算可以得出将1.00 mg硝态氮还原至亚硝态氮需要消耗1.46 mg乙酸钠,相当于1.14 mg COD;而每还原1.00 mg亚硝态氮至N2,需2.20 mg乙酸钠,相当于1.72 mg COD。通过实验数据计算,本研究反应初期COD去除量远大于理论值,之后COD趋于平稳,而反硝化反应继续进行;分析其原因可能是微生物在反应初期吸附大量乙酸钠,导致COD快速降低,随后微生物利用吸附的乙酸钠进行反硝化反应。BEUN等[15]在研究反硝化规律时也发现,反硝化菌在碳源充足时将储存有机物以供碳源缺乏时使用。
3.3 反硝化过程pH变化
由实验结果可知,在较高温度、较高C/N比下,反硝化过程中系统pH先快速上升至峰值后,又逐渐下降;当系统中硝态氮完全去除,开始发生亚硝态氮的还原反应时,pH再次上升。分析其原因,由于反应初期溶液中存在大量乙酸钠,乙酸钠具有一定的弱碱性,导致反应开始时pH迅速上升;随着反应的进行,乙酸钠被分解成CO2,致使反应系统pH下降;当硝态氮完全去除后,开始发生亚硝态氮还原反应,亚硝态氮被还原成氮气的过程中产生大量OH-,导致pH再次升高。GONG等[16]在以乙酸钠为碳源研究反硝化规律时发现,反硝化过程中pH迅速上升后逐渐下降,未出现本研究中pH再次升高的现象。产生差异的主要原因是反硝化过程中亚硝态氮累积的机制不同,本研究中硝态氮的存在抑制了亚硝态氮还原,当硝态氮基本去除,才开始发生亚硝态氮的还原反应;而在GONG等的研究中,硝态氮还原的同时存在亚硝态氮的还原,但硝态氮还原速率快于亚硝态氮还原速率,导致亚硝态氮的大量积累,虽然在亚硝态氮还原过程中产生OH-,但是由于乙酸钠分解产生大量CO2,CO2溶于水的过程中产生的H+大于亚硝态氮还原过程中OH-的生成量,引起pH持续下降。也有学者研究发现,pH在整个反硝化过程中持续升高,主要原因是硝态氮还原速率仅略高于亚硝态氮还原速率,亚硝态氮累积量较小,因亚硝态氮还原过程中产生大量的OH-,导致反应过程中pH持续升高[17-18]。由上述分析可知,反硝化过程中亚硝态氮累积的机制不同,反应过程中pH的变化存在较大差异。
此外,相同温度下C/N比越大,碳源浓度越高,被微生物吸附所需要的时间越长,则pH到达峰值的时间越晚。在相同C/N比下,温度越高,系统内亚硝态氮积累量越大,亚硝酸还原成氮气时产生OH-量越多,pH越大。
以上结果表明,不同的反硝化过程具有不同的pH变化规律,可以利用pH的变化控制反硝化过程。当系统亚硝态氮积累机制为硝态氮抑制亚硝态氮还原时,可以将pH再次上升的时间点作为亚硝态氮开始还原的标志,以此终止反硝化的进行,阻止亚硝态氮进一步还原成氮气,从而实现亚硝态氮的最大累积,为厌氧氨氧化反应提供充足的电子受体。
4 结 论
(1) 在同一温度下,随着C/N比增加,亚硝态氮最大累积率随之呈增加趋势;温度为15 ℃,C/N比由1.03增加到4.16时,亚硝态氮最大累积率由18.8%增至83.9%;在较高温度下(25、35 ℃),较高C/N比(约为3、4),亚硝态氮最大累积率均在70%以上。在同一水平的C/N比下,随着温度升高,亚硝态氮最大累积率也呈增加的趋势,且C/N比较低时,温度对亚硝态氮最大累积率的影响较大;C/N比在1左右时,15 ℃时亚硝态氮最大累积率仅为18.8%,而25 ℃时亚硝态氮最大累积率达到51.7%。
(2) 低温下要实现亚硝态氮的充分累积,需给系统提供较充足的碳源,系统初始C/N比要控制在4左右。在较高温度(25~35 ℃)下,要使亚硝态氮能充分累积,系统初始C/N比可降至3左右。
(3) 在较高温度、较高C/N比下,以乙酸钠为碳源时,反应初期COD迅速下降,导致系统中pH迅速上升达到峰值;在硝态氮被还原为亚硝态氮的过程中,乙酸钠被分解成CO2,致使系统中pH下降;当硝态氮完全去除时,亚硝态氮开始发生还原反应,pH再次上升。
[1] MULDER A,GRAAF A A V D,ROBERTSON L A,et al.Anaerobic ammonium oxidation discovered in a denitrifying fluidized bed reactor[J].FEMS Microbiology Ecology,1995,16(3):177-184.
[2] 林琳,李玉平,曹宏斌,等.焦化废水厌氧氨氧化生物脱氮的研究[J].中国环境科学,2010,30(9):1201-1206.
[3] 彭永臻,马斌.低C/N比条件下高效生物脱氮策略分析[J].环境科学学报,2009,29(2):225-230.
[4] 谢新立,王欣.短程硝化反硝化生物脱氮的影响因素分析[J].工业用水与废水,2011,42(2):11-13.
[5] 江清华,王荣昌,杨殿海.污水低氧脱氮机制及其应用研究进展[J].环境污染与防治,2009,31(11):68-74.
[6] 曹相生,张树立,赵续东.基于短程反硝化和厌氧氨氧化的城镇污水处理新工艺[J].北京水务,2012(3):26-28.
[7] GAO Fan,ZHANG Hanmin,YANG Fenglin,et al.The contrast study of anammox-denitrifying system in two non-woven fixed-bed bioreactors (NFBR) treating different low C/N ratio sewage[J].Bioresource Technology,2012,114(2):54-61.
[8] 国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法[M].4版.北京:环境科学出版社,2002.
[9] KONWLES R.Denitrification[J].Microbiological Reviews,1982,46(1):43-70.
[10] 曹相生,钱栋,孟雪征.乙酸钠为碳源时的污水反硝化规律研究[J].中国给水排水,2011,27(21):76-79.
[11] PAYNE W J,RILEY P S.Suppression by nitrate of enzymatic reduction of nitric oxide[J].Experimental Biology and Medicine,1969,132(1):258-260.
[12] OH J,SILVERSTEIN J A.Acetate limitation and nitrite accumulation during denitrification[J].Journal of Environmental Engineering,2015,125(3):234-243.
[13] 殷芳芳,王淑莹,昂雪野,等.碳源类型对低温条件下生物反硝化的影响[J].环境科学,2009,30(1):108-113.
[14] KORNAROS M,LYBERATOS G.Kinetics of denitrtrification byPseudomonasdenitrificans under growth conditions limited by carbon and/or nitrite or nitrite[J].Water Environment Research,1996,68(5):934-945.
[15] BEUN J J,VERHOEF E V,LOOSDRECHT M C M V,et al.Stoichiometry and kinetics of poly-β- hydroxylbutyrate metabolism under denitrifying conditions in activated sludge cultures[J].Biotechnology and Bioengineering,2000,68(5):496-507.
[16] GONG Lingxiao,HUO Mingxin,YANG Qing,et al.Performance of heterotrophic partial denitrification under feast-famine condition of electron donor: a case study using acetate as external carbon source[J].Bioresource Technology,2013,133:263-269.
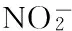
[18] GE S J,PENG Y Z,WANG S,et al.Nitrite accumulation under constant temperature in anoxic denitrification process: the effects of carbon sources and COD/NO3-N[J].Bioresource Technology,2012,114(3):137-143.
Studyonnitrite-NaccumulationcharacteristicsduringdenitrificationprocessinlowC/Nratiosewage
LILingling,LIUXiaoping,YANGZhaoxue.
(CollegeofEnvironmentandSafetyEngineering,QingdaoUniversityofScience&Technology,QingdaoShandong266042)
Batch denitrification experiments were carried out,using sodium acetate as carbon source,to investigate the effects of temperature on nitrite accumulation of low C/N ratio sewage during denitrification process. The results showed that nitrite accumulation was observed at different temperatures in sewage with different C/N ratio. At the same temperature,higher maximum nitrite accumulation ratio (NAR) could be obtained as a result of the increase of C/N ratio. The highest increment of maximum NAR appeared at 15 ℃,with maximum NAR was only 18.8% at C/N ratio of 1.03,and the maximum NAR reached 83.9% at C/N ratio of 4.16. At the same C/N ratio,higher maximum NAR could be observed at higher temperature. When the temperature was increased from 15 ℃ to 25 ℃,the maximum NAR was also increased from 18.8% to 51.7% at C/N ratio of about 1. As the alkalescence of sodium acetate,pH went up to the maximum value at the initial reaction stage. When nitrate was reduced to nitrite,sodium acetate was converted into carbon dioxide,which resulted in the decreasing pH values. When nitrate was completely removed,nitrite began to be further reduced and pH went up again.
temperature; low C/N ratio; nitrite-N accumulation; pH
李玲玲,女,1974年生,博士,副教授,主要从事污水生物处理研究。#
。
10.15985/j.cnki.1001-3865.2016.12.014
编辑:丁 怀 (
2016-06-25)

