离子液体绿色脱硫机理及应用进展
林 燕,王 芳,张志庆,杨 洁,魏 颖
(中国石油大学(华东)理学院,山东 青岛 266580)
油品中硫化物的存在严重影响着油品的质量,造成诸多危害[1],如腐蚀石油加工设备、使用于油品精制的催化剂中毒、降低油品的氧化稳定性使其易变黑发臭等。并且含硫油品燃烧产生的含氧硫化物是酸雨形成、温室效应和大气污染的一个重要因素。因此,控制油品中硫化物的含量势在必行。随着世界各国对汽、柴油中硫含量的要求日益严格[2],我国也采取了相应的措施,但是考虑到我国的实际情况,将分阶段控制油品硫化物含量,逐步与国际接轨,达到低硫目标[3]。
研发一种有效的脱硫工艺是控制油品硫含量的最重要途径。目前,传统加氢脱硫是脱硫工艺发展的主流[4],但操作条件严格(温度>300 ℃,压力>40 atm)且耗费大量的氢气和昂贵的催化剂[5],投资成本高、催化剂技术发展缓慢,脱硫效果也不能达到深度脱硫标准,而且往往会降低汽油的辛烷值。并且加氢脱硫虽然可以除去脂肪族和脂环烃硫化物,但是由于没有合适的催化剂和立体障碍的原因,噻吩、硫芴及其衍生物的脱除就很困难了[6-9]。为了适应发展,一些先进的非加氢脱硫技术发展起来,如生物脱硫[10]、氧化脱硫[11]、吸附脱硫[12]、萃取脱硫[13]等。其中,萃取脱硫能耗低,操作控制简单容易,同时避免了汽油辛烷值的损失,具有极大优势[14]。溶剂脱硫的萃取剂一般为有机溶剂,毒性大,脱硫率也不高。近十几年兴起的离子液体是一种非常清洁的液液萃取介质,应用于脱硫,相比于传统的分子溶剂很有优势[15]。
离子液体就是在室温或近室温条件下以液态存在的有机熔盐,它完全由离子组成,具有良好的物化特性,如挥发性小、可回收利用等,其中一个显著优点就是可以通过选择不同类型的阴阳离子合成选择性的液液分离萃取剂。诸多研究表明,具有芳香结构的离子液体在室温条件下对同样含芳香结构的硫化物有很好的脱除效果。
本文将从离子液体脱硫的影响因素、脱硫机理、脱硫的方法及新型离子液体——负载化离子液体等几个方面阐述离子液体在油品脱硫中的应用。
1 影响离子液体脱硫效率的因素探讨
文献中对影响离子液体脱硫效果的因素研究主要集中于3个方面,即离子液体结构(包括阴阳离子的结构)、硫化物结构和油品的非含硫组分的影响。
1.1 离子液体阴阳离子结构对脱硫效果的影响
Bössman等[16]研究了一些离子液体萃取脱硫能力,首先发现了离子液体萃取脱硫效果受其阴阳离子尺寸大小的影响很大。Nie等[17]的研究结果验证了上述结论。
Mochizuki等[18]制备了 6种 1-烷基(R1)-3-烷基(R2)-咪唑硫酸烷基(R3)盐并用于对硫芴/正十二烷模拟油的脱硫,结果显示R1、R2、R3不管是哪个烷基链增长都能使得脱硫率增大,尤其是阳离子部分R2的影响更显著。在Nie等[17]所研究的咪唑类离子液体中,对同一芳香硫化物,阴离子相同的离子液体脱硫能力随咪唑环上取代基增大而增大。周瀚成等[15]研究了 1-烷基-3-甲基咪唑四氟硼酸盐与六氟磷酸盐([CnMIM][BF4]与[CnMIM][PF6],n=2,4,8)6种咪唑类离子液体的脱硫性能,结果也表明,较长碳链的[C8MIM][BF4]有较好的脱硫效果。
从以上研究可知,增大离子液体阳离子体积对提高脱硫率是有利的。对此可解释为:一方面,阳离子的体积增大,阴阳离子之间的库仑作用减弱,所形成的“堆垛”结构没有那么紧密,使得可插入的芳香硫化物的分子数增多。另一方面,以咪唑类离子液体为例,阳离子上的烷基取代基链越长,咪唑环的对称性越差,阳离子极化性就越强,与噻吩类硫化物的络合作用就越强,并且烷基是给电子基,可以增强硫原子与咪唑环的π-π作用。但是,过长的烷基侧链由于空间位阻效应较大,反而影响萃取脱硫效果[18-19]。
在上述Mochizuki的研究[18]中,阴离子部分的R3增大,脱硫率也增大。胡松青等[20]研究也发现,对于同一阳离子BMIM+,阴离子不同的离子液体其脱硫效果也不同,其大小顺序为:PF6−离子液体>BF4−离子液体>Cl−离子液体,验证了阴离子体积增大脱硫率增大的结论。对此的解释是,硫化物在离子液体中的溶解度受空间效应的影响,阴离子体积增大使得阳离子不会靠得很近,离子液体间的芳香环电流作用降低,“堆垛”结构没有那么紧密了,可插入的硫化物分子数增多,脱硫率提高。
由此可见,离子液体的结构影响其萃取脱硫效果,在一定限度内增大阴阳离子的体积有助于提高脱硫率。
1.2 不同含硫化合物对脱硫效果的影响
油品中的硫化物可分为两类[21]:能与金属直接发生反应的硫化物称活性硫,包括元素硫、硫化氢和硫醇等;不与金属直接发生反应的硫化物称非活性硫,包括硫醚、二硫化物、噻吩及其衍生物等。燃油中有80%以上的硫是以噻吩及其衍生物等非活性硫形式存在的[22],因此有效地脱除这部分硫化物意义重大,图1为几种常见芳香硫化物的结构式。

图1 几种常见芳香含硫化物
由于咪唑类离子液体对芳香硫化物的脱除主要是由于它们之间的π-π络合作用,相同离子液体与不同硫化物的作用效果不同,对其的萃取能力也就不同,Esser等[23]的研究结果表明,离子液体对DBT的萃取能力最佳,其次依次是BT、4,6-DMDBT和 TS。冯婕等[24]研究的磷酸酯类离子液体脱硫率由大到小也有DBT>BT>3-MT的顺序。对此的解释是,在TS支链上引入烷基后,不仅降低了芳香环π电子云的密度,而且增加了位阻效应,降低了脱硫率,但是当在支链上引入芳香环后,大π键的作用增加导致其与离子液体的π-π作用也增强了,离子液体萃取能力大大增加并抵消了空间位阻带来的反作用。而对于不含芳环的硫醇、硫醚等脂肪族硫化物,离子液体对其的萃取能力极弱[19]。
1.3 油品中的其它非含硫组分对脱硫效果的影响
影响脱硫效果的因素除了上述两方面外,油品中的其它非含硫组分的存在也是一个不可忽视的因素。Nie等[17]用一步法合成了一系列二烷基磷酸盐的离子液体,并以甲苯为代表讨论了模拟油中非含硫芳香物对噻吩脱除率的影响,结果表明随甲苯在模拟油中含量增加,离子液体的脱硫率下降。原因是甲苯也有较高的芳香电子密度,与离子液体作用时也易被极化,也有π-π络合效应,与芳香硫化物存在竞争作用,使得离子液体更易饱和,脱硫率下降。而油品中的其它脂肪族化合物虽然可极化电子很少,但也会或多或少地插入离子液体“堆垛”结构中,影响离子液体的脱硫率。
研究离子液体脱硫影响因素将有利于理解离子液体脱硫机理。
2 离子液体脱硫机理探讨
吸收了有机硫的离子液体可以通过蒸馏等方法再生,并回收噻吩类硫化物[25-26],这点说明它们之间的作用并不是化学作用。离子液体与芳香硫化物之间存在芳香环电流作用(即π-π作用),氢键作用等,但π-π作用是最主要的。
离子液体中阳离子,如咪唑阳离子或吡啶阳离子和油品中噻吩等硫化物都有很强的芳香性,氮原子上的孤对电子使其极性很强,而噻吩类硫化物 π电子云密度较大,离子液体与噻吩类硫化物接触后,诱导其离散π键产生极化作用,极化后的π键与咪唑环或吡啶环的大π键产生π-π络合效应,从而增强离子液体与芳香硫化物之间的作用力,使其易被萃取至离子液体相中。并且,由于离子液体分子结构较大,其阴阳离子可以形成“堆垛”结构[27],这样就使硫化物分子可以插入其“堆垛”结构中,形成液相包合物,达到了脱硫的目的。
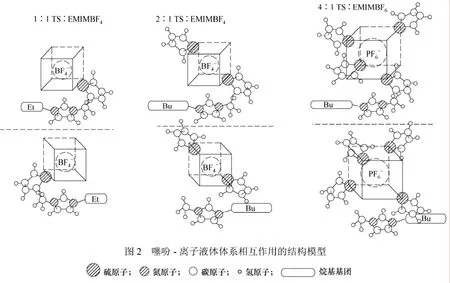
Su等[28]用1H、19F、11B、31P核磁共振法研究了噻吩与[BMIM][PF6]、[BMIM][BF4]和[EMIM][BF4]3种离子液体之间的作用。研究表明离子液体的脱硫率取决于其阴阳离子的结构。1H NMR研究还表明噻吩环碳质子的化学位移比离子液体咪唑环碳质子的化学位移位于更高场,这说明噻吩环碳上的平均电子云密度比离子液体咪唑环碳上的大。当将二者混合且噻吩含量增大时,离子液体咪唑环碳质子及烷基取代基质子的化学位移都向高场移动,而噻吩环碳上质子的化学位移向低场移动,这说明噻吩与离子液体之间产生了相互作用,这种作用主要是芳香环电流作用,利用化学位移高低场移动量的大小可以判断它们之间作用的强弱。处于芳环屏蔽区上方或下方的化合物的化学位移情况不同,利用这点可以判断分析噻吩与离子液体阴阳离子之间的位置关系。1H NMR结果显示,EMIMBF4-噻吩体系中EMIMBF4化学位移向低场移动得最大,说明其与噻吩的作用最强。但是因为 EMIMBF4咪唑阳离子上比BMIMBF4和BMIMPF6小且阴离子BF4−也比PF6−小,EMIMBF4的“堆垛”结构最紧密,“堆垛”结构越紧密,可插入的硫化物分子数就少,所以出现了脱硫率 BMIMPF6>BMIMBF4>EMIMBF4的结果。他们还根据1H、19F、11B、31P核磁共振数据绘制了离子液体-噻吩体系的相互作用模型,见图2:噻吩分子平面朝向离子液体阳离子,而硫原子指向阴离子,形成了不同分子数比例的噻吩/离子液体的重复“堆垛”结构(实验结果表明对BMIMPF6是4∶1,BMIMBF4是 2∶1,EMIMBF4是 1∶1,由此也说明BMIMPF6脱除噻吩的效率较高)。
Revelli等[29]做了类似的研究,他们用1H 和31P NMR研究了 1-丁基-3-甲基咪唑硫氰酸盐([BMIM][SCN])、[BMIM][BF4]和 1-甲基-3-甲基咪唑磷酸甲酯盐([MMIM][MP])3种离子液体与噻吩之间的作用,得到相似的结论。结果显示噻吩与[BMIM][SCN]形成“堆垛”结构,分子数之比为3.95∶1,相比于其它两种要好([BMIM][BF4]为2∶1,[MMIM][MP]为 0.91∶1),是较为理想的脱硫剂。
3 离子液体用于油品脱硫的方法
目前,国内外用于油品脱硫的离子液体阳离子主要为咪唑类、吡啶类和吡咯类,阴离子的选取范围则相对较广,Lewis酸类、氟硼酸类、氟磷酸类、酸酯类等均具有很好的脱硫效果。现在研究的离子液体脱硫方法主要有直接萃取脱硫法、氧化-萃取脱硫法、烷基化脱硫法和电化学聚合脱硫法。
3.1 直接萃取脱硫
这种方法将离子液体与油品混合,一定温度下搅拌使硫化合物萃取到离子液体相中。此项工艺一般包括萃取分离和离子液体回收再生两部分。其工艺流程图如图 3[30],高硫油从塔低进入萃取塔,与塔顶进入的离子液体充分混合后,静置分层,上层是低硫油,下层是含硫离子液体,下层含硫离子液体再进入再生塔,再生后重复进入萃取塔。
2001年,Bössman等[16]发表了首篇离子液体用于柴油硫化物的选择性脱除的论文,他们分别将氯化 1-丁基-3-甲基咪唑和氯化 1-乙基-3-甲基咪唑与AlCl3混合得到两种Lewis酸离子液体,并研究了它们的脱硫特性,结果表明它们都能有效脱除硫化物。但是此类离子液体会产生黑色沉淀且对水非常敏感,易水解产生HCl,在空气中不稳定,因此,实际应用有困难。

图3 离子液体直接萃取脱硫工艺流程示意
一些学者研究了相对不易水解的含BF4−、PF6−的咪唑类离子液体[31-33],结果表明芳香硫化物优先从油品中脱除,与此同时,其它非含硫的芳香化合物也有一定程度的损失,导致辛烷值有所降低。而且含BF4−、PF6−的离子液体合成起始原料较昂贵,温度较高时遇水也会产生腐蚀性的HF[34]。
可以采用无卤素的离子液体克服腐蚀性和稳定性的问题。Alonso等[35-36]制备了1-乙基-3-甲基咪唑硫酸乙基盐([EMIM][EtSO4])应用于油品脱硫的研究,液液平衡数据表明[EMIM][EtSO4]用于油品脱硫是十分有效的。Nie等[37-38]研究了1-丁基-3-甲基咪唑磷酸二丁酯盐([BMIM][DBP])、1-乙基-3-甲基咪唑磷酸二乙酯盐([EMIM][DEP])和 1-甲基-3-甲基咪唑磷酸二甲酯盐([MMIM][DMP])3种离子液体的脱硫效果,得到脱硫能力[BMIM][DBP]>[EMIM][DEP]>> [MMIM][DMP]的结果。Huang等[39]合成氯化1-甲基3-丁基咪唑/氯化铜,这也是一种在水和空气中可以稳定存在的离子液体,并且由于Cu(I)与芳香硫化物的π-π配合作用较强,直接萃取脱硫效果很好,可以使汽油中的含硫化合物降低37%。
离子液体在油品中有一定的溶解度,不仅会造成油品二次污染,还增加了离子液体回收成本,限制其在油品脱硫中的应用。Gao等[40]发现吡啶类离子液体在油品中几乎不溶,他们研究了N-丁基吡啶四氟硼酸盐([BPy][BF4])、N-己基吡啶四氟硼酸盐([HPy][BF4])和N-辛基吡啶四氟硼酸盐([OPy][BF4])对柴油中芳香硫化物的选择性脱除,结果表明这3种离子液体脱硫效果很好,并且吡啶上烷基取代基链越长脱硫效果越好。他们还用高效液相色谱分析了饱和此类离子液体的柴油组分,没有出现离子液体的峰,说明其不会污染油品。此研究小组[41]在此基础上又考察了 3-甲基吡啶类离子液体室温脱除柴油中芳香硫化物的能力,得到了相似结论,并认为此类离子液体是一种非常有前景的脱硫萃取剂。Francisco等[42]分别研究了1-己基-3,5-二甲基吡啶双三氟甲磺酸亚胺盐([hmmpy][Ntf2])+噻吩+烷烃(正己烷、正十二烷、正十六烷)三元体系在298.15K大气压下的液液平衡数据,结果表明此离子液体有很好的脱硫效果,相比于其它几种咪唑类离子液体,[hmmpy][Ntf2]有最好的萃取硫容,将其应用于真实油品,也表现出很好的脱硫效果,最后并未检测出已脱硫油品中有此离子液体的存在。Holbrey等[43]考察了不同阳离子(咪唑盐、吡啶盐、吡咯盐和喹啉盐)和不同阴离子的离子液体脱除模拟油中DBT的能力,结果表明阳离子的种类影响脱硫效果,相同阴离子的离子液体的脱离能力顺序是甲基吡啶盐≥吡啶盐≈咪唑盐≈吡咯盐,并且他们还发现当阴离子为乙酸根和硫氰酸根时脱硫效果最好,这两种阴离子的吡啶类离子液体表现出最好的脱硫特性,单次萃取 DBT的效率可达81%~83%。
目前,离子液体脱硫研究多集中于离子液体的脱硫能力,很少考虑萃取过程中离子液体黏度大导致平衡时间长的问题,而这对实际工业应用将产生不可忽视的影响。Asumana等[44]研究了阴离子为二腈胺根([N(CN)2]−)低黏度离子液体在油品脱硫中的应用:[BMIM][N(CN)2]、[EMIM][N(CN)2]、四氢噻吩二腈胺盐([S2][N(CN)2])和乙基二甲基硫二腈胺盐([EtMe2S][N(CN)2]),研究结果表明[BMIM][N(CN)2]的脱硫效果最好,并且在油品中几乎不溶,萃取平衡时间非常短(室温下小于5 min),温度和初始硫浓度对其萃取率影响不大,可回收利用性好。Yu等[45]也考察了低黏度离子液体[EMIM][N(CN)2]的直接萃取和氧化-萃取脱硫效果,直接萃取不到5min达到平衡,几次萃取后油品中硫含量仅剩下约10 μg/g,但是此离子液体的氧化-萃取脱硫效果不佳,他们从分子计算角度解释了这一结果。
3.2 氧化-萃取脱硫法
这是一种相对较复杂的脱硫法。其原理是:硫化物萃取至离子液体相后,被氧化剂氧化成极性更大的砜或亚砜,继续留在离子液体中,而随着未被氧化的硫化物在离子液体中含量降低,导致其在两相中的萃取平衡被打破,这样会使得更多的硫化物被萃取到离子液体相被氧化,从而脱硫率大大提高了,过程如图4所示[19]。

图4 DBT离子液体氧化-萃取过程
Wei 等[46]以[BMIM][BF4]和[BMIM][PF6]为萃取剂,H2O2为氧化剂,乙酸为催化剂,对由 DBT和十四烷烃模拟油进行了萃取-氧化的研究。以[BMIM][BF4]、[BMIM][PF6]为萃取剂直接萃取脱除DBT,脱硫率为39%和47%,但若与氧化法结合脱硫率大大提高,在70℃,反应进行10 h,[BMIM][BF4]和[BMIM][PF6]的脱硫率分别达到55%和85%。
Liu等[47]用氯化三甲基一苄基铵/氯化锌离子液体(Me3NCH2C6H5Cl /2ZnCl2)对模拟油中DBT进行氧化-萃取脱除,以H2O2为氧化剂,乙酸为催化剂,在优化条件下DBT的脱除率可达到94%,比单用离子液体高很多(28.9%),回收利用6次活性无明显损失,他们还对DBT的氧化脱除过程进行了动力学研究,表明这是一个速率常数为 0.0482 min−1、半衰期是8.23 min的一级反应过程。
Li等[48]合成了四丁基铵十聚钨酸盐([(C4H9)4N]4W10O32)、四甲基铵十聚钨酸盐([(CH3)4N]4W10O32)和三乙基-苄基铵十聚钨酸盐([(C2H5)3NC7H7]4W10O32)3种物质,作为萃取-氧化脱硫的催化剂,以H2O2为氧化剂,[BMIM][PF6]为萃取剂,结果表明[(C4H9)4N]4W10O32的催化活性最好,在优化的条件下,可使以DBT和正辛烷组成的模拟油中硫含量从1000 μg/g降低到8 μg/g,完全达到了深度脱硫的要求。
外加催化剂(乙酸、钨化物等)虽然可以有效地应用于氧化-萃取脱硫,但是却存在难分离、难回收的问题,而且痕量催化剂的溶解也会污染油品。而有些离子液体本身就可以作为氧化脱硫的催化剂。Lu等[49]以[HMIM][BF4]为萃取剂和催化剂,以H2O2为氧化剂,对DBT和正辛烷组成的模拟油进行了脱硫实验,在 70 ℃、80 ℃、90 ℃时,脱硫率分别为65%、70%、93%。Zhao等[50]在N-甲基吡咯烷酮四氟硼酸盐([Hnmp][BF4])和氧化剂 H2O2共存的情况下,对模拟油和柴油进行了氧化-萃取脱硫研究,研究结果表明此体系对模拟油中DBT的脱除率可达到100%,即使回收利用7次后脱硫率仍能达到95%,将其应用于真实柴油,脱硫率也达到了99.4%,此过程中[Hnmp][BF4]既是萃取剂也是催化剂。后来Zhao等[51]又以N-甲基吡咯烷酮磷酸氢盐离子液体([Hnmp][H2PO4])为萃取剂和催化剂,以H2O2为氧化剂,在最优条件下将99.8%的DBT从模拟油中脱除,应用在真实油品也能脱除 64.3%的硫化物。Gao等[52]以 Brønsted酸离子液体 1-丁基-3-甲基咪唑硫酸氢盐([BMIM][HSO4])和N-丁基吡啶硫酸氢盐([C4Py][HSO4])作为柴油氧化-萃取脱硫的萃取剂和催化剂,优化条件下模拟油中的DBT的脱除率达到99.6%,应用于真实柴油脱硫率也可达到85.5%(单用离子液体脱硫率仅为11.0%)。Yu等[53]以 Lewis酸离子液体,氯化1-丁基-3-甲基咪唑/氯化锌([BMIM][Cl]/2ZnCl2和[BMIM][Cl]/ZnCl2),Brønsted 酸离子液体 1-甲基-3-乙酸基硫酸氢盐([CH2COOH mim][HSO4])、1-甲基-3-(丁基-4-亚磺酸基)咪唑硫酸氢盐([SO3HC4mim][HSO4])、1-甲基咪唑硫酸氢盐([HMIM][HSO4])和[BMIM][HSO4]为氧化-萃取脱硫的萃取剂和催化剂,结果表明除了[CH2COOHmim][HSO4]外,其余各离子液体都能很好的脱除模拟油中的DBT,尤其是[BMIM][Cl]/2ZnCl2和[SO3HC4mim ][HSO4],脱硫率甚至可达到100%,[BMIM][Cl]/2ZnCl2对真实柴油的脱硫率也达到了 87.7%,但是对于硫含量很高(5380 μg/g)的油品脱硫效果很不理想,因此可用本文研究的离子液体对加氢脱硫后的油品继续深度脱硫。
从上述研究可以看出离子液体氧化-萃取脱硫法能大大提高脱硫率。
3.3 烷基化脱硫
烷基化脱硫也是一种非加氢脱硫方法,即采用酸性催化剂使油品中的噻吩类硫化物与烯烃进行烷基化反应得到相对分子质量更大的烷基噻吩,使其沸点升高以至超出原料油的馏程范围,通过蒸馏的方法就可将这些硫化物除去,实现脱硫目的[54-55]。离子液体物理化学性质优良,其酸性可调的性质使其可成为良好的烷基化脱硫催化剂。
Chauvin等[56-57]早期研究了由氯化 1-丁基-3-甲基咪唑与AlCl3制得的离子液体催化异丁烷与2-丁烯的烷基化反应,发现将某些过渡金属无机盐引入咪唑或吡啶类离子液体中有利于提高烷基化的选择性。黄蔚霞等[58]研究了新型AlCl3-叔胺离子液体催化剂在催化裂化(FCC)汽油脱硫中的应用。研究结果表明,此离子液体用于FCC汽油烷基化脱硫,脱硫率可达80%以上。处理后油样烯烃含量明显下降,而环烷烃与异构烷烃含量有所增加,辛烷值变化不大。刘植昌等[59]将胺盐离子液体用于FCC汽油烷基化脱硫实验,考察了不同阳离子、阴离子和阴阳离子摩尔比对FCC汽油脱硫率的影响。结果表明,由A1Cl3与(C2H5)3NHCl按摩尔比为2∶1合成的离子液体烷基化脱硫效果最佳,脱硫率在70% 以上,汽油收率在95 %以上,辛烷值基本无变化。柯明等[55]研究了 Brønsted酸离子液体[BMIM][HSO4]与H2SO4复配体系在FCC汽油烷基化脱硫中的应用。研究结果表明,催化剂酸性增强,汽油脱硫率增大;加入少量二烯烃可明显提高脱硫率。在优化的条件下(30 ℃、反应2 h、5%复配催化剂)加入适量二烯烃,可使石家庄 FCC汽油硫质量浓度由608 mg/L降至105 mg/L,大港FCC汽油硫含量由122 mg/L降至32 mg/L,且辛烷值变化不大。
3.4 离子液体-电化学聚合脱硫法
电化学反应通常在常温常压下进行,毒性和危害性都较小,也是清洁技术的重要组成部分。而离子液体具有很高的电导率,十分低的蒸汽压,电化学窗口又较宽,因此可以作为电解质溶剂在电化学聚合上发挥重大作用[60]。
石家华等[61]在离子液体[BMIM][PF6]中通过电化学聚合的方法使汽油中噻吩及其衍生物聚合成难溶的聚合物,进而通过过滤或蒸馏的方法将其除掉。亓西敏等[62]用电化学方法脱除了模拟汽油中的噻吩。他们考察了噻吩在[HMIM][BF4]、[BMIM][BF4]和[BMIM][PF6]三种离子液体中的电化学聚合情况,结果表明,噻吩在这3种离子液体中均能聚合,脱除率达到50%~90%。
采用电化学聚合法可以在离子液体中脱除油品中能够聚合的硫化物(主要为噻吩类),而汽油的辛烷值不变,因此有一定的应用前景,但是目前离子液体在这方面的研究还不是很多。
4 离子液体的回收
离子液体的回收方法因离子液体的种类和脱硫情况而异。文献中离子液体回收的方法主要有 3种:①加热离子液体除去硫化物;②离子液体加入水使硫化物沉淀;③使用低沸点的烃类来二次萃取硫化物。对于疏水类离子液体如[BMIM][PF6],可通过蒸馏的方法回收[63],这种方法需要消耗大量的热量,并且只对低沸点的硫化物(如TS)有效。对于亲水且对水稳定的离子液体(如[EMIM][BF4])可以加入适量水,使硫化物被释放成为单一相,再将水从水/离子液体混合相中蒸馏并分离[64],此法也要消耗大量的热量,因此仅适用于实验室研究,工业化应用有困难。对于沸点很高的二苯并噻吩及其烷基取代物,离子液体的回收就变得十分困难了,可采用先加入二次萃取溶剂,然后再蒸馏分离二次萃取溶剂和硫化物的方法,最有前景的二次萃取溶剂是低沸点的烃类(如戊烷和己烷)。除此之外,也可以使用超临界CO2将硫化物从离子液体中分离,此方法要考察硫化物在离子液体和超临界CO2间的分配系数[65]。
不管用哪种方法,离子液体的回收再利用过程都是比较繁琐复杂的,而且离子液体脱硫往往需要多级萃取才能达到要求。但若将离子液体负载到某一固相上,且保证其在固相载体不会流失的同时,本身的活性也不损失,就可以通过简单的热处理或溶剂洗提来回收,此体系还能用于固定床,保证脱硫效果的同时简化操作。
5 负载化离子液体的应用
常用的离子液体负载方法[66]主要包括物理吸附、化学键合和纳米化负载等,用来作为负载化的载体一般为活性炭、多孔硅胶、表面有活性基团的聚合物等材料。
2009年,Tian等[67]将氯化1-甲基咪唑离子液体负载到硅胶上并用来分离丹参中的丹参酮,这是首篇将硅胶负载化离子液体应用于固相萃取(SPE)的研究报道。此后他们[68]又用硅胶负载化氯化 2-乙基-4-甲基咪唑离子液体从欧亚甘草和内服药中分离萃取甘草黄甙和甘草酸,取得了很不错的效果。Vidal等[69]综述了近几年来负载化离子液体应用于SPE中一些研究发展现状,说明负载化离子液体应用于物质分离是十分有效的。
Xie等[70]合成了3种氯甲基聚苯乙烯负载化离子液体(分别为咪唑类、吡啶类和三乙基胺类)并将其应用于柴油中氮化物的选择性脱除,首先考察了 3种负载化离子液体在硫芴和咔唑的甲苯/正十二烷烃模拟油中的脱硫脱氮效果,结果显示三乙基胺类离子液体几乎无脱硫脱氮效果,而咪唑类、吡啶类有一定的效果并且对氮化物的脱除选择性较高。他们的研究从侧面说明负载化离子液体用于油品脱硫是可行的。
Kuhlmann等[71]合成了多孔硅胶负载化咪唑类离子液体,首次将其应用于模拟油脱硫研究。因为多孔硅胶表面积很大,离子液体只在上面分布了一薄层,从而避免了传质局限,此负载化离子液体脱硫效果非常好,可将其应用于简单的填充柱脱硫。
Wang等[72]合成了3种氯甲基聚苯乙烯负载化金属卤化物/咪唑离子液体(M/CMPS-ImCl,M=CuCl、ZnCl2、FeCl3),并将其应用于模拟油中噻吩及其同系物的脱除研究。结果表明这3种负载化离子液体室温对硫化物的脱除十分有效,CuCl/CMPS-ImCl的脱硫效果最好,原因是Cu+与噻吩的π-π络合作用最强。再生利用实验结果表明此负载化离子液体回收利用6次后,脱硫活性没有明显的损失。
6 结 语
目前,离子液体应用于油品脱硫的研究已引起国内外专家学者的广泛关注。离子液体虽然显示了较好的脱硫效果,但其价格较昂贵,应用于油品脱硫时需多级萃取,易造成损失,且回收利用困难。要解决离子液体用于油品脱硫的现实问题,还需进一步加强离子液体在合成工艺、脱硫选择性及回收再生等方面的研究。
负载化离子液体综合了离子液体和固相载体的优点,应用于油品脱硫,在一定程度上克服了单纯用离子液体的弊病,减少了离子液体的用量,并且操作装置简单,易自动化。将离子液体有效地负载于固相载体上还是相对比较复杂的,需选择合适的固相载体,设计可行的负载路线,但是随着对负载化离子液体研究的深入,其合成方法将逐渐成熟,由此我们认为,将负载化离子液体应用于油品脱硫发展前景广阔。
[1]余江,王亚林,孙同华,等.活性炭纤维吸附型固相微萃取方法检测油品中含硫化合物的研究[J].石油与天然气化工,2004,6:444-446.
[2]Francisco M,Arce A,Soto A,et al.Ionic liquids on desulfurization of fuel oils[J].Fluid Phase Equilibria,2010,294:39-48.
[3]张建伟,方茂东.从汽车排放控制谈我国汽油质量战略[J].汽车工程,2006,28(1):43-47.
[4]刘影,徐忠贤.汽油脱硫意义及脱硫技术浅述[J].石油商技,2002,20(5):22-24.
[5]唐晓东,赖先熔,李晓贞,等.直馏柴油络合萃取脱硫的实验研究[J].石油炼制与化工,2010,41(12):16-19.
[6]Rothlisberger A,Prins R.Intermediates in the hydrodesulfurization of 4,6-dimethyl-dibenzothiophene over Pd/gamma-Al2O3[J].Journal of Catalysis,2005,235(1):229-240.
[7]Jiang Z,Liu Y,Sun X,et a1.Activated carbons chemically modified by concentrated H2SO4for the adsorption of the pollutants from waste water and the dibenzothiophene from fuel oils[J].Langmuir,2003,19(3):731-736.
[8]Ma X,Sakanishi K,Mochida I,et a1.Hydrodesulfurization reactivities of various sulfur compounds in diesel fuel[J].Ind.Eng.Chem.Res.,1994,33 (2):218–222.
[9]Shafi R,Hutcnings G J.Hydrodesulfurization of hindered dibenzothiophenes:An overview[J].Catal.Today,2000,59 (3-4):423-442.
[10]Boron D J,Deever W R,Atlas R M,et a1.Biodesulfurization of gasoline:An assessment of technical and economic feasibility and outline of R & D roadmap toward commercialization[C]//1999 NPRA Annual Meeting,AM-99-54.
[11]Shiraishi Y,Tachibana K,Hirai T,et a1.Desulfurization and denitrogenation process for light oils based on chemical oxidation followed by liquid-liquid extraction[J].Ind.Eng.Chem.Res.,2002,41(17):4362-4375.
[12]李倩,杨西萍.汽油吸附脱硫吸附剂的研究进展[J].中国石油和化工标准与质量,2011,31(8):285-286.
[13]Fadeev A G,Meagher M M.Opportunities for ionic liquids in recovery of biofuel[J].Chem.Commun.,2001,295-296.
[14]贾睿生.汽油氧化脱硫和离子液体萃取脱硫的研究[D].天津:河北工业大学,2009.
[15]周瀚成,陈楠,石峰,等.离子液体萃取脱硫新工艺研究[J].分子催化,2005,19(2):94-97.
[16]Bösmann A,Datsevich L,Jess A,et a1.Deep desulfurization of diesel fuel by extraction with ionic liquids[J].Chem.Commun.,2001:2494-2495.
[17]Nie Y,Li C X,Hong M,et a1.N,N-dialkylimidazolium dialkylphosphate ionic liquids:Their extractive performance for thiophene series compounds from fuel oils versus the length of alkyl group[J].Full Processing Technology,2008,89:978-983.
[18]Mochizuki Y,Sugawara K.Removal of organic sulfur from hydrocarbon resources using ionic liquids[J].Energy & Fuels,2008,22(5):3303-3307.
[19]黄廷昌,苑建.离子液体应用于燃油脱硫技术的研究进展[J].河北化工,2011,34(5):44-47.
[20]胡松青,张军,刘冰,等.离子液体萃取脱硫的探索性研究[J].石油学报:石油加工,2007,23(1):100-103.
[21]杨洪云,赵德智,沈耀亚.油品脱硫工艺技术及其发展趋势[J].石油化工高等学校学报,2001,14(3):26-30.
[22]周二鹏,刘会茹,赵地顺,等.离子液体在清洁燃油中的应用研究进展[J].河北化工,2011,34(7):41-45.
[23]Esser J,Wasserscheid P,Jess A.Deep desulfurization of oil refinery streams by extraction with ionic liquids[J].Green Chem.,2004,6:316-322.
[24]冯婕,李春喜,孟洪,等.磷酸酯类离子液体在燃油深度脱硫中的应用[J].石油化工,2006,35(3):272-276.
[25]Zhang S G,Zhang Q L,Zhang Z C.Extractive desulfurization and denitrogenation of fuels using ionic liquids[J].Ind.Eng.Chem.Res.,2004,43:614-622.
[26]胡义,王光辉,曾丹林,等.离子液体在回收模拟粗苯中噻吩的研究[J].化学工程,2011,39(8):65-68.
[27]Margulis C J,Stern H A,Berne B J.Computer simulation of a “green chemistry” room-temperature ionic solvent[J].J.Phys.Chem.B,2002,106(46):12017-12021.
[28]Su B M,Zhang S G,Zhang Z C.Structural elucidation of thiophene interaction with ionic liquids by multinuclear NMR spectroscopy[J].J.Phys.Chem.B,2004,108:19510-19517.
[29]Revelli A L,Mutelet F,et al.Extraction of benzene or thiophene fromn-heptane using ionic liquids:NMR and thermodynamic study[J].J.Phys.Chem.B,2010,114:4600-4608.
[30]刘先军,王宝辉,刘淑芝,等.离子液体在燃油脱硫技术领域的应用[J].应用化工,2011,40(5):888-891.
[31]Zhang S,Zhang Z C.Novel properties of ionic liquids in selective sulfur removal from fuels at room temperature[J].Green Chem.,2002,4:376-379.
[32]Zhang S,Zhang Q,Zhang Z C.Extractive desulfurization and denitrogenation of fuels using ionic liquids[J].Ind.Eng.Chem.Res.,2004,43:614-622.
[33]Chu X,Hu Y,Li J,et a1.Desulfurization of diesel fuel by extraction with [BF4]-based ionic lquids [J].Chin.J.Chem.Eng.,2008,16(6):881-884.
[34]Swatloski R P,Holbrey J D,Rogers R D.Ionic liquids are not always green: Hydrolysis of 1-butyl-3-methylimidazolium hexafluorophosphate[J].Green Chem.,2003,5:361-363.
[35]Alonso L,Arce A,Francisco M,et a1.Thiophene separation from aliphatic hydrocarbons using the 1-ethyl-3-methylimidazolium ethylsulfate ionic liquid[J].Fluid Phase Equilib.,2008,270:97-102.
[36]Alonso L,Arce A,Francisco M,et a1.Liquid-liquid equilibria of([C2mim][EtSO4]+thiophene+2,2,4-trimethylpentane) and([C2mim][EtSO4]+thiophene+toluene):Experimental data and correlation[J].J.Solution Chem.,37:1355-1363.
[37]Nie Y,Li C,Sun A,et a1.Extractive desulfurization of gasoline using imidazolium-based phosphoric ionic liquids[J].Energy Fuels,2006,20(5):2083-2087.
[38]Nie Y,Li C,Wang Z H.Extractive desulfurization of fuel oil using alkylimidazole and its mixture with dialkylphosphate ionic liquids[J].Ind.Eng.Chem.Res.,2007,46(15):5108-5112.
[39]Huang C,Chen B,Zhang J,et a1.Desulfurization of gasoline by extraction with new ionic liquids[J].Energy Fuels,2004,18:1862-1864.
[40]Gao HS,Luo M F,Xing JM,et al.Desulfurization of fuel by extraction with pyridinium-based ionic liquids[J].Ind.Eng.Chem.Res.,2008,47:8384-8388.
[41]Gao H S,Li Y G,Wu Y,et al.Extractive desulfurization of fuel using 3-methylpyridinium-based ionic liquids[J].Energy & Fuels,2009,23:2690-2694.
[42]Francisco M ,Arce A ,Soto A,et al.Ionic liquids on desulfurization of fuel oils[J].Fluid Phase Equilibria,2010,294:39-48.
[43]Holbrey J D,López-Martin I,Rothenberg G,et al.Desulfurisation of oils using ionic liquids:Selection of cationic and anionic components to enhance extraction efficiency[J].Green Chem.,2008,10:87-92.
[44]Asumana C ,Yu G G ,Li X ,et al.Extractive desulfurization of fuel oils with low-viscosity dicyanamide-based ionic liquids[J].Green Chem.,2010,12:2030-2037.
[45]Yu G G ,Li X ,Liu X X,et al.Deep desulfurization of fuel oils using low-viscosity 1-ethyl-3-methylimidazolium dicyanamide ionic liquid[J].Ind.Eng.Chem.Res.,2011,50:2236-2244.
[46]Lo W H,Yang H Y,Wei G T.One-pot desulfurization of light oils by chemicaloxidation and solvent extraction with room temperature ionic liquids[J].Green Chem.,2003,5(5):639-642.
[47]Li F T,Liu R H,Wen J H,et al.Desulfurization of dibenzothiophene by chemical oxidation and solvent extraction with Me3NCH2C6H5Cl·2ZnCl2ionic liquid[J].Green Chem.,2009,11:883-888.
[48]Li H M,Jiang X,Zhu W S,et a1.Deep oxidative desulfurization of fuel oils catalyzed by decatungstates in the ionic liquid of[Bmim]PF6[J].Ind.Eng.Chem.Res.,2009,48:9034-9039.
[49]Lu L,Cheng S F,Gao J B,et a1.Deep oxidative desulfurization of fuels catalyzed by ionic liquid in the presence of H2O2[J].Energy Fuels,2007,21:383-384.
[50]Zhao D S,Wang J L,Zhou E P.Oxidative desulfurization of diesel fuel using a Brønsted acid room temperature ionic liquid in the presence of H2O2[J].Green Chem.,2007,9:1219-1222.
[51]Zhao D S,Sun Z M,Li F T,et a1.Optimization of oxidative desulfurization of dibenzothiophene using acidic ionic liquid as catalytic solvent[J].Journal of Fuel Chemistry and Technology,2009,37(2):194-198.
[52]Gao H S,Guo C,Xing J M,et al.Extraction and oxidative desulfurization of diesel fuel catalyzed by a Brønsted acidic ionic liquid at room temperature[J].Green Chem.,2010,12:1220-1224.
[53]Yu G G,Zhao J J,Song D D,et al.Deep oxidative desulfurization of diesel fuels by acidic ionic liquids[J].Ind.Eng.Chem.Res.,2011,50:1690-11697.
[54]刘淑芝,曾庆雪,刘先军,等.离子液体在燃料油脱硫中的应用[J].化工科技,2010,18(6):74-77.
[55]柯明,汤奕婷,曹文智,等.离子液体在FCC汽油脱硫中的应用研究[J].西南石油大学学报,2010,32(3):145-149.
[56]Chauvin Y,Olivier H.Nonaqueous ionic liquids and reaction solvents[J].Chem.Tech.,1995,25:26-30.
[57]Chauvin Y,Einloft S,Olivier H.Catalytic dimerization of propene by nickel phosphinecomplexes in 1-butyl-3-methylimidazoliumchloride/AlEtxCl3-x(x=0,1) ionic liquids[J].Ind.Eng.Chem.Res.,1995,34:1149-1155.
[58]黄蔚霞,李云龙,汪燮卿.离子液体在催化裂化汽油脱硫中的应用[J].化工进展,2004,23(3):297-299.
[59]刘植昌,胡建茹,高金森,等.离子液体用于催化裂化汽油烷基化脱硫的实验室研究[J].石油炼制与化工,2006,37(10):23-27.
[60]李桂花.离子液体用于汽油脱硫的研究进展[J].河北化工,2009,32(12):5-6.
[61]石家华,杨春和,高青雨,等.聚噻吩在离子液体中的电化学合成研究[J].化学物理学报,2005,17(4):503-507.
[62]亓西敏,张爱健,张贵荣,等.噻吩在离子液体中的电化学聚合及其在模拟汽油脱硫中的应用[J].环境化学,2006,25(2):183-186.
[63]Zhang S,Zhang Z C.Novel properties of ionic liquids in selective sulfur removal from fuels at room temperature[J].Green Chem.,2002,4:376-379.
[64]Seeberger A,Jess A.Desulfurization of diesel oil by selective oxidation and extraction of sulfur compounds by ionic liquids-a contribution to a competitive process design[J].Green Chem.,2010,12:602-608.
[65]Roth M.Partitioning behaviour of organic compounds between ionic liquids and supercritical fluids[J].Journal of chromatography A,2009,1216:1861-1880.
[66]林棋,付海燕,陈华,等.负载离子液体纳米钯催化芳卤羰化反应[J].物理化学学报,2006,22(10):1272-1276.
[67]Tian M,Yan H,Row K H.Solid-phase extraction of tanshinones from Salvia Miltiorrhiza Bunge using ionic liquid-modified silica sorbents[J].J.Chromatogr.B,2009,877:738-742.
[68]Tian M,Bi W,Row K H.Solid-phase extraction of liquiritin and glycyrrhizic acid from licorice using ionic liquid-based silica sorbent[J].J.Sep.Sci.,2009,32:4033-4039.
[69]Vidal L,Riekkola M L,Canals A.Ionic liquid-modified materials for solid-phase extraction and separation:A review[J].Analytica Chimica Acta,2012,715:19-41.
[70]Xie L L,Favre-Reguillon A,Wang X X.Selective extraction of neutral nitrogen-containing compounds from straight-run diesel feed using polymer-supported ionic liquid moieties[J].Ind.Eng.Chem.Res.,2009,48:3973-3977.
[71]Kuhlmann E,Haumann M,Jess A,et al.Ionic liquids in refinery desulfurization :Comparison between biphasic and supported ionic liquid phase suspension processes[J].Chem.Sus.Chem.,2009,2:969-977.
[72]Wang X M,Wan H,Han M J,et al.Removal of thiophene and its derivatives from model gasoline using polymer-supported metal chlorides ionic liquid moieties[J].Ind.Eng.Chem.Res.,2012,51:3418-3424.

