急性脑梗死两种溶栓治疗方法的安全性与疗效比较
李国斌,李冬梅,高 天,徐 祎,杜世伟,毛更生
缺血性脑血管病占脑卒中的60% ~90%[1],其中急性脑梗死(combined intra-arterial ,ACI)具有发病急、高致残率、高病死率等特点,严重影响患者的预后和生存质量。根据“缺血半暗带原理”[2],溶栓治疗能够再通闭塞动脉,恢复缺血脑组织的血供,挽救“处于半缺血状态的神经元”[3]。目前,动静脉联合溶栓的疗效及安全性仍未被广泛肯定。为此,笔者选取我院2011-02 至2012-09 收治的68例ACI 患者,行动静脉联合溶栓或静脉溶栓治疗,并比较其安全性及疗效。
1 对象与方法
1.1 对象 68 例中,男45 例,女23 例,年龄45 ~76 岁,平均(58.16 ±8.89)岁。就诊时,全部患者均有不同程度的偏瘫、感觉障碍、语言障碍等神经功能缺失。根据动、静脉溶栓的适应证、禁忌证,37 例行动静脉联合溶栓治疗,为联合组;31 例行静脉溶栓治疗,为静脉组。两组患者的年龄组成、性别比例、既往史、伴发病和入院NIHSS 评分均无统计学差异。
1.2 入选标准 (1)年龄<80 岁;(2)发病时间<6 h;(3)术前头颅CTA 示无脑出血,亦未见与神经功能缺损相对应的低密度病灶;(4)无明显意识障碍,但后循环闭塞病例有意识障碍者也可行溶栓治疗;(5)脑功能损害体征持续在1 h 以上,且比较严重(NIHSS 评分在7 ~22 分);(6)排除颅内肿瘤、脑动脉瘤、脑血管畸形及可疑蛛网膜下腔出血;(7)无出血倾向、无严重心、肝、肾等实质脏器疾病;(8)血压<180/100 mmHg;(9)家属同意,且患者或家属签署知情同意书[4]。
1.3 两组筛分标准 (1)符合上述溶栓治疗标准的患者,发病在4.5 ~6 h,或发病时间<4.5 h,但术前头颅CTA 示病变部位在颈内动脉或大脑中动脉主干及其主要分支,给予行动静脉联合溶栓治疗;(2)符合上述溶栓治疗标准的患者,发病时间<4.5 h,且头颅CTA 示病变部位为远端小动脉,给予行静脉溶栓治疗。
1.4 治疗方法 两组患者急诊入院后积极完善术前检查及准备。两组术后均给予以下辅助治疗:(1)术后24 h 开始给予抗凝药物或抗血小板药物以改善局部微循环,给予拜阿司匹林,100 mg,口服,1次/d;(2)神经保护药,包括神经节苷脂、依达拉奉及丁苯酞等;(3)监测血压,维持适当的脑灌注压;(4)定期检测凝血水平,以协助调整治疗方案。分别在术前、术后24 h、术后7d 进行NIHSS 评分。对比两组患者术后出血并发症发生率和病死率。
联合组应用重组组织型纤溶酶原激活剂(rt-PA),以0.6 mg/kg(最大剂量60 mg),先静脉推注10%(1 min 内),余量30 min 持续静脉滴注[5]。同时准备行超选择性动脉溶栓。给予常规消毒、铺单、局麻。右侧股动脉Seldinger 法穿刺,置动脉鞘。常规行双侧颈总动脉、椎动脉(或锁骨下动脉)造影,结合患者临床症状评估造影结果,明确病变部位。全身肝素化,置入导引导管,在微导丝引导下,将微导管穿过血栓,微量造影以明确血管无夹层及病变远端血管通畅。然后给予rt-PA,以0.3 mg/kg(最大剂量24 mg),2 h 内经微导管持续灌注。灌注过程中,间断行微量造影,直接观察血栓溶解情况,便于控制用药剂量。静脉组应用rt-PA,以0. 9 mg/kg(最大剂量90 mg),先静脉推注10%(1 min内),余量60 min 持续静脉滴注。
1.5 血管再通标准 (1)0 级,无变化;1 级,栓子移动但无相应的血液灌注改善;(2)2 级,部分再通并有<50%的缺血区灌注;(3)3 级,完全或接近完全再通,缺血区完全恢复灌注。将上述0 级和1 级合并视为未通,2 级为部分再通,3 级为完全再通[6]。
1.6 统计学处理 所有数据采用SPSS Statistics17.0 统计学软件处理和分析,以P <0.05 为差异有统计学意义。
2 结果
2.1 血管再通率 联合组患者术前造影共检出闭塞血管38 例,术后部分再通+完全再通共25 例,总体血管再通率为65.79%。静脉组患者术前CTA 共检出闭塞血管28 例,术后部分再通+完全再通共11 例,总体血管再通率为39.29%(表1)。联合组血管再通率高于静脉组(P <0.05,表2)。本组一例患者,主因“右侧肢体无力伴言语不能4 h”急诊入院。给予动静脉联合溶栓治疗。术前造影示左侧M1 段完全闭塞;术后造影示左侧M1 段闭塞再通,远端显影良好(图1)。
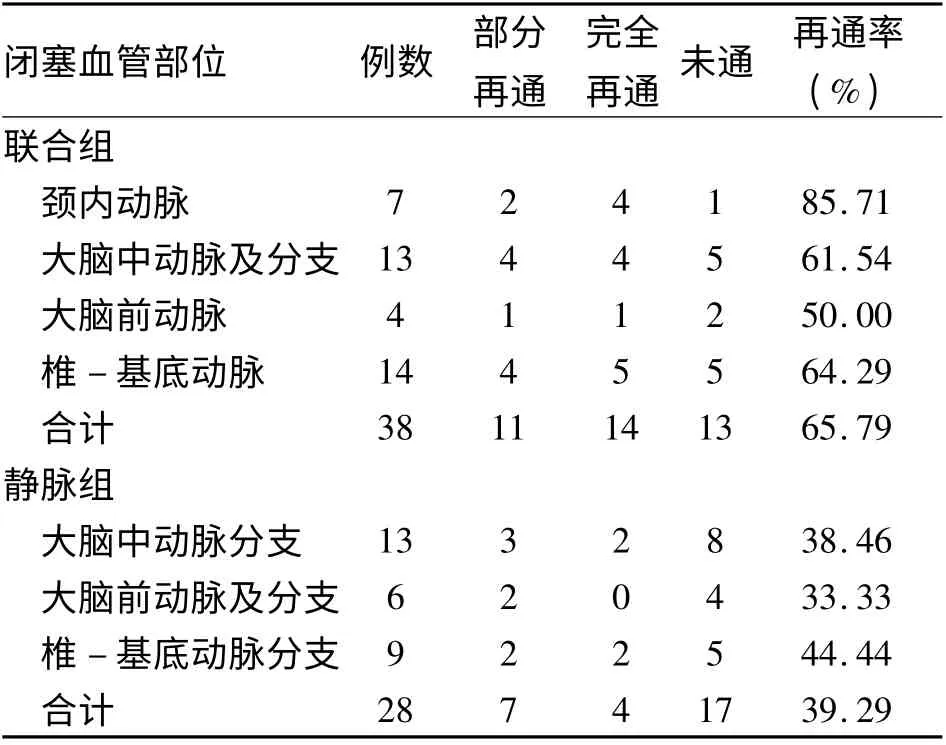
表1 联合组和静脉组ACI 患者术后血管再通情况(n)

表2 两组患者术后血管再通情况(n)
2.2 NIHSS 评分 联合组和静脉组患者术前与术后7 d NIHSS 评分比较,差异有统计学意义(P <0.01或P <0.05);两组患者术后24 h NIHSS 评分差异有统计学意义(P <0.05);两组患者术后7 d NIHSS 评分差异有统计学意义(P <0.05,表3)。
表3 两组患者术前与术后NIHSS 评分 (±s)

表3 两组患者术前与术后NIHSS 评分 (±s)
注:与联合组术前NIHSS 评分比较,①P <0.05;与静脉组术前NIHSS 评分比较,②P <0.01
组别术前术后24 h术后7 d联合组18.45 ±4.049.11 ±5.296.23 ±7.44①静脉组16.91 ±3.88 11.59 ±4.729.74 ±6.36②
2.3 并发症 联合组术后发生症状性脑出血3例,随访期内(1 个月)死亡4 例,症状性脑出血的发生率为8.10%,病死率为10.81%。静脉组术后发生症状性脑出血3 例,随访期内死亡4 例,症状性脑出血的发生率为9.68%,病死率为12.90%。两组患者术后出血发生率及病死率无差别。
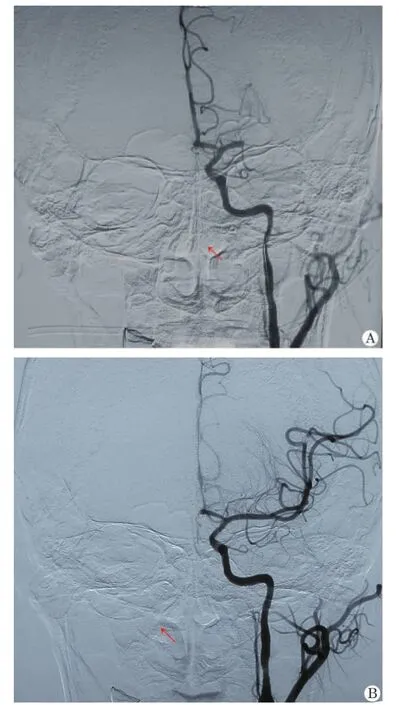
图1 左侧大脑中动脉第一段(M1)造影
3 讨论
对于ACI 患者,术前急诊进行头颅CTA 或磁共振的DWI 和PWI 检查是很有必要的,这些影像学信息,可以协助诊断超早期脑梗死及其梗死类型,判断是否还存在可以挽救的脑组织,从而进行筛选病例和判断预后。同时,还可以协助明确病因及血管闭塞位置,以进行更有针对性的治疗。
ACI 具有高发病率、高病死率,而且发病急、进展快、病情凶险的特点,本研究中68 例病死率为11.76%。通过本次研究,结合国内外以往的临床试验结果不难看出,溶栓治疗ACI 后疗效较好的多为年龄小于75 岁的患者[7]。根据IP 理论,时间窗的选择也是溶栓成败的关键之一。笔者认为,颈内动脉供血区域的梗死溶栓治疗时间若超过6 h,出血风险性很高,且临床预后很差;椎-基底动脉供血区域的梗死溶血时间窗可适当延长[8]。
静脉溶栓对4.5 h 内发病的ACI 的疗效是明显的,且费用低、方便快捷、可降低整个脑血流的高凝状态和预防早期血栓形成。然而,静脉溶栓对颈内动脉或大脑中动脉主干闭塞的血管再通率很低,研究表明静脉内溶栓治疗颈内动脉闭塞的血管再通率仅约10%,治疗大脑中动脉主干闭塞的血管再通率也不足30%[9],而且采用全身抗凝不良反应大,疗效欠佳。本研究中静脉组的总体血管再通率仅为39.29%。动脉溶栓能使病变局部保持相对较高的药物浓度,结合机械碎栓[10]、血管内成形等技术,闭塞血管再通率较高,并可有效控制给药剂量。本研究中联合组的总体血管再通率达到65.79%。已有相关文献报道,对发病时间在6 h 内的脑梗死行动脉溶栓时,将rt-PA 的剂量控制在20 ~40 mg 是安全有效的[11]。此外,溶栓治疗前,行血管造影还可以明确闭塞血管病变部位和侧支循环的建立情况。但动脉溶栓较静脉溶栓延误了治疗时间,而对于ACI,开始治疗时间每延迟20 ~30 min,其疗效就会降低10%[12]。而且,动脉溶栓难以改善整个脑血流的高凝状态。因此,动静脉联合溶栓技术似乎是治疗ACI、再通闭塞血管的一种好方法。本研究通过对比分析动静脉联合溶栓和静脉溶栓治疗ACI的相关临床资料,可以看出,在严格筛选发病时间在6 h 以内的前提下,动静脉联合溶栓治疗ACI 可兼有静脉溶栓的方便快捷和动脉溶栓的高再通率。同时,其出血等并发症的发生率及病死率与静脉溶栓相比差异不显著。进一步证明了动静脉联合溶栓治疗ACI 的有效性和安全性。当然,本研究还存在一定的不足,如调查的样本较小、取样范围较窄、样本分组未能做到绝对随机等。因此,为了彻底地探明溶栓疗法治疗ACI 的原则,针对不同疾病类型和不同病因的患者,采用不同的溶栓药物、剂量以及给药途径,并获得较高的血管再通率和较好的临床疗效,将脑出血等并发症发生率降至最小,有必要进一步开展大规模、多中心、随机、对照临床试验来确定它的有效性和安全性。
[1] 贾建平. 神经病学[M].6 版. 北京:人民卫生出版社,2008:175-185.
[2] Astrup J,Siesjo B K,Symon L. Thresholds in cerebral ischemia- the ischemic penumbra[J]. Stroke,1981,12 (6):723-725.
[3] Rymner M M,Akhtar N,Martin C,et al. Management of acute ischemic stroke:time is brain[J]. Mo Med,2010,107 (5):333-337.
[4] 赖芳芳. rt-PA 对缺血性脑血管病的临床治疗分析[J]. 吉林医学,2011,32(21):4353-4354.
[5] 贺茂林. 应重视急性缺血性卒中动静脉联合溶栓治疗的研究[J]. 中国脑血管病杂志,2004,1(8):337-338.
[6] 付 睿,赵星辉,黄 栋,等. 急性缺血性脑卒中动脉溶栓中血管再闭塞的临床分析[J]. 实用医学杂志,2011,20:3737-3739.
[7] Sundararajan S,Morgenstern L B. Thrombolysis for acute stroke:is it for everyone [J]?Curr Atheroscler Rep,2000,2(2):97-103.
[8] Dubey N,Bakshi R,Wasay M,et al. Early computed tomography hypodensity predicts hemorrhage after intravenous tissue plasminogen activator in acute ischemic stroke[J]. J Neuroimaging,2001,11(2):184-188.
[9] 贺茂林,陈清棠. 急性脑梗死溶栓治疗的血管再通率[J]. 中华老年心脑血管病杂志,1999,1:57-60.
[10] 杨 艳,黄立安,徐安定. 急性缺血性卒中溶栓治疗进展[J]. 中华临床医师杂志(电子版),2009,3(7):1197-1203.
[11] Christoforidis G A,Slivka A P,Karakasis C,et al.Hemorrhage rates and outcomes when using up to 100 mg intra-arterial t-PA for thrombolysis in acute ischemic stroke[J]. Interv Neuroradiol,2010,16(3):297-305.
[12] Hacke W,Kaste M,Bluhmki E,et al. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke[J]. N Engl J Med,2008,359(13):1317-1329.

