幽门螺杆菌与非甾体抗炎药引发胃溃疡的内镜特征分析
刘谦,许晓芳,夏兴洲 (郑州大学第五附属医院消化内科,河南 郑州 450052)
在我国胃溃疡的老年患者中,90%以上都受到幽门螺杆菌(H.pylori)的感染[1]。而对于老年患者多需要使用非甾体抗炎药(NSAIDs)(布洛芬IBF、阿司匹林、LDA)以预防心血管疾病的发生[2],但同时它们会增加胃黏膜损伤和溃疡的风险。因此幽门螺杆菌和NSAID是老年患者消化性溃疡发生的两个最重要的致病因素,然而幽门螺杆菌感染和NSAIDs在消化性溃疡发生中是否有协同作用目前还未定论[3]。同时也没有人对在幽门螺杆菌感染与未发生幽门螺杆菌感染的情况下,由不同NSAIDs药物(IBF和LDA)引起的溃疡在形态上的特征进行研究。因此,本研究回顾性地研究了处于活跃期的胃溃疡的患者的内镜结果特点,了解幽门螺杆菌感染与服用NSAIDs后在消化性溃疡及其并发症发生中是否具有协同致病作用,对推断溃疡的起因和发生具有临床意义。
1 对象与方法
1.1 研究对象 从2005年6月-2011年5月,我院共对25508例患者进行了上消化道内镜检查,内镜结果根据Sakita-Miwa等级分类,通过鉴定,有410例患者的胃溃疡处于活跃阶段(A1或A2期)。内镜下胃溃疡的形态学为在黏膜损伤部位表面覆盖了一层白色的直径至少3 mm的物质,同时从组织样本中检测没有发现瘤状物质(胃癌)。试验组为在观察到的溃疡病例中使用了IBF/或LDA的患者。其中定期服用甾体抗炎药超过1个月的患者被认为是“定期甾体抗炎药使用者”,而那些仅当他们表现出症状时服用或者使用甾体抗炎药不超过1周的患者,被定义为“临时甾体抗炎药使用者”。排除标准为:患者有严重的脏器功能不全(心肺脑肾等)或者凝血机制障碍。对于无NSAID的幽门螺杆菌感染呈阴性的胃溃疡患者(n=15,3.7%),由于其溃疡的原因不清楚,所以将这些患者从本研究中排除。此外,由于同时服用IBF和LDA的患者的数量(n=16)太少不能进行数据分析,这些数据被从本研究中排除,最终对患有活跃阶段溃疡的379例患者进行了研究。
1.2 分组和研究方法 符合研究标准的患者被分成3组:IBF组、LDA组和对照组。对照组由没有服用NSAID类药物的幽门螺杆菌阳性的胃溃疡患者组成。对所有患者均观察了以下特性:年龄 (≥65岁);性别;饮酒和/或吸烟;幽门螺杆菌感染状况;IBF和LDA的使用情况;消化道溃疡史;黏膜萎缩程度 (轻、中和重);是否有肝硬化;是否有血液透析。每组中幽门螺杆菌感染或者没有感染患者的内镜特征。幽门螺杆菌感染主要通过检测血清中幽门螺杆菌抗体(酶联免疫分析试剂盒,试剂购自华美生物工程公司),如果患者对幽门螺杆菌呈阴性需进行下列附加测试:快速尿素酶检测,或者尿素呼气试验。在这些检测的一项或多项中,有一项对幽门螺杆菌呈阳性的患者被认为是幽门螺杆菌阳性感染。幽门螺杆菌阴性状态包括药物根除之后的状态和自然清除后的状态。
1.3 内窥镜图像分析方法 对每一例患者从咽部到十二指肠拍摄至少50张内窥镜照片。胃溃疡的内窥镜照片分别由3名内窥镜方面专家进行评估,如果这3个评价没有达成一致,最终的评价将通过3人讨论决定。对于每一个病例,都分析确定了溃疡发病的位置,数目,形状。其中溃疡发生的位置被划分为3个区域:(1)下部,胃窦;(2)中部,胃角和躯体;(3)上部,贲门和胃底。若患者存在二处以上溃疡,被被定义为多重溃疡。在这种多重溃疡的情况下,主要溃疡的位置视为溃疡发病位置。非圆形或椭圆形的溃疡被归类为不规则溃疡。
1.4 统计学分析 通过Mann-Whitney U检验、χ2检验、Fisher精确检验对3组患者的数据进行了统计学比较,统计学软件为SPSS 16,P<0.05认为具有统计学意义。
2 结果
2.1 患者的一般情况 本研究纳入了处于活跃阶段胃溃疡的379例患者 (男266例,女113例),平均年龄为(65.2±12)岁 (26~90岁)。在这些患者中,通过检查发现346例 (91.3%)幽门螺杆菌为阳性,其中有216例 (57.0%)患者未使用 NSAID类药物,故这216例患者做为对照组。100例患者使用了IBF,63例患者使用了LDA。表1为患者的基线特征。IBF组和LDA组患者的平均年龄明显高于对照组 (分别为P<0.05和P<0.01)。IBF组和LDA组之间在患者的平均年龄上无显著性差异。对照组的男女比例显著高于IBF和LDA组(P<0.01)。LDA组吸烟患者的数目明显高于IBF组和对照组 (P<0.01)。内镜结果发现有溃疡萎缩程度在3组中没有显著差异。IBF和LDA组抗酸剂、质子泵抑制剂 (PPI)或组胺 H2受体拮抗剂(H2RA)的结合使用率明显高于对照组 (P<0.01)。
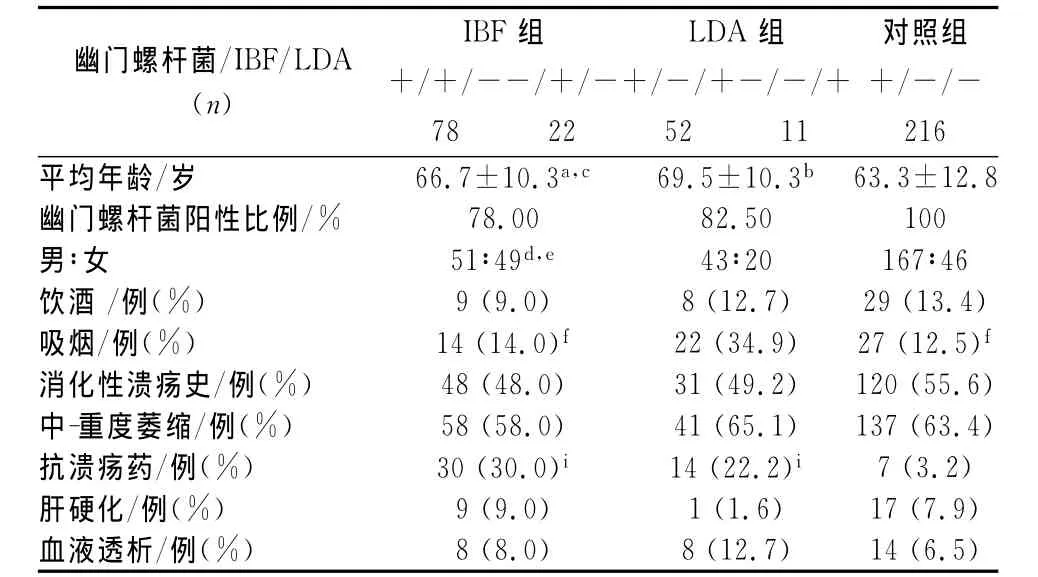
表1 各组患者的基线特征Tab 1 Baseline characteristics of patients in each group
2.2 服用不同NSAIDs引起的有/无幽门螺杆菌感染胃溃疡的内镜特征比较 见图1。由图可见,a在各组中胃较低部分胃溃疡的发生率显著高于对照组,并且这种趋势在幽门螺杆菌-阴性患者中比在幽门螺杆菌-阳性患者中更加明显。然而,幽门螺杆菌-阳性LDA组在胃的较低部分的胃溃疡的发生率与对照组没有差异。b,c相反,在胃的中部或上部胃溃疡的发生率对照组显著高于幽门螺杆菌-阴性IBF组和LDA组患者。幽门螺杆菌-阳性患者胃下部溃疡在临时IBF使用者为40.9% (18/44),在临时LDA 组为32.4% (11/34),因此,2组之间没有显著差异。同样,在定期(72.7%,8/11)和临时应用IBF(63.6%,7/11)的幽门螺杆菌-阴性患者之间不存在显著差异性。
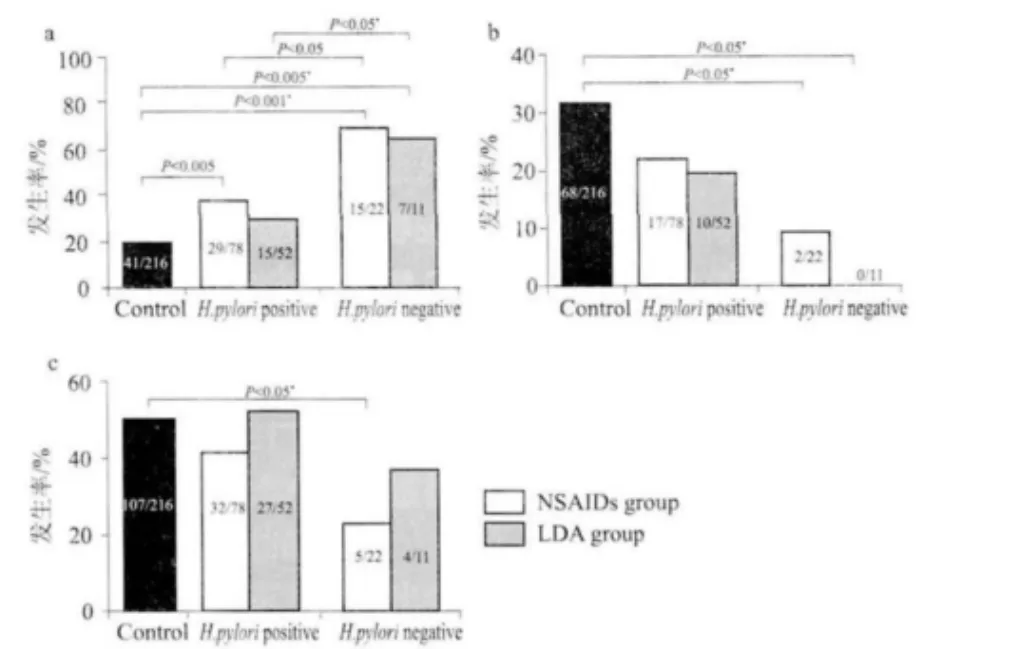
图1 在胃的3个部位胃溃疡的发生率a:较低部分,b:中部,c上部,*:Fisher精确检验。对照线,幽门螺杆菌阳性,幽门螺杆菌阴性Fig 1 The incidences of gastric ulcers in three sites of the stomacha.lower part;b.middle part;c.upper part;*Fisher's exact test,control,H.pylori postive,H.pylori negative
2.3 各组多重胃溃疡的发生率 见图2。由图可见,与胃下部溃疡的发生率相似,多重溃疡发生率在IBF组 和 LDA 组显著高于对照组 (31.0%,67/216),这种趋势在幽门螺杆菌-阴性患者中比在幽门螺杆菌-阳性患者中更加明显。此外,在LDA组,幽门螺杆菌-阴性患者比幽门螺杆菌-阳性患者具有更高的多重溃疡发生率 (P<0.05)。
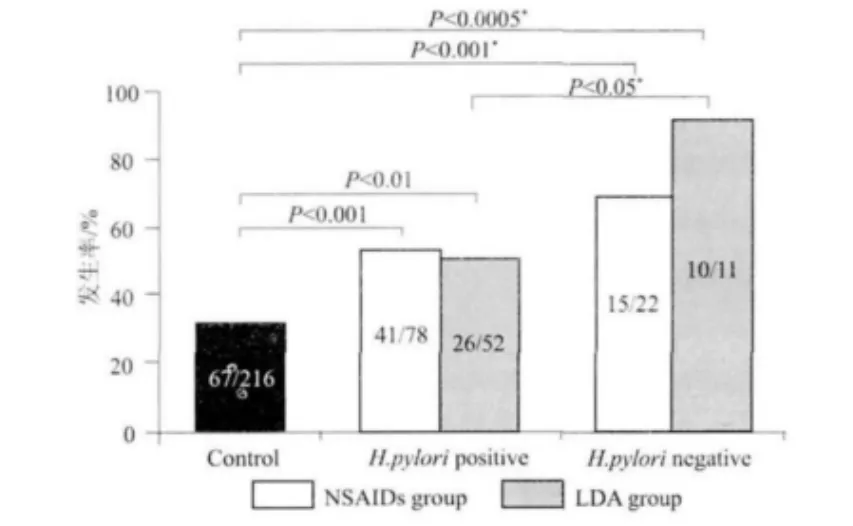
图2 多重胃溃疡发生率Fig 2 The incidence of multiple gastric ulcers
2.4 不规则形状胃溃疡的发生率 见图3。由图可见,无论是否有幽门螺杆菌感染,IBF组中这种溃疡的发生率都高于对照组,但是LDA组相对于对照组并没有较高发生率.与溃疡部位和多重溃疡不同,不规则形状溃疡的发生率在LDA或IBF组的幽门螺杆菌-阳性与幽门螺杆菌-阴性患者之间比较没有差异。在幽门螺杆菌-阳性患者中,不规则形状溃疡的发生率在IBF组显著高于LDA组 (P<0.05)。
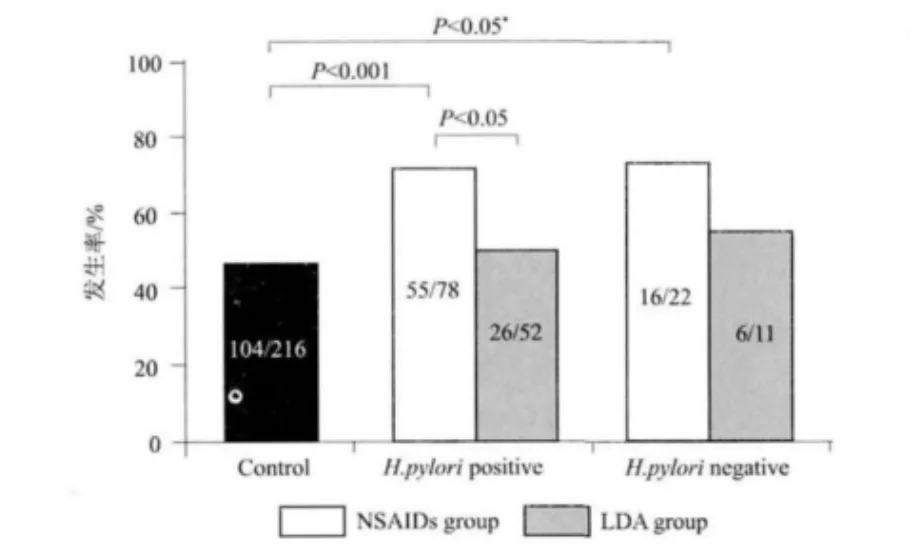
图3 不规则形状胃溃疡的发生率Fig 3 The incidence of irregularly shaped gastric ulcers.
3 讨论
胃溃疡是一种常见的疾病,致病原因很多,当服用IBF或LDA的人发生消化性溃疡且未感染幽门螺杆菌时,胃溃疡一般被认为是由IBF或LDA诱发的。然而,当溃疡常发生在使用了NSAID并同时感染了幽门螺杆菌的患者,就很难确定溃疡是主要由幽门螺杆菌感染引起的还是主要由NSAID使用引起的。在欧洲和美国,IBF和LDA的使用非常普遍,但是幽门螺杆菌感染率却很低。相反,在发展中国家(包括我国),幽门螺杆菌感染率很高。因此通过对幽门螺杆菌、IBF或LDA诱发溃疡的不同内镜特征,可以明确溃疡的主要病因。通过研究我们发现,由IBF或LDA诱发的胃溃疡主要发生在胃窦并且有多个病灶,而多重胃溃疡的发生率在使用IBF或LDA的患者中会显著高于对照组。无论有无幽门螺杆菌感染,由IBF诱发的胃下部(胃窦)的溃疡比对照组发生率更高。这种趋势在未被幽门螺杆菌感染的患者中更加明显。多重的溃疡发生部位在使用LDA的幽门螺杆菌-阴性患者中与对照组的患者相似。根据Hart等[4]最近报道,其原因在于幽门螺杆菌感染有可能部分地防御了LDA诱发的溃疡,因为LDA诱发的胃黏膜损伤的严重程度与胃内的pH值密切相关,幽门螺杆菌感染引起的胃萎缩很可能升高了胃液的pH,这可能防止了LDA诱发的黏膜损伤的发生。同样,由IBF诱发的多重胃溃疡的发生率在幽门螺杆菌-阴性患者中显著高于幽门螺杆菌-阳性患者。目前幽门螺杆菌感染对IBF诱发的溃疡的影响是有争议的。一些研究人员报道,幽门螺杆菌-阳性IBF使用者与幽门螺杆菌-阴性IBF使用者相比,溃疡的风险增加,出现分歧可能的原因是这些研究调查了由包括阿司匹林在内的大量NSAID诱发的溃疡,而我们的研究则分别评估了不同NSAID药物诱发的溃疡。在Kamada等[5]的研究中发现:在使用NSAID幽门螺杆菌-阳性胃溃疡患者中,溃疡经常发生在胃体,而在幽门螺杆菌-阴性患者中溃疡经常发生在胃窦,我们观察到了相似的结果。这是因为IBF诱发的溃疡机制是由IBF抑制了环氧合酶而使得前列腺素的合成降低而引起的[6],因此导致胃黏膜保护功能发生障碍[7],而胃窦内具有许多前列腺素受体 (EP4),从而使得其更容易受到IBF的影响。在本研究中,还发现无论幽门螺杆菌感染状况如何,IBF诱发的溃疡都是趋向于不规则形状的[8],然而,LDA-诱发的溃疡并未有这种趋势,这说明IBF和LDA诱发的胃溃疡的机制之间存在差异[9]。这些差异可能影响由IBF或LDA诱发的溃疡形状[10]。根据以上药物相关内镜调查结果,我们可以认为LDA溃疡受到幽门螺杆菌感染的影响,然而幽门螺杆菌感染对IBF溃疡的影响较弱[11-12]。
总之,本研究阐明了发生在使用IBF或LDA这二种常用的非甾体类药物在引发幽门螺杆菌感染或未发生幽门螺杆菌感染胃溃疡的形态特征。由IBF诱发的溃疡经常发生在胃下部(胃窦),且无论是否发生幽门螺杆菌感染都表现出不规则的形状。而LDA引发的溃疡则具有较高的多重溃疡发生率。研究结果对于从内镜下溃疡的形态特征推断溃疡的主要原因具有临床意义。
[1]Asaka M,Kato M,Sugiyama T,et al.Follow-up survey of a large-scale multicenter,double-blind study of triple therapy with lansoprazole,amoxicillin,and clarithromycin for eradication of Helicobacter pylori in Japanese peptic ulcer patients[J].J Gastroenterol,2009,38(3):339-347.
[2]Ford AC,Delaney B,Forman D,et al.Eradication therapy for peptic ulcer disease in Helicobacter pylori positive patients[J].Cochrane Database Syst Rev,2009,(2):CD003840.
[3]Huang JQ,Sridhar S,Hunt RH.Role of Helicobacter pylori infection and non-steroidal anti-inflammatory drugs in pepticulcer disease:a meta-analysis[J].Lancet,2010,359(43):14-22.
[4]Hart J,Hawkey CJ,Lanas A,et al.l.Predictors of gastroduodenal erosions in patients taking low-dose aspirin[J].Aliment Pharmacol Ther,2010,31(1):143-149.
[5]Kamada T,Hata J,Kusunoki H,et al.Eradication of Helicobacter pylori increases the incidence of hyperlipidaemia and obesity in peptic ulcer patients[J].Dig Liver Dis,2011,37(4):39-43.
[6]Niv Y,Battler A,Abuksis G,et al.Endoscopy in asymptomatic minidose aspirin consumers[J].Dig Dis Sci,2010,50(21):78-80.
[7]Graham DY,Opekun AR, Willingham FF,et al. Visible small-intestinal mucosal injury in chronic NSAID users[J].Clin Gastroenterol Hepatol,2009,3(1):55-59.
[8]Lanas A,Garc a-Rodr guez LA,Arroyo MT,et al.Risk of upper gastrointestinal ulcer bleeding associated with selective cyclo-oxygenase-2 inhibitors,traditional non-aspirin non-steroidal anti-inflammatory drugs,aspirin and combinations[J].Gut,2009,55(11):1731-1738.
[9]Kamada T,Hata J,Kusunoki H,et al.Endoscopic characteristics and Helicobacter pylori infection in NSAID-associated gastric ulcer[J].J Gastroenterol Hepatol,2006,21(1 Pt 1):98-102.
[10]Kato S,Matsukura N,Tsukada K,et al.Helicobacter pylori infection-negative gastric cancer in Japanese hospital patients:incidence and pathological characteristics[J].Cancer Sci,2011,98(26):790-794.
[11]Hart J,Hawkey CJ,Lanas A,et al.Predictors of gastroduodenal erosions in patients taking low-dose aspirin[J].Aliment Pharmacol Ther,2010,31(5):143-149.
[12]Mizokami Y,Narushima K,Shiraishi T,et al.Non-Helicobacter pylori ulcer disease in rheumatoid arthritis patients receiving long-term NSAID therapy[J].J Gastroenterol,2010,35(Suppl 12):38-41.

