缬沙坦的血药浓度测定
郭影坤, 隋 阳
(东北制药集团供销有限公司, 辽宁 沈阳 110023)
缬沙坦是一种非肽类的血管紧张素 II 受体AT1拮抗剂,选择性作用于AT1受体亚型,从而阻断血管紧张素II介导的生理效应。缬沙坦对血管紧张素转化酶(ACE)没有抑制作用,不引起缓激肽和 P物质的储留,因而不引起咳嗽等不良反应[1]。缬沙坦能扩张血管,改善心室及血管的重塑,抑制醛固酮,保钾排钠,从而达到降压作用。缬沙坦用于治疗各类轻至中度高血压,尤其适用肾脏损害所致继发性高血压。此外,缬沙坦还可显著减少尿蛋白排出量,对慢性肾小球肾炎病人有益[2]。有关缬沙坦浓度测定的高效液相色谱法国内外都有报道[3-10],本实验建立了一种高效液相色谱法测定缬沙坦血浆浓度, 在国内外文献的基础上改进了血样预处理方法, 重新选择了内标物, 优化了流动相的组成, 采用液-液萃取法进行血浆预处理,具有方法简便, 回收率高, 重复性好的优点,能够灵敏、快速检测人血浆中缬沙坦的浓度,可用于缬沙坦的体内分析及临床药学研究,为人体药代动力学研究提供了测定方法。
1 实验部分
1.1 仪 器
SHIMADZU LC10-AT系列高效液相色谱仪、HY-4调速多用振荡器、XW-80A旋涡混合器、电热恒温水浴锅、WM-2A型无油气体压缩机、LD4-2A低速离心机。
1.2 药品与试剂
代文(缬沙坦胶囊),规格:80 mg/粒,北京诺华制药有限公司生产,批号:X0372,有效期2年,遮光,密闭保存。缬沙坦对照品:中国药品生物制品检定所,批号 100651-200401,含量 98.8%。磷酸二氢钾、磷酸、二氯甲烷为分析纯,乙腈和甲醇为色谱纯,水为二重蒸馏水。空白血浆由中国医科大学附属盛京医院输血科提供。
2 方法与结果
2.1 血浆样品的分析方法
2.1.1 血浆样品的预处理
取 0.2 mL血浆于具塞玻璃试管中,加入内标0.5 μg·mL-1替米沙坦 50 μL,补加 50 μL 甲醇,加 1 mol·L-1HC l100 μL, 再加入 3 mL 二氯甲烷,震荡提取15 min,3 500 r/minpm离心10 min, 取下层有机相,与50 ℃水浴中氮气吹干,于残渣中加入400 μL流动相,涡旋混合30 s,进样10 μL
2.1.2 色谱条件
Agilent ZORBAZX Eclipse XDB-C18 柱(4.6×150 mm, 5 μm);流动相:乙腈:0.01 mol·L-1KH2PO4(pH=2.96)=48︰52(V/V);流速:1.0 mL·min-1;检测波长:激发波长265 nm,发射波长378 nm;柱温:30 ℃。
2.2 分析方法确证
2.2.1 方法的专属性
分别取6名受试者混合空白血浆0.2 mL,按“血浆样品的分析方法”项下操作,进样 10 μL,得色谱图1-A;将一定浓度的缬沙坦加入空白血浆中,依同法操作,得色谱图1-B;取健康受试者给药后收集的血浆样品,依同法操作,得色谱图1-C。结果表明,血浆中的内源性物质不干扰缬沙坦和内标替米沙坦的测定。
2.2.2 标准曲线的制备
取空白血浆0.2 mL,依次加入浓度为50,100,200,500,1 000,2 000,5 000,10 000,20 000 ng·mL-1的缬沙坦标准系列的甲醇溶液,配制相当于 12.5,50,125,250,500,1 250,2 500,5 000 ng·mL-1的血浆样品,按“血浆样品的分析方法”项下的方法操作,制备标准曲线。以血浆中待测物的浓度为横坐标,以待测物与内标的峰面积比为纵坐标,用加权最小二乘法进行回归计算,求得直线回归方程,即为标准曲线。标准曲线回归方程见表 1。本方法的最低定量限为 12.5 ng·mL-1,线性范围为12.5~5000 ng·mL-1。

表1 方法确证标准曲线Table 1 Confirming standard curve
2.2.3 准确度与精密度
取空白血浆0.2 mL,按“标准曲线的制备”项下操作,制备缬沙坦低、中、高3个浓度(分别为25,250,2 500 ng·mL-1)的质量控制样品(QC),6个样本,重复3个分析批,并与标准曲线同批测定,以当日的标准曲线计算QC样品的测得浓度,与配制的浓度对照,求得本法的准确度与精密度,数据见表2。

表2 HPLC法测定血浆中缬沙坦的准确度与精密度Table 2 Accuracy and precision of determining valsartan in human plasma by HPLC method
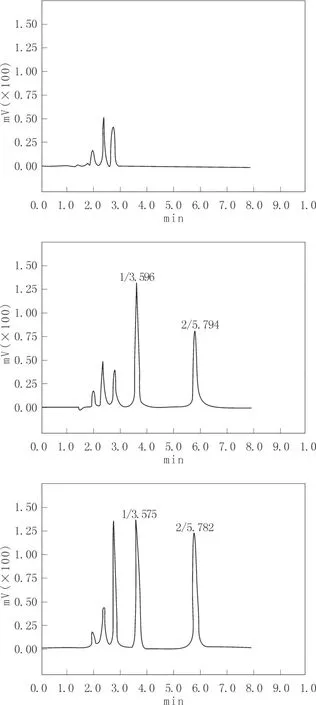
图1 HPLC法测定血浆中缬沙坦色谱图Fig.1 Determination of valsartan in human plasma by HPLC
A 空白血浆样品图 B 空白血浆样品加缬沙坦、替米沙坦标准品的色谱图(替米沙坦 500 ng·mL-1,峰 1; 缬沙坦 2 000 ng·mL-1,峰 2)C 受试者口服缬沙坦胶囊后1.0 h的血浆样品色谱图
2.2.4 提取回收率
取空白血浆0.2 mL,按“标准曲线的制备”项下操作,制备缬沙坦低、中、高3个浓度(分别为25,250,2500 ng·mL-1)的样本,每个浓度进行 6样本分析。同时另取相同浓度的标准溶液进行分析,获得相应峰面积的平均值,以每一浓度两种处理方法的峰面积,计算提取回收率。结果表明,低、中、高三个浓度的平均提取回收率分别为(54.5±4.79)%、(57.1±3.85)%和(64.5±3.01)%,结果见表3。

表3 HPLC法测定血浆中缬沙坦的提取回收率Table 3 Extraction recovery in determination of valsartan in human plasma by HPLC method
2.2.5 稳定性考察
血浆样品经-20 ℃反复3次冻融,预处理后室温放置24 h,-20 ℃冰冻放置1个月后,测定样品浓度。结果显示所有测定值与初始值的相对误差(RE %)均小于15%,说明分析测试过程中的样品较为稳定,结果见表4、表5和表6。
本试验采取HPLC法测定人血浆样品中缬沙坦浓度,结果表明,血浆中的内源性物质不干扰待测物的测定。本方法具有快速、专属、准确、灵敏度高德特点,适合缬沙坦的药代动力学研究。
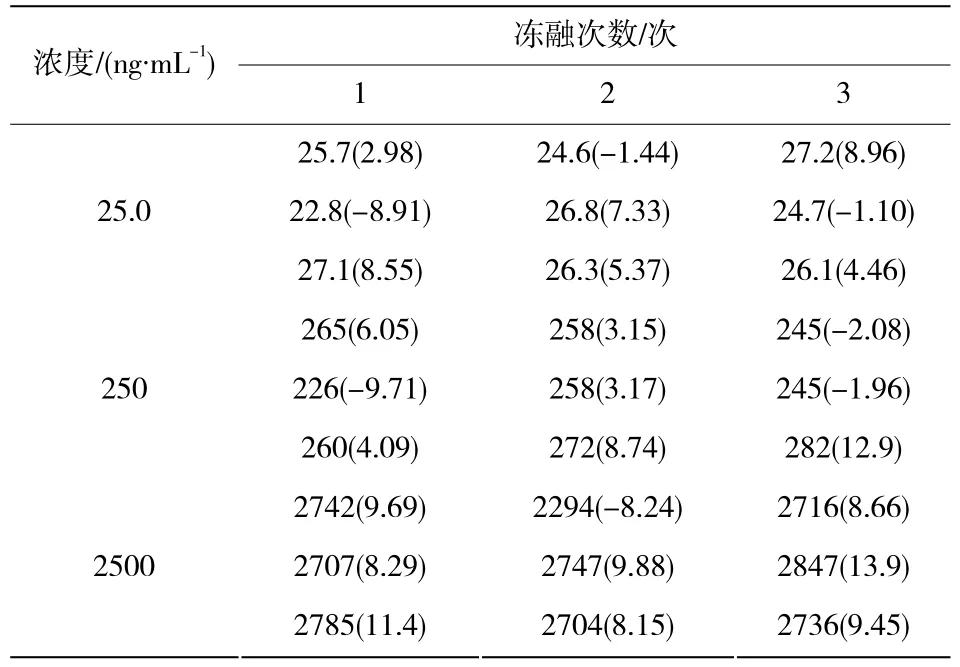
表4 HPLC法测定血浆中缬沙坦的稳定性(-20 ℃反复3次冻融)Table 4 The stability of sample in the determination of valsartan by HPLC method(after three times freezing and thawing at -20 ℃)
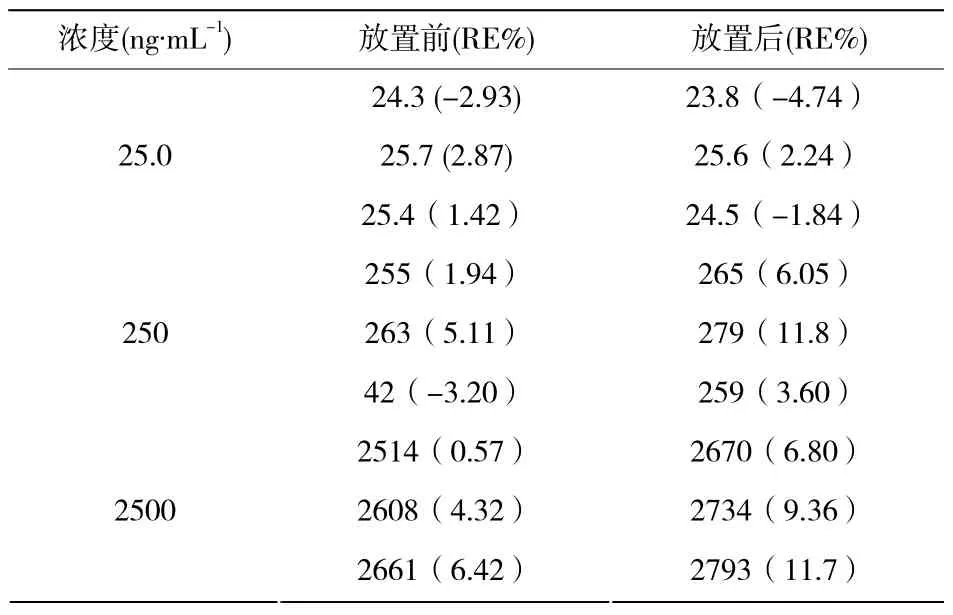
表5 HPLC法测定血浆中缬沙坦的稳定性(室温放置24 h)Table 5 The stability of sample in the determination of valsartan by HPLC method (before and after placing 24 h at room temperature)
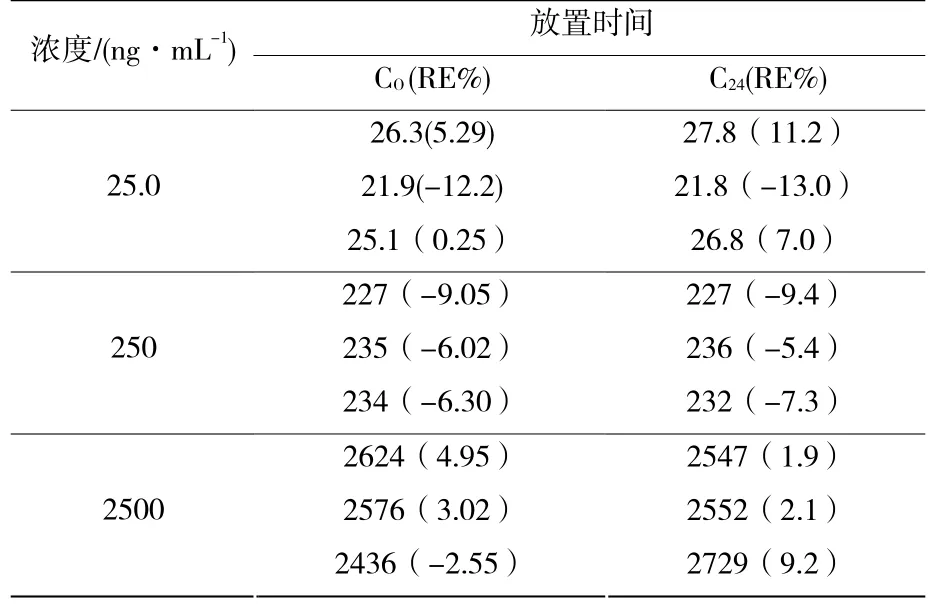
表6 HPLC法测定血浆中缬沙坦的稳定性(-20 ℃冰冻放置1个月)Table 6 The stability of sample in the determination of valsartan by HPLC method(after freezing for one month at -20 ℃)
2.3 缬沙坦胶囊药代动力学的研究
2.3.1 受试者选择
选择 20名健康男性志愿者,年龄为(23.4±1.64)岁,体质量为(65.2±7.84)kg,体重指数均在 19~24 内。受试者一般体格检查、心电图及血尿常规、肝肾功能等实验室检查均为正常。受试者无既往慢性病史,无药物过敏史,无药物滥用、酗酒、嗜烟史。试验前3周内及试验期间未服用其他药物,试验前3个月内未献血或失血,试验前3个月内未参加其它临床试验。试验前书面告知受试者研究的性质、目的和风险,受试者在充分了解的基础上自愿签署知情同意书。
2.3.2 给药方案与样品采集
20名受试者于试验前1日晚进标准晚餐后,禁食不禁水10 h过夜,试验期间禁饮茶、咖啡及含咖啡因及醇类的饮料,并禁止吸烟。试验当日晨起空腹口服缬沙坦胶囊 1片(代文,相当于缬沙坦 80 mg),用200 mL温开水送服,给药后2 h后可进统一早餐,4 h后进统一清淡午餐,其间饮水适量。于服药前和服药后0.5,1.0,1.5,2.0,3.0,4.0,6.0,8.0,12.0,24.0,30.0 h分别采取前臂静脉血5 mL,置入肝素化离心试管中,离心(3 500 r·min-1)10 min,分离血浆,血浆于-20 ℃冷冻保存。
2.3.3 药代动力学结果
20名健康受试者口服缬沙坦胶囊1粒后在规定时间内进行血样采集,用HPLC法对采集到的血浆样品进行血药浓度测定,结果见表 7,所得血药浓度-时间曲线见图2。
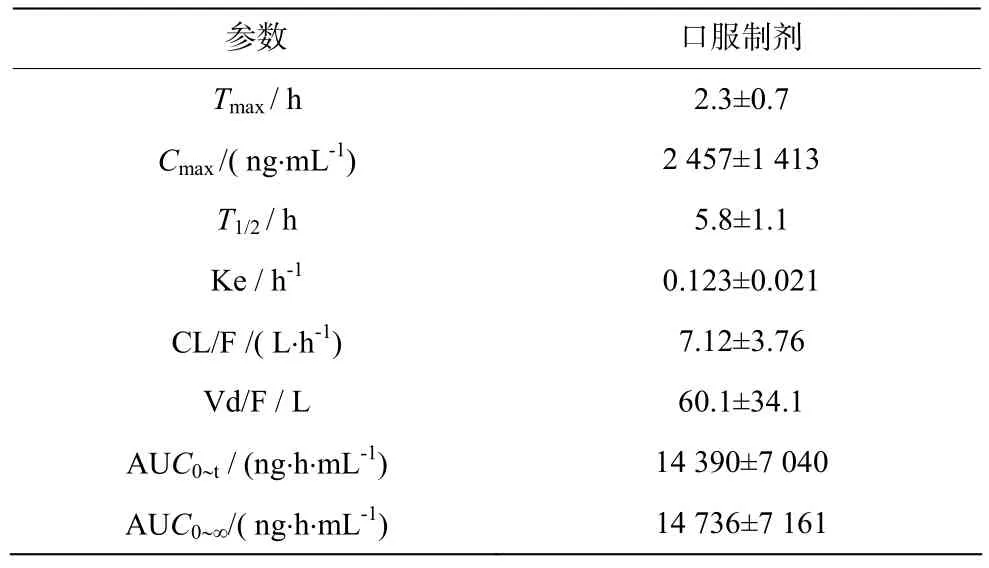
表7 20名健康受试者口服缬沙坦胶囊的药物动力学参数Table 7 Pharmacokinetics parameters of oral administration valsartan capsule
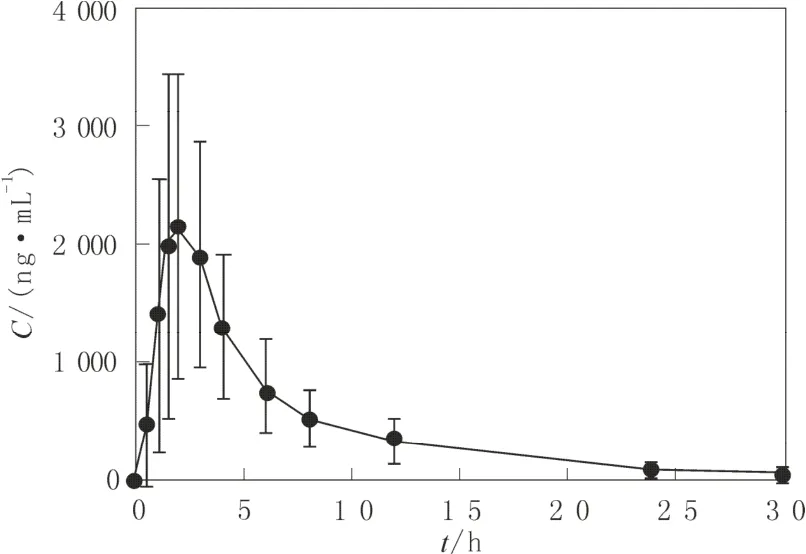
图2 20名受试者口服缬沙坦胶囊的平均药浓度-时间曲线Fig.2 Mean drug concentration-time curve of oral administration valsartan capsule
3 结 论
缬沙坦的HPLC分析方法已有多篇报道[3-10]。
本次实验采用高效液相色谱法,其方法用来测定血浆中缬沙坦浓度、研究血浆中缬沙坦的药代动力学,测定了20名健康男性志愿受试者口服缬沙坦胶囊后的不同时刻血浆中缬沙坦的浓度,并根据测定结果求算缬沙坦的药代动力学参数为与文献报道基本一致。
缬沙坦分散片的主要药动学参数:Tmax为(2.3±0.7)h;Cmax为(2 457±1 413)ng·mL-1;T1/2为(5.8±1.1)h;AUC0-t为(14 390±7 040)ng·h·mL-1;AUC0-∞为 (14 736±7 161)ng·h·mL-1。
[1]曹文,凌树森,张启高,等. 血管紧张素转换酶基因多态性与原发性高血压及血管紧张素转换酶抑制降压作用[J]. 药学通报,1999,84(9):655-657.
[2]谢燕,李声宏,沈蕾,等. 缬沙坦在慢性肾小球肾炎病人中的应用[J]. 中国新药与临床杂志,2001, 20(6):427-430.
[3]SIOUFI A,MARFIL F,JAOUEN A,et al. The effect of age on the pharmacokinetics of valsartan[J]. Biopharm Drug Dispos ,1998,19(4):237-244.
[4]李晔,赵志刚,陈旭,等. 高效液相色谱法测定缬沙坦的血浆药物浓度[J]. 药物分析杂志2000, 20(6):404-406.
[5]许长江,刘骁,王海学,等. 缬沙坦胶囊在人体的药物动力学及相对生物利用度[J]. 中国临床药学杂志,2002,11(2):91-94.
[6]宫文会,李高,斯陆勤,等. 食物对复方缬沙坦片中缬沙坦人体药动学特征的影响[J]. 中国药师,2005,8(12):988-990.
[7]Daneshtalab N,Lewanczuk RZ,Jamali F. High2performance liquid chromatographic analysis of angiotensin II receptor antagonist valsartan using a liquid extraction method[J]. J Chromatogr B,2002 ,766 (6):345-349.
[8]赵志刚,李晔,陈旭,等. 缬沙坦胶囊生物等效性研究[J]. 中国药学杂志,2002,37(9):686-689.
[9]Gonzalez L,Lopez JA,Alonso RM. Fast screening method for the determination of angiotensin II receptor antagonists in human plasma by high2performance liquid chromatography with fluorimetric detection[J]. J Chromatogr A,2002,949(122):49-60.
[10]Sioufi A,Marfil F,Godbillon J. Automated determination of an an2 giotensin Ⅱ receptor antagonist , CGP48 933 , in plasma by high performance liquid chromatography. [J]. Liq Chromatogr,1994,17(10):2179-2186.

