酸性离子液体萃取催化氧化脱除模拟油中噻吩
黎俊波,曹灿灿,余响林,胡启辉,廖海星
(1.武汉工程大学化工与制药学院,湖北 武汉 430074;2.长江大学化学与环境工程学院,湖北 荆州 434020)
0 引 言
汽车尾气中的SOX直接排放到大气中会造成严重的空气污染.为此,很多国家对燃料油中硫含量提出严格要求[1-3].2010年左右,我国环境保护总局规定北京、上海、广州等城市还将执行欧Ⅳ标准,规定油品中硫含量要小于50μg/g[4].因此,开发利用低硫油品和安全的脱硫技术成为人们关注的焦点.
油品中的硫化物主要有噻吩及其衍生物和二硫化物、硫醇、硫醚等[5-6].工业上主要的脱硫方法是催化加氢脱硫,此方法可脱出油品中简单的小分子有机硫化物,但不能完全脱除噻吩及其衍生物,而车用汽油噻吩类硫化物占86.9%[7].由于加氢脱硫有反应成本高同时还会使辛烷值改变等技术缺陷[8-10],研究者开发出非加氢脱硫技术,如氧化脱硫[11]、吸附脱硫[12-13]、生物脱硫[14]等.在室温下呈液态的离子液体是一种新型绿色溶剂,一般由有机阳离子和无机阴离子组成.它具有可设计,熔点高,液态范围宽,电化学窗口大,蒸汽压低,热化学稳定性好等优点[15].经研究表明离子液体可以使油品中的硫含量下降,且辛烷值不变[16-19].同时,由于离子液体不挥发,选择合适的离子液体,反应完成后油相和离子液体相便于分离,可以重复使用,该脱硫的过程被认为是高效、安全的绿色反应过程[20].
酸性离子液体用于脱硫的有:柯明等[21]研究[BMIM]HSO4与H2SO4复配体系为催化剂和萃取剂,共轭二烯烃为烷基化试剂,在催化裂化FCC汽油烷基化脱硫中应用具有很好的脱硫效果且辛烷值变化不大.随后,Zhang等[22]研究了酸性[BMIM]HSO4同时作为萃取剂和催化剂,对含二苯并噻吩模拟油进行深度脱硫,优化反应条件后,最后脱硫率达100%.Gao等[23]分别以酸性[BMIM]HSO4和[C4Py]HSO4为萃取剂和催化剂,H2O2为氧化剂,两种脱硫体系的脱硫率分别为99.6%和32.8%.Gui等[24]以[(CH2)2COOHmim]HSO4为萃取剂和催化剂,质量分数为30%H2O2为氧化剂,脱硫率为96.7%.本研究拟对不同类型的酸性离子液体在模拟油中脱硫效果进行比较,以[BMIM]HSO4为萃取剂和催化剂,双氧水为氧化剂,并探讨了其工艺条件对脱硫效果的影响.本文的创新点是在离子液体的阳离子咪唑环接上不同碳链长的烷基,比较它们的脱硫效果.之所以选择咪唑类的离子液体作为研究对象,是因为咪唑类离子液体对油品中噻吩类的化合物有较好的萃取能力,而阴离子选择具有催化效果的HSO4-的盐,这样[Rmim]HSO4可以同时做萃取剂和催化剂.
1 实验部分
1.1 仪器与药品
高效液相色谱(戴安UltiMate 3000).
N-甲基咪唑(分析纯,湖北方乐达科技有限公司),溴乙烷(分析纯,天津市福晨化学试剂厂),溴代正丁烷(分析纯,上海五联化工厂),溴代正辛烷(分析纯,上海五联化工厂),硫酸氢钠(分析纯,国药集团化学试剂有限公司),正辛烷(分析纯,天津市福晨化学试剂厂),噻吩(分析纯,鼎润化工原料股份有限公司),质量分数30%双氧水(国药集团化学试剂有限公司),乙腈(分析纯,天津市福晨化学试剂厂),乙酸乙酯(分析纯,天津市福晨化学试剂厂),甲醇(色谱纯,国药集团化学试剂有限公司),娃哈哈纯净水.
1.2 实验方法
1.2.1 离子液体合成 采用两步法合成离子液体.按照文献[22,25-26]的方法,第一步合成溴代中间体,反应式如下:
称取1 mol N-甲基咪唑于三口烧瓶中,在冰水浴条件下逐滴加入1.2 mol RBr,待滴加完室温反应2 h,缓慢升温至60℃反应24 h,自然冷却至室温.得到粘稠的液体用乙酸乙酯洗涤,减压蒸去乙酸乙酯,于70℃真空干燥24 h,得到[Rmim]Br.第二步通过置换反应合成HSO4-类离子液体.将一定量的[Rmim]Br溶解在乙腈中,加入等摩尔的Na HSO4,室温机械搅拌4天过滤,减压蒸去乙腈,用乙酸乙酯洗涤3次,蒸干乙酸乙酯,于70℃真空干燥24 h,得到[Rmim]HSO4.
1.2.2 模拟油的配制 取5 mg噻吩(T)溶解在10 g的正辛烷溶液中,配制成500 ug/g的模拟油.
1.2.3 离子液体脱硫操作步骤 准确称取一定量的离子液体和模拟油于茄形瓶中,加入一定量的双氧水,在一定温度下搅拌一定时间进行萃取-催化氧化脱硫,反应后静置分层,取上层油样用高效液相分析硫含量.
1.2.4 高效液相操作条件 流动相:甲醇∶水=9∶1;流速:1 m L/min;柱温:25℃;波长:220 nm;进样量:20 u L.
2 结果与讨论
2.1 离子液体萃取-催化氧化脱除模拟油中噻吩的过程和机理
萃取-催化氧化脱硫是一个两相反应体系:咪唑类的离子液体阳离子和噻吩都具有芳环结构,含有大π键的离子液体阳离子于极易极化的噻吩相互接触时易形成络合物,从而将噻吩类化合物萃取至离子液体相中,同时,H2O2在体系中分解产生的羟基自由基和过羟基自由基有强氧化性,在酸性离子液体催化作用下,可将噻吩氧化成相应的砜和亚砜,具有较大极性的砜和亚砜溶解在离子液体相中,进而达到脱除噻吩的目的.反应过程如图1所示.
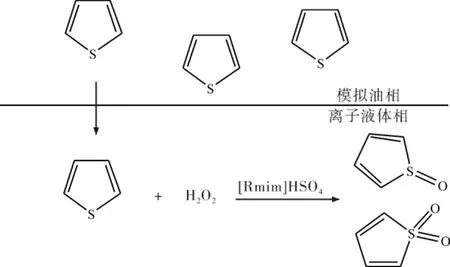
图1 H 2 O2-[Rmim]HSO4体系用于模拟油脱硫过程Fig.1 H 2 O2-[Rmim]HSO4 system For the simulation of oil desulfurization process
2.2 反应温度对脱硫率的影响
反应温度对脱硫率有明显的影响.由图2可知,在离子液体-模拟油体系中,温度由25℃上升至55℃时,脱硫率上升的较慢,当温度高于55℃时,脱硫率上升的较快,这是因为一方面随着温度的升高离子液体的粘度在减小,离子液体萃取脱硫的能力在提高[23];另一方面,随着温度的升高,产生羟基自由基的速率在增加,对噻吩的氧化能力在增加,所以噻吩的脱硫率一直在增加.因此反应温度选择85℃为宜.
2.3 氧硫比对脱硫率的影响
从图3可知,当O/S为20时,脱硫率仅为69.3%,较低的原因可能是H2O2产生的羟基自由基数量较少,只有一部分噻吩被氧化.当O/S高于24时,随着分解产生的羟基自由基量的增加脱硫率也在明显增大.当O/S高于28时,脱硫率无明显增加,说明分解生成的羟基自由基数量足够氧化模拟油中噻吩,所以O/S为28为宜.
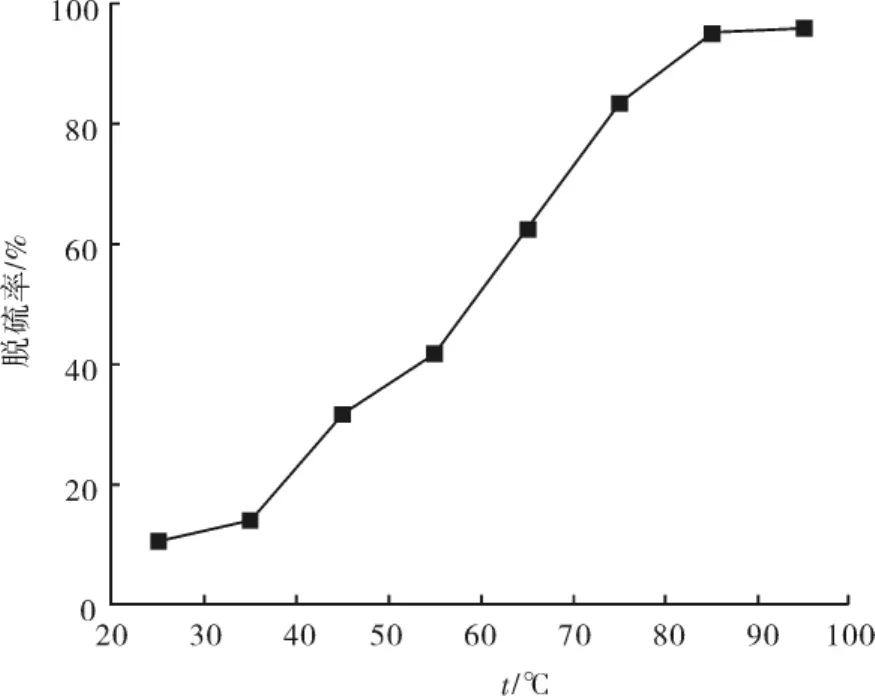
图2 反应温度对脱硫率的影响.Fig.2 Effect of reaction temperature on the desulfurization rate.
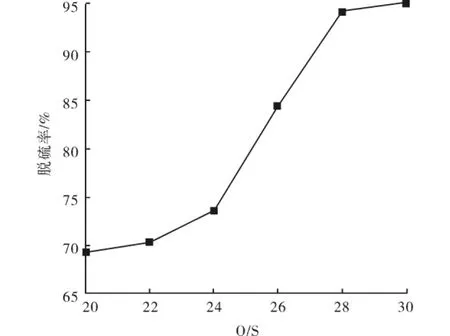
图3 氧硫比对脱硫率的影响Fig.3 Effect of O/S ratios on the desulfurization rate
2.4 反应时间对脱硫率的影响
从图4可知,在0.5 h时,脱硫率仅有27.8%,可能是因为反应开始时,油相中的噻吩首先被[Bmim]HSO4萃取至离子液体相中.而后随着反应时间的延长,脱硫率在逐步提高.在反应时间为4 h后,脱硫率无明显增加,所以反应时间为4 h为宜.
2.5 剂油质量比对脱硫率的影响
从图5可知,剂油质量比小于1时,随着剂油比的增加,脱硫率在增大,原因是随着[Bmim]HSO4用量的增多,离子液体溶解氧化产砜和亚砜的能力增大,脱硫率增加.剂油比为1时,达到最大脱硫率为97.6%.当剂油比大于1时,脱硫率在减小,这是因为[Bmim]HSO4用量的增加导致氧化剂H2O2的相对浓度降低,H2O2的量不能使模拟油中的噻吩完全被氧化.所以剂油比为1时为宜.

图4 反应时间对脱硫率的影响.Fig.4 Effect of reaction time on the desulfurization rate
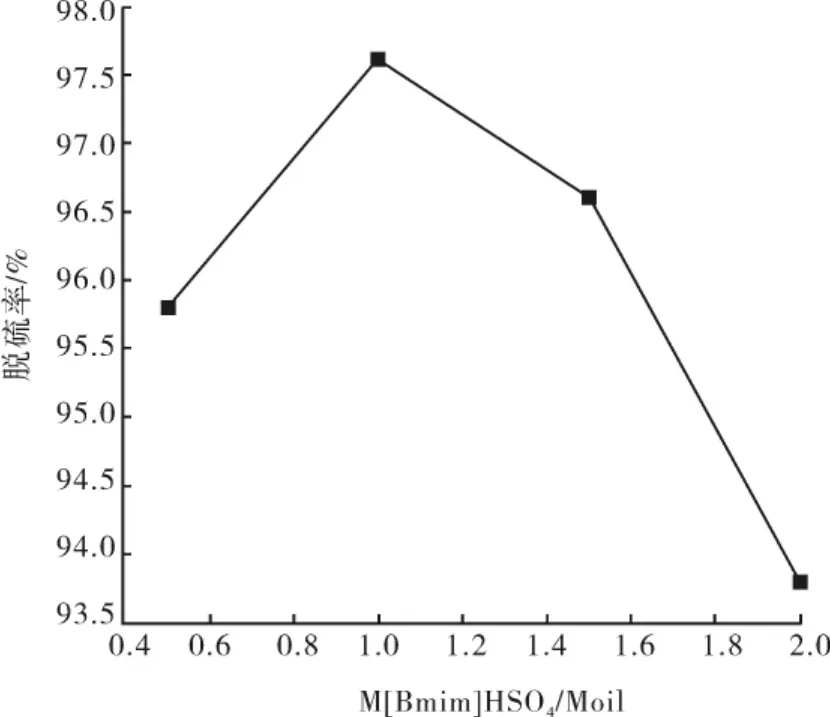
图5 剂油质量比对脱硫率的影响Fig.5 Effect of solvent-oil ratio on the desulfurization rate
2.6 不同离子液体对脱硫率的影响
用不同的离子液体对模拟油进行萃取-催化氧化脱硫,实验结果从表1可知,1-甲基-3-乙基咪唑硫酸氢根盐([Emim]HSO4)<1-甲基-3-丁基咪唑硫酸氢根盐([Bmim]HSO4)<1-甲基-3-辛基咪唑硫酸氢根盐([Omim]HSO4).这是因为一方面随着离子液体的阳离子的烷基链的增加,离子液体的粘度在减小,增加了离子液体萃取的能力;另一方面,咪唑类的离子液体阳离子具有芳香性,引入较长的碳链,降低了阳离子的对称性,同时其极性增强,使其与噻吩之间的作用力增大,进而脱硫率提高.在所测的离子液体中,[Omim]HSO4的脱硫率坐高达98.9%,原因是相比于其他离子液体[Omim]HSO4阳离子所接的碳链最长,粘性最小,极性最大,所以脱硫效果最佳.
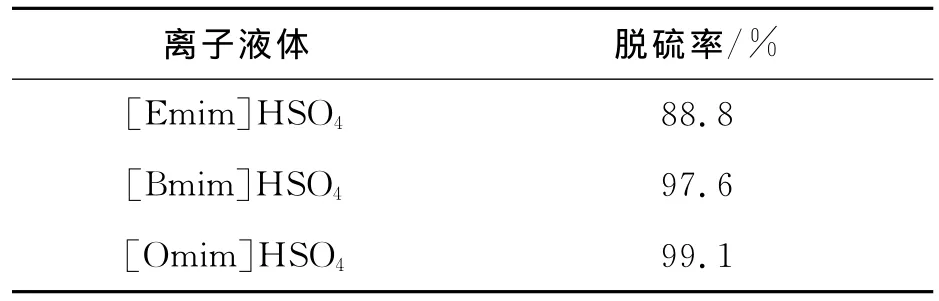
表1 不同离子液体的脱硫率Table 1 The desulfurization rate of different ionic liquids
3 结 语
利用离子液体的合成原理将乙基、丁基和辛基接到咪唑环上,合成相应的离子液体[Emim]HSO4、[Bmim]HSO4和[Omim]HSO4,应用于噻吩溶解在正辛烷制成的模拟油进行萃取-催化氧化脱硫实验,得到如下结论:
a.在[Rmim]HSO4-H2O2体系中,酸性离子液体为萃取剂和催化剂,H2O2为氧化剂,模拟油中的噻吩先被[Rmim]HSO4萃取至离子液体相中,再由H2O2分解产生的羟基自由基氧化为砜或亚砜,保留在[Rmim]HSO4相中,进而达到深度脱硫的目的;
b.用两步法合成了三种不同结构的酸性离子液体,并对他们的脱硫效果进行比较,实验结果表明,阴离子相同的离子液体,咪唑环上所连的烷基链越长,脱硫效果越好;
c.[Bmim]HSO4用于模拟油脱硫的最佳工艺条件为:剂油比1.0,反应温度85℃,反应时间为4 h,氧硫比为28时,脱硫率达97.6%.
致谢
感谢国家自然科学基金,湖北省自然科学基金,湖北省教育厅优秀中青年项目,绿色化工过程教育部重点实验室开放基金的资助.
[1]Alessandro N,Tonucci L,Bonetti M,et a1.Oxidation of dibenzothiophene by hydrogen peroxide or monopomulfate and metal-sulfophthalcyanine catalysts:an easy access to biphenylsuhonen or 2-(2-hydroxybipheny1)sulfonate under mild conditions[J].New J Chem,2003,27(6):989-993.
[2]张力,张波,徐亚荣,等.直馏高硫柴油选择性催化氧化-萃取脱硫研究[J].化工生产与技术,2009,16(5):14-l7.
[3]罗会明,熊麟,颜学敏.燃料油选择性吸附脱硫研究进展[J].精细石油化工进展,2009,10(6):51-55.
[4]王云芳,尹风利,史德清,等.车用燃料油吸附法深度脱硫技术进展[J].石油化工,2006,35(1):94-99.
[5]Bae J S,Choi K,Moon S H,et a1.Hydrodesulfurization of DBT,4-MDBT and 4,6-DMDBT on fluorinated Co MoS/Al2O3catalysts[J].Appl Catal A,2000,200(122):233-242.
[6]Shafi R,Hutchings G J.Hydrodesulfurization of hindered dibenzothiophenes:an overview[J].Catal Today,2000,59(4):423-442.
[7]Chu X M,Hu Y F,Li J G,et a1.Desulfurization of diesel fuel by extraction with [BF4]-based ionic liquids[J].Chin J Chem Eng,2008,8(16):881-884.
[8]Liu S Z,Wang B H,Cui B C,et a1.Deep desulfurization of diesel oil oxidized by Fe(VI)systems[J].Fuel,2008,87(3):422-428.
[9]Schmitz C,Datsevitchl,Jess A.Deep desulfurization of diesel oil:kinetic studies and process-improvement by the use of a two-phasereactor with presaturator[J].Chem Eng Sci,2004,59(14):2821-2829.
[10]Tilleur R G,Ravigli J,Quenza S,et a1.Catalyst for ultra-low sulfur and aromatic diesel[J].Appl Catal A:General,2005,282(1-2):227-235.
[11]Garca-Gutierrez J L,Fuentes G A,Hemandez-Teran M E,et al.Ultra-deep oxidative desulfurization of diesel fuel with H2O2catalyzed under mild conditions by polymolybdates supported on Al2O3[J].Appl Catal,A,2006,305(1):15-20.
[12]Greenwood G J,Dennis K.Next Generation sulfur removal technology[C].San Antonio,NPRA Annual Meeting,2000.
[13]Tucker C,Sughm E,Vanderlaan J.Production of ultra-low sulfur fuels:today and tomorrow[C].San Antonio,NPRA Annual Meeting,2003.
[14]Toshiki F,Yoshitaka I,Ken-Ichi N,et a1.Thermophilic biodes-ulfurization of hydrodesulfurized light gas oils by mycobacterium phlei WU-F1[J].FEMS Microbiol Lett,2003,221(1):137-142.
[15]石家华,孙逊,杨春和.离子液体研究进展[J].化学通报,2002,65(4):243-250.
[16]Swatloski R P,Holbrey J D,Rogers R D.Ionic liquids are not always green:hydrolysis of 1-butyl-3-methylimidazolium hexafluoroborate[J].Green Chem,2003,5(4):361-363.
[17]Wasserscheid P,van H R,Bosmann A.1-n-butyl-3-methylimidazolium ([Bmim ]) octylsulfate-an even'Greener'ionic liquid[J].Green Chem.2002,4(4):400-404.
[18]周瀚成,陈楠,石峰,等.离子液体萃取脱硫新工艺研究[J].分子催化,2005,19(2):94-97.
[19]冯婕,李春喜,孟洪,等.磷酸酯类离子液体在燃油深度脱硫中的应用[J].石油化工,2006,35(3):272-276.
[20]李桂花,王安峰,李增喜.离子液体在石化工业中的应用现状[J].精细石油化工,2007,24(1):74-78.
[21]柯明,汤奕婷,曹文智,等.离子液体在FCC汽油脱硫中的应用研究[J].西南石油大学学报,2010,32(3):145-149.
[22]Zhang W,Xu K,Zhang Q,et al.Oxidative desulfurization of dibenzothiophene catalyzed by ionic liquid[BMIM]HSO4[J].Ind Eng Chem Res,2010,49(22):11760-11763.
[23]Gao H S,Guo C,Xing J M,et al.Extraction and oxidative desulfurization of diesel fuel catalyzed by a Bronsted acidic ionic liquid at room temperature[J].Green Chem,2010,12:1220-1224.
[24]Gui J Z,Liu D,Sun Z L,et al.Deep oxidative desulfurization with task-specific ionic liquids:an experimental and computational study[J].J Mol Catal A:Chem,2010,331:64-70.
[25]马江华,李玉平,李会泉,等.[Emim]HSO4离子液体的合成及其在氧化铝电解中的应用[J].过程工程学报,2007,7(6):1083-1088.
[26]黄英蕾,于长顺,王岩,等.酸性离子液体中异丁烷和丁烯的烷基化反应[J].大连工业大学学报,2009,28(1):33-35.

