无催化多不饱和脂肪酸甘油酯的合成和优化
何寿林,徐 玮,辛高峰,孙 成
(武汉工程大学湖北省新型反应器与绿色化学工艺重点实验室,湖北 武汉 430074)
0 引 言
ω-3系列多不饱和脂肪酸作为一种功能性保健食品,具有预防和治疗心血管疾病[1]、改善记忆力和益智[2-3]等功效,但其产品多以品质和安全得不到保证的游离脂肪酸型和乙酯型存在,研究证明甘油酯型是最好的产品形式[4-5].
多不饱和脂肪酸甘油酯的合成主要有生物酶法[6-7]、化学催化法[8-9]和无催化合成法[10].生物酶法的缺点为反应中有有机溶剂的存在,不可避免溶剂残留在产物中,影响产物的品质且生产周期长,转化率低.传统化学方法合成甘油酯多采用强碱(KOH、NaOH)等作催化剂,存在反应温度过高,产品色泽差,需要水洗、中和、干燥等后处理工序,并且设备腐蚀严重、有三废排放、对环境造成污染等缺点.无催化合成法所得产品色泽清亮,无溶剂残留,后续处理简单,不会造成环境污染且易于扩大化生产.
1 实验部分
1.1 主要药品和仪器
KOH,分析纯;丙三醇,分析纯;多不饱和脂肪酸产自山东东营广元生物工程有限公司.纯SHB-Ⅲ循环水式多用真空泵;DF-101S集热式恒温加热磁力搅拌器;AR1140电子分析天平;GC-9790气相色谱仪;HP6890GC/5973MSD气质联用色谱分析仪.
1.2 实验步骤
实验步骤在文献[11]里已有详细介绍,这里不再赘述.
1.3 分析方法
1.3.1 酸值的测定 鱼油酸值的测定方法及计算公式详见文献[12].

式中:v——中和滴定所耗 KOH 的体积,单位m L;
c——标准KOH溶液的浓度,单位mol/L.
1.3.2 转化率的计算 采用上步酸值的结果,计算多不饱和脂肪酸的转化率.
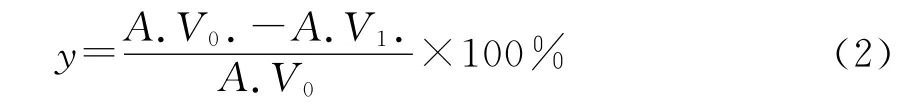
式中:A.V1.——产物的酸值,单位 mg(KOH)/g;
A.V0.——原料的酸值,单位 mg(KOH)/g.
2 结果与讨论
2.1 多不饱和脂肪酸甘油酯的合成路线
多不饱和脂肪酸甘油酯的合成反应是在减压条件下加热进行的,因此可以假设为吸热不可逆反应.多不饱和脂肪酸甘油酯的合成反应是复杂的连续反应,产物有甘一酯、甘二酯、甘三酯等,反应流程为:
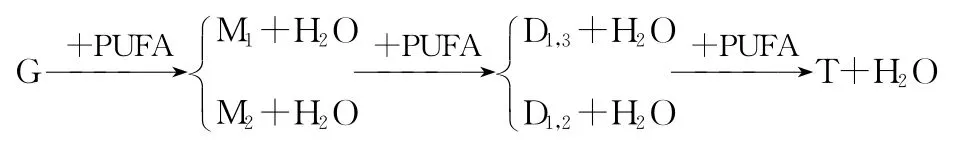
流程图中G为丙三醇,M1为1-甘一酯、M2为2-甘一酯、D1,2/D1,3为甘二酯、T为甘三酯.
2.2 合成产物的鉴定
2.2.1 薄层色谱法鉴定产物的组成 将红花油标样通过以硅胶G板为固定相、以氯仿/丙酮/甲醇(体积比为95/4.5/1.5)为展开剂的薄层板进行薄层色谱分析得到标样的色谱图(1#),将合成的产物通过柱色谱分成三个样品(2#、3#和4#),通过薄层色谱分析分别得到色谱图,结果见图1.
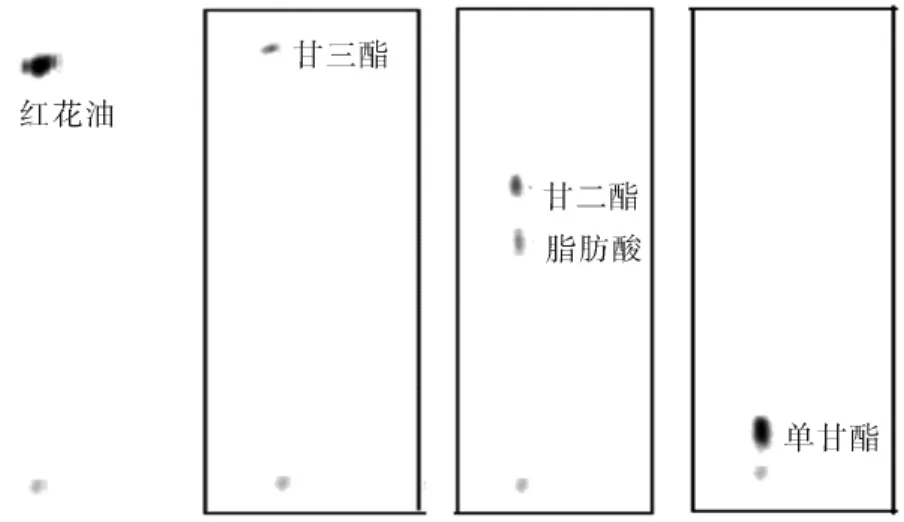
图1 合成产物的薄层色谱图Fig.1 TLC of the synthetic products graph
以主要成分为甘三酯的红花油作为标样,通过对其薄层色谱图(图1 1#)的位移与所合成产物的薄层色谱图对比可知,2#与1#的位移最为接近,推断其为甘油三酯.从合成反应路线可知,既然有三酯生成,产物中必定存在一酯和二酯,推断3#为甘二酯,4#为单甘酯.为了进一步鉴定甘油酯的存在形式,对薄层色谱的2#、3#、4#样品进行了红外吸收光谱的分析.
2.2.2 红外光谱分析结果 图2为薄层色谱分析2#、3#和4#样品以及5#标准样品的红外吸收光谱图.
由图2可知,在3 670~3 230 cm-1区内,2#、3#和4#谱图的峰面积变化较大,因为游离的羟基产生的吸收峰尖锐,出峰位置大于3 600 cm-1;而氢键的形成又会导致吸收峰向低波数移动,出峰位置小于3 600 cm-1,随缔合程度的增大,峰越来越宽,越向低波数处靠近.4#谱图在3 350~3 250 cm-1处出现与标准样5#类似的较宽峰,即硬脂酸甘一酯分子中羟基的伸缩振动区,可以确定4#为甘一酯.谱图表示,2#样品羟基伸缩振动区的峰面积最小,根据前面的分析可推断其为甘三酯,与薄层色谱分析结论一致.3#的羟基伸缩振动区的峰面积介于2#与4#之间,推断其为甘二酯.综上分析,推断2#、3#和4#样品分别为甘一酯、甘二酯和甘三酯.

图2 合成产物的红外吸收光谱Fig.2 Infrared absorption spectrum(IR)of the synthetic products graph
2.2.3 通过GC-MS分析鉴定产物的成分 取一定量的样品,用GC-MS仪分析产物中脂肪酸的成分.见图3及表1.

图3 鱼油的总离子流图Fig.3 Total ion flow diagram of fish oil graph

表1 鱼油脂肪酸成分分析Table 1 Component analysis of the fatty acids of fish oil
通过GC-MS分析可知产物中含有多种ω系列多不饱和脂肪酸,包括二十二碳六烯酸(DHA)和二十碳五烯酸(EPA).
2.2.4 气相色谱分析产物中脂肪酸的质量分数
取一定量的样品,用气相色谱仪分析鱼油中主要脂肪酸的质量分数,色谱图见图4,用面积归一法得出脂肪酸的质量分数见表2.

图4 合成产物色谱图Fig.4 GC graph of the synthetic products

表2 合成产物中主要脂肪酸的质量分数Table 2 The content of primary fatty acids of the synthetic products
通过气相色谱分析,可知产物中EPA的质量分数为34.91%,DHA的质量分数为22.83%.
通过前面的分析,可以判断出多不饱和脂肪酸甘油酯合成的产物主要是由多不饱和脂肪酸为碳链的甘一酯、甘二酯和甘三酯组成.

表3 试验因素和水平Table 3 Factors and levels
2.2 回归方程的建立
本实验在前期研究单因素多水平和一次正交实验分析的基础上,对多不饱和脂肪酸甘油酯合成工艺[11]进行进一步优化,分别取用x1、x2和x3表示温度、时间和醇酸比,对于评价指标多不饱和脂肪酸的转化率用y表示,做二次回归正交试验.试验因素水平表见表3.二次正交回归矩阵及结果见表4,采用Fortran程序对二次正交试验结果进行运算,并进行方差分析,得出回归方程的回归系数及各项回归方程方差分析的各项值,见表5和表6.

表4 二次正交回归矩阵及结果Table 4 The results of quadratic orthogonal combination design
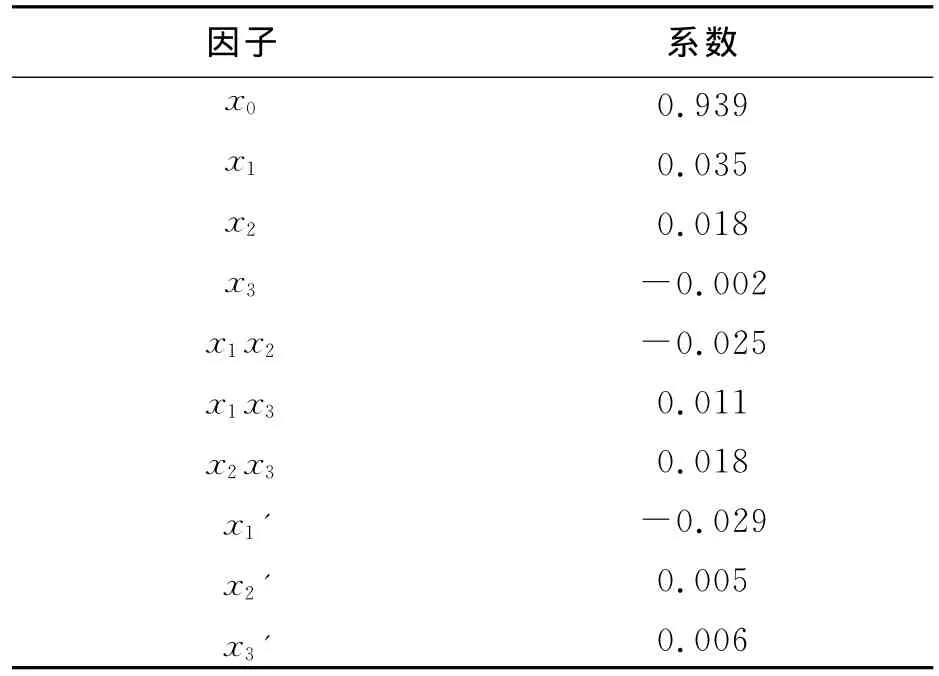
表5 回归方程的回归系数值Table 5 Regression coefficient value of regression equation
通过对回归结果分析,剔除对结果的很不显著项,可以得出回归方程:

式中:y-多不饱和脂肪酸的转化率,%;
x1-温度,℃;
x2-时间,h;
x3-醇酸比.

表6 多不饱和脂肪酸甘油酯合成回归模型方差分析表Table 6 Range analysis of regression model of the synthesis of PUFAs glyceride
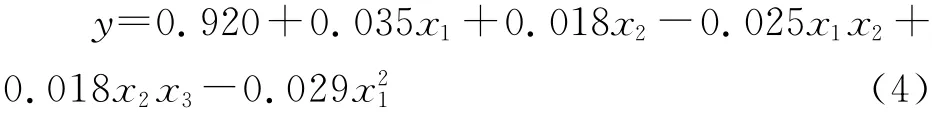
通过偏微分求出极值,可以计算出x1=0.603,x2=0,x3=-0.162



可以计算出极值对应的各因素的值:
A=194.28,B=5,C=0.94
即多不饱和脂肪酸甘油酯合成的最优工艺条件为:温度为194.28℃,时间5 h,醇酸比0.94,其转化率为93.06%.
2.3 数学模型的验证
从表4中随意选取8组数据,在对应条件下用回归方程求出回归值y,与多不饱和脂肪酸转化率的实验值相比较,结果见表7.

表7 实验值与回归值的比较Table 7 Comparison between experimental value and regression value
从表7可知,通过回归方程得出的回归值与实验值的比较得出其平均相对误差为3.62%,证明利用二次回归正交实验设计求得的温度、时间和醇酸比三个因素对多不饱和脂肪酸甘油酯合成影响的数学模型是可行的,具有一定的实用价值.
3 结 语
a.通过薄层色谱、红外光谱和GC-MS对产品进行分析,得出多不饱和脂肪酸甘油酯合成的主要产物是由多不饱和脂肪酸为碳链的甘一酯、甘二酯和甘三酯.
b.通过二次回归正交试验研究得出,多不饱和脂肪酸甘油酯合成的最优工艺条件为:温度为194.28 ℃,时间 5 h,醇酸比 0.94,其转化率为93.06%.
c.通过二次回归数据,拟合多不饱和脂肪酸甘油酯合成的回归方程为:y=0.920+0.035x1+对拟合方程进行验证,回归值与实验值平均相对误差为3.62%,证明了设计求得的温度、时间和醇酸比三个因素对多不饱和脂肪酸甘油酯合成影响的数学模型的可靠性,具有一定的实用价值.
致谢
感谢研究生黄奠坤对实验过程给予的帮助,感谢研究生张红丽在论文写作中的贡献.
[1]徐建国,潘娅静,赵洁.ω-3多不饱和脂肪酸与心血管疾病[J].临床内科杂志,2008,25(12):855-856.
[2]李春香,刘永杰.DHA和EPA的生理功能及开发前景[J].唐山师范学院学报,2002,24(5):71-72.
[3]齐婕,尹桂香,罗红.植物油多不饱和脂肪酸对机体健脑作用的研究[J].北华大学学报,2007,8(4):328-329.
[4]Larry D L,Bronwyn G H.Human absorption of fish oil fatty acids as triacylglycerol,free acids,or ethyl esters[J].Biochemical and Biophysical Research Communication,1988,152(1):328-335.
[5]Ikuo I,Eiji S,Haruko Y,et al.Digestion and lymphatic transport of eicosapentaenoic and docosahexaenoic acids given in the form of triacylglycerol,free acid and ethyl ester in rats[J].Biochimica et Biophysica Acta,1995,1259(3):297-304.
[6]吴可克.酶促鱼油选择性水解制备EPA、DHA甘油酯的研究[J].中国油脂,2002,27(3):91-93.
[7]王卫飞,李行方,高红娟,等.固定化脂肪酶催化合成共轭亚油酸的甘油酯[J].中国油脂,2008,33(6):33-36.
[8]张亚刚,吾满江·艾力,文彬,等.酯交换法合成共轭亚油酸甘油酯[J].精细化工,2003,20(6):353-355.
[9]黄迎春,程健.负载固体酸合成共轭亚油酸甘油酯研究[J].长江大学学报:自然版理工卷,2007,4(2):29-31.
[10]东营广元生物工程有限公司.无催化共轭亚油酸甘油酯的制备方法:中国,2007101151333[P]2007-11-23.
[11]何寿林,黄奠坤,张红丽.多不饱和脂肪酸甘油酯的合成工艺研究[J].武汉理工大学学报,2012,34(3):35-37.
[12]李桂华.油料油脂检测与分析[M].北京:化学工业出版社,2005.

