离子色谱法同时测定烟草中的硝酸盐与亚硝酸盐
张建平,黄朝章,邓其馨,苏明亮,谢卫,许寒春,刘泽春,吴清辉
福建中烟工业有限责任公司技术中心,福建省厦门市海沧区新阳工业区新景路1号 361022
硝酸盐和亚硝酸盐是烟草中一类重要的含氮化合物,其含量的多少不但直接影响烟叶的吃味和品质[1],还会影响其他含氮化合物的形成和含量。其中,亚硝酸盐更是烟草特有亚硝胺的直接前体物,它的含量与烟草特有亚硝胺的含量显著相关[2]。随着人们对烟草特有亚硝胺的日益关注,如何快速准确地对硝酸盐和亚硝酸盐进行定量分析也显得愈发重要。
然而,目前烟草行业仍缺乏一套能同时测定烟草中硝酸盐与亚硝酸盐的方法,相关的仅有YC/T 296-2009 烟草及烟草制品硝酸盐的测定-连续流动法[3],其测定的是氮氧化物的总量,因此急需摸索并建立相应的检测方法,以保证烟草安全性评价及减害工作的顺利进行。目前,国内外用于测定硝酸盐和亚硝酸盐的方法主要集中于水体、食品、蔬菜等领域,根据其测定原理的不同,主要分为光谱法[4-7]、色谱法[8-10]、电化学法[11-15]等三大类。离子色谱法具有样品前处理简单、检测灵敏度高、仪器操作方便等优点,已成为国内外众多标准中亚硝酸盐与硝酸盐检测的经典方法。因此,本文尝试采用离子色谱,优化相关条件,建立一种能够同时测定烟草及烟草制品中硝酸盐和亚硝酸盐的方法。
l 实验部分
1.1 仪器与试剂
戴安ICS-300离子色谱仪,配AS-4mm电导检测器,ASRS300-4mm阴离子抑制器,IonPac AS11-HG色谱柱4 mm ×250 mm(带AS11-HG保护柱4 mm×50 mm),KOH洗脱液发生器;4.5μm微孔过滤膜;SH300超声波发生器(超声频率40 KHz,美国Elmasonic公司);BSA2245-CW电子天平(感量:0.0001 g,德国Sartorius公司)。
硝酸钠、亚硝酸钠标准品(纯度99.5%,购于美国Accustandard);水,符合GB/T6682中一级水的要求;实验用烟样均由福建中烟工业有限责任公司技术中心提供。
1.2 标准工作溶液
准确称取0.06 g(精确至0.1 mg)亚硝酸钠、1.37 g(精确至0.1 mg)硝酸钠用水溶解,定容为1000 mL,即配制成NO2-、NO3
-浓度分别为40 mg/L、1000 mg/L的储备液。根据需要配成如下浓度范围的工作溶液:c(NO2-):0.032、0.040、0.100、0.200、0.400、0.800、1.600 mg/L; c(NO3-):0.800、1.000、2.500、5.000、10.000、20.000、40.000 mg/L。
1.3 样品前处理
将烟叶或烟丝放人烘箱中,40 ℃下烘干,研磨,过2 mm筛,得到的烟草粉末立即装入洁净干燥的广口瓶中,密封保存待测。
称取0.5 g(精确到0.1 mg)待测样品于250 mL锥形瓶中,准确加入50 mL水,具塞后置于超声波发生器超声处理60 min。静置后,取上层清液经0.45µm水相滤膜过滤后待测。
1.4 仪器条件
流动相:水;流速1.2 mL/min;柱温30℃;进样量25 μL;KOH梯度洗脱程序见表1,抑制器电流179mA,以AS-4mm电导检测器作为检测器。
1.5 定性定量方法
按照1.4仪器测试条件测定1.2标准工作溶液和1.3试样萃取液,依保留时间定性,外标法定量。试样中NO2-、NO3-的含量(X)由式(1)计算得出,结果以mg/kg表示:

式中:
X ——试样中NO2-、NO3-的含量,单位为毫克每千克(mg/kg);
k ——稀释倍数;
c ——由标准工作曲线得出的NO2-、NO3-浓度,单位为毫克每升(mg/L);
c ——由标准工作曲线得出的空白中NO-、NO-o23浓度,单位为毫克每升(mg/L);
V ——试样萃取液定容体积,单位为毫升(mL);
m ——试样的质量,单位为克(g);
W ——试样水分的质量分数。

表1 KOH梯度洗脱程序
2 结果与讨论
2.1 色谱条件
2.1.1 色谱柱的选择
目前,烟草行业阴离子色谱柱配备较多的是以表面胺化的乙基乙烯基苯交联55%的二乙烯基苯为固定相的AS11柱和AS11-HC柱。图1为美国戴安公司使用AS11柱和AS11-HC柱分析同一样品色谱图,从图中可以看出,AS11-HC柱分离亚硝酸和硝酸效果要比AS11柱好。这可能是因为AS11-HC柱的基质微粒是直径为9 µm的大孔树脂,而AS11柱的基质微粒是直径为13 µm的微孔树脂,AS11-HC柱的柱效和柱容量都比AS11高。因此,本实验选用IonPac AS11-HC(4 mm×250 mm)阴离子交换柱来作为分析柱。

图1 IonPac AS11柱与AS11-HC分离同一样品的色谱对比图
2.1.2 洗脱液的选择
由于碳酸氢根洗脱液(碳酸根-碳酸氢根混合物)抑制后形成的碳酸易于部分电离,从而导致背景电导和基线噪声都比希望的高[16],因此选择氢氧根洗脱溶液作为洗脱液。
在1 mL/min的流速下,比较了5 mmol/L、10 mmol/L、15 mmol/L、25 mmol/L、30 mmol/L、40 mmol/L KOH 浓度下的 CH3COO-、HCOO-、F-、Cl-、NO2-、CO32-、NO3-、SO42-混合标样色谱分离的情况。如图3所示,当KOH溶液浓度小于或等于 15 mmol/L时, NO2-、NO3-与周边离子达到较好的基线分离。

图2 各等度洗脱条件下0.5mg/L CH3COO-、HCOO-、F-、Cl-、NO2-、CO32-、NO3-、SO42-混合标样的色谱图
由于在实际样品中可能存在其它未知离子对目标峰的干扰,通过文献调研[17]和样品普查,实验最终采用了表1的梯度洗脱程序:开始0到20分钟采用低浓度KOH溶液洗脱液,以保证NO2-和NO3-的分离不受其它离子峰的干扰;而后提高KOH溶液浓度到60 mmol/L,加快洗脱CO32-、SO42-等多价离子及一些难洗脱的离子以避免对柱的污染;而后降低KOH溶液浓度,使柱子平衡,为下一个样品做准备;整个梯度过程仅需28分钟。
在这一梯度洗脱条件下,标样及样品分离结果如图3、4所示。
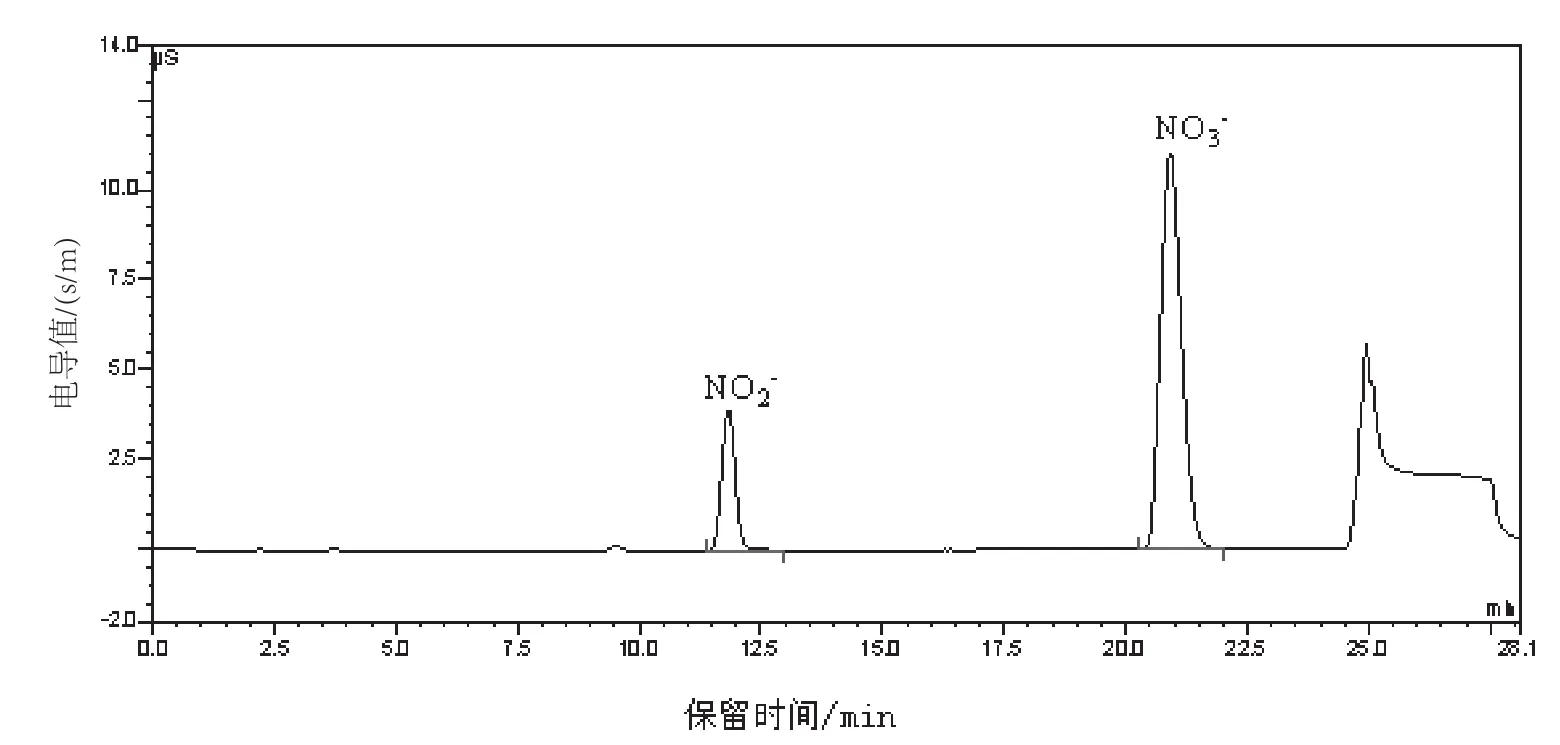
图3 梯度条件下标准溶液色谱图

图4 梯度条件下样品萃取液色谱图
由标样及样品的色谱图可以看出,在此梯度条件下待测离子得到很好的分离。
2.2 样品前处理
为了兼顾样品的类型和浓度范围,实验选取了样品1(烤烟)、样品2(香料烟)、样品3(白肋烟)来做为考察对象,对样品前处理的条件进行摸索。
2.2.1 萃取剂的选择
实验考察了酸性、中性、碱性水溶液对烟草样品中亚硝酸盐、硝酸盐萃取能力的影响,结果如表2、3所示:对于不同的样品,碱性溶液与超纯水提取的效果优于酸性溶液;配对t检验结果发现:︱t NO-2︱<2.92(查表t0.05(2)值),P>0.05;︱t NO3-︱<2.78(查表t0.05(2)值),P>0.05;碱性溶液与超纯水提取的效果无显著性差异。以上结果与庹苏行[18]、杨蕾等[19]报道的结果相一致。考虑到碱性萃取剂可能对基线造成干扰,本实验采用超纯水作为萃取剂。

表2 不同萃取剂对NO2-萃取能力的比较 (mg/kg,n=5)

表3 不同萃取剂对NO3-萃取能力的比较 (mg/kg,n=5)
2.2.2 萃取方式的选择
对超声和振荡两种萃取方式进行比较,结果如表4所示:在考察范围内,振荡萃取的效果要比超声萃取差,因此本实验采用超声萃取方式。
2.2.3 萃取剂用量的确定
为确定萃取剂的用量,实验考察了25 mL、50 mL、75 mL、100 mL四种不同的萃取剂体积,结果如表5、6所示:在考察范围内,提取结果无明显差异,但萃取体积较大时信号较小,易受基线噪音影响;而萃取体积较小时信号值背景值较大,影响测定结果。为了兼顾样品萃取的完全和检测的准确性,萃取剂的用量采用50 mL。

表4 不同萃取方式对检测结果的影响 (mg/kg,n=5)

表5 不同萃取体积对NO- 萃取效率的影响 (mg/kg, n=5)2

表6 不同萃取体积对NO3-萃取效率的影响 (mg/kg, n=5)
2.2.4 萃取温度和时间的优化
为选择合适的萃取温度和时间,分别在45 ℃、60 ℃、75 ℃条件下超声萃取20 min、40 min、60 min、80 min,结果如表7所示:在考察范围内,温度对萃取的效率影响不大,不做限定;萃取效率随萃取时间增大而增大,当萃取时间大于40 min后达到平衡。考虑萃取的完全与样品的差异性,同时兼顾萃取效率,选择60 min为萃取时间。

表7 不同萃取温度和时间对检测结果的影响 (mg/kg, n=5)
2.3 方法验证
2.3.1 线性关系、检测限
将配制好的一系列亚硝酸盐、硝酸盐标准溶液按1.4仪器条件进样检测,以相应浓度(mg/L)为横坐标,其响应峰面积为纵坐标,绘制标准曲线。得到亚硝酸盐回归方程为:y= 1.6752 x + 0.00113,R2=0.9997,线性范围0.032~1.600 mg/L;硝酸盐回归方程为:y = 1.357x + 0.0065,R2= 0.9998,线性范围0.800~40.000 mg/L。
取最低浓度标准溶液连续重复进样10次,将10次测定的峰面积代入标准曲线的回归方程求出浓度值,再计算10次测定浓度值的标准偏差(SD),分别以3SD和10SD为C代入1.5中样品测定计算公式计算检测限和定量限。得到该法测定亚硝酸盐的检测限和定量限分别为1.23 mg/kg、3.72 mg/kg,硝酸盐的检测限和定量限分别为1.06 mg/kg、3.16 mg/kg。
2.3.2 样品回收率
采用标准加入法测定方法的回收率。以已知含量的样品为实验本底,在本底样品中准确加入亚硝酸盐、硝酸盐标样。按照实验方法操作,测得低、中、高3个加标水平下的亚硝酸盐、硝酸盐含量值。每个水平平行测定3个样品,取检测值进行加标回收率的计算,测试结果如表8所示。结果表明本方法检测亚硝酸盐的回收率为96.1%~101.6%,平均回收率为97.9%;硝酸盐的回收率为96.3%~99.0%,平均回收率为98.0%,满足定量分析要求。
2.3.3 精密度实验
为考察方法的精密度,对方法的日内及日间重现性进行了考察,结果如表9、10所示,日内及日间RSD均在5%以下,方法的精密度良好。

表8 方法回收率
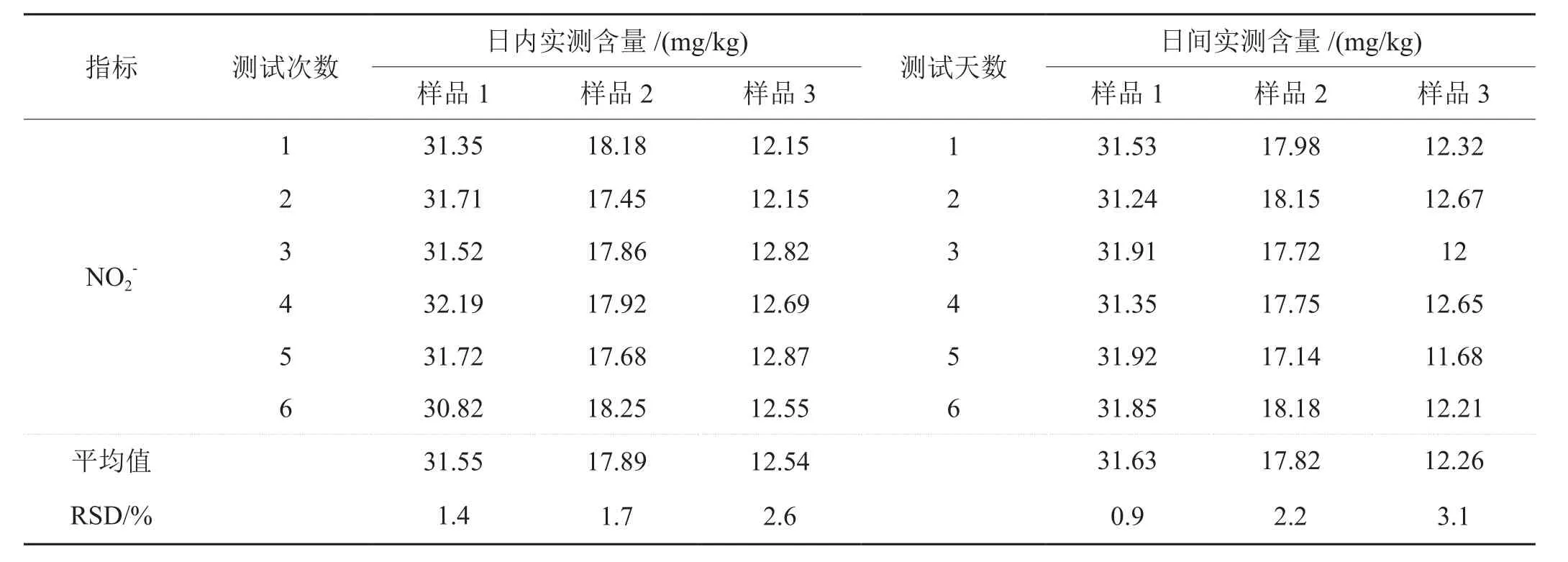
表9 方法检测NO2-的日内及日间精密度

表10 方法检测NO3-的日内及日间精密度
2.3.4 与经典方法的比对
与经典的连续流动分光光度法进行比对,如表11所示,结果发现:相对平均偏差均小于5%,与经典的连续流动分光光度法测定结果一致。
2.4 样品测定
应用本方法检测了部分样品NO2-和NO3-的含量,结果如表12所示:NO2-的含量不大,在8.45~36.30 mg/kg之间,不同类型的样品差异较小;NO3-在不同类型的样品中差异较大,在31.11~19151.42 mg/kg之间,含量大致规律为:白肋烟>梗丝>香料烟>再造烟叶>烤烟;混合型卷烟>烤烟型卷烟。
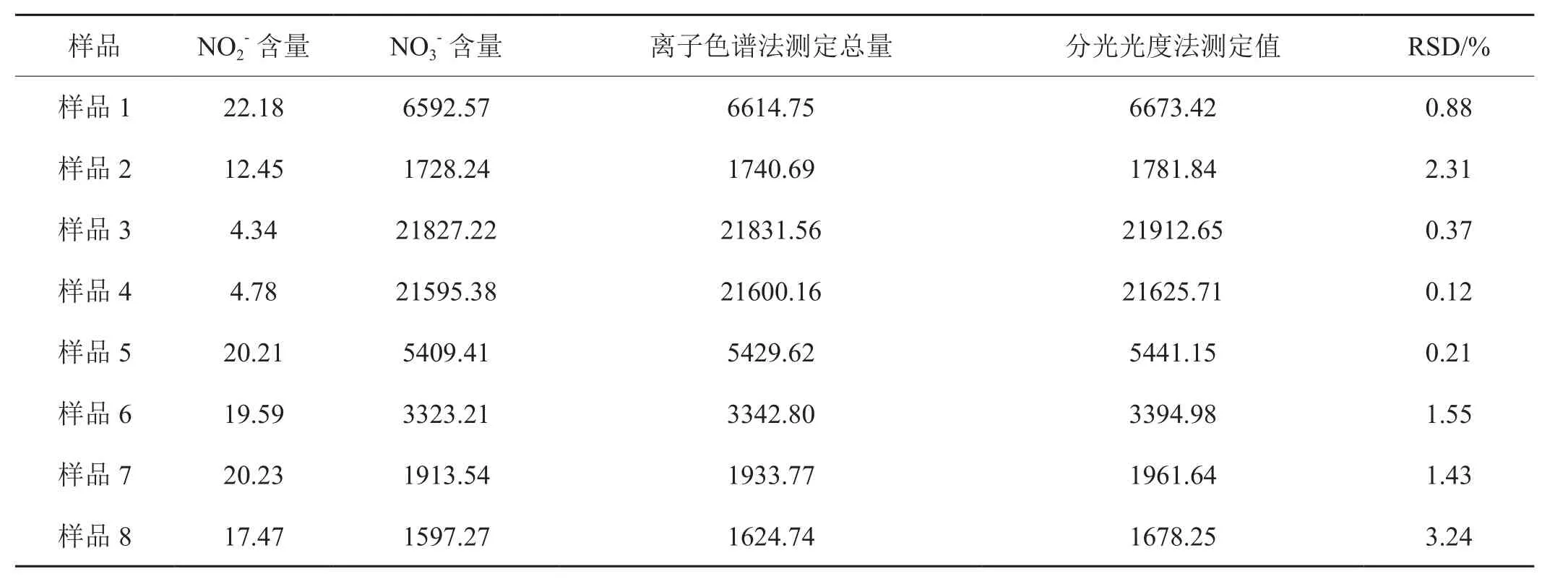
表11 与分光光度法比对实验 (mg/kg)

表12 样品检测数据 (mg/kg)

续表12
3 小结
通过实验,建立了烟草与烟草制品中亚硝酸盐、硝酸盐的离子色谱方法。采用超纯水超声提取的方法处理烟草样品,以氢氧化钾溶液为洗脱液、阴离子交换柱分离、电导检测器检测。该方法作为烟草与烟草制品中硝酸盐与亚硝酸盐的测定方法,操作简便、准确、快捷,选择性好,具有较强的实用价值。
[1]肖协忠.烟草化学.北京:中国农业科技出版社[M].1997.
[2]Burton H R,Dye N K, Bush L P.Relationship between tobacco-speci fi c nitrosamines and nitrite from different aircured tobacco varieties[J].J Agric Food Chem,1994,42:2007-2011.
[3]YC/T 296-2009烟草及烟草制品硝酸盐的测定 连续流动法[S].
[4]GB/T 15401.94,水果、蔬菜及其制品亚硝酸盐和硝酸盐含量的测定.
[5]黄彩海,杨丽绢,陈花果.紫外分光光度法同时测定水样中硝酸盐和亚硝酸盐氮[J].中国环境监测,1988,4(15):15-18.
[6]刘长增.动力学催化光度法测定痕量亚硝酸根[J].分析化学,2000,26(11):1362-1365.
[7]张克忠,等.催化光度法测定痕量亚硝酸根[J].分析化学,1998,26(4):494-499.
[8]吴仲可,徐允梁,顾荷英.高效液相色谱法同时测定蔬菜中的硝酸盐和亚硝酸盐[J].上海农学院学报,1993,1l(1):7-11.
[9]周梅素,郭东龙.离子色谱法测定蔬菜中硝酸盐含量[J].分析化学,2000,28(8):1056-1060.
[10]蒋蓉,金玉娥,汪国权.离子色谱法测定蔬菜、水果中的亚硝酸盐和硝酸盐[J].分析仪器,2003,4:29-3l.
[11]GB/T 5009.33-2003,食品中亚硝酸盐和硝酸盐含量的测定[S].
[12]王耀光.基于偶联反应新极谱法测定痕量亚硝酸根的研究Ⅱ.以苯酚为偶联剂[J].分析化学,1994,22(8):767-770.
[13]Jimidar M,Hartmann C,Cousement N,et a1.Determination of nitrate and nitrite in vegetables by capillary electrophoresis with indirect detection [J]. J Chromatog A,1995,706:479-492.
[14]ztekin N,Nutku M S,Erim F B,Simultaneous determination of nitrite and nitrate in meat products and vegetables by capillary electrophoresis[J]. Food Chem,2002,76:103-106.
[15]Ximenes M I N,Rath S,Reyes F G R. Polarographic determination of nitrate in vegetables[J]. Talanta,2000,51:49-56.
[16]Haddad. Ion chromatography [J]. Anal Bioanal Chem,2004,379 : 341-343.
[17]彭慧敏,吴名剑,任凤莲,等.离子色谱法测定卷烟主流烟气中的氮氧化物[J]. 分析化学,2007(2):289-292.
[18]庹苏行,吴名剑,李辉,等.离子色谱法同时测定烟叶中的6种无机阴离子[J]. 烟草科技,2006(11):37-41.
[19]杨蕾,侯英,王保兴,等. 梯度洗脱/离子色谱法对烟草及烟草制品中7种无机阴离子的快速测定[J]. 分析测试学报,2010,29(2):165-170.

