SO42-/TiO2-Al2O3催化水解花生壳制备乙酰丙酸的研究
张 宁,晁彩林,刘冬莲,刘 爽
(1. 唐山师范学院 化学系,河北 唐山 063000;2. 唐山师范学院 滦州分校,河北 唐山 063700)
SO42-/TiO2-Al2O3催化水解花生壳制备乙酰丙酸的研究
张 宁1,晁彩林2,刘冬莲1,刘 爽1
(1. 唐山师范学院 化学系,河北 唐山 063000;2. 唐山师范学院 滦州分校,河北 唐山 063700)
以花生壳为原料,以SO42-/TiO2-Al2O3固体酸为水解催化剂制备乙酰丙酸,探讨了固体酸用量,水解时间,水解温度,液固比对乙酰丙酸得率的影响。研究结果表明,当固体酸用量3.5%、水解时间150 min、水解温度250 ℃、液固比21:1(L/mg)时为较优的制备工艺。在该工艺条件下,乙酰丙酸得率为12.35%。
乙酰丙酸;固体酸;花生壳;水解
乙酰丙酸(Levulinic acid,LA)是一种新型平台化合物,兼有羧酸和酮的特性[1],通过酯化、卤化、加氢、氧化脱氢、缩合以及其它化学反应,可制得各种各样的产品,广泛用于食品、化工、环保、医疗、生物制药等多个领域。目前,利用以纤维素、半纤维素和木质素为主要成分的可再生生物质资源,采用固体酸为催化剂制备乙酰丙酸成为化学热点研究领域之一[2]。已有的研究表明[3-6],含纤维素大分子的稻草、玉米秸秆、木屑、棉籽壳、甘蔗渣、高粱等在适当的条件下能生成水解纤维素,并能进一步生成乙酰丙酸。但以花生壳为原料制备乙酰丙酸的研究尚未见报道。
花生是我国的重要农作物之一,花生壳是一种可再生资源。然而,花生壳的主要成分粗纤维并未充分利用,目前大部分用做燃料或当作废渣弃去。本研究将固体酸SO42-/TiO2-Al2O3用于水解花生壳制备乙酰丙酸,就固体酸用量,反应时间,反应温度,液固比等因素对乙酰丙酸得率的影响进行探讨,并对制备工艺进行优化。
1 材料与方法
1.1 材料
花生壳取自河北唐山农村,经水洗、干燥、粉碎后过40目筛备用;二氧化钛,硝酸铝,氨水,硫酸,氢氧化钠(粒),乙酰丙酸,苯甲酸及无水甲醇均为分析纯。
1.2 主要仪器
FW-177型中草药高速万能粉碎机(天津市泰斯特仪器有限公司);SX2-4-10箱式电阻炉(天津市中环实验电阻炉有限公司);150 mL不锈钢反应釜(东台市溱东镇开庄工业区);GC-7900型气相色谱仪(Techcomp);TENSOR 37型傅立叶红外光谱仪(德国布鲁克光谱仪器公司)。
1.3 实验方法
1.3.1 固体酸的制备
采用化学共沉淀法制备样品。按n(Al):n(Ti)为2:1(物质的量)的比例称取一定量的硝酸铝,二氧化钛于蒸馏水中,剧烈搅拌下滴加浓氨水至pH为8~9。陈化过夜后,用蒸馏水洗涤沉淀使其不含SO42-(用BaCl2检测),减压抽滤,滤饼于100 ℃烘箱中烘干12 h,研磨、过100目筛。用2 mol·L-1硫酸浸渍2 h。减压过滤,滤饼于100 ℃烘箱中烘干,研磨后置于箱式电阻炉中450 ℃焙烧4 h。
1.3.2 花生壳的碱预处理
称取一定量的花生壳粉末,加入到质量分数为8%的氢氧化钠溶液中,在温度为80 ℃的恒温水浴中提取3 h。过滤,滤渣水洗至中性,干燥,研磨备用[4]。
1.3.3 乙酰丙酸的制备
将1.0 g碱处理后的花生壳粉末、蒸馏水和一定质量分数的固体酸,加入不锈钢反应釜中,加热反应一定时间后,过滤,水洗,收集滤液,将滤液定容至10 mL,测定乙酰丙酸得率[7-8]。
花生壳主要成分包括纤维素、半纤维素。纤维素在酸的催化水解作用下分解成单糖,再在酸的持续水解下脱水形成5-羟甲基糠醛,最终进一步脱羧生成乙酰丙酸。反应原理如下:
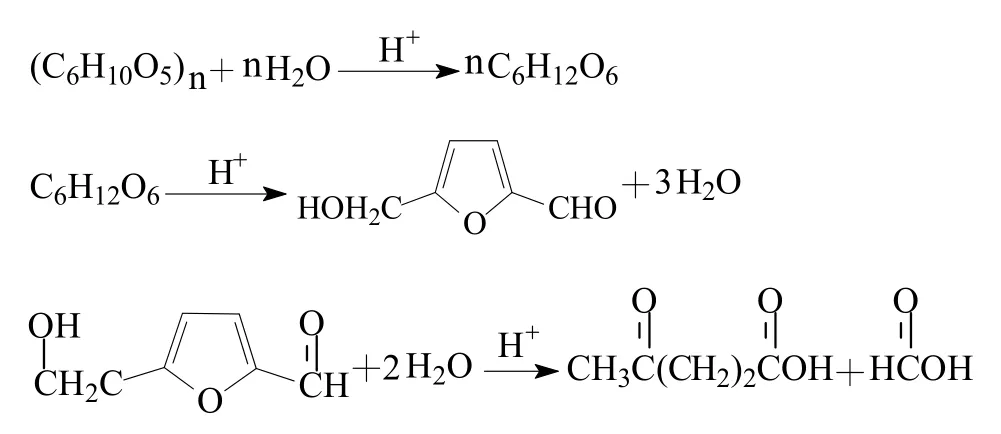
1.3.4 水解液中乙酰丙酸含量的测定
以苯甲酸为内标物、甲醇为溶剂,采用气相色谱法测定水解液中乙酰丙酸的含量(质量浓度)。色谱操作条件:柱温150 ℃,保留时间9 min,气化室温度250 ℃,检测器温度250 ℃,分流比30:1,进样量1 μL。
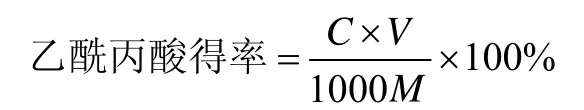
式中,C为色谱法测定水解液中乙酰丙酸的质量浓度,
g·L-1;V为水解液的体积,mL;M为原料中绝干纤维素的质量,g。
2 结果与分析
2.1 固体酸红外光谱
固体酸SO42-/TiO2-Al2O3经KBr压片后,用红外光谱仪测得红外谱图如图1所示。
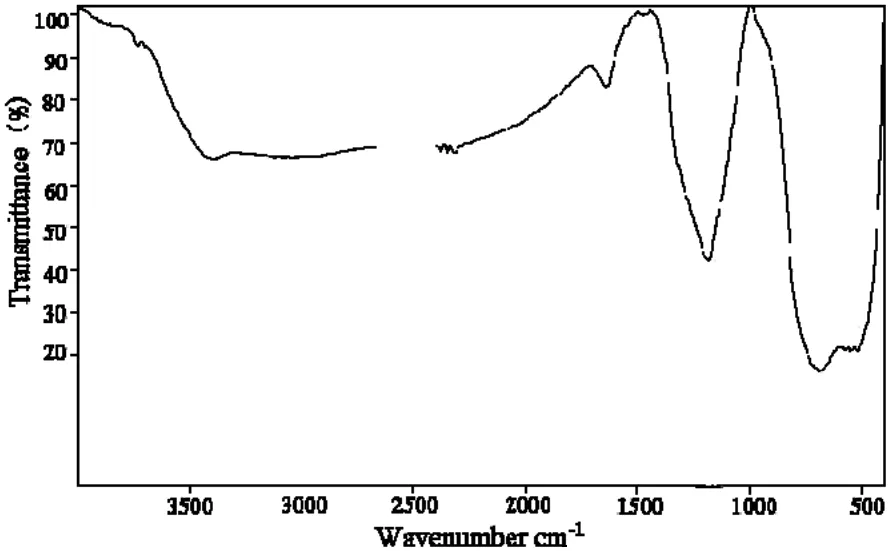
图1 固体酸的红外光谱图
SO42-/MxOy型固体超强酸的活性来源于硫酸根对氧化物表面金属原子的配位。据文献[9-10]报道,SO42-/MxOy型固体超强酸在低波数900~1 300 cm-1处出现较宽化的吸收峰为硫酸S=O振动。从图1可以看出,在1 150 cm-1附近有较宽化超强酸中心结构的特征峰,表明硫酸根已经负载到催化剂表面。在1 636 cm-1附近的红外吸收峰为催化剂中存在的水分,归属于H-O-H的弯曲振动。此外,根据S=O的红外最高振动吸收峰可以判断SO42-离子与Al2O3的配位形式(图2),若S=O的红外吸收在1 200 cm-1以上,则认为是以螯合双配位为主;若S=O在低波数1 080~1 150 cm-1处的吸收则以桥式配位为主[11],这表明S=O既具有部分双键特性又具有共价键的特性,其共价性越强,则酸性也越强。从图1可以看出,实验所制得的固体酸催化剂在1 150 cm-1处附近有一个较强的吸收峰,因此是以桥式配位为主。
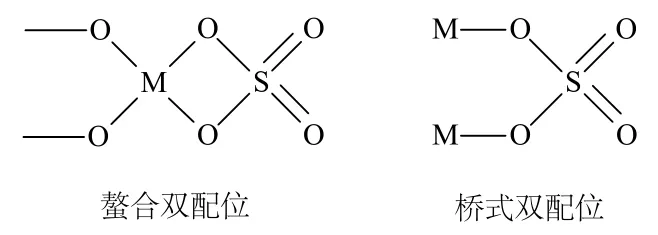
图2 SO42-与金属氧化物的配位方式
2.2 单因素实验
2.2.1 固体酸用量对乙酰丙酸得率的影响
固定反应温度230 ℃、反应时间100 min、液固比为18:1,考察不同固体酸用量对乙酰丙酸得率的影响,结果如表1。

表1 固体酸用量对乙酰丙酸得率的影响
由表1可以看出,随着固体酸用量的增加,乙酰丙酸的得率先增加后减小。当固体酸的用量偏低时,提供给反应体系的活化中心数目减少,反应体系中固体酸对花生壳的催化水解能力下降,催化效果也相应降低;而当固体酸的用量偏大时,实验发现水解滤渣中夹杂黑色物质,可能是部分原料在未水解之前就被炭化,从而影响了水解效果。因此,固体酸用量过低或过高均会影响乙酰丙酸的得率。综合考虑各种因素,选择固体酸用量为3.5%为宜。
2.2.2 液固比对乙酰丙酸得率的影响
固定反应温度230 ℃、反应时间100 min、固体酸用量为3.5%,考察不同的液固比对乙酰丙酸得率的影响,结果如表2。

表2 液固比对乙酰丙酸得率的影响
由表2可知,随着液固比的增加,乙酰丙酸的得率逐渐增加,因为液固比越大越有利于固体与液体的充分接触,从而有利于反应的进行。当液固比达到18:1以后,乙酰丙酸的得率增幅很小,因此18:1为较宜的水解反应液固比。
2.2.3 反应时间对乙酰丙酸得率的影响
固定反应温度230 ℃、液固比18:1、固体酸用量3.5%,通过改变反应时间考察其对乙酰丙酸得率的影响,结果如表3所示。
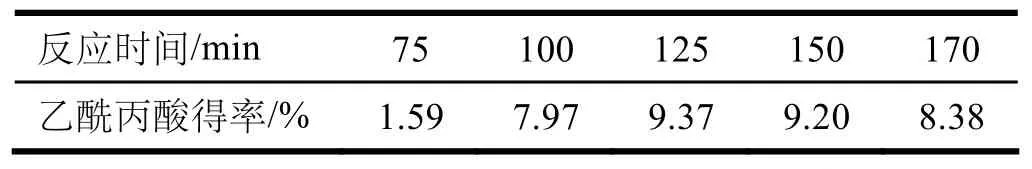
表3 反应时间对乙酰丙酸得率的影响
由表3可知,水解时间为75 min时乙酰丙酸的得率很低,可能是反应时间太短导致反应不充分。当水解时间为125 min时得率最高,再延长反应时间乙酰丙酸得率有缓慢降低的趋势。反应时间过长可能使反应体系中副产物的量逐渐增多,致使乙酰丙酸自身分解并和副反应产物进行缩合。这一点可以从水解液颜色的变化得到证明:随着水解时间的增加,反应体系从无色到淡黄色再到黄色,最后到棕色。因此反应时间125 min为宜。
2.2.4 反应温度对乙酰丙酸得率的影响
固定液固比18:1、固体酸用量3.5%、反应时间125 min的条件,控制不同的反应温度测定水解液中乙酰丙酸得率,结果如表4。

表4 反应温度对乙酰丙酸得率的影响
由表4可知,反应温度低于210 ℃时乙酰丙酸的得率较低,当温度大于230 ℃时得率显著提高,250 ℃时乙酰丙酸得率最高为10.49%,260 ℃时得率反而有所降低。可能是由于反应温度过高时,体系中副反应增多。所以反应温度250 ℃为宜。
2.3 正交实验
在单因素实验的基础上进行正交实验,正交因素条件如表5,正交实验结果见表6。
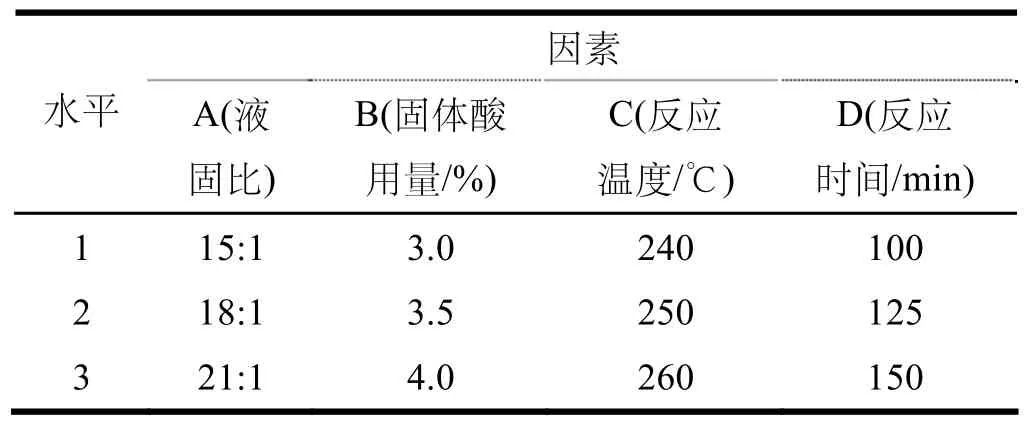
表5 正交实验的因素与水平
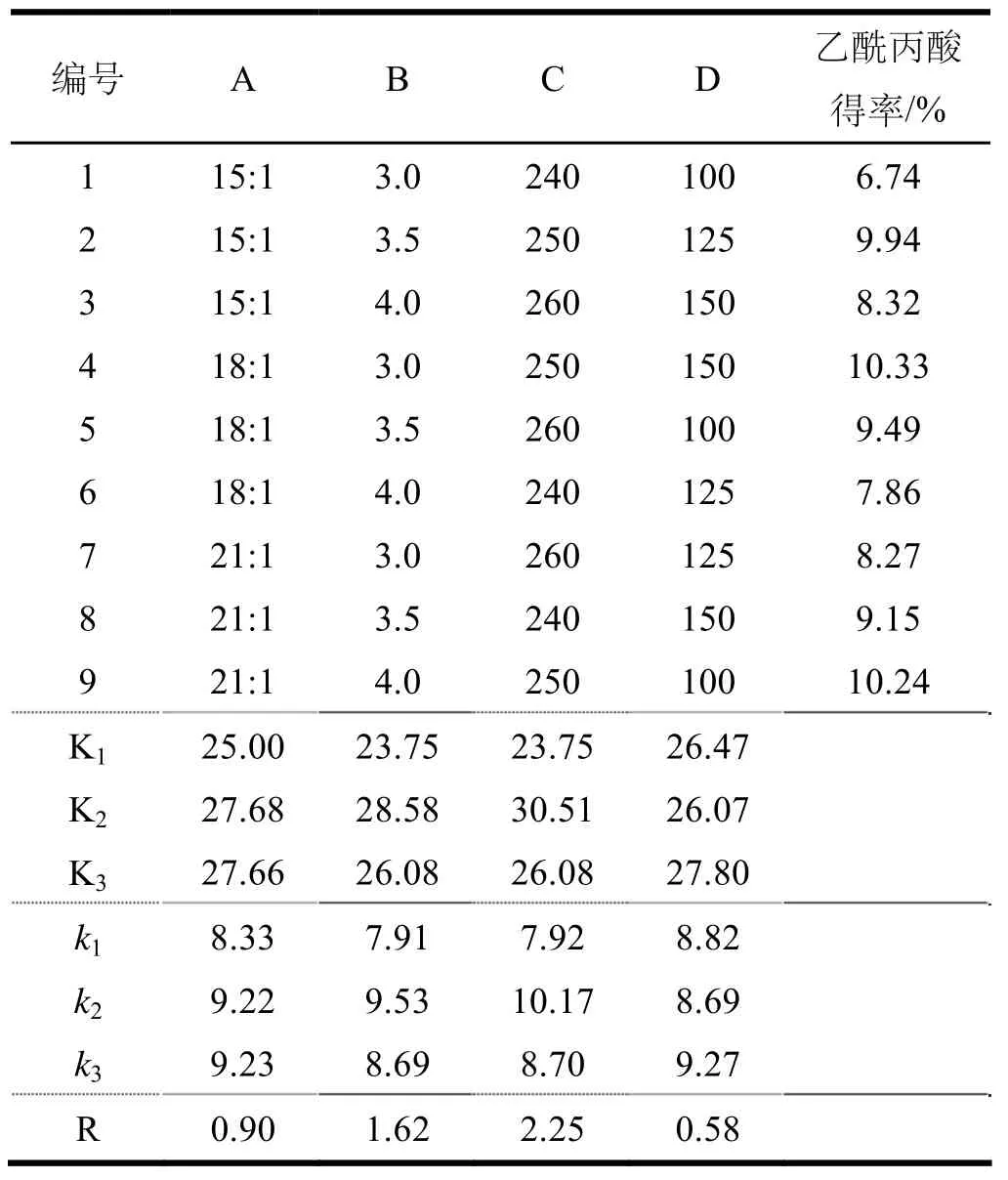
表6 正交实验结果
用极差分析法对实验结果进行分析。由表6中的R值可知影响乙酰丙酸得率的因素主次关系为:C>B>A>D,即反应温度>固体酸用量>液固比>反应时间。最佳工艺组合为A3B2C2D3:液固比21:1,固体酸用量3.5%,反应温度250 ℃,反应时间150 min。按上述最优条件追加3次实验,固体酸催化水解制备乙酰丙酸的平均得率为12.35%。
3 结论
花生壳能够在SO42-/TiO2-Al2O3固体酸的催化作用下水解生成乙酰丙酸,而且固体酸容易与水解液分离。乙酰丙酸的得率与固体酸用量、反应温度、固液比和反应时间等工艺因素有关。通过正交试验对花生壳制备乙酰丙酸工艺条件的优化分析,确定较优的工艺条件为:液固比21:1,固体酸用量3.5%,反应温度250 ℃,反应时间150 min,乙酰丙酸得率可达12.35%。
[1] Bozell J J, Moens L, Elliontt D C, et al. Production oflevulinc acid and use as a platform chemical for derived products[J]. Resources, Conservation and Recycling. 2000, 28: 227-239.
[2] 常春,马晓建,方书起,等.可再生资源制备平台化合物乙酰丙酸的研究进展[J].化工新型材料,2005,33(8):69-70.
[3] 于先纯,孙德林.固体酸催化水解杉木制备乙酰丙酸的研究[J].中南林业科技大学学报,2009,29(5):120-122.
[4] 刘凯,方桂珍,马艳丽,等.稻草酸水解制备乙酰丙酸的研究[J].生物质化学工程,2007,41(4):13-16.
[5] 李湘苏,余先纯.超声波预处理协同固体酸水解小麦秸秆制备乙酰丙酸的研究[J].安徽农业科学,2010,38(26): 14236-14238.
[6] 余先纯,孙德林.响应面法优化固体酸水解玉米秸秆制备乙酰丙酸的研究[J].湖北农业科学,2010,49(10):2517-2520.
[7] 蔡磊,吕秀阳,何龙,等.气相色谱法直接分析生物质水解产物中的乙酰丙酸[J].分析测试学报,2004,23(6):104-105.
[8] Qi Fang, Milforda, Hanna. Experimental studies for levulinic acid production from whole kernelgrain sorghum[J]. Bioresource Technology, 2002, 81: 187-192.
[9] 韩周冰,陈先明,赵帆.SO42-/ZrO2型固体超强酸的制备与表征[J].精细石油化工进展,2008,9(7):20-23.
[10] 陈少峰,侯兰凤,董利.固体超强Fe/SO42--SnO2的合成和表征研究[J].当代化工,2010,39(6):644-645.
[11] 姜华昌,曾翎,尹炳龙,等.SO42-/Fe2O3-Al2O3-SiO2固体超强酸的制备及其催化水解蔗糖生成乙酰丙酸[J].林产化学与工业,2010,30(6):61-65.
(责任编辑、校对:琚行松)
Preparation of Levulinic Acid from Peanut Shells Hydrolyzed by Solid Acid of SO42-/TiO2-Al2O3
ZHANG Ning1, CHAO Cai-ling2,LIU Dong-lian1, LIU Shuang1
(1. Department of Chemistry, Tangshan Teachers College, Tangshan 063000, China; 2. Luanzhou Branch School, Tangshan Teachers College, Tangshan 063700, China)
Levulinic acid (LA) can be prepared from peanut shells with SO42-/TiO2-Al2O3solid acid as hydrolysis catalyst. The effects on the amount of solid acid, hydrolysis time, hydrolysis temperature and liquid-solid ratios on the LA yield had been discussed in this thesis. The experimental results showed that the optimal conditions as follow: solid acid was 3.5%, hydrolysis time was 150 min, hydrolysis temperature was 250 ℃, and liquid-solid ratio was 21:1(L/mg). Under this condition, the LA yield could reach to 12.35%.
levulinic acid; solid acid; peanut shells; hydrolysis
TQ353.6
A
1009-9115(2013)02-0010-04
10.3969/j.issn.1009-9115.2013.02.004
唐山师范学院科学研究基金项目(07C20)
2012-06-23
张宁(1979-),女,河北石家庄人,硕士,讲师,研究方向为无机功能材料及高分子材料。

